Изобретение относится к офтальмологии и может быть использовано при хирургическом лечении первичной глаукомы. Известен способ лечения глаукомы посредством проведения проникающей операции фистулизирующего типа - трабекулэктомии [Cairns J.F. Trabeculectomy. Am. J. Ophthalmol., 1968;60:673-678]. Однако данная фистулизирующая операция, обладая достаточно высоким гипотензивным эффектом, сопровождается и большим числом осложнений (в раннем периоде – это отслойка сосудистой оболочки, гифема, синдром мелкой передней камеры и др., в позднем – развитие и прогрессирование катаракты и др.), которые негативно отражаются на функциональных и гипотензивных результатах хирургического вмешательства. Кроме того, в некоторых случаях при закрытоугольной глаукоме выраженная фистулизация может привести к развитию злокачественной глаукомы. Известен также способ лечения глаукомы в виде проведения непроникающей антиглаукомной операции - непроникающей глубокой склерэктомии (НГСЭ) [С.Н.Федоров, В.И.Козлов, Н.Т.Тимошкина и др. Непроникающая глубокая склерэктомия при открытоугольной глаукоме. Офтальмохирургия. 1989;3-4:52-55], заключающийся в выкраивании конъюнктивального и поверхностного склерального лоскутов с последующим формированием и удалением участка наружной стенки шлеммова канала и участка глубоких слоев склеры над цилиарным телом с сохранением отдельных волокон склеры на поверхности последнего. Однако, как показали клинические исследования, гипотензивная эффективность только одной НГСЭ небольшая, особенно в отдаленные сроки. Причинами неэффективности традиционной НГСЭ, по своей технологии, выполняемой без проведения иридэктомии, и, поэтому только при открытоугольной глаукоме, являются избыточное рубцевание в зоне операции, несостоятельность трабекулы, нарушение дренирующей функции трабекуло-десцеметовой мембраны. Кроме того, для обеспечения гипотензивного эффекта НГСЭ в большинстве случаев требуется своевременное проведение дополнительного лазерного лечения - десцеметогониопунктуры, которая является даже обязательной при выполнении данной операции в микроинвазивном варианте. Поэтому в последующем НГСЭ стала комбинироваться с элементами проникающей (фистулизирующей) хирургии. В частности, известен способ хирургического лечения глаукомы [Бикбов М.М., Исрафилова Г.З., Бабушкин А.Э., Оренбуркина О.И. Способ лечения первичной открытоугольной глаукомы. Патент РФ № 2735378 С1 от 30.10. 2020. Способ лечения первичной открытоугольной глаукомы, Бюл. изобр. № 31 от 30.10.2020 г.], характеризующийся тем, что после формирования поверхностного и глубокого лоскутов склеры, в 2 мм от лимба и параллельно ему производят разрез склеры до цилиарного тела в пределах склерального ложа. Из сформированного ранее глубокого лоскута склеры путем разреза до основания формируют две полоски, одну из которых с помощью микрошпателя заправляют в переднюю камеру, а другую, после предварительного заднего циклодиализа, имплантируют через циклодиализную щель в супрахориоидальное пространство по направлению к своду. Однако гипотензивный эффект данной частично фистулизирующей операции оказался недостаточно стойким. К тому же, данный способ может применяться в основном только в начальных стадиях открытоугольной первичной глаукомы. За ближайший аналог принят способ хирургического лечения глаукомы, заключающийся в том, что с целью устранения препятствий оттоку внутриглазной жидкости на всех уровнях дренажной системы, выполняется комбинированная операция, сочетающая НГСЭ и трабекулотомию ab externo [Булгар С.Н., Ахметшин Р.Ф., Малинин Д.Е. Сравнительные результаты операций нефистулизирующего типа при лечении первичной открытоугольной глаукомы. Казанский медицинский журнал.2012; 93(6):996-999]. Техника операции. Отступя от лимба на 6 мм, выполняют разрез конъюнктивы длиной 5 мм, осуществляют гемостаз. Отсепаровывают поверхностный склеральный лоскут прямоугольной формы до роговичной части лимба, выкраивают глубокий склеральный лоскут до трабекулярной стенки шлеммова канала и лимбальной части десцеметовой мембраны, заходя в слои роговицы на 1-2 мм, с последующим иссечением глубокого склерального лоскута. Далее из просвета вскрытого шлеммова канала с помощью введенного туда трабекулотома обратным его движением выполняют рассечение внутренней стенки шлеммова канала. В результате образуются пространственные дефекты в тканях внутренней стенки шлеммова канала по обе стороны от иссечѐнного глубокого склерального лоскута, но вне его проекции. Далее проводят герметизацию операционного доступа - на поверхностный склеральный лоскут накладывают два узловых шва, на конъюнктиву - непрерывный шов. Показания к операции, по мнению авторов, ограничены открытоугольной глаукомой с умеренным поражением дренажного аппарата, т.е. начальной и развитой стадиями заболевания. При далекозашедшей стадии ПОУГ эффект, как правило, отсутствует или кратковременный и часто недостаточный, а при закрытоугольной (узкоугольной) глаукоме со зрачковым блоком его нет из-за отсутствия в технологии операции иридэктомии. Задачей изобретения является разработка способа хирургического лечения первичной глаукомы, обеспечивающего улучшение функциональных результатов лечения. Технический результат при использовании изобретения - повышение стабильности гипотензивного эффекта и зрительных функций, расширение показаний к применению антиглаукомной операции для лечения разных форм и стадий первичной глаукомы.
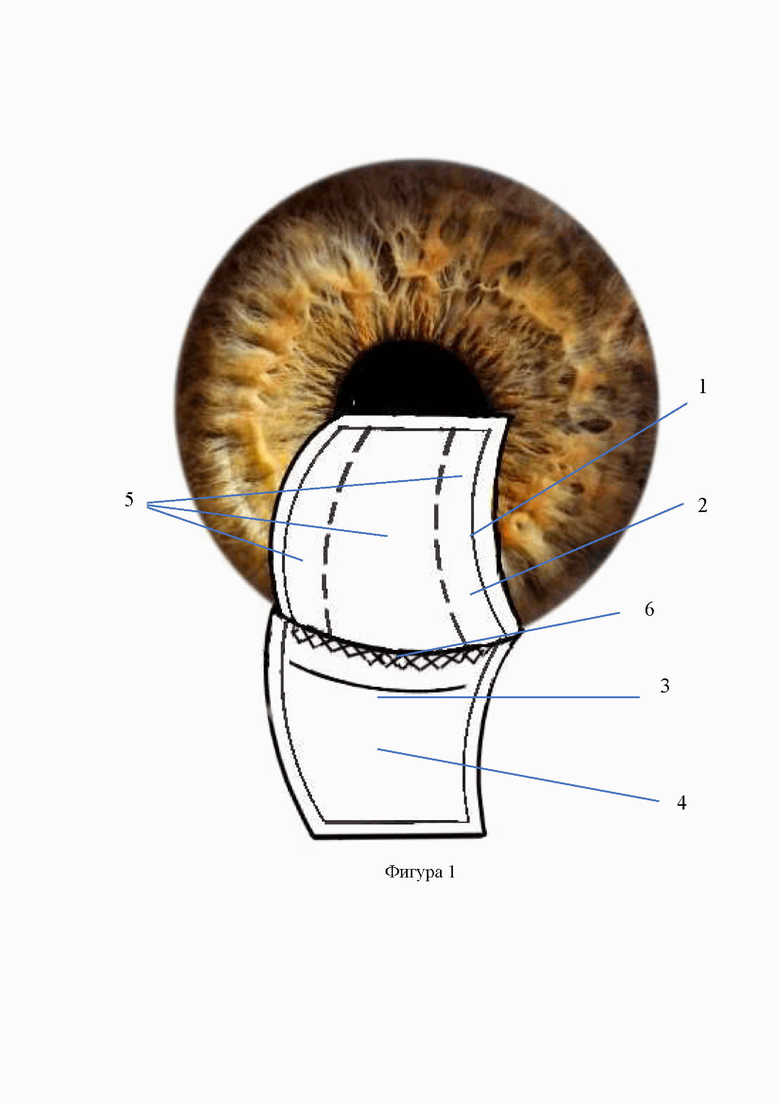
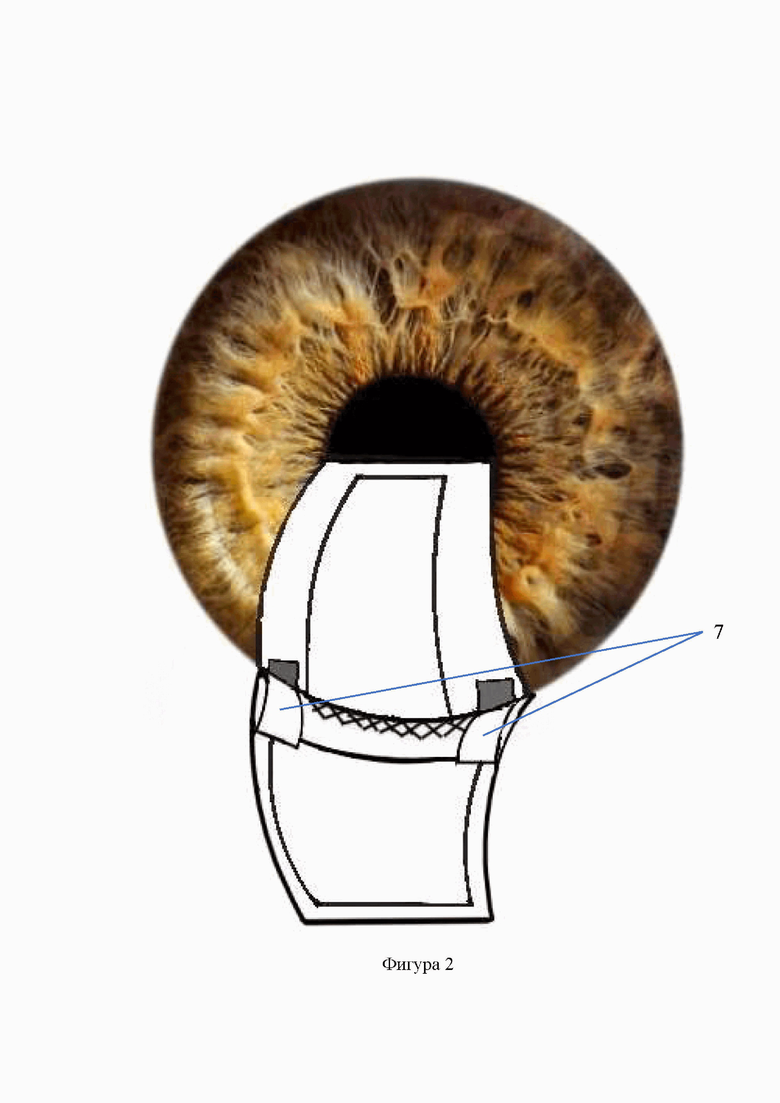
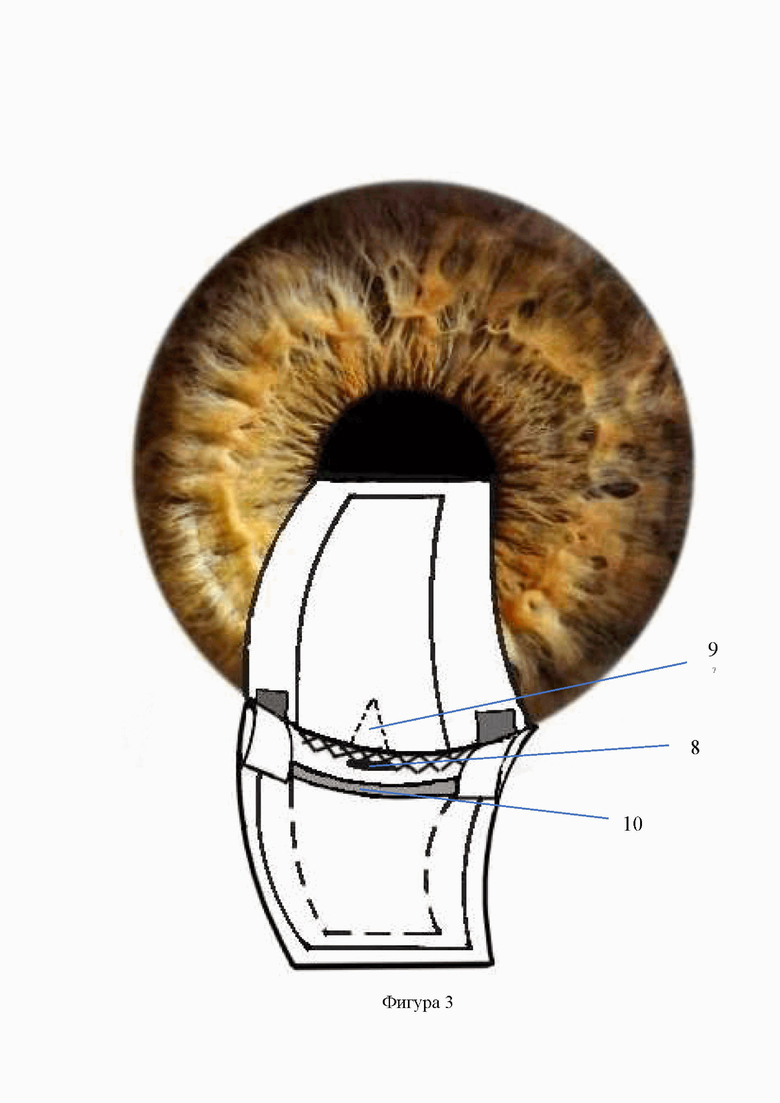
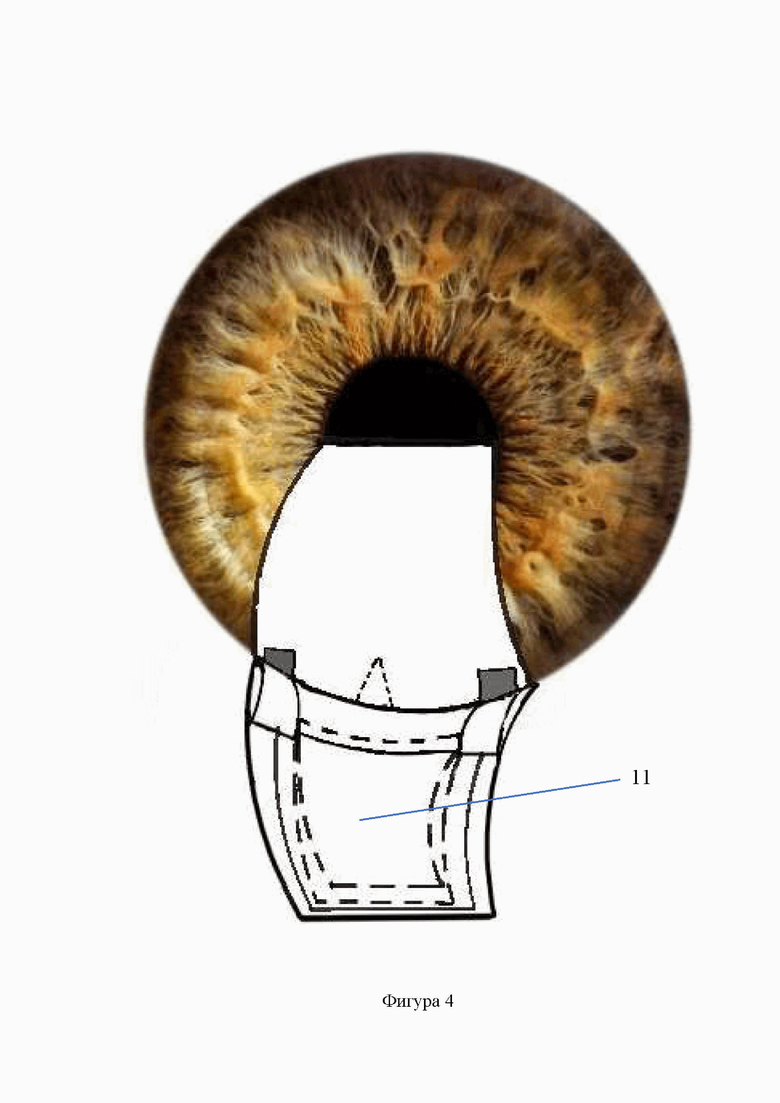
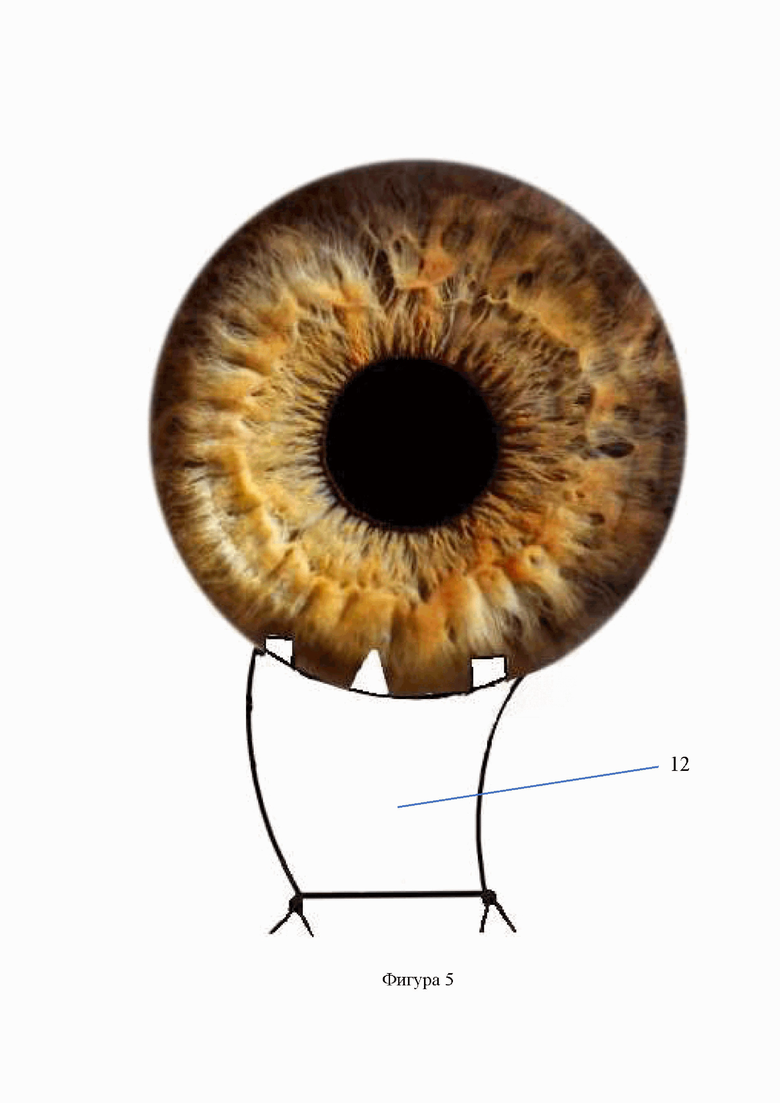
Изобретение иллюстрируется фигурами №№1-5, на которых схематично изображены этапы предлагаемого способа, где: 1 - поверхностный склеральный лоскут, 2 -лоскут из средних слоев склеры трапециевидной формы, 3 - трабекуло-десцеметовая мембрана, 4 - ложе глубокого лоскута склеры, 5 - разрез лоскута из средних слоев склеры с формированием трех полосок, 6 - параллельный лимбу разрез глубоких слоев склеры до цилиарного тела, 7 - боковые полоски склеры, имплантированные через разрез глубоких слоев склеры в угол передней камеры, 8 - трабекулотомия, 9 - базальная иридэктомия, 10 - аллотрансплантат, имплантированный после предварительного заднего циклодиализа в супрацилиарное пространство, 11 - центральная полоска склеры, введенная в супрахориоидальное пространство поверх аллотрансплантата, 12 - поверхностный склеральный лоскут, укрепленный 2 узловыми швами.
Предлагаемый способ хирургического лечения первичной глаукомы осуществляется следующим образом. Отступя от лимба на 5,5-6 мм выполняют разрез конъюнктивы длиной 6-7 мм, осуществляют гемостаз. Отсепаровывают поверхностный склеральный лоскут на 1/3 толщины склеры трапециевидной формы длиной лимбальной части 8 мм, склеральной - 6 мм и шириной 5 мм. Из средних слоев склеры выкраивают лоскут также трапециевидной формы основанием к лимбу до обнажения трабекулы и периферической части десцеметовой оболочки на 1-2 мм. Затем из лоскута средних слоев склеры посредством двух разрезов, параллельных его краям и перпендикулярно его основанию формируют три полоски склеры. Ширина крайних полосок склеры – 1,5 мм, ширина центральной полоски в проксимальной к лимбу части – 5 мм, а в дистальной – 3 мм. Затем в 2 мм от лимба на протяжении склерального ложа производят сквозной параллельный лимбу разрез до цилиарного тела длиной 7 мм, из которого выполняют передний циклодиализ. Как правило, его выполнение сопровождается истечением небольшой порции влаги из передней камеры, которая, однако, полностью при этом не опорожняется. Убедившись, что зрачок занимает центральное положение, крайние полоски склеры поочередно с помощью шпателя имплантируют в угол передней камеры (УПК). Далее у основания центральной полоски производят сквозной разрез трабекулы длиной 2-2,5 мм, через который выполняют базальную иридэктомию. Далее через разрез глубоких слоев склеры в области ложа и после предварительного заднего (в сторону свода) циклодиализа, в супрахориоидальное пространство имплантируют биоматериал «Аллоплант» для реваскуляризации зрительного нерва [Аллотрансплантаты для хирургии «Аллоплант»® по ТУ 9398-001-04537642-2011] шириной по лимбу 6 мм длиной 5 мм, а затем поверх него – оставшуюся центральную полоску из средних слоев склеры. Поверхностный склеральный лоскут укладывают на свое место и фиксируют двумя узловыми швами, а конъюнктивальный разрез - непрерывным швом (фиг. 1-5).
Для объективной оценки предлагаемого способа было обследовано 55 пациентов (55 глаз) в возрасте от 51 года до 83 лет (при этом возраст большинства пациентов 81,8% или 45 человек на момент операции был старше 60 лет), из них мужчин - 26, женщин - 29. Общие сопутствующие заболевания (сердечно-сосудистой системы, сахарный диабет, ЖКТ и т.д.) зафиксированы у 51 (92,7%) пациента. В среднем уровень ВГД до операции на фоне медикаментов при пневмотонометрии составил 29,1±1,4 мм рт.ст. Псевдоэксфолиации на передней капсуле хрусталика (при расширенном зрачке) обнаружены на 20 (36,4%) глазах.
Выделены 3 группы первично оперированных больных: первая, состоящая из 21 пациента, которым была выполнена операция по предлагаемому способу; вторая группа из 18 пациентов – им проведена антиглаукомная операция по способу-прототипу; в третьей группе 16 пациентам сделана классическая фистулизирующая операция (трабекулэктомия).
Распределение пациентов по формам и стадиям глаукомы было следующим. Первичная открытоугольная глаукома (ПОУГ) в 1 группе имела место у 10 пациентов (47,6%), во 2-й – у 9 (50,0%) и в 3-й – у 7(43,8%). Наличие хронической формы первичной закрытоугольной глаукомы (ПЗУГ) зафиксировано у 8 пациентов (38,1%) 1 группы, у 6 - второй (33,3%) и 6 - третьей (37,5%) групп. И, наконец, смешанная форма первичной глаукомы была отмечена у 3 пациентов в каждой из сравниваемых групп, что составило соответственно 14,3%, 16,7% и 18,8%. Начальная стадия - 14,3% (3 глаза) в 1 группе, 11,1% (2 глаза) - во второй группе и 12,5% (2 глазах) - в третьей группе. Пациенты с развитой стадией глаукомы составили: 47,6% в 1 группе (10 глаз), 50,0% (9 глаза) – во второй и 50,0% (8 глаз) – в третьей. Далекозашедшая глаукома диагностирована на 8 глазах в 1-й (38,1%) и на 7 глазах 2-й (38,9%) группы и на 6 глазах (37,5%) - в третьей группе. Умеренный уровень ВГД в 1 группе наблюдался в 57,1%, во 2 группе – в 61,1%, в 3 группе - 43,8%, высокий – соответственно в 42,9%, 56,2%, 31,2% на фоне максимальной медикаментозной нагрузки (2,7±1,3, 2,4±1,4, 2,9±1,5). Следует отметить, что сравниваемые группы были сопоставимы по форме первичной глаукомы, полу, возрасту, стадиям заболевания и уровню ВГД (последний показатель хоть и отличался большей долей высокого ВГД в 3-й группе, но это отличие не оказалось статистически достоверным). Максимальный срок наблюдения за пациентами составил 1 год и 8 месяцев (в среднем 12,7 месяцев). Из ранних послеоперационных осложнений в сравниваемых группах наблюдали гифему у 3 пациентов 1-й (14,3%) и 2-й (16,7%) групп и у 2 (12,5%) 3 группы. Цилиохориоидальная отслойка (ЦХО) сетчатки была отмечена по одному случаю в первой (4,8%) и во второй (5,6%) группах и в 2 случаях (12,5%) - в 3-й группе. При этом выпускание субхориоидальной жидкости потребовалось в обоих случаях ЦХО после выполнения трабекулэктомии. В первой и второй группах плоская ЦХО была купирована медикаментозно. Гипотензивный эффект после антиглаукомных операций при выписке пациентов из стационара в сравниваемых группах был достигнут у всех больных. Однако, в ранние сроки (до 4 месяцев) во 2 группе в двух случаях для нормализации офтальмотонуса потребовалось назначение медикаментозной коррекции (в 1 случае – тафлупроста, а в другом - тимолола + бримонидина). Кроме этого, в 3 группе в 1 случае (6,3%) у пациентки с ПЗУГ III стадии и наличием артифакии (полгода назад) и ПЗО – 22,15 мм через 2 недели после трабекулэктомии развился витреохрусталиковый блок (очень мелкая передняя камера, высокое ВГД, исчезновение фильтрационной подушки), который был купирован проведением витрэктомии с реконструкцией передней камеры и ликвидацией гониосинехий. В отдаленные сроки (через 6 и более месяцев, максимальный срок – 17, 2 месяцев, а в среднем – 12,8±3,3) было осмотрено 47 пациентов (18 из 1 группы, 15 – из 2-й и 14 – из 3 группы). Абсолютный гипотензивный эффект в 1 группе был достигнут в 83,3% (в 15 глазах) случаев, во 2 группе - в 60,0% (в 9) и в 3 группе - в 85,7% (в 12). Относительный (с применением медикаментозной нагрузки 1,0, 1,75, 1,0 соответственно) гипотензивный эффект в 1 группе получен в 11,1% случаев (в 2 глазах), во 2 группе - в 26,7% (в 4 глазах) и в 3 группе - 7,1% случаев (в 1 глазу). Отсутствие эффекта (уровень офтальмотонуса на максимальной медикаментозной терапии – не более 3-х препаратов) в 1 группе отмечали в 5,6% (в 1 случае), во 2 группе - в 13,3% (в 2 глазах) и в 3 группе - в 7,1% (в 1 случае). В 1 группе рецидив повышения ВГД был практически компенсирован с помощью лазерного лечения и комбинированной гипотензивной терапии (в итоге ВГД - 20-23 мм рт.ст. на фоне стабильных зрительных функций), в 3 группе потребовалось хирургическое лечение в виде нидлинга фильтрационной «псевдоподушки» и введения в ее область стероида. Во второй же группе в обоих случаях было принято решение о проведении фистулизирующей реоперации с применением дренажа Глаутекс в другом секторе УПК (после операции в 1 случае отмечена гифема, в другом – ЦХО). Динамика остроты зрения в сторону улучшения или ухудшения принималась во внимание лишь тогда, когда она изменялась не менее, чем на 0,2 при исходной остроте зрения 0,6-1,0 и не менее, чем на 0,1 при остроте зрения 0,1-0,5. В случаях значительного понижения остроты зрения (менее 0,09) за достоверный сдвиг принималась величина, равная 0,01 и больше. Острота зрения в отдаленные сроки наблюдения осталась на дооперационном уровне (в 12 глазах, 66,7%) или даже повысилась (в 4 глазах, 22,2% - она улучшилась в среднем на 0,09±0,03) в 1 группе в 88,9% случаев (всего в 16 глазах), во 2 группе она зафиксирована стабильной (в 12 или 80,0%) или улучшилась (в 1 глазу,6,7%) в 86,7% (всего в 13 глазах) и в 3 группе в 78,5% случаев (в 11 глазах) отмечалось сохранение только исходной остроты зрения. При этом в 1 случае в 1 группе и в 2 случаях – в 3 группе после антиглаукомной операции в связи с прогрессированием помутнения в хрусталике потребовалось его удаление (факоэмульсификация катаракты). При контроле поля зрения за норму принималась величина в 520 суммарных градусов при кинетической периметрии, а изменением его считалось сужение или расширение его не меньше, чем на 30 градусов при I и II стадиях заболевания и не менее, чем на 15 суммарных градусов при далекозашедшей глаукоме. Мониторинг поля зрения показал стабилизацию (в 11 или 61,1%) или расширение (в 6 глазах, 33,3% в среднем на 52±6,3°) поля зрения в 1 группе в 94,4% случаев (всего в 17 глазах), тогда как во 2 группе - в 86,7% (в 13) и в 3 группе - в 85,7% (в 12) были зафиксирована только его сохранность на дооперационном уровне. В остальных же случаях было диагностировано прогрессирование глаукомы.
Таким образом, предлагаемый способ нормализует ВГД у больных глаукомой с помощью создания новых путей оттока, в частности улучшения увеосклерального пути оттока, для предупреждения рубцевания в зоне хирургического вмешательства, а также для повышения зрительных функций. В частности, операция по предлагаемому способу в изученные отдаленные сроки обеспечила более высокий и стабильный абсолютный (в 83,3% случаев) и общий (в 94,4%) гипотензивный эффект в сравнении со способом-прототипом (60,0% и 86,7% соответственно). Отсутствие гипотензивного результата после выполнения предлагаемой операции (5,6%) было в 2,4 раза реже, чем по способу-прототипу, после которого в 13,3% случаев с целью нормализации офтальмотонуса были проведены реоперации с дренажом. Послеоперационный анализ также показал, что в отдаленные изученные сроки предлагаемый способ оказался эффективным у всех 3 пациентов с начальной стадией глаукомы. В развитой стадии абсолютный (без дополнительной терапии) результат оказался равен 87,5% (у 7 из 8 пациентов), но с использованием местной медикаментозной коррекции (еще у 1 пациента) эффект оказался 100%. В далекозашедшей стадии заболевания гипотензивный эффект оказался также достаточно высоким – 85,7% (у 6 из 7). Что же касается результативности предлагаемого способа в зависимости от формы первичной глаукомы, то при ПОУГ абсолютный гипотензивный эффект был зафиксирован в 75,0% случаев (в 6 из 8) и относительный (с медикаментозной нагрузкой) – в 25% (в 2 случаях), т.е. в целом в 100% случаев. При смешанной форме первичной глаукомы абсолютный эффект получен в 66,7% случаев (в 2 из 3 случаев), относительный – в 33,3% (в 1 случае), таким образом общий – в 100% случаев. При ПЗУГ эффективность предлагаемого способа составила 85,7% (в 6 из 7). Выше, чем при использовании способа-прототипа, оказалась также сохранность зрительных функций: остроты и особенно поля зрения – соответственно в 88,9% и 94,4% против 86,7%. Вместе с тем, полученный в отдаленные сроки абсолютный и общий гипотензивный результат предлагаемого способа хирургического вмешательства был практически такой же высокий, как после наиболее радикальной из сравниваемых антиглаукомных операций и обладающей фистулизирующим эффектом – трабекулэктомии: соответственно 85,7% и 92,8%. При этом, однако, относительные показатели сохранности остроты зрения (78,5%) в отдаленные сроки после трабекулэктомии оказались значительно хуже вследствие более частого прогрессирования катаракты. Сущность изобретения поясняется следующими клиническими примерами.
Клинический пример 1.
Пациент Ж., 55 лет. Диагноз: Первичная открытоугольная глаукома, II «c» стадия левого глаза. 5 лет назад установлена глаукома, закапывает в левый глаз фиксирующую комбинацию латанопрост+тимолол 1 раз в сутки и бримонидин 0,005% 1 раз в день. В анамнезе операций не было. Острота зрения левого глаза - 0,5; ВГД, измеренное пневмотонометром, составляет 28 мм рт.ст. на фоне местной гипотензивной терапии. Гониоскопически угол передней камеры левого глаза открыт, 2-3 ст, пигментация III. При осмотре: глаз спокоен, роговица прозрачная, передняя камера средней глубины, единичные псевдоэксфолиации на капсулы хрусталика, который прозрачный. Глазное дно: диск зрительного нерва бледный, экскавация 0,8 диаметра диска зрительного нерва (ДЗН). Поле зрения: сужение поля зрения левого глаза с верхней и нижненосовой стороны до 35°.
Пациенту выполнена антиглаукомная операция по предлагаемому способу. Отступя от лимба на 5,5 мм выполнили разрез конъюнктивы длиной 6мм, осуществили гемостаз. Затем выкроили поверхностный склеральный лоскут трапециевидной формы длиной лимбальной части 8 мм, склеральной - 6 мм и шириной 5 мм. Из средних слоев склеры выкроили лоскут тоже трапециевидной формы основанием к лимбу до обнажения трабекулы и периферической части десцеметовой оболочки на 2 мм. Затем из лоскута средних слоев склеры посредством двух разрезов параллельных его краям и перпендикулярно его основанию сформировали три полоски склеры: ширина крайних полосок склеры – 1,5 мм, средней в проксимальной к лимбу части – 5 мм, в дистальной – 3 мм. Затем в 2 мм от лимба на протяжении склерального ложа произвели сквозной и параллельный лимбу разрез до цилиарного тела длиной 7 мм, из которого выполнили передний циклодиализ. Его выполнение сопровождалось истечением небольшой порции влаги из передней камеры, которая при этом полностью не опорожнилась. Следующим этапом крайние полоски склеры поочередно с помощью шпателя имплантировали в УПК. Далее у основания центральной полоски произвели сквозной разрез трабекулярной ткани длиной 2,5 мм, через который выполнили базальную иридэктомию. Затем через разрез глубоких слоев склеры в области ложа и после предварительного заднего (в сторону свода) циклодиализа, в супрахориоидальное пространство имплантировали биоматериал серии «Аллоплант» для реваскуляризации зрительного нерва, размером 6х5 мм, а затем поверх него – оставшуюся полоску из средних слоев склеры. Поверхностный склеральный лоскут уложили на свое место и фиксировали двумя узловыми швами, конъюнктивальный разрез - непрерывным швом. Операция и послеоперационный период прошли без осложнений. В отдаленные сроки наблюдения за пациентом (максимальный срок – 1,5 года) зафиксирована разлитая фильтрационная подушка, острота зрения – 0,5, ВГД (бесконтактный тонометр) - 14 мм рт.ст. (варианты: от 13 до 17 мм рт.ст.) без применения каких-либо гипотензивных препаратов. Глаз спокоен, среды прозрачные, глазное дно - ДЗН бледный, экскавация 0,7-0,8 диаметра ДЗН. Границы поля зрения, измеренные по 8 меридианам, стабильны в сравнении с дооперационными.
Клинический пример 2.
Пациентка Ю., 69 лет. Диагноз: Первичная закрытоугольная глаукома III «в» стадии правого глаза. Больной себя считает около 7 лет, когда впервые ее был выставлен диагноз ПЗУГ 1-2 ст. В настоящее время она закапывает в правый глаз дорзоламид 2 раза в день и пилокарпин 1 раз в день. В анамнезе – лазериридэктомия (однократно), ножевых операций не было. ПЗО – 22,5 мм. Острота зрения правого глаза - 0,2-0,3; ВГД - 29 мм рт.ст. Гониоскопия - угол передней камеры практически закрыт, но не всем протяжении, пигментация 3, единичные гониосинехии. Роговица прозрачная, передняя камера средней глубины, на дистрофично измененной радужке на 6 ч. не функционирующая колобома, начальные помутнения в ядерных слоях хрусталика. Глазное дно: диск зрительного нерва серовотого цвета, экскавация 0,9 диаметра ДЗН. Практически концентрическое сужение поля зрения правого глаза до 15-35°. Пациентке произвели операцию по предлагаемому способу. Отступя от лимба на 5,5 мм выполнили разрез конъюнктивы длиной 6мм, осуществили гемостаз. Затем выкроили поверхностный склеральный лоскут трапециевидной формы длиной лимбальной части 8 мм, склеральной - 6 мм и шириной 5 мм. Из средних слоев склеры выкроили лоскут тоже трапециевидной формы основанием к лимбу до обнажения трабекулы и периферической части десцеметовой оболочки на 1 мм. Затем из лоскута средних слоев склеры посредством двух разрезов параллельных его краям и перпендикулярно его основанию сформировали три полоски склеры: ширина крайних полосок склеры – 1,5 мм, центральной в проксимальной части – 5 мм, в дистальной – 3 мм. Потом в 2 мм от лимба на протяжении склерального ложа произвели сквозной и параллельный лимбу разрез до цилиарного тела длиной 7 мм, из которого выполнили передний циклодиализ. Затем крайние полоски склеры через сквозной разрез склеры в области ложа поочередно с помощью шпателя имплантировали в УПК. Далее у основания центральной полоски произвели сквозной разрез трабекулярной ткани длиной 2 мм и произвели периферическую иридэктомию. Далее в супрахориоидальное пространство через разрез склерального ложа имплантировали биматериал серии «Аллоплант» для реваскуляризации зрительного нерва, размером 6х5 мм, а поверх него – оставшуюся полоску из средних слоев склеры. Склеральный лоскут зафиксировали двумя узловыми шелковыми швами (8/0), а на конъюнктивальный разрез был наложен непрерывный шов. В послеоперационном периоде не отмечалось развития каких-либо осложнений. За весь период наблюдения до 14 месяцев имела место разлитая фильтрационная подушка, стабильные острота (0,2) и поле зрения, которое после операции стало даже несколько шире (15-20-45°), о чем свидетельствовало стабильное состояние ДЗН. ВГД при измерении бесконтактным тонометром варьировало от 12 до 15 мм рт.ст.
Клинический пример 3.
Пациентка З., 75 лет. Диагноз: Первичная смешанноугольная глаукома II «в» стадии левого глаза. Больной себя считает около 10 лет, когда впервые ее был выставлен диагноз ПСУГ 1-2 ст. В настоящее время она закапывает в правый глаз дорзоламид 2 раза в день и прилокарпин 1 раз в день. Острота зрения левого глаза - 0,3; ВГД - 31 мм рт.ст. Гониоскопия - угол передней камеры прикрыт на всем протяжении, пигментация 3. Роговица прозрачная, передняя камера средней глубины, начальные помутнения в ядерных слоях хрусталика. Глазное дно: диск зрительного нерва бледный, экскавация 0,7 диаметра ДЗН. Сужение поля зрения левого глаза до 45°. Пациентке произвели операцию по предлагаемому способу. Отступя от лимба на 5,5 мм выполнили разрез конъюнктивы длиной 6мм, осуществили гемостаз. Затем выкроили поверхностный склеральный лоскут трапециевидной формы длиной лимбальной части 8 мм, склеральной - 6 мм и шириной 5 мм. Из средних слоев склеры выкроили лоскут тоже трапециевидной формы основанием к лимбу до обнажения трабекулы и периферической части десцеметовой оболочки на 1 мм. Затем из лоскута средних слоев склеры посредством двух разрезов параллельных его краям и перпендикулярно его основанию сформировали три полоски склеры: ширина крайних полосок склеры – 1,5 мм, центральной в проксимальной части – 5 мм, в дистальной – 3 мм. Потом в 2 мм от лимба на протяжении склерального ложа произвели сквозной и параллельный лимбу разрез до цилиарного тела длиной 7 мм, из которого выполнили передний циклодиализ. Затем крайние полоски склеры через сквозной разрез склеры в области ложа поочередно с помощью шпателя имплантировали в УПК. Далее у основания центральной полоски произвели сквозной разрез трабекулярной ткани длиной 2 мм и произвели периферическую иридэктомию. Далее в супрахориоидальное пространство через разрез склерального ложа имплантировали биматериал серии «Аллоплант» для реваскуляризации зрительного нерва, размером 6х5 мм, а поверх него – оставшуюся полоску из средних слоев склеры. Склеральный лоскут зафиксировали двумя узловыми шелковыми швами (8/0), а на конъюнктивальный разрез был наложен непрерывный шов. В послеоперационном периоде не отмечалось развития каких-либо осложнений. За весь период наблюдения до 14 месяцев имела место разлитая фильтрационная подушка, стабильные острота (0,3) и поле зрения, которое после операции стало шире (55°), о чем свидетельствовало стабильное состояние ДЗН. ВГД при измерении бесконтактным тонометром варьировало от 11 до 17 мм рт.ст.
Таким образом, предлагаемый способ нормализует ВГД у больных глаукомой с помощью создания новых путей оттока, в частности улучшения увеосклерального пути оттока, для предупреждения рубцевания в зоне хирургического вмешательства, а также для повышения зрительных функций. Он обеспечивает более высокий и устойчивый гипотензивный эффект, чем хирургическое вмешательство по способу-прототипу. Предлагаемый способ обеспечивает повышение гипотензивного эффекта вследствие частичной фистулизации и активации увеосклерального оттока, что обусловлено элементом дилатации супрахориоидального пространства и комбинированным стойким умеренным оттоком ВГЖ через вскрытую трабекулу и периферическую часть десцеметовой мембраны, циклодиализную щель вдоль аутосклеральных имплантатов под склеральный лоскут и далее в субтеноново пространство. Кроме того, предлагаемый способ предусматривает устранение резкого перепада ВГД за счет проведения переднего циклодиализа, что уменьшает вероятность развития осложнений, в частности, отслойки сосудистой оболочки, и обеспечивает профилактику склеро-склеральных сращений из-за удаления глубоких слоев склеры. Все это создает условия для формирования более надежных путей оттока, снижая вероятность рубцевания в области фильтрации. При этом предлагаемый способ лечения сравним с прототипом по числу осложнений (19,1% в сравнении с 22,3%), что очень важно. Минимальное число таких осложнений, как отслойка сосудистой оболочки и гифема и введение аутосклеры и аллотрансплантата в супрахориоидальное пространство при выполнении предлагаемого способа способствует сохранению зрительных функций у большего числа больных, особенно остроты зрения (88,9%) в связи с более низким катарактогенным эффектом, чем у трабекулэктомии (78,5%).
Использование аутоматериала по технологии предлагаемой антиглаукомной операции не требует дополнительных материальных затрат на специальное техническое оснащение, донорский материал и, связанные с ним юридическо-правовые проблемы. Выполнение предлагаемого способа рекомендуется при I-III стадиях первичной открытоугольной, смешанной и закрытоугольной (узкоугольной) глаукоме независимо от формы ретенции и уровня ВГД.
Таким образом, предлагаемая операция - непроникающая глубокая склерэктомия с трабекулотомией, усиленная бигониоциклоретракцией, увеосклеральной дилатацией и введением аутосклеры и аллотрансплантата в супрахориоидальное пространство, позволяет добиться стойкого гипотензивного эффекта и улучшения состояния зрительных функций у больных с начальной, развитой и далекозашедшей стадиями первичной открытоугольной, закрытоугольной и смешанной глауком.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ лечения первичной открытоугольной глаукомы | 2019 |
|
RU2735378C1 |
| Способ лечения первичной открытоугольной глаукомы | 2023 |
|
RU2815951C1 |
| Комбинированный способ активации различных механизмов оттока внутриглазной жидкости при глаукоме | 2021 |
|
RU2766730C1 |
| Способ активации основных и дополнительных путей оттока внутриглазной жидкости при глаукоме | 2024 |
|
RU2833766C1 |
| Хирургический способ одномоментной активации путей оттока внутриглазной жидкости при глаукоме | 2021 |
|
RU2782126C1 |
| СПОСОБ ЛЕЧЕНИЯ ЗАКРЫТОУГОЛЬНОЙ ГЛАУКОМЫ | 1995 |
|
RU2121325C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ПСЕВДОЭКСФОЛИАТИВНОЙ ГЛАУКОМЫ | 2015 |
|
RU2576782C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ГЛАУКОМЫ ПУТЕМ РЕЗЕКЦИИ СКЛЕРЫ | 2015 |
|
RU2587856C1 |
| Способ активации увеосклерального пути оттока внутриглазной жидкости | 2018 |
|
RU2712640C1 |
| Способ хирургического лечения открытоугольной глаукомы | 2024 |
|
RU2840207C1 |
Изобретение относится к медицине, а именно к офтальмологии. Проводят непроникающую глубокую склерэктомию и трабекулотомию с формированием конъюнктивального разреза и поверхностного склерального лоскута. Отсепаровывают поверхностный склеральный лоскут на 1/3 толщины склеры трапециевидной формы длиной лимбальной части 8 мм, склеральной - 6 мм и шириной 5 мм. Из средних слоев склеры выкраивают лоскут трапециевидной формы основанием к лимбу до обнажения трабекулы и периферической части десцеметовой оболочки на 1–2 мм. Затем из лоскута средних слоев склеры посредством двух разрезов, параллельных его краям и перпендикулярно его основанию формируют три полоски склеры, ширина крайних полосок склеры 1,5 мм, ширина центральной полоски в проксимальной к лимбу части 5 мм, в дистальной – 3 мм. Далее в 2 мм от лимба на протяжении склерального ложа производят сквозной параллельный лимбу разрез до цилиарного тела длиной 7 мм, из которого выполняют передний циклодиализ. Крайние полоски склеры поочередно имплантируют в угол передней камеры, у основания центральной полоски производят сквозной разрез трабекулы длиной 2-2,5 мм, через который выполняют базальную иридэктомию. Через разрез глубоких слоев склеры в области ложа и после предварительного заднего циклодиализа в супрахориоидальное пространство имплантируют биоматериал «Аллоплант» для реваскуляризации зрительного нерва шириной по лимбу 6 мм длиной 5 мм, а затем поверх него оставшуюся центральную полоску из средних слоев склеры. Способ позволяет добиться стойкого гипотензивного эффекта и улучшения состояния зрительных функций у больных с начальной, развитой и далекозашедшей стадиями первичной открытоугольной, закрытоугольной и смешанной глауком. 5 ил., 3 пр.
Способ хирургического лечения первичной глаукомы, включающий проведение непроникающей глубокой склерэктомии и трабекулотомии с формированием конъюнктивального разреза и поверхностного склерального лоскута, отличающийся тем, что отсепаровывают поверхностный склеральный лоскут на 1/3 толщины склеры трапециевидной формы длиной лимбальной части 8 мм, склеральной - 6 мм и шириной 5 мм, из средних слоев склеры выкраивают лоскут трапециевидной формы основанием к лимбу до обнажения трабекулы и периферической части десцеметовой оболочки на 1–2 мм, затем из лоскута средних слоев склеры посредством двух разрезов, параллельных его краям и перпендикулярно его основанию формируют три полоски склеры, ширина крайних полосок склеры 1,5 мм, ширина центральной полоски в проксимальной к лимбу части 5 мм, в дистальной – 3 мм; затем в 2 мм от лимба на протяжении склерального ложа производят сквозной параллельный лимбу разрез до цилиарного тела длиной 7 мм, из которого выполняют передний циклодиализ; крайние полоски склеры поочередно имплантируют в угол передней камеры, у основания центральной полоски производят сквозной разрез трабекулы длиной 2-2,5 мм, через который выполняют базальную иридэктомию; через разрез глубоких слоев склеры в области ложа и после предварительного заднего циклодиализа в супрахориоидальное пространство имплантируют биоматериал «Аллоплант» для реваскуляризации зрительного нерва шириной по лимбу 6 мм длиной 5 мм, а затем поверх него оставшуюся центральную полоску из средних слоев склеры.
| Булгар С.Н | |||
| и др | |||
| Сравнительные результаты операций нефистулизирующего типа при лечении первичной открытоугольной глаукомы | |||
| Казанский медицинский журнал | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Способ минимизации индуцированных оптических аберраций при хирургическом лечении глаукомы | 2019 |
|
RU2723608C1 |
| ПРИСПОСОБЛЕНИЕ К КРУЖЕВНОЙ МАШИНЕ ДЛЯ РЕЗКИ КРУЖЕВ ТРЕБУЕМОЙ ШИРИНЫ | 1929 |
|
SU13653A1 |
| Способ хирургического лечения первичной закрытоугольной глаукомы с функциональной блокадой угла передней камеры | 2019 |
|
RU2704476C1 |
| Бикбов М.М | |||
| и др | |||
| Клиническая оценка различных методик глубокой склерэктомии в лечении | |||
Авторы
Даты
2025-03-17—Публикация
2024-09-17—Подача