Изобретение относится к офтальмологии и может быть использовано при хирургическом лечении первичной открытоугольной глаукомы (ПОУГ).
Известен способ лечения ПОУГ посредством проведения проникающей операции фистулизирующего типа - трабекулэктомии [Cairns J.F. Trabeculectomy. Am. J. Ophthalmol., 1968; 60:673-678]. Однако данная фистулизирующая операция, обладая достаточно высоким гипотензивным эффектом, сопровождается и большим числом осложнений (в раннем периоде - это отслойка сосудистой оболочки, гифема, синдром мелкой передней камеры и др., в позднем - развитие и прогрессирование катаракты и др.), которые негативно отражаются на гипотензивных и функциональных результатах хирургического вмешательства.
Известен также способ лечения открытоугольной глаукомы в виде проведения непроникающей антиглаукомной операции - непроникающей глубокой склерэктомии [С.Н. Федоров, В.И. Козлов, Н.Т. Тимошкина и др. Непроникающая глубокая склерэктомия при открытоугольной глаукоме. Офтальмохирургия. 1989; 3-4:52-55], заключающийся в выкраивании конъюнктивального и поверхностного склерального лоскутов с последующим формированием и удалением участка наружной стенки шлеммова канала и участка глубоких слоев склеры над цилиарным телом с сохранением отдельных волокон склеры на поверхности последнего. Однако существенным недостатком непроникающей глубокой склерэктомии (НГСЭ) является кратковременность гипотензивного эффекта с повышением внутриглазного давления (ВГД). Причинами неэффективности НГСЭ являются избыточное рубцевание в зоне операции, несостоятельность трабекулы, нарушение дренирующей функции трабекуло-десцеметовой мембраны. Кроме того, для обеспечения гипотензивного эффекта НГСЭ в большинстве случаев требуется своевременное проведение дополнительного лазерного лечения - десцеметогониопунктуры, которая является обязательной при выполнении данной операции в микроинвазивном варианте.
Наиболее близким аналогом предлагаемого изобретения является способ хирургического лечения открытоугольной глаукомы, включающий НГСЭ и передний циклодиализ [Бабушкин А.Э, Рахматуллин А.Л. Непроникающая глубокая склерэктомия с циклодиализом в лечении открытоугольной глаукомы. Сб. науч. тр. «Актуальные проблемы офтальмологии». Уфа, 1999: 180-183]. Операция осуществляется следующим образом. После формирования традиционного конъюнктивального лоскута выкраивают поверхностный склеральный лоскут 5×5 или 6×6 мм, толщиной в 1/3 склеры и на 1,5 мм с заходом в прозрачные слои роговицы в пределах лимба. Удаляют глубокую пластинку склеры над цилиарным телом (оставляя только очень тонкий слой склеры над ним) вместе с наружной стенкой шлеммова канала и стромой роговицы с обнажением периферической части десцеметовой оболочки. Затем в 2-2,5 мм от лимба и параллельно ему производят разрез склеры до цилиарного тела в пределах склерального ложа. Из образованной раны выполняют передний циклодиализ, сопровождающийся истечением небольшой порции камерной влаги. Верхушку склерального лоскута после предварительного заднего циклодиализа имплантируют и, таким образом, фиксируют в супраувеальном пространстве в направлении свода с образованием склерального валика. Конъюнктиву ушивают непрерывным швом. Однако гипотензивный эффект данной частично фистулизирующей операции ограничен тем, что в ряде случаев в течение 3-6 месяцев происходит рубцевание циклодиализной щели и рецидив повышения офтальмотонуса вследствие нарушения фистулизации камерной влаги из передней камеры. При этом, как показала ревизия зоны первичной операции, в некоторых случаях обнаруживается дислокация верхушки поверхностного склерального лоскута из супрахориоидального пространства (куда она была заправлена) на склеральное ложе.
Задачей изобретения является повышение и пролонгирование гипотензивного эффекта антиглаукомной операции для лечения первичной открытоугольной глаукомы.
Технический результат при использовании изобретения - улучшение функциональных результатов за счет компенсации внутриглазного давления, длительного сохранения нормализации офтальмотонуса и уменьшения числа послеоперационных осложнений.
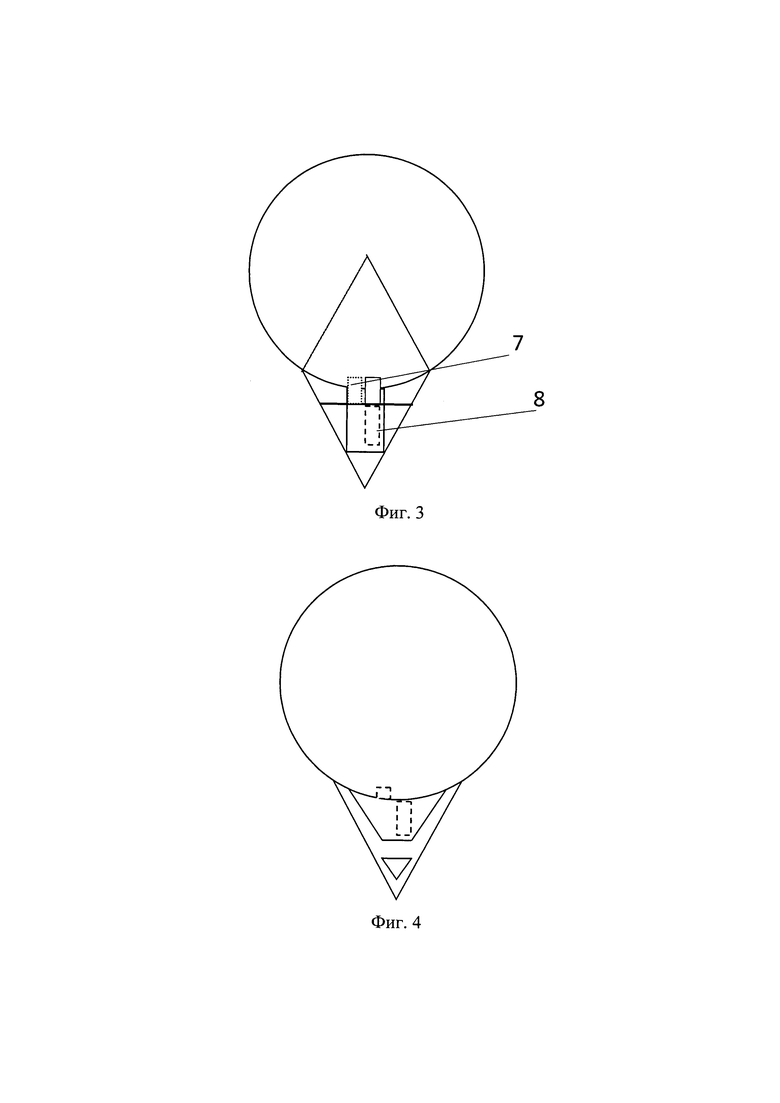
Изобретение иллюстрируется фигурами 1-4, на которых схематично изображены этапы предлагаемого способа, где: 1 - поверхностный склеральный лоскут, 2 - глубокий лоскут склеры прямоугольной формы, 3 - трабекуло-десцеметовая мембрана, 4 - ложе глубокого лоскута склеры, 5 - разрез глубокого лоскута склеры с формированием двух полосок, 6 - разрез склеры до цилиарного тела, 7 - полоска склеры, имплантированная через циклодиализную щель в переднюю камеру, 8 - полоска склеры, имплантированная в супрахориоидальное пространство.
Предлагаемый способ хирургического лечения первичной открытоугольной глаукомы осуществляется следующим образом. После формирования Г-образного конъюнктивального лоскута выкраивают поверхностный склеральный лоскут треугольной формы основанием 4,0 мм, высотой 5-5,5 мм и толщиной в 1/3 склеры с заходом до 1,5 мм в прозрачные слои роговицы. Под ним формируют глубокий лоскут склеры, прямоугольной формы над цилиарным телом, оставляя только очень тонкий слой склеры над ним, вместе с наружной стенкой шлеммова канала и стромой роговицы с обнажением периферической части десцеметовой оболочки (фиг. 1). Затем в 2 мм от лимба и параллельно ему производят разрез склеры до цилиарного тела в пределах склерального ложа. Из образованной раны на всю ее длину выполняют передний циклодиализ, сопровождающийся, как правило, истечением небольшой порции камерной влаги. Из сформированного ранее глубокого лоскута склеры путем разреза до основания (фиг. 2) формируют две полоски, одну из которых с помощью микрошпателя заправляют в переднюю камеру, а другую, после предварительного заднего циклодиализа, имплантируют через циклодиализную щель в супрахориоидальное пространство по направлению к своду (фиг. 3). Затем в 3,5 и 4,5 мм от лимба и параллельно ему на протяжении склерального ложа производят еще два сквозных разреза склеры до супраувеального пространства. В эти разрезы с помощью микрошпателя по направлению к экватору (своду) заправляют верхушку склерального лоскута, где и укрепляют посредством защемления (фиг. 4). Конъюнктиву герметизируют двумя узловыми швами.
Для объективной оценки предлагаемого способа было обследовано 49 пациентов (59 глаз) в возрасте от 56 до 77 лет, из них мужчин - 22, женщин - 27. Было сформированы 3 группы больных. Первая группа - 15 пациентов (17 глаз), которым выполнена частично фистулизирующая операция предлагаемым способом. Во второй группе (16 пациентов, 19 глаз) больным проведена антиглаукомная операция по способу-прототипу. В третьей группе (18 пациентов, 23 глаз) больным выполнена фистулизирующая операция - трабекулэктомия.
Основную долю составили пациенты с развитой стадией глаукомы: 54,5% (9 глаз) в первой группе, 58,4% (11 глаз) - во второй группе и 56,6% (13 глаз) в третьей группе. Пациенты с начальной стадией глаукомы составили: 21,3% в первой группе (4 глаза), 19,7% (4 глаза) - во второй и 22,3% (5 глаз) - в третьей. Далекозашедшая глаукома, по данным обследования, диагностирована на 4 глазах в первой (24,2%) и второй (21,9%) групп и на 5 глазах (21,1%) в третьей группе. Умеренный уровень ВГД в 1 группе зафиксирован в 65,9%, во 2 группе - 68,2%, в 3 группе - 68,3%, высокий 34,1%, 31,8%, 31,7% соответственно. Следует отметить, что сравниваемые группы были сопоставимы по полу, возрасту, стадиям заболевания и уровню ВГД. Максимальный срок наблюдения за пациентами составил 2 года 1 месяц (в среднем 19 месяцев).
Из ранних послеоперационных осложнений в сравниваемых группах чаще всего наблюдали: гифему, цилиохориоидальную отслойку (ЦХО) и синдром мелкой передней камеры. Цилиохориоидальная отслойка сетчатки была отмечена по одному случаю в первой (5,9%) и во второй (5,3%) группах и в 3 (13%) глазах в третьей группе. При этом выпускание субхориоидальной жидкости потребовалось в двух из трех случаев ЦХО после выполнения трабекулэктомии. В первой и второй группах ЦХО была купирована медикаментозно.
Гипотензивный эффект после антиглаукомных операций при выписке пациентов из стационара в сравниваемых группах был достигнут у всех больных. Однако, в ранние сроки (до 3 месяцев) во 2 группе в одном случае для нормализации офтальмотонуса потребовалось назначение местных гипотензивных средств (тимолол + латанопрост). В отдаленные сроки было осмотрено 42 больных (51 глаз). Абсолютный гипотензивный эффект в 1 группе был достигнут в 71,4% (в 10 глазах из 14) случаев, во 2 группе - в 66,7% (в 10 глазах из 15) и в 3 группе - в 72,7% (в 16 глазах из 22).
Относительный (с применением дополнительной гипотензивной терапии с 1 или 2 препаратами) гипотензивный эффект в 1 группе получен в 21,4% случаев (в 3 глазах), во 2 группе - в 13,3% (в 2 глазах) и в 3 группе - 22,7% случаев (в 5 глазах).
Отсутствие эффекта в 1 группе отмечали в 7,1% (в 1 случае), во 2 группе - в 20,0% (в 3 глазах) и в 3 группе - в 4,5% (в 1 случае). В 1 и 3 группах рецидив повышения ВГД был компенсирован медикаментозно с помощью комбинированной гипотензивной терапии, во 2-й же группе в 2 (66,7%) глазах из 3 для нормализации офтальмотонуса пришлось прибегнуть к фистулизирующей реоперации с применением дренажа Глаутекс.
Острота зрения в отдаленные сроки наблюдения осталась на дооперационном уровне в 1 группе в 92,9% случаев (в 13 глазах из 14), во 2 группе - в 86,7% (в 13 глазах из 15) и в 3 группе - в 81,8% (в 18 глазах из 22). При этом в 2 случаях после перенесенной трабекулэктомии (3 группа) в связи с прогрессированием катаракты произвели ее факоэмульсификацию. Поле зрения, исследованное методом кинетической периметрии по 8 меридианам, оказалось стабильным в 1 группе в 13 глазах или в 92,9% случаев, во 2 группе в 12 глазах (в 80,0%) и в 3 группе - в 20 глазах (в 90,9%). В остальных случаях было отмечено прогрессирование заболевания.
Таким образом, операция по предлагаемому способу в изученные отдаленные сроки в сравнении со способом-прототипом обеспечила наибольший абсолютный (71,4%) и общий (92,8%) гипотензивный эффект, (против 66,7% и 80,0% соответственно), а также лучшую сохранность зрительных функций. При этом следует отметить, что неэффективность хирургического вмешательства после выполнения предлагаемой операции было зафиксировано в 2,8 раза реже, чем по способу-прототипу (7,1% против 20,0%). К тому же, после выполнения последнего в большинстве случаев (66,7%) для нормализации ВГД потребовалось проведение повторного хирургического вмешательства. Следует также указать, что полученный гипотензивный эффект в отдаленные сроки в результате частично фистулизирующей операции по предложенному способу (92,8%) оказался вполне сопоставимым с таковым после чисто фистулизирующей операции - трабекулэктомии (95,4%). При этом, катарактогенный эффект предложенной операции был отмечен реже, чем после трабекулэктомии.
Клинический пример 1.
Больной Д., 69 лет. Диагноз: первичная открытоугольная глаукома II «с» правого глаза, начальная катаракта. Глаукомой страдает 2 года, закапывает в правый глаз комбиган × 2 раза в день, а последние 5 месяцев еще и Траватан 0,004% × 1 раз в день. Наличие каких-либо глазных операций отрицает. Острота зрения правого глаза - 0,5 с корр. -0,75 Д=0,8; внутриглазное давление - 26 мм рт. ст. (на медикаментозном лечении). Отмечается сужение поля зрения левого глаза с верхне- и нижне-носовой стороны - до 35-40°. При биомикроскопии: роговица прозрачная, передняя камера средней глубины, начальные помутнения в кортикальных слоях хрусталика. Гониоскопия - угол передней камеры открыт, средней ширины, пигментация II ст. Глазное дно: диск зрительного нерва несколько деколорирован, экскавация плоская, отношение ее диаметра к диску (Э/Д) - 0,6-0,7.
Больному произведена операция по предлагаемому способу. В верхнем сегменте, после формирования Г-образного конъюнктивального лоскута выкраивали поверхностный склеральный лоскут треугольной формы основанием 4,0 мм, высотой 5-5,5 мм и толщиной в 1/3 склеры с заходом до 1,5 мм в прозрачные слои роговицы. Под ним формировали глубокий лоскут склеры, прямоугольной формы над цилиарным телом (оставляя только очень тонкий слой склеры над ним) вместе с наружной стенкой шлеммова канала и стромой роговицы с обнажением периферической части десцеметовой оболочки. Затем в 2 мм от лимба и параллельно ему производили разрез склеры до цилиарного тела, в пределах склерального ложа. Из образованной раны на всю ее длину выполняли передний циклодиализ, сопровождающийся, как правило, истечением небольшой порции камерной влаги. Из сформированного ранее глубокого лоскута склеры путем разреза до основания, формировали две полоски, одну из которых с помощью микрошпателя заправляли в переднюю камеру, а другую, после предварительного заднего циклодиализа, имплантировали через циклодиализную щель в супрахориоидальное пространство в направлении к своду. Затем в 3,5 и 4,5 мм от лимба и параллельно ему на протяжении склерального ложа производили еще два сквозных разреза склеры до супраувеального пространства. В эти разрезы с помощью микрошпателя по направлению к экватору заправляли верхушку склерального лоскута, где и укрепляли ее посредством защемления. Конъюнктиву герметизировали двумя узловыми швами.
Операция и послеоперационный период - без осложнений. При выписке острота зрения правого глаза - 0,7-0,8 н/к; внутриглазное давление - 13 мм рт. ст., в зоне операции сформировалась плоская фильтрационная подушка, швы состоятельные (сняты через неделю).
За весь период наблюдения в течение 25 месяцев отмечалось наличие плоско-разлитой фильтрационной подушки, острота зрения при последнем осмотре - 0,5-0,6 с корр. -1,0Д=0,8, ВГД, измеренное бесконтактным тонометром, составило 15 мм рт. ст. (без использования каких-либо медикаментов). Поле зрения по сумме градусов (СГПЗ) в восьми меридианах в сравнении исходным (до операции) не существенно даже расширилось. При проведении биомикроскопии роговица прозрачная, передняя камера средней глубины, начальные помутнения в кортикальных слоях хрусталика. Глазное дно: диск зрительного нерва несколько деколорирован, экскавация плоская, Э/Д - 0,6-0,7. Таким образом, данные ВГД, зрительных функций (остроты и поля зрения), а также состояния ДЗН свидетельствовали о стабилизации глаукомного процесса в результате хирургического лечения по предложенному способу.
Клинический пример 2.
Больная Ц., 72 лет. Диагноз: первичная открытоугольная глаукома III «с», начальная катаракта левого глаза. Глаукома установлена 4 года назад. В настоящее время закапывает в левый глаз арутимол 0,5%, дорзопт 2% × 2 раза в день и ксалатан 0,005% × 1 раз в день. В анамнезе операций не было. Острота зрения левого глаза - 0,3-0,4 не корригирует; внутриглазное давление - 28 мм рт. ст. на фоне гипотензивной терапии. Гониоскопия - угол передней камеры открыт, средней ширины, пигментация - III ст. При биомикроскопии: роговица прозрачная, передняя камера средней глубины, начальные помутнения в ядерных слоях хрусталика. Глазное дно: диск зрительного нерва сероватого цвета, сдвиг сосудистого пучка, экскавация глубокая, Э/Д - 0,8. Отмечалось сужение поля зрения левого глаза с верхне-носовой и верхней стороны до 15°.
Больной произведена операция по предлагаемому способу. В верхнем сегменте, после формирования Г-образного конъюнктивального лоскута выкраивали поверхностный склеральный лоскут треугольной формы основанием 4,0 мм, высотой 5-5,5 мм и толщиной в 1/3 склеры с заходом до 1,5 мм в прозрачные слои роговицы. Под ним формировали глубокий лоскут склеры, прямоугольной формы над цилиарным телом (оставляя только очень тонкий слой склеры над ним) вместе с наружной стенкой шлеммова канала и стромой роговицы с обнажением периферической части десцеметовой оболочки. Затем в 2 мм от лимба и параллельно ему производили разрез склеры до цилиарного тела, в пределах склерального ложа. Из образованной раны на всю ее длину выполняли передний циклодиализ, сопровождающийся, как правило, истечением небольшой порции камерной влаги. Из сформированного ранее глубокого лоскута склеры путем разреза до основания, формировали две полоски, одну из которых с помощью микрошпателя заправляли в переднюю камеру, а другую, после предварительного заднего циклодиализа, имплантировали через циклодиализную щель в супрахориоидальное пространство по направлению к своду. Затем в 3,5 и 4,5 мм от лимба и параллельно ему на протяжении склерального ложа производили еще два сквозных разреза склеры до супраувеального пространства. В эти разрезы с помощью микрошпателя по направлению к экватору заправляли верхушку склерального лоскута, где и укрепляли ее посредством защемления. Конъюнктиву герметизировали двумя узловыми швами.
Во время операции и в послеоперационном периоде не отмечалось развития каких-либо осложнений. При выписке через 4 дня оперированный глаз незначительно раздражен. На 12 ч. плоская, ограниченная фильтрационная подушка. Острота зрения 0,4-0,5 н/к, внутриглазное давление - 12 мм рт. ст. Через 5 дней глаз спокоен, были сняты швы с конъюнктивы.
При контроле через 2 года на оперированном глазу была отмечена разлитая фильтрационная подушка, острота зрения - 0,4 н/к, внутриглазное давление при бесконтактной тонометрии - 14 мм рт. ст. При биомикроскопии: роговица прозрачная, передняя камера средней глубины, начальные помутнения в хрусталике без признаков прогрессирования. Глазное дно: диск зрительного нерва сероватого цвета, сдвиг сосудистого пучка, экскавация глубокая, Э/Д - 0,8. По данным периметрии (СГПЗ) поле зрения, по сравнению с дооперационным, не изменилось, что свидетельствовало о стабилизации глаукомного процесса.
Таким образом, использование предлагаемого способа обеспечивает более высокий и устойчивый гипотензивный эффект, чем хирургическое вмешательство по способу-прототипу. Предлагаемый способ обеспечивает повышение гипотензивного эффекта вследствие частичной фистулизации и активации увеосклерального оттока, что обусловлено элементом аутосклеродренирования передней камеры, супрахориоидального пространства и дополнительным стойким умеренным оттоком ВГЖ через циклодиализную щель под склеральный лоскут и далее в субтеноново пространство. Кроме того, предлагаемый способ предусматривает устранение резкого перепада ВГД за счет проведения переднего циклодиализа (что уменьшает вероятность развития осложнений, в частности, отслойки сосудистой оболочки) и профилактику склеро-склеральных сращений из-за удаления глубоких слоев склеры и бесшовного укрепления поверхностного склерального лоскута. L-образное формирование конъюнктивального лоскута также создает условия для формирования более надежных путей оттока, снижая вероятность рубцевания непосредственно в области фильтрации. При этом предлагаемый способ лечения сравним с прототипом по числу осложнений, что очень важно. Технически предлагаемый способ выполняется проще, чем проникающая операция типа трабекулэктомии. В частности, в ней отсутствует элемент иссечения участка дренажной зоны склеры и укрепление послойного лоскута склеры швами. Минимальное число таких осложнений, как отслойка сосудистой оболочки и гифема при выполнении предлагаемого способа способствует сохранению зрительных функций у большего числа больных, в связи с более низким катарактогенным эффектом, чем у трабекулэктомии.
Использование аутоматериала при выполнении антиглаукомной операции по предлагаемому способу не требует специального технического оснащения, применения донорского материала, (что исключает проблему с юридическо-правовыми вопросами по его применению) и не требует дополнительных материальных затрат. Выполнение предлагаемого способа рекомендуется при I-III стадиях ПОУГ (в т.ч. при узкоугольной глаукоме) и небольшой степени ожидаемого послеоперационного рубцевания, независимо от формы ретенции и уровня ВГД.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ хирургического лечения первичной глаукомы | 2024 |
|
RU2836542C1 |
| Комбинированный способ активации различных механизмов оттока внутриглазной жидкости при глаукоме | 2021 |
|
RU2766730C1 |
| Способ лечения первичной открытоугольной глаукомы | 2023 |
|
RU2815951C1 |
| Способ активации основных и дополнительных путей оттока внутриглазной жидкости при глаукоме | 2024 |
|
RU2833766C1 |
| Хирургический способ одномоментной активации путей оттока внутриглазной жидкости при глаукоме | 2021 |
|
RU2782126C1 |
| СПОСОБ ЛЕЧЕНИЯ ГЛАУКОМЫ | 1996 |
|
RU2097010C1 |
| Способ активации увеосклерального пути оттока внутриглазной жидкости | 2018 |
|
RU2712640C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РЕФРАКТОРНЫХ ГЛАУКОМ | 2005 |
|
RU2297815C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ПЕРВИЧНОЙ ГЛАУКОМЫ | 2011 |
|
RU2456970C1 |
| Способ лечения открытоугольной глаукомы | 2024 |
|
RU2830376C1 |

Изобретение относится к медицине, а именно к офтальмологии. Осуществляют формирование конъюнктивального лоскута, поверхностного склерального лоскута треугольной формы и толщиной в 1/3 склеры с заходом до 1,5 мм в прозрачные слои роговицы, глубокого лоскута склеры прямоугольной формы над цилиарным телом вместе с наружной стенкой шлеммова канала и стромой роговицы с обнажением периферической части десцеметовой оболочки. Разрез склеры осуществляют до цилиарного тела в пределах склерального ложа в 2 мм от лимба и параллельно ему, передний циклодиализ из образованной раны на всю ее длину. Далее осуществляют фиксацию верхушки склерального лоскута, герметизацию конъюнктивы. Из сформированного глубокого лоскута склеры путем разреза до основания формируют две полоски, одну из которых заправляют в переднюю камеру, а другую после предварительного заднего циклодиализа имплантируют через циклодиализную щель в супрахориоидальное пространство по направлению к своду. Для фиксации верхушки склерального лоскута в 3,5 и 4,5 мм от лимба и параллельно ему на протяжении склерального ложа производят два сквозных разреза склеры до супраувеального пространства. В разрезы по направлению к экватору заправляют верхушку склерального лоскута. При этом поверхностный склеральный лоскут формируют основанием 4,0 мм, высотой 5-5,5 мм. Способ обеспечивает компенсацию внутриглазного давления, длительное сохранение нормализации офтальмотонуса при минимальном числе послеоперационных осложнений. 1 з.п. ф-лы, 2 пр., 4 ил.
1. Способ хирургического лечения открытоугольной глаукомы, включающий проведение непроникающей глубокой склерэктомии, предусматривающей формирование конъюнктивального лоскута, поверхностного склерального лоскута треугольной формы и толщиной в 1/3 склеры с заходом до 1,5 мм в прозрачные слои роговицы, глубокого лоскута склеры прямоугольной формы над цилиарным телом вместе с наружной стенкой шлеммова канала и стромой роговицы с обнажением периферической части десцеметовой оболочки; разрез склеры до цилиарного тела в пределах склерального ложа в 2 мм от лимба и параллельно ему, передний циклодиализ из образованной раны на всю ее длину, фиксацию верхушки склерального лоскута, герметизацию конъюнктивы, отличающийся тем, что из сформированного глубокого лоскута склеры путем разреза до основания формируют две полоски, одну из которых заправляют в переднюю камеру, а другую после предварительного заднего циклодиализа имплантируют через циклодиализную щель в супрахориоидальное пространство по направлению к своду, а для фиксации верхушки склерального лоскута в 3,5 и 4,5 мм от лимба и параллельно ему на протяжении склерального ложа производят два сквозных разреза склеры до супраувеального пространства, в разрезы по направлению к экватору заправляют верхушку склерального лоскута.
2. Способ по п. 1, отличающийся тем, что поверхностный склеральный лоскут формируют основанием 4,0 мм, высотой 5-5,5 мм.
| Хирургическое лечение глаукомы методом синустрабекулэктомии с базальной иридэктомией в сочетании с глубокой склерэктомией и активацией увеосклерального пути аутосклерой | 2017 |
|
RU2674088C1 |
| Комбинированный хирургический способ лечения глаукомы в сочетании с катарактой | 2016 |
|
RU2612525C1 |
| Приспособление для присоединения катодных ламп с баком охлаждения | 1929 |
|
SU12077A1 |
| Kammer J.A | |||
| et al | |||
| Suprachoroidal Devices in Glaucoma Surgery | |||
| Middle East Afr J Ophthalmol | |||
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| Мамиконян В.Р | |||
| и др | |||
| Циклодиализ в лечении глаукомы | |||
| История и современность | |||
| Национальный журнал глаукомы | |||
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| Бикбов М.М., и др | |||
Авторы
Даты
2020-10-30—Публикация
2019-12-16—Подача