Область техники, к которой относится изобретение
Изобретение относится к медицине, а именно к травматологии и ортопедии, и может быть использовано для профилактики осложнений у пациентов после проведения артроскопических операций на коленном суставе с использованием аутологичных тромбоцитов, активированных с помощью низкоимпульсного лазерного излучения. Способ может быть использован при лечении пациентов с артроскопическими операциями, проводимыми по поводу разрыва передней крестообразной связки, разрыва наружного и/или внутреннего мениска, наличия хондромаляций и гонартроза и др. Способ позволяет добиться ускорения резорбции отека и гематомы, купирования болевого синдрома, стимулирования регенерации тканей.
Уровень техники
В настоящее время артроскопия является основным методом диагностики и лечения внутрисуставных повреждений коленного сустава и их последствий. После проведения артроскопических операций на коленном суставе в послеоперационный период часто отмечаются такие осложнения, как синовит, гемартроз, параартикулярный отёк и болевой синдром [Павлов А.И., Щегольков А.М., Сидоркин Д.Н. Современная программа медицинской реабилитации больных, перенесших артроскопические операции на коленном суставе, включающая применение высокоинтенсивной лазерной терапии // Госпитальная медицина: наука и практика. 2021. Т. 4. №2. С. 31-39]. В связи с этим ведется активный поиск и разработка инъекционных биологических препаратов, стимулирующих репаративные процессы в коленном суставе. Большую популярность приобретает использование препаратов на основе аутологичной богатой тромбоцитами плазмы (БоТП). Тем не менее, в настоящее время методики лечения дефектов коленного сустава с использованием БоТП не стандартизированы [Filardo G, Previtali D, Napoli F, Candrian C, Zaffagnini S, Grassi A. PRP Injections for the Treatment of Knee Osteoarthritis: A Meta-Analysis of Randomized Controlled Trials. Cartilage. 2021 Dec;13(1_suppl):364S-375S]. Тромбоциты человека являются высокореактивными и легко повреждающимися клетками, поэтому очень важной является оптимизация методики подготовки тромбоцитов к клиническому использованию. Показано, что при лечении дефектов опорно-двигательного аппарата предварительная активация тромбоцитов усиливает клинический эффект препаратов на основе БоТП. В процессе активации тромбоциты не только участвуют в свертывании крови, но и реализуют свой репаративный и регенеративный потенциал, выделяют большое количество биологически активных веществ [Nurden A.T., Nurden P., Sanchez M. Platelets and wound healing // Frontiers in Bioscience. - 2008. - Vol. 13, №9. - P. 3532-3548]. Этот эффект используется при производстве лекарственных препаратов на основе активированной богатой тромбоцитами плазмы (БоТП). При этом в ряде случаев для активации тромбоцитов не рекомендуется использовать индукторы, широкодоступные в клинической практике (хлорид кальция, перекись водорода). Препараты, полученные путем криодеструкции (заморозки) БоТП, могут вызывать значительный болевой эффект при инъекционном введении [Kubrova E., Martinez Alvarez G.A., Her Y.F., Pagan-Rosado R., Qu W., D'Souza R.S. Platelet Rich Plasma and Platelet-Related Products in the Treatment of Radiculopathy-A Systematic Review of the Literature. Biomedicines. 2022; 10(11): 2813]. Возникает необходимость активации тромбоцитов в закрытой емкости без внесения дополнительных химических агентов и без выраженного повреждения тромбоцитов.
Для получения препаратов на основе БоТП с активированными тромбоцитами представляется перспективным использование низкоимпульсного лазерного излучения (НИЛИ). Под действием НИЛИ в видимом и инфракрасном диапазоне увеличивается пролиферативная активность клеток, ангиогенез, секреция ростовых факторов и антиоксидантов [Москвин С.В., Шаяхметова Т.А. Лазерная терапия в педиатрии, особенности и схемы применения метода (обзор литературы) // Вестник новых медицинских технологий. Электронное издание. 2018. № 6. С. 136-147]. Эффект фотобиостимуляции клеток под действием НИЛИ в значительной степени обусловлен активацией систем внутриклеточного сигналинга без прямого участия поверхностных рецепторов или других индукторов клеточной активации [Taradaj J., Shay B., Dymarek R., Sopel M., Walewicz K., Beeckman D., Schoonhoven L., Gefen A., Rosińczuk J. Effect of laser therapy on expression of angio- and fibrogenic factors, and cytokine concentrations during the healing process of human pressure ulcers // Int J Med Sci. 2018. Vol.15, N 11. P. 1105-1112]. Показано, что под действием НИЛИ в дальнем видимом диапазоне и инфракрасном спектре происходит выделение ростовых факторов в БоТП [Irmak G., Demirtaş T.T., Gümüşderelioğlu M. Sustained release of growth factors from photoactivated platelet rich plasma (PRP). Eur J Pharm Biopharm. 2020. 148:67-76], однако существенное влияние на процесс активации тромбоцитов оказывают параметры НИЛИ - мощность, длина волны и время воздействия.
Из уровня техники известен способ лечения дефектов хрящевой ткани коленного сустава с помощью аутологичной БоТП, активированной in vitro ультрафиолетовым светом на приборе Adi-Light 2 device J. [Freitag, A. Barnard, A. Rotstein Photoactivated platelet-rich plasma therapy for a traumatic knee chondral lesion // BMJ Case Rep. -2012. -Vol. 2012. -Р.bcr2012006858]. Однако данный способ не учитывает исходное качество тромбоцитов и морфофункциональный статус активированных клеток, возможное повреждение тромбоцитов и их компонентов под действием ультрафиолета, которые в совокупности влияют на эффективность проводимого лечения. Кроме того, в известном способе отсутствует схема введения полученного препарата, которая влияет на результат проводимого лечения.
Известен способ лечения пациентов с остеоартритом, включающий инъекционное введение фото-активированных тромбоцитов БоТП [Paterson K.L., Nicholls M., Bennell K.L., Bates D. Intra-articular injection of photo-activated platelet-rich plasma in patients with knee osteoarthritis: a double-blind, randomized controlled pilot study. BMC Musculoskelet Disord. 2016 Feb 9;17:67]. У пациента отбирают 48,5 мл венозной крови, центрифугируют при 2000 об/мин в течение 5 мин, отбирают плазму и повторно центрифугируют при 3000 об/мин в течение 3 мин для концентрирования тромбоцитов. После осаждения тромбоцитов удаляют 3/4 объема плазмы, вносят 0,2 мл бикарбоната натрия и ресуспендируют осадок тромбоцитов. Для фото-активации тромбоцитов пробирку с БоТП in vitro облучают ультрафиолетовым светом на приборе Adi-Light 2 device в течение 10 мин. Коленный сустав обрабатывают хлоргексидином и местно вводят анестетик ксилокаин, затем в область дефекта инъекционно вводят 3 мл активированной БоТП. Для оценки эффективности лечения используют модифицированную шкалу боли ВАШ (100 mm Visual Analogue Scale), также оценивают сгибательную активность конечности и общее качество жизни. Инъекции фото-активированной БоТП позволяли снизить болевые ощущения через 4 недели после введения, увеличить функциональную активность конечности, улучшить общее качество жизни. Через 12 недель эффект сохранялся, но был менее выраженным. Однако предложенный способ, содержащий этап активирования БоТП и схему его введения в дефект коленного сустава, направлен на лечение пациентов с остеоартритом, характеризующимся воспалением синовиальной оболочки сустава, вследствие которого разрушаются хрящевая и костная ткани. Выполнение артроскопических операций на коленных суставах сопряжено с развитием послеоперационного отека и воспаления, которые распространяются на окружающие мягкие ткани, сопровождаются замедленным процессом заживления и болевым эффектом, препятствуют восстановлению межклеточного матрикса. Купирование отека связано с нормализацией работы сосудистого русла в области тканевого дефекта, снижением про-воспалительной активности клеток крови, нормализацией биохимического состава ткани в области отека. Сухожилие человека имеет низкую плотность сосудов и поэтому неспособно купировать отеки близлежащих тканей. Кроме того, отек тканей после артроскопических операций может препятствовать нормальной интеграции сухожилия и его ремоделирования. Необходимо учитывать, что объем БоТП, вводимой при лечении остеоартритов, обусловлен необходимостью стимулировать пролиферацию большого числа клеток и одновременно с этим необходимостью восстановить объем хрящевой ткани. При остеоартрите и остеоартрозе хрящевая ткань теряет значительную часть воды и других растворимых компонентов межклеточного матрикса. Напротив, при артроскопических операциях хрящевая ткань сустава сохраняет нормальный биохимический состав, и ее дефекты связаны только с механическим повреждением. Таким образом, лечение дефектов хрящевой ткани с помощью фото-активированной БоТП, нельзя напрямую использовать при артроскопических операциях.
Таким образом, эффективность лечения при проведении артроскопической операции на коленных суставах и профилактики послеоперационных осложнений с использованием активированных БоТП зависит от многих факторов, в числе которых, качество вводимых тромбоцитов, их морфофункциональный статус после фото-активации БоТП без использования дополнительных химических веществ, схема введения БоТП, при этом количество вводимой БоТП зависит от размера интраоперционного и послеоперационного отека и гематомы коленного сустава, который может быть определен визуально и инструментально. Из уровня техники не известны способы лечения пациентов и профилактики осложнений после артроскопических операций на коленных суставах с использованием активированных БоТП, учитывающих совокупность перечисленных выше факторов, повышающих эффективность лечения.
Технической проблемой является разработка способа профилактики осложнений у пациентов после артроскопических операций на коленном суставе с использованием аутологичных тромбоцитов, активированных с помощью низкоимпульсного лазерного излучения in vitro без использования индукторов активации и дополнительных химических реагентов.
Раскрытие сущности изобретения
Техническим результатом, на достижение которого направлено заявленное изобретение, является разработка способа профилактики осложнений у пациентов после артроскопических операций на коленном суставе (в числе которых гемартроз, отек параартикулярных тканей), болевой эффект, за счет использования предварительно НИЛИ-активированной аутологичной БоТП, содержащей не менее 500 тыс. тромбоцитов с гранулами в 1 мкл до облучения БоТП in vitro и не менее 20% активированных (100 тыс. в 1 мкл) тромбоцитов с гранулами после облучения in vitro в БоТП в совокупности с предложенной схемой ее введения. Дозы БоТП, содержащие менее 500 тыс. тромбоцитов с гранулами до облучения и менее 20% активированных тромбоцитов с гранулами после облучения, имеют более низкую клиническую эффективность, снижают способность тромбоцитов БоТП купировать развития отека тканей после операции. Введение 3 мл и более полученной БоТП внутрисуставно и околосуставно после ушивания послеоперационных ран является показанным при критическом увеличении охвата конечности - более чем на 10% - в области коленного сустава, и/или голени, и/или бедра, по сравнению с указанными параметрами, измеренными до операции или на здоровой конечности.
Технический результат достигается способом профилактики осложнений у пациентов с артроскопическими операциями на коленном суставе с использованием аутологичных тромбоцитов, включающим забор венозной крови у пациента не менее чем за 2 часа до начала операции с получением из нее не менее 3 мл аутологичной богатой тромбоцитами плазмы (БоТП), содержащей не менее 500 тыс. тромбоцитов с гранулами в 1 мкл, облучение БоТП in vitro низкоимпульсным лазерным излучением (НИЛИ) с длиной волны 635-660 нм и мощностью 1-20 Вт в течение 10 мин для получения не менее 20% тромбоцитов с гранулами (не менее 100 тыс. в 1 мкл), с последующим введением полученной БоТП внутрисуставно и околосуставно после ушивания послеоперационных ран, при этом внутрисуставно через медиальный или латеральный порт вводят не менее 2 мл БоТП, околосуставно - не менее 1 мл БоТП, обкалывая прилегающие к суставу мягкие ткани. Медиальный или латеральный порт представляет собой разрез в колене длиной до 1 см, который наносится стандартным скальпелем для приближения непосредственно к тканям сустава. После окончания операции разрез (порт) зашивают стандартным медицинским швом, без применения дополнительных устройств или имплантов.
Аутологичная БоТП из венозной крови может быть получена путем ее двухэтапного центрифугирования: исходную кровь центрифугируют 5 минут с ускорением 300 g, отбирают супернатантную плазму с тромбоцитами и центрифугируют 17 минут с ускорением 700 g для осаждения и концентрирования тромбоцитов, из пробирки отбирают большую часть плазмы, бедной тромбоцитами, затем ресуспендируют осадок тромбоцитов в оставшемся объеме плазмы, в результате получают богатую тромбоцитами плазму (БоТП) с концентрацией клеток выше 1000 тыс/мкл (тромбоцитов с гранулами и без гранул).
БоТП вводят при помощи одноразового шприца Luer с инъекционной иглой 0,8х40 мм 21G.
Технический результат достигается путем выделения из 30-40 мл крови пациента не менее 3 мл аутологичной БоТП, содержащей не менее 500 тыс. тромбоцитов с гранулами в 1 мкл, облучением БоТП in vitro НИЛИ с длиной волны 635-660 нм и мощностью 1-20 Вт в течение 10 мин с целью активации тромбоцитов. НИЛИ-активация БоТП считается эффективной, если после облучения in vitro происходит дегрануляция и активация не менее 20% тромбоцитов с гранулами в БоТП. После ушивания послеоперационных ран полученную аутологичную активированную БоТП вводят в ушитый медиальный или латеральный артроскопический порт одноразовой медицинской инъекционной иглой 0,8х40 мм 21G для шприцов Luer, при помощи инъекционного одноразового шприца: 2 мл БоТП вводят внутрисуставно, 1 мл БоТП вводят околосуставно, обкалывая прилегающие к суставу мягкие ткани. Только внутрисуставное введение БоТП без обкалывания мягких тканей не позволяет эффективно купировать развитие послеоперационных гематом. Внутрисуставное введение менее 2 мл НИЛИ-активированной БоТП не позволяет достоверно эффективно снизить отек больной конечности, выраженное снижение отека конечности наблюдалось только при внутрисуставном введении 2 мл НИЛИ-активированной БоТП. После окончания операции для контроля эффективности оценивают уровень боли по шкале ВАШ, в баллах; размер (охват) бедра, коленного сустава и голени, объем гематомы при УЗИ-исследовании, см3.
Краткое описание чертежей
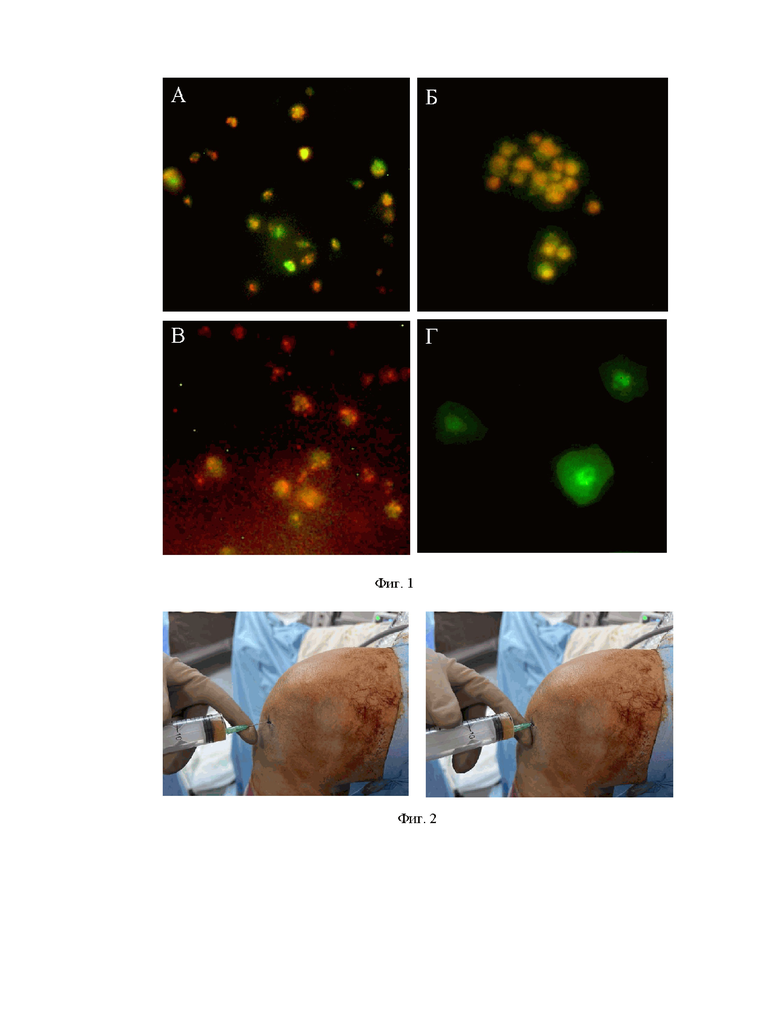
Изобретение поясняется чертежами, где на фиг. 1 представлены цифровые фотографии тромбоцитов БоТП через 10 мин воздействия in vitro НИЛИ с длиной волны 635 нм и мощностью 1 Вт (красный лазер). Витальное окрашивание трипафлавином-акридиновым оранжевым. Увеличение х1000. А - тромбоциты до воздействия НИЛИ; Б - Г - тромбоциты после воздействия НИЛИ: Б - образование тромбоцитарных конгломератов; В - выход гранул за пределы тромбоцитов; Г - интенсивный рост ламеллы в адгезирующих тромбоцитов под действием НИЛИ; на фиг. 2 показано введение НИЛИ-активированной аутологичной БоТП на завершающем этапе артроскопической операции.
Осуществление изобретения
Способ профилактики осложнений у пациентов с артроскопическими операциями на коленном суставе с использованием аутологичных тромбоцитов, активированных с помощью низкоимпульсного лазерного излучения, включает следующие этапы:
1. У пациента за 2 часа до предполагаемой операции осуществляют забор крови при помощи системы для вакуумного забора крови, в которую входят: игла двусторонняя VISIO Plus зеленая стандартная (размер иглы 0,8х38 мм, 21G х1 1/2), держатель BD Vacutainer одноразовый, VACUETTE пробирки с консервантом ЭДТА для гематологических исследований без резьбы, объем 4-5 мл. Венепункция проводится в области локтевой ямки. Забор крови осуществляют по правилам асептики и антисептики, после наложения одноразового резинового жгута выше предполагаемой венепункции на 7,5 см, спиртовыми одноразовыми салфетками обрабатывают область локтевой ямки. Объем забранной венозной крови составляет 30 - 40 мл. Такой объем крови необходим для изготовления 3-3,5 мл БоТП (1 терапевтическая доза БоТП).
2. Аутологичную БоТП выделяют из крови пациента путем двухэтапного центрифугирования: исходную кровь центрифугируют 5 минут с ускорением 300 g, отбирают супернатантную плазму с тромбоцитами и центрифугируют 17 минут с ускорением 700 g для осаждения и концентрирования тромбоцитов. Перечисленные параметры центрифугирования могут отличаться от указанных точных значений на величину, не более ±10%. Из пробирки отбирают большую часть плазмы, бедной тромбоцитами (от 2/3 до 3/4 всего объема БедПл в пробирке), затем ресуспендируют осадок тромбоцитов в оставшемся объеме плазмы. В результате получают богатую тромбоцитами плазму (БоТП) с общей концентрацией клеток выше 1000 тыс/мкл и концентрацией тромбоцитов с гранулами не меньше 500 тыс/мкл, объем БоТП - 3,0-3,5 мл. Для оценки качества тромбоцитов отбирают 100 мкл БоТП. Оценку качества БоТП проводят с помощью метода оценки морфофункционального статуса тромбоцитов [Патент РФ№2485502, авт. Хубутия М.Ш., Макаров М.С., Хватов В.Б., Высочин И.В., Кобзева Е.Н., Конюшко О.И., опубл. 20.06.2013, Бюл. № 17]. Если концентрация тромбоцитов с гранулами в БоТП составляет меньше 500 тыс/мкл, БоТП повторно центрифугируют с ускорением 700 в течение 10-15 мин и ресуспендируют в меньшем объеме плазмы. Готовая БоТП находится в стеклянной или пластиковой пробирке.
3. Облучение БоТП проводят в стерильных условия через открытую крышку пробирки или через стенку закрытой пробирки. Расстояние столба БоТП от источника НИЛИ составляет 5-10 см при облучении открытой пробирки и 1-3 см при облучении закрытой пробирки. Облучение БоТП в закрытой пробирке возможно как в стерильных, так и в нестерильных условиях. БоТП in vitro подвергают воздействию НИЛИ с длиной волны 635-660 нм и мощностью 1-20 Вт в течение 10 мин, после этого снова отбирают аликвоту 100 мкл для оценки активации тромбоцитов под действием НИЛИ. НИЛИ-активация БоТП считается эффективной, если после облучения in vitro происходит дегрануляция и активация не менее 20% тромбоцитов с гранулами в БоТП. Степень активации тромбоцитов проверяют с помощью метода оценки морфофункционального статуса тромбоцитов [Патент РФ№ 2485502, авт. Хубутия М.Ш., Макаров М.С., Хватов В.Б., Высочин И.В., Кобзева Е.Н., Конюшко О.И., опубл. 20.06.2013, Бюл. №17]. Если после НИЛИ-облучения активируется менее 20% тромбоцитов с гранулами, БоТП подвергают повторному облучению в течение 10-20 мин.
4. Введение НИЛИ-активированной аутологичной БоТП проводят после ушивания послеоперационных ран в ушитый медиальный или латеральный артроскопический порт одноразовой медицинской инъекционной иглой 0,8х40 мм 21G для шприцов Luer, при помощи инъекционного одноразового шприца. 2 мл БоТП вводят внутрисутставно, 1 мл БоТП вводят околосуставно, обкалывая прилегающие к суставу мягкие ткани. После окончания операции для контроля эффективности лечения оценивают уровень боли по шкале ВАШ, в баллах; размер (охват) бедра, коленного сустава и голени, объем гематомы при УЗИ-исследовании, см3.
Заявленный способ был разработан по результатам проведенных исследований.
На первом этапе исследования была отработана методика активации БоТП с помощью НИЛИ in vitro. В работе использовали богатую тромбоцитами плазму (БоТП), выделенную из крови здоровых доноров-добровольцев. Венозную кровь у доноров забирали из локтевой вены в стандартные одноразовые вакуумные пробирки (консервант ЭДТА). Сначала пробирки с кровью центрифугировали в течение 4-5 минут с ускорением 300-350 g, затем отбирали супернатантную плазму с тромбоцитами и переносили ее в сухие стеклянные пробирки, после чего центрифугировали их в течение 17 минут с ускорением 700 g. В результате на дне формировался осадок тромбоцитов. Из пробирок удаляли от 2/3 до 3/4 от всего объема супернатантной плазмы и ресуспендировали осадок тромбоцитов в оставшемся объеме. Общий объем богатой тромбоцитами плазмы (БоТП) в опытных пробирках составлял 0,5-1,0 мл, толщина стенки 0,7-0,8 мм, диаметр - 13 мм. Воздействие НИЛИ на тромбоциты осуществлялось через стенку пробирки с расстояния 1-2 см от источника НИЛИ до пробирки, время воздействия составляло 5-10 мин. В работе использовали НИЛИ со следующими характеристиками: длина волны 635 нм, мощность 1 Вт, диаметр пучка 7 мм (лазерная указка); длина волны 635 нм, мощность 2 мВт, диаметр пучка 1 мм и 3 мм (аппарат для внутривенного лазерного освечивания крови); длина волны 488 нм, мощность 1 Вт, диаметр пучка 7 мм (лазерная установка сортера клеток MoFlo); длина волны 355 нм, мощность 400 мВт, диаметр пучка 7 мм (лазерная установка сортера клеток MoFlo). Анализ тромбоцитов проводили с помощью оригинального способа оценки морфофункционального статуса тромбоцитов, включающего окраску клеток с последующим их анализом во флуоресцентном микроскопе [Патент РФ№ 2485502, авт. Хубутия М.Ш., Макаров М.С., Хватов В.Б., Высочин И.В., Кобзева Е.Н., Конюшко О.И., опубл. 20.06.2013, Бюл. № 17]. В образцах БоТП до и после воздействия НИЛИ определяли уровень тромбоцитов с гранулами (биологически полноценные тромбоциты) в процентах по отношению ко всей популяции тромбоцитов (норма 35-75%); морфофункциональный статус тромбоцитов, МФСТ (отражает структурную целостность и функциональную активность), в баллах (норма 75-130 баллов); изменение формы тромбоцитов и рисунка распределения в них гранул; наличие и размер тромбоцитарных конгломератов.
Было установлено, что воздействие НИЛИ с длиной волны 635 нм на тромбоциты in vitro в течение 5-6 минут вызывает активацию только отдельных клеток, что не влияет на активность всей популяции тромбоцитов. Через 10 мин после действия НИЛИ 635 нм и мощностью 1 Вт в образцах БоТП уровень тромбоцитов с гранулами и МФСТ достоверно снижался - в среднем, в 2,0 и 1,6 раза по сравнению с исходными образцами (табл. 1). В составе БоТП многие тромбоциты принимали округлую «блинообразную» или многоотросчатую форму, характерную для активированных тромбоцитов, гранулы в таких тромбоцитах не выявлялись или выявлялись у самой клеточной границы (фиг. 1Б), также можно было видеть отдельные тромбоцитарные гранулы за пределами тромбоцитов или связанные с тромбоцитами только узким мостиком цитоплазмы (фиг. 1В). При помещении БоТП после облучения на предметное стекло наблюдалась ускоренная адгезия тромбоцитов с гранулами, можно было видеть тромбоциты, у которых за 5-10 минут контакта со стеклом формировалась обширная ламелла (фиг. 1Г). Одновременно через 10 мин воздействия в суспензии отмечалось формирование тромбоцитарных конгломератов диаметром до 15 мкм (фиг. 1Б). Следует отметить, что плотность клеток в таких конгломератах была ниже, чем в тромбоцитных агрегатах, которые формируются при необратимой активации тромбоцитов. С другой стороны, в составе конгломератов многие тромбоциты имели измененную морфологию, характерную для активированных тромбоцитов, наблюдалось снижение яркости цитоплазмы и дегрануляция многих тромбоцитов в составе конгломератов. Морфофункциональный анализ показал, что только 20-30% от образующих конгломерат тромбоцитов сохраняли нормальную яркость цитоплазмы и гранулы в своем составе. Таким образом, через 10 мин воздействия НИЛИ с длиной волны 635 нм и мощностью 1 Вт в пробирках с БоТП наблюдалась активация тромбоцитов с гранулами, при этом полной активации всех тромбоцитной популяции не происходило. НИЛИ с длиной волны 635 нм мощностью 2 мВт и НИЛИ с длиной волны 488 нм не вызывало значимых изменения морфофункционального статуса тромбоцитов. При воздействии НИЛИ с длиной волны 355 нм (ультрафиолетовый свет) наблюдалась массовая деформация тромбоцитов, резкое снижение их морфофункционального статуса без образования агрегатов и дегрануляции (табл. 1).
Таблица 1. Изменение морфофункционального статуса тромбоцитов под действием НИЛИ с разной длиной волны in vitro
Ме [25%;75%]
/7 мм
Активирующий эффект НИЛИ в красном диапазоне и мощностью не менее 1 Вт также проверяли на больших объемах БоТП (2-4 мл), которые используются в клинической практике. Облучение БоТП проводили в пластиковых пробирках диаметром 17-20 мм, толщина стенки 0,5-0,8 мм, время облучения составляло 10 мин. Для облучения использовали НИЛИ с длиной волны 635-660 нм, мощность излучения - от 1 до 20 Вт, ширина пучка - от 3 до 20 мм. Облучение БоТП проводили в стерильных условия через открытую крышку пробирки или в нестерильных условиях через стенку закрытой пробирки. Расстояние столба БоТП от источника НИЛИ составляло 5-10 см при облучении открытой пробирки и 1-3 см при облучении закрытой пробирки. При исследовании НИЛИ с длиной волны 635-660 нм во всех случаях в БоТП после облучения в 2-5 раз возрастала доля больших округлых тромбоцитов со смещением гранул к клеточной границе, дегрануляция части тромбоцитов с гранулами, при помещении БоТП на предметное стекло тромбоциты проявляли ускоренную адгезию. В 50% случаев тромбоциты формировали конгломераты. Увеличение мощности и ширины пучка ускоряло скорость дегрануляции тромбоцитов (табл.2)
Таблица 2. Активация тромбоцитов in vitro под действием НИЛИ в красном видимом диапазоне
Таким образом, НИЛИ с длиной волны 630-660 нм и мощностью не менее 1 Вт позволяла активировать тромбоциты в дозах БоТП, которые могут быть использованы непосредственно для инъекционного введения. Для ускорения активации тромбоцитов более предпочтительно использовать источники НИЛИ с широким пучком.
На втором этапе была проведена оценка клинического эффекта НИЛИ-активированной БоТП. Обследовали пациентов с артроскопическими операциями, проводимыми по поводу разрыва передней крестообразной связки, разрыва наружного/внутреннего мениска, наличия хондромаляций и гонартроза. Забор крови пациента для изготовления аутологичной БоТП осуществляли за 2 часа до предполагаемой операции при помощи системы для вакуумного забора крови, в которую входят: игла двусторонняя VISIO Plus зеленая стандартная (размер иглы 0,8х38 мм, 21G х1 1/2), держатель BD Vacutainer одноразовый, VACUETTE пробирки с консервантом ЭДТА для гематологических исследований без резьбы, объем 4-5 мл. Венепункцию проводили в области локтевой ямки. Забор крови осуществляли по правилам асептики и антисептики, после наложения одноразового резинового жгута выше предполагаемой венепункции на 7,5 см, спиртовыми одноразовыми салфетками обрабатывали область локтевой ямки. Объем забранной венозной крови составлял 30 - 32 мл. Аутологичную БоТП выделяли из крови путем двухэтапного центрифугирования: исходную кровь центрифугируют 5 минут с ускорением 300 g, отбирают супернатантную плазму с тромбоцитами и центрифугируют 17 минут с ускорением 700 g для осаждения и концентрирования тромбоцитов. Из пробирки отбирали большую часть плазмы, бедной тромбоцитами (от 2/3 до 3/4 всего объема БедПл в пробирке), затем ресуспендировали осадок тромбоцитов в оставшемся объеме плазмы. В результате получали богатую тромбоцитами плазму (БоТП) с концентрацией клеток выше 1000 тыс/мкл. Из 30-40 мл крови пациента выделяли 3,0-3,5 мл БоТП. Для оценки качества тромбоцитов отбирали 100 мкл БоТП. БоТП подвергали воздействию НИЛИ с длиной волны 635-660 нм и мощностью не менее 1 Вт в течение 10 мин, после этого снова отбирали аликвоту 100 мкл для оценки активации тромбоцитов под действием НИЛИ. Облучение БоТП проводили в закрытой пластиковой пробирке объемом 10-15 мл в течение 10 мин в условиях неподвижности пробирки.
Пациенты были разделены на 3 группы - в 1 группе (8 человек) операцию проводили без использования тромбоцитных препаратов (группа сравнения), во 2 группе (8 человек) интраоперационно вводили неактивированную БоТП в объеме 3 мл, в 3 группе (8 человек) интраоперационно вводили НИЛИ-активированную БоТП в объеме 3 мл. Группы были сопоставимы по гендерно-возрастным характеристика и характеру патологии. Качество тромбоцитов в исходной БоТП не различалось во 2 и 3 группах. Всем пациентам выполнялись артроскопические операции коленного сустава. В зависимости от поврежденных структур и локализации повреждения выполнялись: резекция мениска, шов мениска, реконструкция передней крестообразной связки, рефиксация передней крестообразной связки. На завершающем этапе операции после ушивания послеоперационных ран пациентам 2 и 3 групп в ушитый медиальный или латеральный артроскопический порт одноразовой медицинской инъекционной иглой 0,8х40 мм 21G для шприцов Luer, при помощи инъекционного одноразового шприца объемом 5 мл, тип наконечника: LUER-SLIP, с заранее набранным препаратом производили введение 1-3 мл БоТП внутрисуставно. Во 2 и 3 группах у 3 пациентов из 8 внутрисуставно вводили 3 мл без обкалывания мягких тканей, у 5 пациентов из 8 внутрисуставно вводили 2 мл БоТП и дополнительно проводили веерное обкалывание мягких тканей 1 мл БоТП, у 2 пациентов из 8 внутрисуставно вводили 1,0-1,5 мл БоТП и дополнительно проводили веерное обкалывание мягких тканей 1 мл БоТП
После окончания операции оценивали наличие следующих осложнений: уровень боли по шкале ВАШ, в баллах; размер (охват) бедра, коленного сустава и голени, см; необходимость дополнительного введения обезболивающих препаратов; объем гематомы при УЗИ-исследовании, см3.
Введение неактивированной БоТП сопровождалось развитием выраженного болевого синдрома, увеличением охвата отделов конечности, как и при лечении без БоТП (табл. 3). Препараты неактивированной БоТП и НИЛИ-активированной БоТП препятствовали развитию гематом при обкалывании мягких тканей 1 мл БоТП, без обкалывания мягких тканей у пациентов 2 и 3 группы наблюдалось формирование гематом как и в группе сравнения. Это указывает на то, что обкалывание мягких тканей с помощью БоТП при артроскопических операциях усиливает репаративный эффект БоТП. Введение неактивированной БоТП во всех случаях требовала дополнительного введения обезболивающих средств. Внутрисуставное введение 1,0-1,5 мл НИЛИ-активированной БоТП не позволяло достоверно снизить отек больной конечности, выраженное снижение отека конечности наблюдалось только при внутрисуставном введении 2 мл НИЛИ-активированной БоТП. При сравнении клинического эффекта неактивированной БоТП и НИЛИ-активированной БоТП установлено, что предварительная активация тромбоцитов с помощью НИЛИ значительно снижает болевой синдром, уменьшает отек конечности и потребность в обезболивающих препаратах (табл. 3). Объем гематомы у пациентов во 2 и 3 группах был сопоставимым. Таким образом, предварительная активация БоТП с помощью НИЛИ с длиной волны 635-660 нм и мощностью не менее 1 Вт позволяла значительно увеличить репаративный эффект тромбоцитов БоТП. У всех пациентов с лечением НИЛИ-активированной БоТП послеоперационный этап проходил без осложнений, наблюдалось значительное улучшение качества жизни и сокращение сроков госпитализации.
Таблица 3. Оценка клинического эффекта препаратов на основе аутологичной БоТП у пациентов с артроскопическими операциями
тыс /мкл
см
Стоит отметить, что клинический эффект НИЛИ-активированной БоТП был наиболее эффективным в тех случаях, когда под действием НИЛИ in vitro дегранулировали 20% и более тромбоцитов с гранулами от их общего числа. В тех случаях, когда под действием НИЛИ in vitro дегранулировали менее 20% всех тромбоцитов с гранулами, болевой эффект и объем гематомы были более выраженными. У разных людей тромбоциты имеют разную реактивность и восприимчивость к активирующим агентам. В случае пониженной чувствительности тромбоцитов БоТП к НИЛИ рекомендуется использовать дозы БоТП с более высоким содержанием тромбоцитов с гранулами. Проведенное наблюдение показало, что наиболее эффективное купирование боли и других осложнение наблюдается при использовании БоТП, содержащей не менее 500 тыс. тромбоцитов с гранулами в 1 мкл и активацией не менее 20% тромбоцитов с гранулами под действием НИЛИ in vitro. Обкалывание мягких тканей, прилегающих к суставу, повышает эффективность действия БоТП и снижает риск развития гематом (табл. 4).
Таблица 4. Наличие и размер гематом в послеоперационном периоде через 1-3 дня после операции у пациентов с артроскопическими операциями после введения НИЛИ-активированной БоТП с разным качеством тромбоцитов
Клинический пример
Больной М., 38 лет, испытывал резкую боль в правом коленном суставе, диагностированы разрыв тела и заднего рога внутреннего мениска правого коленного сустава. Пациент был госпитализирован для планового оперативного лечения. Операция выполнена через 1 день после госпитализации: артроскопия правого коленного сустава, резекция заднего рога и тела внутреннего мениска, иссечение гипертрофированного тела Гоффа, абразивная хондропластика.
На завершающем этапе лечения проведена инъекция аутологичной БоТП, активированной НИЛИ с длиной волны 635 нм и мощностью 1 Вт. Исходная БоТП содержала 510 тыс. тромбоцитов с гранулами, степень активации тромбоцитов с гранулами под действием НИЛИ - 21%. 2 мл БоТП введено внутрисуставно, 1 мл БоТП использовано для обкалывания мягких тканей вокруг сустава. Пациенту осуществляли однократное введение Трамадола спустя 3 часа после операции (стандартный препарат), дополнительных обезболивающих препаратов не вводили в связи с отсутствием боли. Через 1 день после операции при ультразвуковом исследовании мягких тканей правого коленного сустава выявлена мелкая гематома объемом 1 см3, без болевых ощущений. Сроки реабилитации: выписан на 5 сутки, начал ходить с полной нагрузкой на оперированную ногу на 7 сутки. При физикальном обследовании пациента спустя 12 суток (снятие швов) - амплитуда движений в коленном суставе в полном объеме, незначительная болезненность в крайней точке сгибания, пациент ходит без дополнительной опоры. Через 2 месяца жалоб не предъявляет, болевых ощущений, которые беспокоили пациента перед операцией, нет.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРИГОТОВЛЕНИЯ ЛИЗАТА ТРОМБОЦИТОВ С ВЫСОКИМ СОДЕРЖАНИЕМ ФАКТОРОВ РОСТА | 2020 |
|
RU2739515C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ТРОМБОФИБРИНОВОГО СГУСТКА, ОБЛАДАЮЩЕГО РОСТСТИМУЛИРУЮЩИМИ СВОЙСТВАМИ | 2018 |
|
RU2679616C1 |
| СПОСОБ ЛЕЧЕНИЯ ПАЦИЕНТОВ С ПЕРЕЛОМОМ ШЕЙКИ ПЛЕЧА | 2018 |
|
RU2681753C1 |
| КОСТНО-ПЛАСТИЧЕСКИЙ МАТЕРИАЛ С ВЫСОКОАДГЕЗИВНЫМИ СВОЙСТВАМИ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2023 |
|
RU2813132C1 |
| КОСТНО-ПЛАСТИЧЕСКИЙ МАТЕРИАЛ С УПРАВЛЯЕМЫМИ СВОЙСТВАМИ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2023 |
|
RU2812733C1 |
| ЭКСПРЕСС-МЕТОД МОРФОФУНКЦИОНАЛЬНОГО АНАЛИЗА ТРОМБОЦИТОВ, ПРИГОДНЫХ ДЛЯ КЛИНИЧЕСКОГО ИСПОЛЬЗОВАНИЯ | 2015 |
|
RU2623074C1 |
| СПОСОБ ПОЛУЧЕНИЯ БОГАТОЙ ТРОМБОЦИТАМИ ПЛАЗМЫ И СПОСОБ ПОЛУЧЕНИЯ ТРОМБОФИБРИНОВОГО ГЕЛЯ ИЛИ СГУСТКА С СЫВОРОТКОЙ, СОДЕРЖАЩИЕ ФАКТОРЫ РОСТА, ИЗ НЕСТАБИЛИЗИРОВАННОЙ ВЕНОЗНОЙ КРОВИ | 2019 |
|
RU2717448C1 |
| СПОСОБ ЛЕЧЕНИЯ ПАЦИЕНТОВ С ХРОНИЧЕСКОЙ ИШЕМИЕЙ НИЖНИХ КОНЕЧНОСТЕЙ | 2021 |
|
RU2759478C1 |
| Способ лечения лимфоцеле ложа нефротрансплантата после аллогенной трансплантации почки | 2020 |
|
RU2739125C1 |
| СПОСОБ ВЫБОРА ТАКТИКИ ЭНДОСКОПИЧЕСКОГО ЛЕЧЕНИЯ ПАЦИЕНТОВ С ХИМИЧЕСКИМИ ОЖОГАМИ ПИЩЕВОДА | 2022 |
|
RU2802745C1 |
Изобретение относится к медицине, а именно к травматологии и ортопедии, и может быть использовано для профилактики осложнений у пациентов после проведения артроскопических операций на коленном суставе. Проводят забор венозной крови у пациента не менее чем за 2 часа до начала операции с получением из нее не менее 3 мл аутологичной богатой тромбоцитами плазмы (БоТП), содержащей не менее 500 тыс. тромбоцитов с гранулами в 1 мкл. Затем на полученную БоТП воздействуют in vitro низкоимпульсным лазерным излучением (НИЛИ) с длиной волны 635-660 нм и мощностью 1-20 Вт в течение 10 мин с активацией не менее 20% тромбоцитов с гранулами от их общего числа в БоТП, с последующим введением полученной БоТП внутрисуставно и околосуставно. При этом внутрисуставно вводят не менее 2 мл БоТП, околосуставно - не менее 1 мл БоТП, обкалывая прилегающие к суставу мягкие ткани. Способ обеспечивает профилактику осложнений у пациентов после артроскопических операций на коленном суставе, в числе которых гемартроз, отек параартикулярных тканей, болевой эффект, за счет использования предварительно НИЛИ-активированной аутологичной БоТП, содержащей не менее 500 тыс. тромбоцитов с гранулами в 1 мкл до облучения БоТП in vitro и не менее 20% активированных (100 тыс. в 1 мкл) тромбоцитов с гранулами после облучения in vitro в БоТП в совокупности с предложенной схемой ее введения. 2 з.п. ф-лы, 2 ил., 4 табл., 1 пр.
1. Способ профилактики осложнений у пациентов после выполнения артроскопических операций на коленном суставе с использованием аутологичных тромбоцитов, включающий забор венозной крови у пациента не менее чем за 2 часа до начала операции с получением из нее не менее 3 мл аутологичной богатой тромбоцитами плазмы (БоТП), содержащей не менее 500 тыс. тромбоцитов с гранулами в 1 мкл, воздействие на БоТП in vitro низкоимпульсным лазерным излучением (НИЛИ) с длиной волны 635-660 нм, мощностью 1-20 Вт и шириной пучка 3-20 мм, в течение 10 мин с активацией не менее 20% тромбоцитов с гранулами от их общего числа в БоТП, с последующим введением полученной БоТП внутрисуставно и околосуставно после ушивания послеоперационных ран, при этом внутрисуставно вводят не менее 2 мл БоТП, околосуставно – не менее 1 мл БоТП, обкалывая прилегающие к суставу мягкие ткани.
2. Способ по п.1, характеризующийся тем, что аутологичную БоТП из венозной крови получают путем ее двухэтапного центрифугирования: исходную кровь центрифугируют 5 минут с ускорением 300 g, отбирают супернатантную плазму с тромбоцитами и центрифугируют 17 минут с ускорением 700 g, из пробирки отбирают от 2/3 до 3/4 объема плазмы, бедной тромбоцитами, затем ресуспендируют осадок тромбоцитов в оставшемся объеме плазмы, в результате получают БоТП с концентрацией клеток выше 1000 тыс/мкл.
3. Способ по п.1, характеризующийся тем, что БоТП вводят при помощи одноразового шприца Luer с инъекционной иглой 0,8×40 мм 21G.
| КЕСЯН Г.А | |||
| и др | |||
| Профилактика гонартроза при хирургическом лечении переломов проксимального отдела большеберцовой кости с применением PRP | |||
| III Международный конгресс ассоциации ревмоортопедов: тезисы докладов конгресса / редкол.: М.А | |||
| Макаров [и др.] ; Ассоциация ревмоортопедов | |||
| - Воронеж: Издательско-полиграфический центр "Научная книга", 2019, |
Авторы
Даты
2025-03-31—Публикация
2024-06-11—Подача