Изобретение относится к медицине, а именно к профилактике нефротоксического и гонадотоксического действия Цисплатина.
Химиотерапия является одним из основных методов лечения местно-распространенных и метастатических форм рака различной локализации.
Одним из широко используемых химиотерапевтических средств является препарат Цисплантин (цис-диамминдихлороплатина (II)), назначаемый для лечения злокачественных заболеваний области головы и шеи, пищевода, мочевого пузыря, яичек, яичников, матки, молочной железы, желудка и некоторых форм рака. Цисплатин относится к группе препаратов цитостатического действия, препятствуя делению клеток с высокой пролиферативной активностью.
Однако цитостатический эффект может оказывать влияние не только на опухолевые клетки, но и на здоровые клетки разных органов, также обладающих высокой степенью пролиферации, к которых относятся эпителий желудочно-кишечного тракта, клетки костного мозга, а также эпителий проксимальных извитых канальцев почки и сперматогенный эпителий. При этом развитие острой почечной недостаточности, вызванной повреждение почечных канальцев, является наиболее частым побочным эффектом терапии этим препаратом, регистрируемым у 30-40% пациентов (Perazella M.A. Onco-nephrology: renal toxicities of chemotherapeutic agents. Clin J Am Soc Nephrol. 2012; 7 (10): 1713-21. https://doi.org/10.2215/CJN.02780312. Dos Santos N.A., Carvalho Rodrigues M.A., Martins N.M., dos Santos A.C. Cisplatin induced nephrotoxicity and targets of nephroprotection: an update. ArchToxicol. 2012; 86 (8): 1233-50. https://doi.org/10.1007/s00204-012-0821-7. Volarevic V., Djokovic B., Jankovic M.G.C. Harrell R., Fellabaum C., Djonov V., Arsenijevic N. Molecular mechanisms of cisplatin-induced nephrotoxicity: a balance on the knife edge between renoprotection and tumor toxicity. Journal of Biomedical Science (2019) 26:25. https://doi.org/10.1186/s12929-019-0518-9). При этом выраженность нарушения функции почек зависит от дозы препарата и кратности введения. При однократной инфузии Цисплатин в дозе 50-75 мг/м2 признаки нефротоксичности выявляют у 25-33% больных, а при увеличении дозы препарата до 100 мг/м2 и более развитие острой почечной недостаточности отмечают у большинства пациентов, причем часто повреждение становится необратимым (Crona D.J., Faso A., Nishijima T.F., McGraw K.A., Galsky M.D., Milowsky M.I. A systematic review of strategies to prevent cisplatin-induced nephrotoxicity. Oncologist. 2017; 22 (5): 609-19. https://doi.org/10.1634/theoncologist.2016-0319).
Развитие почечной дисфункции существенно ограничивает возможности противоопухолевой терапии.
Другим существенным побочным действием химиотерапии с использованием Цисплатин у мужчин является нарушение функции яичек с развитием андрогенной недостаточности и нарушением сперматогенеза, что может приводить к эректильной дисфункции и бесплодию (Brydoy, M.; Fossa, S.D.; Klepp, O.; Bremnes, R.M.; Wist, E.A.; Wentzel-Larsen, T.; Dahl, O. Paternity and testicular function among testicular cancer survivors treated with two to four cycles of cisplatin-based chemotherapy. Eur. Urol. 2010, 58, 134-140. Santabarbara G, Maione P, Rossi A, Gridelli C. Pharmacotherapeutic options for treating adverse effects of Cisplatin chemotherapy. Expert Opin Pharmacother. 2016; 17: 561-70). Хотя это негативное действие химиопрепарата не является жизнеугрожающим, как нефротоксичность, тем не менее он существенно ухудшает качество жизни пациентов, подвергнутых химиотерапии.
Для профилактики развития нефротоксического эффекта Цисплатин используют несколько вариантов терапии.
Известен способ профилактики нефротоксичности Цисплатин путем инфузионной гидратационной терапии с введением больших объемов жидкости (1-6 л) в течение 2-6 часов, в том числе с дополнительной стимуляцией диуреза мочегонными препаратами (фуросемид, маннитол) (Crona D.J., Faso A., Nishijima T.F., McGraw K.A., Galsky M.D., Milowsky M.I. A systematic review of strategies to prevent cisplatin-induced nephrotoxicity. Oncologist. 2017; 22 (5): 609-19. https://doi.org/10.1634/theoncologist.2016-0319). Суть метода заключается в уменьшении концентрации препарата в крови и моче, что способствует снижению его накопления в клетках эпителия проксимальных канальцев и уменьшению выраженности повреждения.
К недостаткам метода относятся его низкая эффективность при необходимости назначения высоких доз химиопрепарата, у больных с сопутствующей артериальной гипертонией, а также невозможность введения достаточно большого объема жидкости при наличии у пациента сердечной недостаточности. Кроме того, данный метод не обеспечивает защиту от токсического действия Цисплатин в отношении других органов, в частности, яичек.
Известен также способ профилактики нефротоксического действия Цисплатин с использованием дополнительного введения препаратов магния в дозе 8-16 мэкв (Oka T., Kimura T., Suzumura T. et al. Magnesium supplementation and high volume hydration reduce the renal toxicity caused by cisplatin-based chemotherapy in patients with lung cancer: A toxicity study. BMC Pharmacol Toxicol 2014; 15:70). Действие данного способа основано на том, что при терапии Цисплатин развивается гипомагнийемия за счет снижения реабсорбции этого катиона из первичной мочи, что ведет к активации переносчика ОСТ2 (organic cation transporter 2) и повышению накопления химиопрепарата в эпителиальных клетках с нарастанием токсического эффекта его метаболитов. Восполнение дефицита магния препятствует этому механизму.
Недостатком метода является его ограниченная эффективность, особенно при необходимости использования высоких доз Цисплатин и у больных с артериальной гипертонией, а также не обеспечивает профилактику гонадотоксичности препарата.
Также известны способы уменьшения токсического влияния Цисплатин на почки с помощью терапии фармакологическими препаратами с разным механизмом действия, в частности цимитидина (ингибитор транспортера ОСТ2), карведиола (антиоксидант), силастатина (ингибитор апоптоза), розиглитазона (противовоспалительное действие) и амифостина (цитотоксический агент) (Chun-yan Fang, Da-yong Lou, Li-qin Zhou, Jin-cheng Wang, Bo Yang, Qiao-jun He, Jia-jia Wang, Qin-jie Weng. Natural products: potential treatments for cisplatin-induced nephrotoxicity. Acta Pharmacologica Sinica (2021) 42: 1951-1969; https://doi.org/10.1038/s41401-021-00620-9).
Однако эти препараты действуют только на отдельные звенья патогенеза токсичности химиопрепарата, что обуславливает их недостаточную эффективность в отношении разных форм рака, а также наличие у них существенных побочных эффектов, ограничивающих возможности терапии.
В отношении профилактики гонадотоксичности Цисплатин стандартных рекомендаций не выявлено.
Имеется ряд публикаций с оценкой протективного действия терапии синтетическими антиоксидантами (L-карнитин, терт-бутилгидрохинон, рутин, кверцетин и др.) или препаратами растительного происхождения (экстракт виноградных семечек, эпигаллокатехин-3-галлат, ресвератрол и др.) (Ghafouri-Fard S., Shoorei H., Abak A., Seify M. et al. Effects of chemotherapeutic agents on male germ cells and possible ameliorating impact of antioxidants. Biomedicine & Pharmacotherapy. Volume 142, October 2021, 112040. https://doi.org/10.1016/j.biopha.2021.112040).
Известно средство для профилактики и коррекции нарушений сперматогенеза, вызванного цитостатическим воздействием (RU 2318529 C1). Предложено применение в качестве средства для профилактики и коррекции нарушений сперматогенеза, вызванных цитостатическим воздействием, экстракта левзеи сафлоровидной (Rhaponticum carthamoides). Экстракт левзеи сафлоровидной является малотоксичным лекарственным средством. Данное изобретение расширяет арсенал средств, используемых для профилактики и коррекции нарушений сперматогенеза, вызванных цитостатическим воздействием без проявления побочных эффектов, а также расширяет сферы использования.
Недостатками такой терапии являются то, что изучение действия этих препаратов находятся в стадии экспериментальных исследований и клиническая их эффективность пока не доказана. Кроме того, все они действуют лишь на одно из звеньев патогенеза гонадотоксичности - развитие оксидантного повреждения клеток вследствие избыточной активации активных форм кислорода, тогда как его патогенез многофакторный и включает также повышение секреции провоспалительных цитокинов с развитием системной воспалительной реакции, активацию апоптоза, блокировку генов, отвечающих за регенерацию клеток. При этом действие этих фармакологических средств в отношении нефротоксичости Цисплатин не доказано.
Задачей изобретения является профилактика нефротоксического и гонадотоксического действия Цисплатин за счет введения фармакологических препаратов, действующих на отдельные звенья патогенеза клеточного повреждения, вызываемого этим химиопрепаратом.
Указанная задача решается тем, что также как и в известном способе вводят фармакологические препараты, действующие на отдельные звенья патогенеза клеточного повреждения, вызываемого этим химиопрепаратом.
Особенностью заявляемого способа является то, что с первого дня химиотерапии проводят ежедневный внутримышечный 10-дневный курс терапии препаратом Целлекс в дозе 0,1 мл/кг.
Заявляемый способ заключается в использовании комплекса продуктов секреции нейрональных стволовых клеток, выделенного из головного мозга эмбрионов свиньи, являющимся активным компонентом препарата фармакопейного препарата «Целлекс».
Способ поясняется подробным описанием, клиническими примерами и иллюстрациями, на которых изображено:
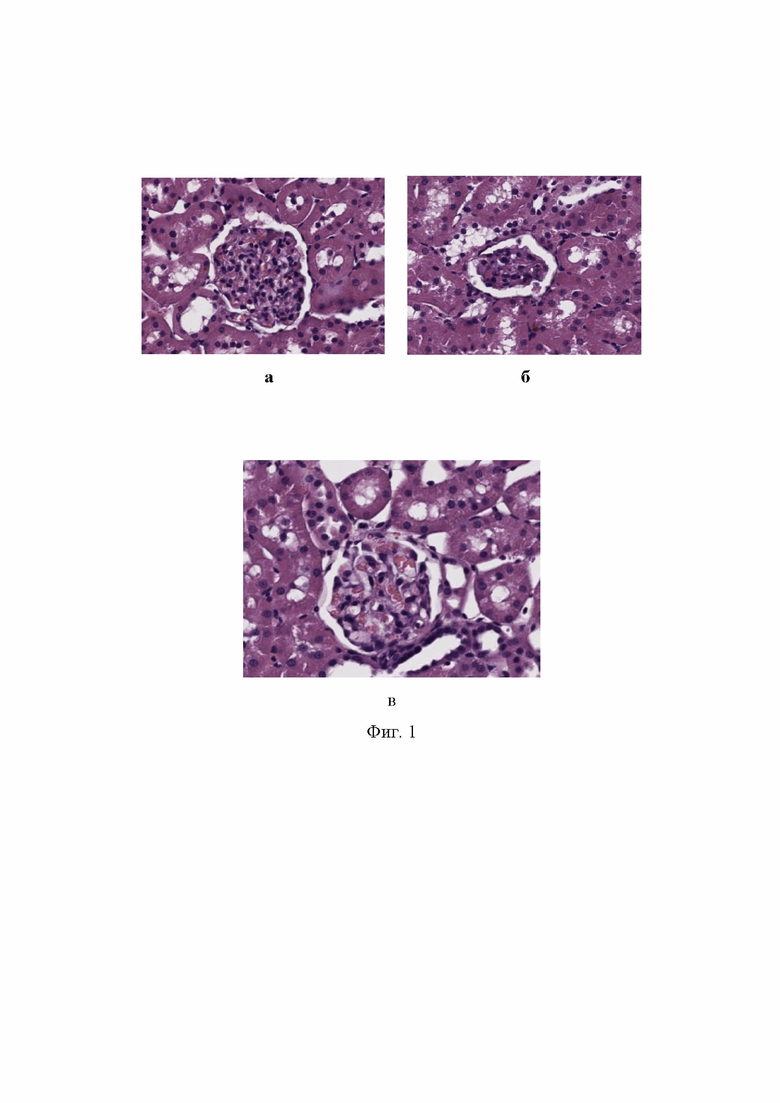
Фиг. 1 - гистологическая картина почек: а) нормальные клубочек и почечные канальцы; б) сморщенный клубочек и почечные канальцы с выраженными дистрофическими изменениями (введение Цисплатин, контроль); в) нормальный клубочек и почечные канальцы с умеренными дистрофическими изменениями. Окраска гематоксилином и эозином. Ув. 400х.
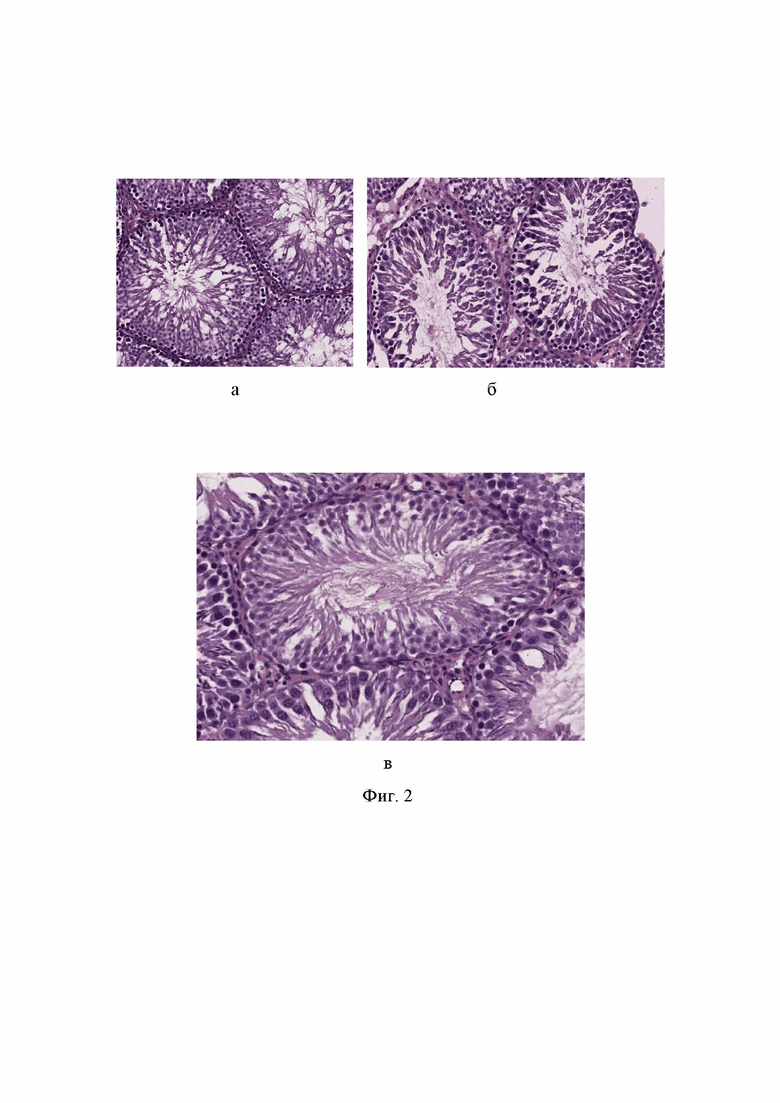
Фиг. 2 - гистологическая картина яичек в разных сериях (окраска гематоксилином и эозином, ув.200х.): а) норма; б) 14 дней после введения Цисплатина; в) 14 дней после введения Цисплатина на фоне терапии Целлексом.
Способ осуществляют следующим образом.
При необходимости химиотерапии с использованием препарата Цисплатин непосредственно после его введения начинают 10-дневный курс терапии с ежедневным внутримышечным введением препарата Целлекс в дозе 0,1 мл/кг (0,1 мг/кг активного вещества).
Эффективность заявляемого способа подтверждается клиническими примерами.
Пример 1
Уменьшение нефропротективного действия Цисплатин при его введении в средне-токсической дозе при терапии Целлексом в соответствии с заявляемым способом.
Десяти крысам-самцам массой 300-340 г внутрибрюшинно вводили химиопрепарат Цисплатин в дозе 5 мг/кг, которая по данным литературы оказывает средне выраженное токсическое действие и не приводит к летальности животных.
После введения химиопрепарата 5 крысам терапии не проводили (1-я серия, контроль). У других 5 крыс с первого дня начинали ежедневные внутримышечные инъекции препарата Целлекс в дозе 0,1 мл/кг в течение 10 дней (2-я серия). Через 3, 7 и 14 дней после введения Цисплатин крыс помещали на сутки в обменные клетки для сбора суточной мочи и брали пробы крови из хвостовой вены. В крови и суточной моче определяли биохимические показатели, характеризующие функциональное состояние почек (мочевина, креатинин, натрий, кальций) и рассчитывали такие показатели, как скорость клубочковой фильтрации (СКФ) и канальцевую реабсорбцию натрия и кальция (RNa, RCa). Также оценивали выживаемость животных в течение 14 суток.
Результаты показали (таблица 1), что у всех крыс развивалась острая почечная недостаточность с развитием полиурии и ухудшением показателей функционального состояния почек. Однако в опытах с терапией Целлексом выраженность функциональных нарушений оказалась существенно меньшей.
Таблица 1
Влияние терапии Целлексом на функциональные показатели почек при введении химиопрепарата Цисплатин в дозе 5 мг/кг
* - различия между опытной и контрольной сериями статистически достоверны при p<0,05, ** - при p<0,01.
Если выраженность полиурии на 3-и сутки в опытной и контрольной сериях достоверно не различались, то в более поздние сроки на фоне терапии Целлексом диурез имел четкую тенденцию к нормализации, тогда как в контроле он оставался постоянно высоким, превышая более чем в 2 раза нормальны значения.
Уровень креатинина крови на 3-и сутки после введения Цисплатин в контрольной серии возрастал с 41±1,8 мкмоль/л до 101±7 мкмоль/л, тогда как при терапии Целлексом он возрастал лишь до 82±5 мкмоль/л (p<0,05). В дальнейшем концентрация креатинина в обеих сериях имела тенденцию к снижению, которое также было более выражено в серии с терапией Целлексом. Чрез 14 суток при терапии Целлексом креатинин крови снижался до субнормальных значений, тогда как в контрольных опытах он оставался существенно повышенным.
Аналогичная динамика выявлена и в отношении концентрации мочевины в крови. В контрольной серии этот показатель возрастал до более высоких значений, чем в опытной серии, и его снижение на фоне терапии Целлексом происходило более выражено, достигая практически нормальных значений к 14-м суткам, тогда как в контроле его уровень сохранялся на повышенных значениях.
Скорость клубочковой фильтрации на 3-и и 7-е сутки после введения Цисплатин на фоне терапии Целлексом снижалась менее значительно, чем в контроле, хотя к 14-м суткам различия нивелировались.
В отношении реабсорбции натрия и кальция также выявлено значительное меньшее нарушение реабсорбции этих катионов на 3-и и 7-е сутки после введения Цисплатин при терапии Целлексом, но через 14 суток различия исчезали.
Таким образом, данный пример иллюстрирует, что терапия Целлексом уменьшает токсическое действие химиопрепарата Цисплатин, введенного в средне-токсической дозе, с проявлением наиболее выраженного нефропротективного эффекта в ранние сроки после токсического воздействия, в так называемую «аварийную» стадию повреждения, которая во многом определяет дальнейшее течение патологического процесса.
Пример 2
Уменьшение нефропротективного действия Цисплатин при его введении в высокотоксической дозе при терапии Целлексом в соответствии с заявляемым способом.
Двадцати крысам-самцам массой 300-340 г внутрибрюшинно вводили химиопрепарат Цисплатин в дозе 7 мг/кг, которая по данным литературы оказывает выраженное токсическое действие и приводит к необратимой почечной недостаточности у части животных.
После введения химиопрепарата 10 крысам терапии не проводили (1-я серия, контроль). У других 10 крыс с первого дня начинали ежедневные внутримышечные инъекции препарата Целлекс (2-я серия), с последующим обследованием животных, как описано в примере 1.
Результаты показали, что в контрольной серии погибло 80% подопытных крыс в сроки от 3 до 10 дней после введения Цисплатин. В опытной серии с терапией Целлексом погибло 50% животных в сроки от 6 до 12 дней.
Функциональные показатели в контрольной серии опытов нарушались в большей степени, чем в опытах со средне-токсичной дозой Цисплатин, но при этом нефропротективный эффект терапии Целлексом проявлялся с высокой степенью достоверности (Таблица 2).
Таблица 2
Влияние терапии Целлексом на функциональные показатели почек при введении химиопрепарата Цисплатин в дозе 7 мг/кг
* - достоверность различий между опытной и контрольной группами: * - p<0,05, ** - p,0,01.
Выраженность полиурии в группе с терапией Целлексом оказалась достоверно меньше на 7-е сутки наблюдения. Уровни креатинина и мочевины крови на фоне терапии Целлексом также повышались в меньшей степени с максимальными различиями на 7-е сутки. Динамика СКФ также оказалась более благоприятной в опытах с терапией Целлексом, при этом к 14-м суткам этот показатель даже приближался к нормальным значениям, тогда как в контроле он оставался ниже нормы практически в 3 раза. Реабсорбция натрия и кальция на всех сроках наблюдения при терапии Целлексом сохранялась на значениях, более близких к норме, чем в контрольной серии.
Важно отметить, что некоторое улучшение показателей в контрольной серии было связано с гибелью животных с наиболее выраженной почечной недостаточностью и выживанием наиболее резистентных особей с высоким уровнем спонтанной регенерации поврежденных клеток. Терапия Целлексом, усиливая регенераторные возможности почечных структур, способствует восстановлению функциональных возможностей органа.
Данный пример иллюстрирует, что терапия препаратом Целлекс оказывает выраженный нефропротективный эффект даже при использовании высокотоксичной дозы Цисплатин.
Пример 3
Уменьшение гонадотоксичности Цисплатин в средне-токсичной дозе при терапии Целлексом в соответствии с заявляемым способом.
Десяти половозрелым крысам-самцам внутрибрюшинно вводили Цисплатин в дозе 5 мг/г. У 5 животных никакой терапии не проводили (1-я серия), а другим 5 крысам с первого дня проводили терапию Целлексом в соответствии с заявляемым способом. До начала эксперимента и через 14 дней после введения химиопрепарата, брали пробы крови для определения уровня тестостерона. Через 14 дней выполняли эвтаназию животных путем ингаляции СО2 и удаляли яички для поведения гистологического и морфометрического исследования.
Исследование уровня тестостерона в крови показало, что через 14 дней после введения Цисплатин уровень тестостерона снизился с 3,77±0,33 нг/мл до 2,31±0,14 нг/мл (p<0,05). В опытах, где после введения Цисплатин проводили терапию Целлексом уровень тестостерона в крови составил 5,37±0,37 нг/мл, что даже превышало нормальные значения этого показателя у интактных крыс (p<0,05). По сравнению с опытами без терапии различия оказались еще более достоверными при p<0,001.
Таким образом, заявляемый способ профилактики гонадотоксичности Цисплатин с использованием курсовой терапии препаратом Целлекс является эффективным методом предотвращения нарушения синтеза тестостерона в яичках.
Пример 4
Уменьшение выраженности морфологических изменений в почках при введении Цисплатин на фоне терапии препаратом Целлекс в соответствии с заявляемым способом.
В опытах на 10 крысах внутрибрюшинно вводили препарат Цисплатин в дозе 5 мг/кг. При этом у 5 крыс никакой терапии не проводили, а у других 5 крыс ежедневно в течение 10 дней внутримышечно вводили препарат Целлекс в дозе 0,1 мл/кг в соответствии с заявляемым способом. Через 14 дней удаляли почки и проводили их гистологическое исследование по стандартной методике с окрашиванием приготовленных парафиновых срезов гематоксилином и эозином. Гистологические препараты подвергали сканированию с последующим анализом с использованием компьютерной программы HistoScan (Санкт-Петербург, Россия). Морфологические показатели сравнивали с гистологической картиной почек нормальных животных (3 крысы).
Результаты показали, что после введения Цисплатин у крыс, не получавших лечения, выявляли выраженные изменения как в клубочковом, так и в канальцевом аппарате почки. Многие клубочки выглядели сморщенными со спавшимися капиллярными петлями и с признаками развития гломерулосклероза (Фиг. 1 а, б, в). В то же время в опытах с терапией Целлексом сморщенные клубочки выявлялись лишь в единичных количествах, а большинство клубочков имели строение, близкое к норме с нормальными размерами и сетью клубочковых капилляров, заполненных эритроцитами. При морфометрическом анализе доля сморщенных клубочков в контрольных опытах составила 9,2±0,2%, тогда как на фоне терапии она уменьшилась до 1,8±0,1% (p<0,001).
В контрольных опытах существенным изменениям подвергся и эпителий почечных канальцев. В большинстве канальцев выявили явления выраженной гидропической дистрофии со слущиванием клеток в просвет канальцев. В отдельных участках выявляли группы некротизированных канальцев и формирующиеся очаги склероза. Морфометрический анализ показал, что в контрольных опытах доля канальцев с выраженными дистрофическими изменениями составила 27,8±1,1%, доля некротизированных канальцев - 0,6±0,1%, тогда как в опытной серии доля канальцев с выраженным повреждением составила лишь 11,3±0,4% (p<0,001), а некротически измененных канальцев и очагов склероза вообще не выявляли.
Данный пример иллюстрирует, что терапия препаратом Целлекс значительно уменьшает выраженность морфологических изменений в почках, обеспечивая нефропротективный эффект.
Пример 5
Уменьшение выраженности морфологических изменений в яичках при введении Цисплатин на фоне терапии препаратом Целлекс в соответствии с заявляемым способом.
Проведенные опыты соответствовали протоколу исследований как в примере 4. Через 14 дней удаляли яички и сравнивали выраженность морфологических изменений между контрольной группой (введение Цисплатин) и опытной группой (введение Цисплатин с терапией Целлексом). Морфометрический анализ проводили на срезах канальцев круглой или близкой к круглой форме, что отражает размер их поперечного сечения.
В нормальных яичках тестикулярные канальцы были окружены четко выраженной базальной мембраной, на которой был расположен плотный слой клеток Сертоли в количестве 10-12 на 100 мкм мембраны. Средняя площадь поперечного сечения канальцев составила 92±2 мкм2. Герминативный эпителий был представлен 5 слоями клеток в разной стадии развития с наличием зрелых сперматозоидов в просвете канальца (Фиг. 2а). В контрольных опытах через 14 суток после введения Цисплатин базальная мембрана и герминативный эпителий выглядели дезинтегрированными, местами отслоенный от базальной мембраны. Число клеток Сертолли на 100 мкм длины мембраны не превышало 8 клеток. Средняя площадь поперечного сечения канальцев составила 62±2 мкм2, что было достоверно меньше нормы (p<0,001). Число слоев геминативного эпителия во многих канальцах уменьшалось до 3. В просвете многих канальцев выявлялись дегенерирующие клетки. Интерстициальное пространство между канальцами выглядело расширенным, вакуолизированным (Фиг. 2 б). В опытной серии с терапией Целлексом гистологическая картина яичек приближалась к норме, хотя часть канальцев была все же изменена. Средняя площадь поперечного сечения канальцев составила 79±4 мкм2, что, хотя и было меньше нормы, но достоверно превышало этот показатель для контрольной серии опытов (p<0,01). Число клеток Сертолли на 100 мкм базальной мембраны было такое же, как в норме (9-10 клеток). Интерстиций выглядел малоизмененным (Фиг. 2 в).
Данный пример иллюстрирует выраженное уменьшение морфологических изменений в семенных канальцах, вызванное токсическим действием Цисплатин.
Таким образом, приведенные примеры доказывают эффективность заявляемого способа уменьшения нефротоксичности и гонадотоксичности химиопрепарата Цисплатин.
Преимуществами заявляемого способа являются:
- комплексное воздействие препарата на основные звенья патогенеза нефротоксического действия химиотерапевтического средства Цисплатин, а именно его противовоспалительное действие, ингибирование апоптоза, а также стимуляция процессов регенерации поврежденных клеток под действием факторов роста и стимуляторов клеточной пролиферации, входящих в состав секретома стволовых клеток;
- оказание протективного эффекта как в отношении почки (профилактика нефротоксичности), так и в отношении яичек (профилактика гонадотоксичности);
- полное отсутствие побочных эффектов терапии, присущих другим фармакологическим препаратам, используемым с целью уменьшения цитотоксичности Цисплатин.
Предложенный способ позволит повысить эффективность химиотерапии больных раком различной локализации, а также уменьшить негативные отдаленные последствия химиотерапии на сексуальную и репродуктивную функцию мужчин.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ терапии и профилактики прогрессирования хронической почечной недостаточности | 2021 |
|
RU2763661C2 |
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ОСТРОЙ ПОСТИШЕМИЧЕСКОЙ ПОЧЕЧНОЙ НЕДОСТАТОЧНОСТИ | 2020 |
|
RU2737802C2 |
| ЖИРНЫЕ КИСЛОТЫ И ГЛИЦЕРИДЫ СО СРЕДНЕЙ ДЛИНОЙ ЦЕПИ В КАЧЕСТВЕ НЕФРОПРОТЕКТИВНЫХ СРЕДСТВ | 2008 |
|
RU2519215C2 |
| СПОСОБ СОЧЕТАННОЙ ТЕРАПИИ СОЕДИНИТЕЛЬНОТКАННОЙ САРКОМЫ М-1 КРЫС С ИСПОЛЬЗОВАНИЕМ КОНЬЮГАТА ДИПРОПОКСИБАКТЕРИОПУРПУРИНА С ДОКСОРУБИЦИНОМ | 2023 |
|
RU2808909C1 |
| СПОСОБ ПРОФИЛАКТИКИ НЕФРОТОКСИЧЕСКОГО ДЕЙСТВИЯ ХРОМА У КРЫС В ЭКСПЕРИМЕНТЕ | 2022 |
|
RU2793548C1 |
| СПОСОБ ПРОФИЛАКТИКИ НЕФРОТОКСИЧЕСКОГО ДЕЙСТВИЯ СУРЬМЫ У КРЫС В ЭКСПЕРИМЕНТЕ | 2023 |
|
RU2815874C1 |
| СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ И КОРРЕКЦИИ НАРУШЕНИЙ СПЕРМАТОГЕНЕЗА, ВЫЗВАННОГО ЦИТОСТАТИЧЕСКИМ ВОЗДЕЙСТВИЕМ | 2006 |
|
RU2318529C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ СОЧЕТАННОГО МЕДИКАМЕНТОЗНОГО ПОРАЖЕНИЯ СЕРДЦА И ПОЧЕК У КРЫС | 2019 |
|
RU2726927C1 |
| СПОСОБ ЛЕЧЕНИЯ ПЛОСКОКЛЕТОЧНОГО Р-16 ПОЗИТИВНОГО РАКА РОТОГЛОТКИ | 2020 |
|
RU2751818C2 |
| СПОСОБ ЛЕЧЕНИЯ ПЕРЕВИВНОЙ СОЕДИНИТЕЛЬНОТКАННОЙ САРКОМЫ М-1 КРЫС ПРИ КОМБИНИРОВАННОМ ВОЗДЕЙСТВИИ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ И ЛУЧЕВОЙ ТЕРАПИИ | 2021 |
|
RU2763663C2 |
Изобретение относится к медицине, а именно к профилактике нефротоксического и гонадотоксического действия Цисплатина в эксперименте. С первого дня химиотерапии проводят ежедневный внутримышечный 10-дневный курс терапии препаратом Целлекс в дозе 0,1 мл/кг. Предложенный способ позволит повысить эффективность химиотерапии больных раком различной локализации, а также уменьшить негативные отдаленные последствия химиотерапии на сексуальную и репродуктивную функцию мужчин. 2 ил., 2 табл., 5 пр.
Способ профилактики развития нефротоксического и гонадотоксического эффектов химиопрепарата Цисплатин в эксперименте, включающий использование фармакологических препаратов, отличающийся тем, с первого дня химиотерапии проводят ежедневный внутримышечный 10-дневный курс терапии препаратом Целлекс в дозе 0,1 мл/кг.
| СПОСОБ ПРОФИЛАКТИКИ ОСЛОЖНЕНИЙ ХИМИОТЕРАПИИ ПРИ ЛЕЧЕНИИ ОНКОЛОГИЧЕСКОГО ЗАБОЛЕВАНИЯ | 2005 |
|
RU2308956C2 |
| СПОСОБ СНИЖЕНИЯ ТОКСИЧНОСТИ ХИМИОТЕРАПИИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ | 2001 |
|
RU2201260C1 |
| Способ терапии и профилактики прогрессирования хронической почечной недостаточности | 2021 |
|
RU2763661C2 |
| US 2014147516 A1, 29.05.2014 | |||
| WO 2010014651 A1, 04.02.2010 | |||
| Громова Е.Г | |||
| и др | |||
| Практические реко мендации по коррекции нефротоксичности противоопухолевых препаратов | |||
| Злокачественные опухоли: Практические рекомендации | |||
| RUSSCO | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| Малеев О.В | |||
Авторы
Даты
2025-05-16—Публикация
2024-10-30—Подача