Изобретение относится к области биологии, в частности к описанию модельной системы для обеспечения оптимальных условия последующего процесса слияния клеток посредством воздействия внешнего электрического поля с контролируемыми значениями длины импульса и его амплитуды. Данная модель может быть применима для медико-биологических и агротехнологических исследований.
Методика электрослияния получила свою известность в 1979 году, когда Сенда и его соавторы продемонстрировали слияние протопластов дрожжей под действием электрических полей [Senda M, J Takeda, S Abe, T Nakamura. Induction of cell fusion of plant protoplasts by electrical stimulation. Plant Cell Physiol 20: 1441-1443 (1979)]. Сильные стороны метода электрослияния заключаются в том, что это простая и быстрая технология, по сравнению с хемосинтезом (ПЭГ и Ca2+) или использованием промежуточных стадий (диэлектрофорез, центрифугирование). Также он универсален для всех видов клеток, несмотря на размер клеток и особенности структуры мембраны.
Первые эксперименты по электрослиянию растительных клеток – протопластов – придерживались двум основным концепциям: 1) подача одного мощного импульса 5–12 мкА, 2) выстраивание клеток в цепочки за счет низковольтного быстроколеблющегося переменного поля (100 В/см, 0,6 МГц), после чего слияние индуцируется применением нескольких коротких импульсов постоянного тока высокого напряжения (800 В/см, длительность 15 мкс) [Zimmerman U., Scheurich P. High frequency fusion of plant protoplasts by electric fields. Planta 151, 26-32 (1981)]. Открытие явления электропорации, т.е. увеличение проницаемости мембран за счет образования дефектов нанометрового размера в ответ на импульсы высокого напряжения, позволило продвинуться в понимании механизма порообразования, но механизм слияния клеток оставался недостаточно исследованным.
Традиционно в технологии электрослияния клеток применялись мили- и микросекундные импульсные источники, что сильно сужало вариативность объектов исследования, так как эффективность таких импульсов зависела от размера клеток. С развитием технологических мощностей и расширением диапазона импульсов до наносекунд, продвинуло технологию электрослияния на новый уровень.
На сегодняшний день, исследования, представленные в этой области, в основном сконцентрированы на выборе полярности импульсов [Патент CN109628438B], подборе соотношений микро- и наносекундных импульсов [Патент CN106834272B] или созданию специализированных ячеек [Патент US20130089931A1]. Однако отсутствие предсказательных моделей не дает возможность определить оптимальные условия для контролируемого электрослияния клеток.
Техническим результатом заявленного изобретения является увеличение вероятности электрослияния без паразитной электропорации.
Технический результат заявленного изобретения достигается тем, что для электрослияния клеток (животных, растений, грибов и бактерий), на основе параметров ячейки для электрослияния и самих клеток строится геометрическая модель по данным микроскопии. В данной модели клетки могут иметь как простую форму шара, так и более сложную. Для построенной геометрической модели проводится компьютерное моделирование электрических полей на мембранах клеток при воздействии импульсов различных длительностей и амплитуды, после чего выбираются те значения напряжения и длительности импульса, при которых достигается максимальное соотношение плотности пор в области контакта клеток к плотности пор на противоположных полюсах клеток.
Сущность заявленного изобретения поясняется подробным описанием, примером и фигурами, на которых изображено:
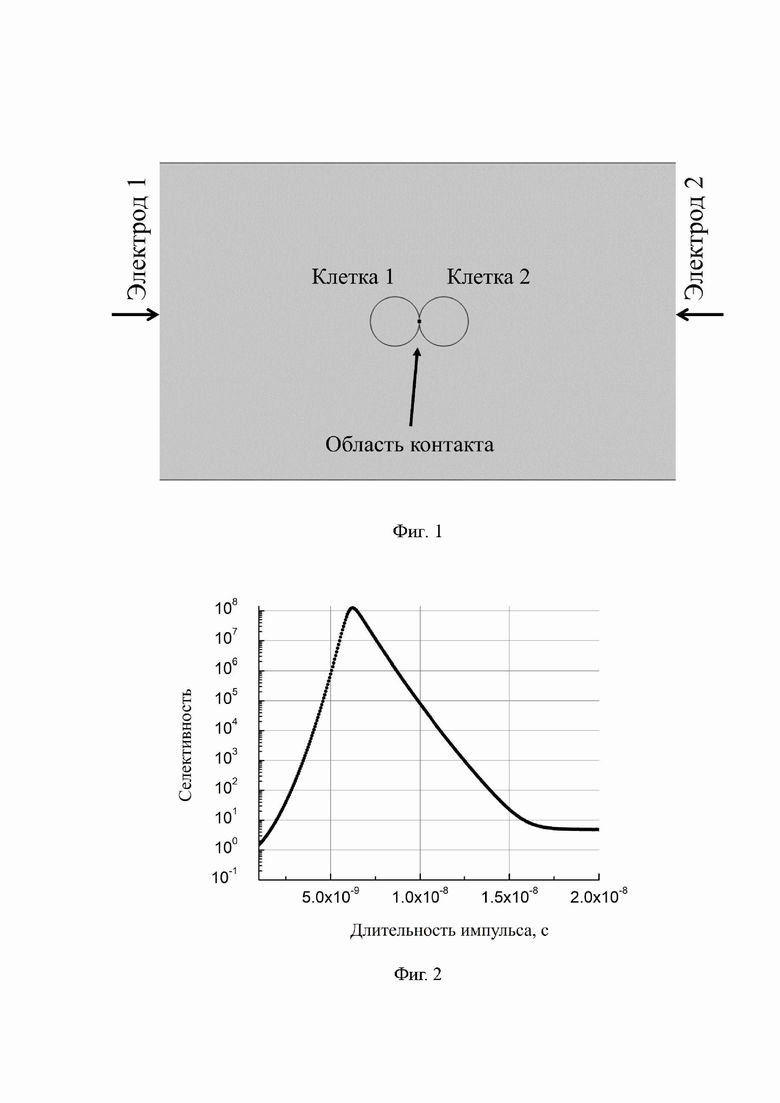
фиг. 1 – Геометрическая модель электрослияния;
фиг. 2 – Зависимость селективности от длины импульса с амплитудой 1500 В.
На основе данных о размере клеток, электрических свойств буфера и общей геометрии ячейки для слияния, предлагается следующая модель.
1) Геометрическая модель
Геометрическая модельстроится на основании знаний о геометрии ячейки для электрослияния, в частности, о форме электродов и расстоянии между ними. Форма клеток, их размер и геометрия области контакта определяются из данных микроскопии. Геометрические модели клеток размещаются равноудаленно от электродов.
2) Электрическая модель мембраны
Для моделирования мембрана представлялась как тонкий слой, ток через который описывался с помощью уравнения [Pucihar, G., Miklavcic, D. & Kotnik, T. A time-dependent numerical model of transmembrane voltage inducement and electroporation of irregularly shaped cells. IEEE Trans. Biomed. Eng. 56, 1491–1501 (2009)]:
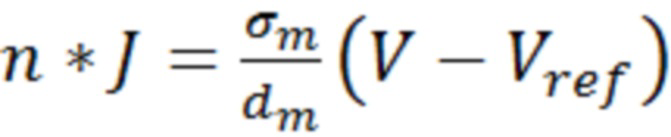 +
+
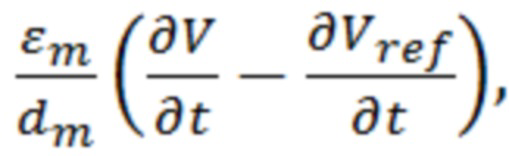
где, n – вектор нормали к поверхности мембраны, J – плотность тока, V – электрический потенциал на внутренней границе мембраны, 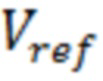 - электрический потенциал на внешней границе мембраны.
- электрический потенциал на внешней границе мембраны.
3) Электрический потенциал
Потенциал в каждом домене модели (цитоплазма, внеклеточная среда) был подсчитан с использованием следующего уравнения:
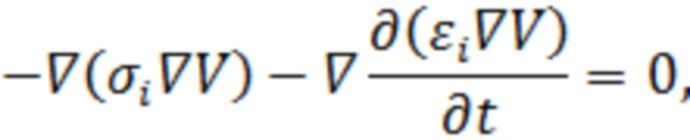
где 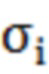 и
и 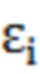 - проводимость и диэлектрическая проницаемость соответствующего домена.
- проводимость и диэлектрическая проницаемость соответствующего домена.
4) Проводимость мембраны
При моделировании проводимость мембраны принималась как сумма пассивной проводимости 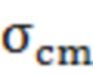 и проводимости, обусловленной электропорацией
и проводимости, обусловленной электропорацией 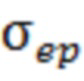 [Li, J. & Lin, H. The current-voltage relation for electropores with conductivity gradients. Biomicrofluidics 4, 013206 (2010)]:
[Li, J. & Lin, H. The current-voltage relation for electropores with conductivity gradients. Biomicrofluidics 4, 013206 (2010)]:
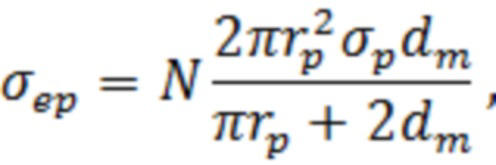
где 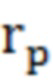 - средний радиус пор,
- средний радиус пор, 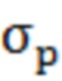 - проводимость поры,
- проводимость поры, 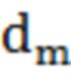 - толщина мембраны, N – поровая плотность.
- толщина мембраны, N – поровая плотность.
5) Поровая плотность
Для расчета поровой плотности вдоль мембраны используется следующее дифференциальное уравнение [DeBruin, K. A. & Krassowska, W. Modeling electroporation in a single cell. I. Effects of field strength and rest potential. Biophys. J. 77, 1213–1224 (1999)]:
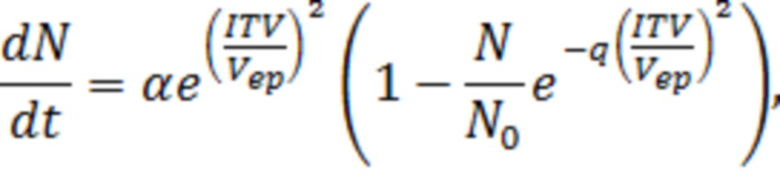
где ITV – разность потенциалов на мембране, N – поровая плотность, Vep – характерное напряжение электропорации, α – коэффициент нуклеации пор, N0 – равновесная поровая плотность, q – коэффициент скорости роста поры, t – время.
6) Система, приведенных выше уравнений решается согласованно методом конечных элементов с шагом по времени менее 10 нс. На границе электродов задается временная зависимость напряжения с формой импульса, соответствующей используемому оборудованию для электрослияния. Расчет повторяют для электрических импульсов различных форм, длительностей и напряжений.
7) Для оценки эффективности электрослияния вводится параметр селективности, представляющий собой отношение плотности пор на мембране в центре границы контакта к плотности пор на противоположном полюсе клетки. Таким образом, чем выше значение селективности, тем выше вероятность электрослияния без паразитной электропорации клетки.
Пример приложения:
Клетки представляют собой окружности радиусом 7.75 мкм, область контакта клеток является общей хордой двух окружностей и имеет длину 2 мкм. Расстояние между электродами равно 200 мкм. Обе клетки помещены во внешнюю среду как показано на фигуре 1.
Значения диэлектрической проницаемости (ε) и проводимости (σ) для внеклеточной среды принимаются равными 70 и 0.01 См/м, а для внутриклеточной среды 80 и 0.25 См/м, соответственно. Для мембраны вне области контакта значения пассивной проводимости, диэлектрической проницаемости, толщины были равны 5·10−7 См/м, 4,5 и 5·10−9 м, соответственно. Длина импульса варьировалась в пределах от 1 до 20 нс для напряжения 1500 В.
На фигуре 2 приведена расчетная зависимость селективности от длительности импульса. Из приведенных расчетов можно сделать вывод, что при воздействии импульсами с амплитудой 1500 В и длительностью 6.3 нс можно ожидать максимальную вероятность электрослияния без паразитной электропорации.
Результатом данной модели является возможность двухстороннего подбора оптимальных условий для проведения электрослияния с известным размером клеток и состава буфера. Во-первых, для существующих мощностей генераторов импульсов подбирать оптимальную геометрию ячейки. Во-вторых, для стандартных ячеек вычислять оптимальные характеристики длины и амплитуды импульсов.
| название | год | авторы | номер документа |
|---|---|---|---|
| УСТРОЙСТВО ДЛЯ ЭЛЕКТРОСТИМУЛИРУЕМОГО СЛИЯНИЯ КАРИОПЛАСТОВ С ЦИТОПЛАСТАМИ | 2008 |
|
RU2390560C1 |
| СПОСОБ ЛАЗЕРНОГО СЛИЯНИЯ БЛАСТОМЕРОВ ВНУТРИ РАННИХ ДОИМПЛАНТАЦИОННЫХ ЭМБРИОНОВ МЛЕКОПИТАЮЩИХ БЕЗ НАРУШЕНИЯ ИХ ЦЕЛОСТНОСТИ | 2012 |
|
RU2495932C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИБРИДНОЙ СТВОЛОВОЙ КЛЕТКИ ЧЕЛОВЕКА | 2007 |
|
RU2352637C1 |
| СИСТЕМА ДЛЯ КЛИНИЧЕСКОГО ПРИМЕНЕНИЯ ЭЛЕКТРОПОРАЦИИ С ОБРАТНОЙ СВЯЗЬЮ, УПРАВЛЯЮЩЕЙ НАПРЯЖЕНИЕМ | 1995 |
|
RU2141853C1 |
| СИСТЕМА С ВЫСОКИМ ИМПЕДАНСОМ ДЛЯ ГЕНЕРИРОВАНИЯ ЭЛЕКТРИЧЕСКИХ ПОЛЕЙ И СПОСОБ ЕЕ ИСПОЛЬЗОВАНИЯ | 2006 |
|
RU2408006C2 |
| СПОСОБ ЛЕЧЕНИЯ С ВВЕДЕНИЕМ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ И ГЕНОВ ПОСРЕДСТВОМ ЭЛЕКТРОПОРАЦИИ | 1996 |
|
RU2168337C2 |
| Штамм гибридных культивируемых клеток Homo sapiens/Mus musculus 1B9C7 - продуцент человеческих моноклональных антител, специфичных к протеолитическому домену ботулинического токсина типа A | 2021 |
|
RU2783897C1 |
| Штамм гибридных культивируемых клеток H.sapiens/Mus musculus 8D4E9-Ba-LF-продуцент человеческих моноклональных антител против летального фактора возбудителя сибирской язвы | 2018 |
|
RU2699193C1 |
| СПОСОБ ВЫЯВЛЕНИЯ ПОВРЕЖДЕНИЯ МЕМБРАН ЭРИТРОЦИТОВ | 2012 |
|
RU2487356C1 |
| СПОСОБ, СИСТЕМА И СКВАЖИННЫЙ ПРИБОР ДЛЯ ОЦЕНКИ ПРОНИЦАЕМОСТИ ПЛАСТА | 2007 |
|
RU2419819C2 |
Изобретение относится к области биотехнологии, в частности к модельной системе для обеспечения оптимальных условий последующего процесса слияния клеток посредством воздействия внешнего электрического поля с контролируемыми значениями длины импульса и его амплитуды. Данная модель может быть применима для медико-биологических и агротехнологических исследований. Технический результат заявленного изобретения достигается тем, что для электрослияния клеток (животных, растений, грибов и бактерий) на основе параметров ячейки для электрослияния и самих клеток строится геометрическая модель по данным микроскопии. Техническим результатом заявленного изобретения является увеличение вероятности электрослияния без паразитной электропорации. 2 ил., 1 пр.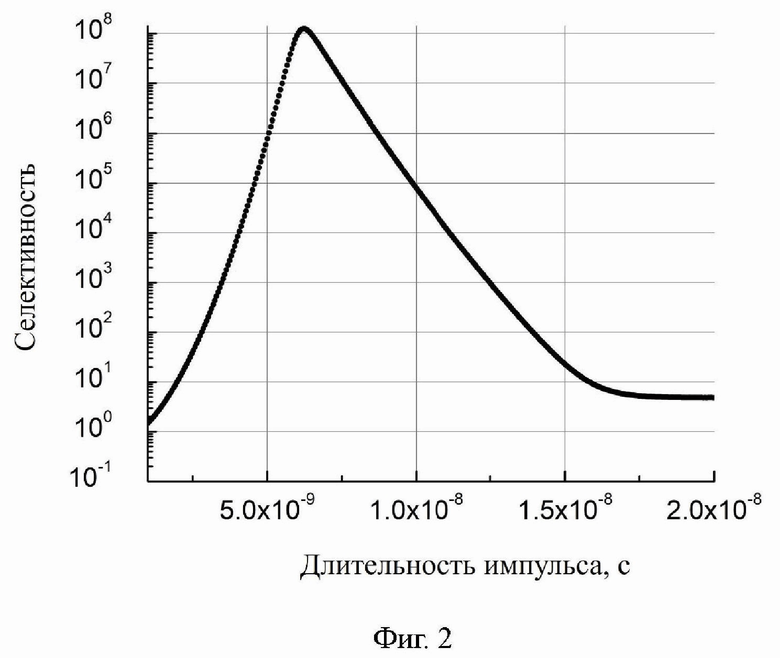
Способ подбора параметров напряжения и длительности импульсов для электрослияния клеток, характеризующийся тем, что на основе формы электродов и расстояния между ними, определяемых из микроскопии формы клеток и геометрии области контакта клеток, методом конечных элементов решается система уравнений электрического потенциала, проводимости мембраны и поровой плотности при воздействии импульсов различных длительностей и амплитуды, после чего выбираются те значения напряжения и длительности импульса, при которых достигается максимальное соотношение плотности пор в области контакта клеток к плотности пор на противоположных полюсах клеток.
| SHERIF S | |||
| et al | |||
| Theoretical analysis for the fluctuation in the electric parameters of the electroporated cells before and during the electrofusion, Med Biol Eng Comput, 2022, vol | |||
| Способ получения молочной кислоты | 1922 |
|
SU60A1 |
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| АРТИЛЛЕРИЙСКИЙ СНАРЯД С РИФЛЕНОЙ НАРУЖНОЙ ПОВЕРХНОСТЬЮ | 1922 |
|
SU3585A1 |
| ONOHARA I | |||
| et al | |||
| Electrofusion of cells with different diameters by generating asymmetrical electric field in the microwell array, Anal | |||
Авторы
Даты
2025-05-19—Публикация
2024-04-17—Подача