Изобретение относится к области медицины, а именно производственной и клинической трансфузиологии, и может быть использовано для оценки гемостатического потенциала концентратов тромбоцитов, заготовленных с помощью аппаратного афереза или путем пулирования тромбоцитных фракций, выделенных из цельной дозы крови.
Изобретение может быть использовано в комплексе с другими тестами для исследования системы гемостаза с целью диагностики нарушений процессов свертывания крови и контроля эффективности проводимых лечебных мероприятий, а также в экспериментальной медицине при испытании новых антиагрегационных фармакологических препаратов.
В настоящее время наблюдается устойчивый рост потребления концентратов тромбоцитов (КТ) в клинике с целью профилактики и лечения критической тромбоцитопении и тромбоцитопенической кровоточивости. Широкое использование КТ неизбежно ставит необходимость адекватной оценки их качества с целью отбора наиболее качественных доз как для трансфузий, так и для длительного хранения и создания банка тромбоцитов. Оценка качества заготавливаемых КТ согласно Постановлению Правительства РФ от 22 июня 2019 года №797 «Об утверждении Правил заготовки, хранения, транспортировки и клинического использования донорской крови и ее компонентов и о признании утратившими силу некоторых актов Правительства РФ» производится на основании показателей безопасности, включающих объем дозы, содержание тромбоцитов, остаточное содержание лейкоцитов, значение рН и стерильность (кроме патоген-редуцированных КТ). Эти параметры не отражают функциональную полноценность тромбоцитов в КТ и их гемостатический потенциал. В связи с этим активно ведется поиск аппаратных методов оценки качества КТ, доступных в общеклинической практике, не требующих редкого или уникального оборудования. В научно-исследовательской практике для определения функциональной активности тромбоцитов КТ используют методы агрегометрии [Рожков Е.В., Кожемяко О.В., Понасенко М.А., Карасева И.А., Рожкова Н.С., Мадзаев С.Р., Жибурт Е.Б. Совершенствование производства концентрата пулированных патогенредуцированных тромбоцитов. Трансфузиология. 2022; 23(1): 16-21], однако такой подход требует использования специальных индукторов активации, не позволяет оценить взаимный эффект активации тромбоцитов и плазменных компонентов гемостаза. Для интегральной оценки коагулогических параметров наиболее оптимальным считается метод тромбоэластографии (ТЭГ).
Известен способ оценки функционального потенциала тромбоцитов с помощью тромбоэластографии на аппарате РОТЕМ (ротационная тромбоэластометрия) [Ярец Ю.И. Тромбоэластография: основные показатели, интерпретация результатов / Ю.И. Ярец, - Гомель: ГУ «РНПЦ РМиЭЧ», 2018. - 26 с. ]. После внесения активатора начинают вращение кюветы с пробой, по мере образования фибриновых нитей и сгустка происходит передача вращающего момента на аналитический стержень, по характеру отклонения которого оценивают интенсивность работы компонентов свертывания, включая тромбоциты. Однако данный способ предназначен для работы с цельной кровью и не содержит алгоритмов исследования аферезных или пулированных КТ, характеризующихся разным функциональным потенциалом тромбоцитов, при этом для оценки активности тромбоцитов используют параметры, которые также зависят от других факторов свертывания, что вносит определенные погрешности в результаты измерений.
Наиболее близким к заявляемому является способ оценки гемостатической активности тромбоцитов с помощью аппарата TEG-5000 [RU2601111. Опубл. 27.10.2016, Бюл. № 30]. Предложенный способ основан на оценке гемостатической активности тромбоцитов в крови, в богатой тромбоцитами плазме или в КТ путем сравнения двух, параллельно получаемых тромбоэластограмм от двух одинаково подготовленных проб, или разделения на две части одной подготовленной пробы, и включает регистрацию показателей тромбоэластограммы, проведение сравнения одноименных данных в виде отношения результата в пробе с раствором кальция и раствором аденозиндифосфата (АДФ) к результату в пробе с раствором кальция, разведенным дистиллированной водой, в соотношении 2:1. В каждой пробе определяют стандартные показатели тромбоэластограммы: время реакции (R, мин), время образования сгустка / фазу усиления, мин (K, мин), угол (Angle, градусы), максимальную амплитуду тромбоэластограммы (МА, мм). Затем производят сравнение показателей R, K, Angle, МА в пробе с раствором кальция и раствором АДФ и в пробе с раствором кальция, разведенным дистиллированной водой в соотношении 2:1. Конечные результаты, отражающие изменение R, K, Angle, МА под действием АДФ (ΔR, ΔK, ΔAngle и ΔМА), выражают в %. Значения показателей ΔAngle и ΔМА более 22,0% при значениях ΔR и ΔK не более 11,1% свидетельствует о повышенной способности тромбоцитов к агрегации и образованию сгустка. Значения показателей ΔAngle и ΔМА менее 11,1% при значениях ΔR и ΔK более 22,0% свидетельствует о низкой способности тромбоцитов к агрегации и образованию сгустка. Значения ΔAngle и ΔМА от 11,1% до 22,0% свидетельствуют о нормальной способности тромбоцитов к агрегации и образованию сгустка. Способ позволяет повысить диагностическую значимость оценки функциональных свойств тромбоцитов в процессе свертывания крови и формирования сгустка на основании измерения количественных параметров тромбоэластограммы.
Однако данный способ при тестировании КТ не учитывает влияние эритроцитов на вязкость среды и ее тромбоэластографические характеристики, требует дополнительных реагентов для активации тромбоцитов, не позволяет смоделировать функциональный ответ тромбоцитов КТ после их трансфузии в кровь донора, не учитывает повреждение и спонтанную активацию тромбоцитов при разведении проб дистиллированной водой, не содержит точной формулы расчета изменения параметров ТЭГ для оценки функционального потенциала тромбоцитов, не позволяет использовать полученные характеристики КТ для оценки гемостатического потенциала КТ, не позволяет сортировать КТ с высоким и низким функциональным потенциалом, содержит противоречивые данные по трактовке функционального потенциала тромбоцитов с помощью параметров ТЭГ.
Таким образом, для повышения точности ТЭГ-оценки функционального потенциала КТ, предназначенных для трансфузии, существенное значение имеет среда, в которой находятся исследуемые тромбоциты (КТ), которая по своим характеристикам должна соответствовать цельной крови человека, т.к. все основные параметры, определяемые в ходе тромбоэластографии и определяющие активность гемостаза, рассчитаны на работу с кровью [Буланов А.Ю., Прасолов Н.В., Яцков К.В. Тромбоэластография в практике анестезии и интенсивной терапии в акушерстве. Клинические рекомендации. Протоколы лечения. Москва]. Из уровня техники не известны способы оценки качества тромбоцитов КТ методом тромбоэластографии в среде, аналогичной цельной крови по своим биологическим и физико-химическим характеристикам.
Технической проблемой является разработка способа оценки качества тромбоцитов КТ методом тромбоэластографии в среде, аналогичной цельной крови.
Раскрытие сущности изобретения
Техническим результатом, на достижение которого направлено заявленное изобретение, является разработка способа оценки гемостатического потенциала концентрата тромбоцитов (КТ) методом тромбоэластографии в среде, аналогичной цельной крови, который отражает истинную функциональную активность тромбоцитов КТ в условиях in vivo. Таким образом, при осуществлении заявленного способа возможно проведение сортировки и отбора КТ с высоким гемостатическим потенциалом тромбоцитов, позволяющих при их использовании повысить эффективность купирования геморрагического синдрома и проведения профилактических трансфузий.
Технический результат достигается способом оценки гемостатического потенциала концентрата тромбоцитов (КТ) с помощью тромбоэластографии, включающим отбор исследуемой пробы КТ, подготовку пробы КТ для проведения исследований методом тромбоэластографии (ТЭГ) с последующей регистрацией процесса образования сгустка в образце с помощью ТЭГ.
Отличие заявленного способа от известных заключается в подготовке пробы КТ для проведения исследований методом ТЭГ, которую проводят в несколько этапов: на первом этапе отбирают образец цельной донорской венозной крови, имеющей аналогичную исследуемому КТ группу крови, и характеризующейся количественным содержанием тромбоцитов в границах нормы (которые могут быть определены в соответствии с Приложением N 6 к Порядку прохождения донорами медицинского обследования, утвержденному приказом Минздрава России от 28 октября 2020 г. N 1166н), часть образца цельной донорской венозной крови используют в качестве положительного контроля при проведении ТЭГ, а из оставшейся части цельной донорской венозной крови на следующих этапах сначала получают образец венозной крови без тромбоцитов, часть которого в свою очередь используют в качестве отрицательного контроля при проведении ТЭГ, а затем оставшуюся часть образца венозной крови без тромбоцитов смешивают с отобранной исследуемой пробой КТ в соотношении 9:1 с последующим добавлением раствора хлористого кальция,
после чего в полученных трех образцах донорской венозной крови - для положительного контроля, для отрицательного контроля, и содержащего пробу исследуемого КТ, методом ТЭГ определяют максимальную амплитуду тромбоэластограммы (МА), мм, фазу усиления (k), мин, по которым рассчитывают коэффициент восстановления гемостатической функции HR,
при получении значения HR > 95% и k < 4 мин гемостатический потенциал КТ считают высоким (характеризующимся высокой способностью тромбоцитов к агрегации и образованию сгустка), при HR от 75% до 95% и k < 4 - нормальным (характеризующимся нормальной способностью тромбоцитов к агрегации и образованию сгустка), при HR < 75% или HR < 95% и k > 4 - низким (характеризующимся низкой способностью тромбоцитов к агрегации и образованию сгустка).
Коэффициент восстановления гемостатической функции HR может быть определен по формуле:
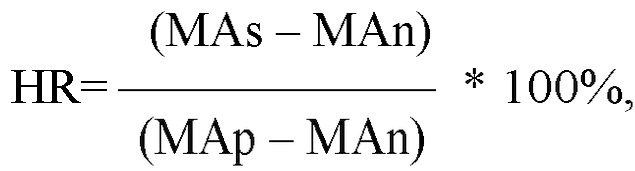
где МАs - максимальная амплитуда образца донорской венозной крови, содержащей пробу КТ; MAn - максимальная амплитуда образца донорской венозной крови для отрицательного контроля - не содержащей тромбоциты; MAp - максимальная амплитуда образца цельной донорской венозной крови для положительного контроля с содержанием тромбоцитов в норме.
Для получения образца донорской венозной крови без тромбоцитов для отрицательного контроля при проведении ТЭГ, соответствующую часть образца донорской цельной венозной крови пропускают через лейкоцитарно-тромбоцитарный фильтр.
КТ с высоким гемостатическим потенциалом рекомендуют для лечебных трансфузий (купирование геморрагического синдрома), КТ с нормальным гемостатическим потенциалом рекомендуют для профилактических трансфузий, КТ с низким гемостатическим потенциалом не рекомендуются для трансфузий.
Краткое описание чертежей
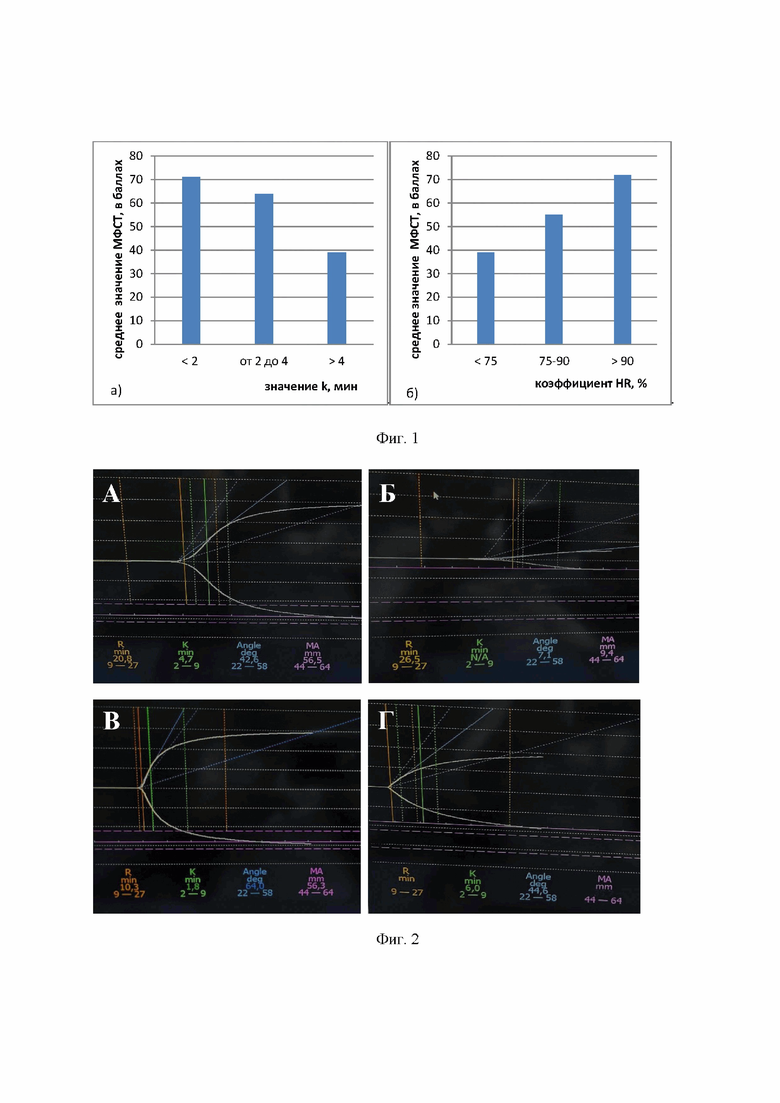
Изобретение поясняется чертежами, где на фиг. 1 представлена взаимосвязь морфофункционального статуса тромбоцитов (МФСТ) с длительностью времени k (а) и коэффициента восстановления гемостатической функции HR (б); на фиг. 2 представлены ТЭГ-кривые, отражающие гемостатическую активность разных образцов крови. А - исходная кровь донора (положительный контроль); Б - кровь донора, фильтрованная через тромбоцитарный фильтр, без тромбоцитов (отрицательный контроль); В - фильтрованная кровь донора, совмещенная с КТ, имеющим высокий гемостатический потенциал тромбоцитов (HR=99%, k=1,8 мин); Г - фильтрованная кровь донора, совмещенная с КТ, имеющим низкий гемостатический потенциал тромбоцитов (HR=67%, k=6,0 мин).
Осуществление изобретения
Способ осуществляют следующим образом.
1. Из исследуемых доз аферезных или пулированных КТ отбирают пробы объемом 100-500 мкл.
2. У доноров той же группы крови, что и у доноров исследуемых КТ, в ходе стандартной процедуры донации из кубитальной вены забирают кровь в стандартные пробирки объемом 4-5 мл с консервантом (раствором натрия цитрата 3,2%). Для получения крови без тромбоцитов образцы цельной консервированной крови, заготовленной у тех же доноров, пропускают через лейкоцитарно-тромбоцитарный фильтр и отбирают 2 мл в стерильный пластиковый контейнер.
3. Смешивают фильтрованную кровь доноров и исследуемый образец КТ в соотношении 9:1.
4. Отбирают 340 мкл фильтрованной крови доноров, содержащей тромбоциты КТ, в пластиковую одноразовую кювету, добавляют 20 мкл 0,2 М раствора хлористого кальция и проводят стандартное ТЭГ-исследование. Параллельно проводят стандартное ТЭГ-исследование исходной крови тех же доноров (положительный контроль) и фильтрованной крови доноров без тромбоцитов (отрицательный контроль). В исследуемых образцах определяют максимальную амплитуду (МА), мм и фазу усиления (k), мин.
5. Рассчитывают коэффициент восстановления гемостатической функции HR по формуле:
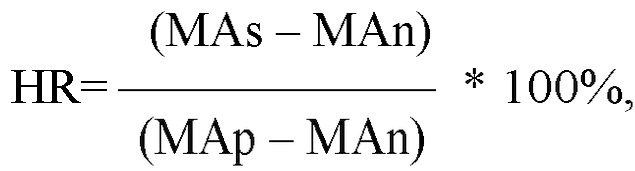
где МАs - максимальная амплитуда фильтрованной крови с добавленным КТ
MAn - максимальная амплитуда фильтрованной крови и MAp - максимальная амплитуда цельной донорской крови.
6. В зависимости от величины коэффициента HR и значений k оценивают гемостатический потенциал КТ. При значениях HR > 95% и k < 4 мин гемостатический потенциал КТ считают высоким, при HR от 75% до 95% и k < 4 - нормальным, при HR < 75% или HR < 95% и k > 4 - низким. КТ с высоким гемостатическим потенциалом рекомендуются для лечебных трансфузий (купирование геморрагического синдрома), КТ с нормальным гемостатическим потенциалом рекомендуются для профилактических трансфузий, КТ с низким гемостатическим потенциалом не рекомендуются для трансфузий.
Заявленный способ был разработан по результатам проведенных исследований.
На первом этапе проводили ТЭГ-исследование образцов консервированной крови доноров, содержащей нормальное количество тромбоцитов, и не содержащей тромбоцитов. У доноров в ходе стандартной процедуры донации из кубитальной вены забирали кровь в стандартные пробирки объемом 4-5 мл с консервантом цитратом. Для получения крови без тромбоцитов образцы цельной консервированной крови, заготовленной у тех же доноров, пропускали через лейкоцитарно-тромбоцитарный фильтр и отбирали 2 мл в стерильный пластиковый контейнер. Концентрация тромбоцитов в исходной крови составила 206 [180; 250]х109/л, в крови после лейкоцитарно-тромбоцитарной фильтрации - 3 [1; 7]х109/л.
Для проведения тромбоэластографического исследования (ТЭГ) 340 мкл крови смешивали с 20 мкл 0,2 М раствора хлористого кальция в одноразовой пластиковой кювете и помещали в анализатор. Анализ проводили на анализаторе Hemoscope Thrombelastograph в программе TEG Analitical Software 4,3. Оценивали следующие параметры: R (время реакции, мин) - время от начала исследования до начала свертывания крови, оценивается по возникновению первых отклонений тромбоэластограммы от прямой линии, норма 9-27 мин; k (фаза усиления/время образования сгустка, мин) - время от начала движений стержня прибора до момента, когда амплитуда тромбоэластограммы составит 20 мм, норма 2-9 мин; Angle (угол касательной к кривой, градусы) - характеризует скорость образования фибринового сгустка, норма 22-58 градусов; MA (максимальная амплитуда ТЭГ в мм) - отражает общие физические свойства сгустка, норма 44-64 мм. В тромбоэластографии для характеристики активности тромбоцитарного звена используется максимальная амплитуда (МА). При переливании концентратов тромбоцитов пациентам также рекомендуется оценивать параметр k. При увеличении активности тромбоцитов отмечается рост МА и снижение/укорочение k, при снижении активности тромбоцитов - соответственно падение МА и удлинение k.
В образцах цельной крови с нормальным содержанием тромбоцитов значения МА составили 56 [54; 58] мм, значения k - 4 [3; 6] мин, что соответствовало нормальным показателям ТЭГ. В образцах крови доноров, фильтрованной через лейкоцитарно-тромбоцитарный фильтр и практически не содержащей тромбоцитов, отмечены очень низкие значения параметров ТЭГ. Значения МА варьировали от 8 до 19 мм, медиана составила 13 [9;15] мм, параметр k в 85% образцов не определялся, что указывает на очень низкую активность тромбоцитов или ее отсутствие. По данным клинических наблюдений, при таких значениях ТЭГ для нормализации гемостаза пациента рекомендуется трансфузия 2 доз концентратов тромбоцитов [Буланов А.Ю. Роль тромбоэластографии в трансфузионной терапии посттравматической коагулопатии. Трансфузиология. 2011. Т. 12. № 4. С. 47-55]. Соотношение общего объема циркулирующей крови и объема переливаемых КТ при этом составляет 9:1. Поэтому такое соотношение было использовано для совмещения фильтрованной крови и тромбоцитов КТ для оценки их активности in vitro с помощью ТЭГ.
При исследовании аферезных и пулированных КТ использовали образцы цельной и фильтрованной крови доноров той же группы, что и у доноров КТ. 450 мкл крови доноров, фильтрованной через лейкоцитарно-тромбоцитарный фильтр, смешивали с 50 мкл концентрата тромбоцитов (соотношение 9:1). Далее 340 мкл полученной смеси добавляли в пластиковую одноразовую кювету, где смешивали с 20 мкл 0,2 М раствора хлористого кальция и помещали в анализатор. Одновременно проводили стандартное ТЭГ-исследование исходной и фильтрованной крови тех же доноров.
Для оценки функционального потенциала тромбоцитов в КТ было предложено оценивать изменение параметра МА между пробой исходной крови доноров и пробой фильтрованной крови после внесения в нее КТ и параметр k в пробе фильтрованной крови после внесения в нее КТ. Для оценки изменения МА предложен коэффициент восстановления гемостатической функции HR, который рассчитывают по формуле:
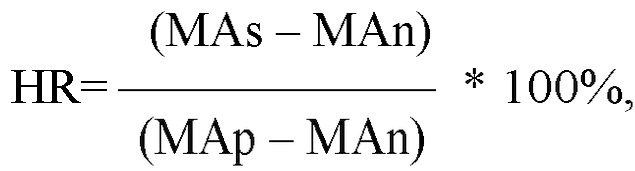
где, МАs - максимальная амплитуда фильтрованной крови с добавленным КТ, MAn - максимальная амплитуда фильтрованной крови без тромбоцитов и MAp - максимальная амплитуда цельной донорской крови.
Морфофункциональный анализ тромбоцитов проводили с помощью метода, основанного на исследовании витально окрашенных клеток с помощью флуоресцентной микроскопии [Макаров М.С., Хубутия М.Ш., Хватов В.Б., Высочин И.В., Кобзева Е.Н., Конюшко О.И. Способ оценки морфофункционального статуса тромбоцитов человека. Патент РФ № 2485502; заявл. 17.02.2012; опубл. 20.06.2013.-Бюл. № 17.- 7с.]. В тромбоцитной популяции тромбоциты с гранулами являются структурно и функционально полноценными клетками, играют решающую роль в стимуляции адгезивной и агрегационной активности тромбоцитов. Оценивали общую концентрацию тромбоцитов в КТ, 109/л; уровень тромбоцитов с гранулами в КТ, % (норма 35-75%); концентрацию тромбоцитов с гранулами в КТ, 109/л; морфофункциональный статус тромбоцитов, МФСТ (норма 75-130 баллов). При статистической обработке данных вычисляли медиану, 1-й и 3-й квартили, для оценки различий результатов использовали критерий Манна-Уитни. Различия считали достоверным при уровне значимости более 95% (р<0,05).
В работе использовали аферезные и пулированные КТ, которые предварительно хранились на шейкере при 20-22°C. Во всех случаях с момента забора тромбоцитов у донора до начала анализа КТ проходило 2 суток. В образцах аферезных КТ концентрация тромбоцитов составляла 1200 [1075; 1240]х109/л, уровень тромбоцитов с гранулами - 40 [32; 45]%, концентрация тромбоцитов с гранулами - 520 [420; 530] х109/л, МФСТ - 82 [76; 92] балла, в ПулКТ эти значения составляли 870 [800; 1030]х109/л, 22 [17; 25]%, 180 [150; 196]х109/л и 47 [45; 50] баллов соответственно. В аферезных КТ концентрация тромбоцитов с гранулами была в среднем в 2,8 раза выше, чем в ПулКТ (р<0,05). Тем не менее, аферезные КТ и ПулКТ проявляли сходную функциональную активность при ТЭГ-исследовании (табл. 1). Это может быть связано с повышенным содержанием в ПулКТ тромбоцитов на ранней стадии активации или в состоянии предактивации, с наличием в ПулКТ свободных тромбоцитарных гранул, которые также обладают гемостатической активностью. В то же время и аферезных КТ, и в ПулКТ наблюдалась высокая вариабельность показателей МА и k. Особо стоит отметить, что после внесения в фильтрованную кровь КТ наблюдалось заметное укорочение времени k. Так, если в цельной крови время k составляло в среднем 4,5±1,0 мин, то после добавления КТ к фильтрованной крови время k укорачивалось до 2,0±0,5 мин. Выявлена корреляционная связь между концентрацией тромбоцитов с гранулами в КТ и значениями k и МА: коэффициент корреляции Спирмена составил -0,392 (р=0,006) и 0,463 (р=0,001), соответственно; между МФСТ и значениями k и МА - -0,402 (р=0,005) и 0,496 (р=0,001), соответственно. Кроме того, выявлена обратная корреляция между показателями k и МА, то есть чем больше максимальная амплитуда, тем короче время k, коэффициент Спирмена = - 0,616 при р= 0,001. Таким образом, МА и k отражают качество тромбоцитов в концентратах. Зависимость коэффициента восстановления гемостатической функции HR, времени k и МФСТ представлена на фиг. 1а и 1б.
Таблица 1. Оценка гемостатического потенциала концентратов тромбоцитов (КТ) разных типов с помощью тромбоэластографии
На втором этапе необходимо было определить референтные значения параметров ТЭГ, определяющие общий функциональный потенциал КТ и их клиническую эффективность. Проводили ТЭГ-исследование аферезных и пулированных КТ, которые использовались в клинической трансфузиологии для купирования или профилактики геморрагического синдрома у пациентов со следующими патологиями: цирроз печени, механическая желтуха, энцефалопатия с септическими осложнениями, трансплантация сердца, сочетанная цереброваскулярная патология с септическими осложнениями, ишемия головного мозга, аневризма грудного отдела аорты. Все примененные дозы КТ не вызывали осложнений после трансфузии. В процессе анализа было установлено, что для купирования кровоточивости и получения эффективного прироста тромбоцитов через 24 часа после трансфузии наиболее эффективны КТ с коэффициентом восстановления гемостатической функции HR более 95 % при длительности времени k менее 4 минут. (Таблица 2).
Таблица 2. Оценка клинического эффекта КТ с разными параметрами функциональной активности
(по шкале ВОЗ)
В результате были получены следующие референтные значения коэффициента восстановления гемостатической функции HR и времени k для оценки гемостатического потенциала КТ с помощью тромбоэластографии. При значениях HR > 95% и k < 4 мин гемостатический потенциал КТ считают высоким, при HR от 75% до 95% и k < 4 - нормальным, при НR < 75% или НR < 95% и k > 4 - низким. КТ с высоким гемостатическим потенциалом рекомендуются для лечебных трансфузий (купирование геморрагического синдрома), КТ с нормальным гемостатическим потенциалом рекомендуются для профилактических трансфузий, КТ с низким гемостатическим потенциалом не рекомендуются для трансфузий.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРИГОТОВЛЕНИЯ ЛИЗАТА ТРОМБОЦИТОВ С ВЫСОКИМ СОДЕРЖАНИЕМ ФАКТОРОВ РОСТА | 2020 |
|
RU2739515C1 |
| СПОСОБ ОЦЕНКИ ГЕМОСТАТИЧЕСКОЙ АКТИВНОСТИ ТРОМБОЦИТОВ | 2015 |
|
RU2601111C1 |
| СПОСОБ ОЦЕНКИ СОСТОЯНИЯ СВЕРТЫВАЮЩЕЙ СИСТЕМЫ КРОВИ У ПАЦИЕНТОВ, НАХОДЯЩИХСЯ В КРИТИЧЕСКОМ СОСТОЯНИИ | 2012 |
|
RU2517116C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ДЕФОРМИРУЕМОСТИ ЭРИТРОЦИТОВ | 2025 |
|
RU2838363C1 |
| СПОСОБ ПОДГОТОВКИ КРИОКОНСЕРВИРОВАННЫХ ТРОМБОЦИТОВ ДЛЯ ТРАНСФУЗИИ | 2016 |
|
RU2623864C1 |
| СПОСОБ ОТБОРА ТРОМБОЦИТОВ ЧЕЛОВЕКА, ПРИГОДНЫХ ДЛЯ КРИОКОНСЕРВИРОВАНИЯ | 2015 |
|
RU2623073C1 |
| СПОСОБ КРИОКОНСЕРВИРОВАНИЯ ТРОМБОЦИТОВ | 2016 |
|
RU2623081C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ТРОМБОФИБРИНОВОГО СГУСТКА, ОБЛАДАЮЩЕГО РОСТСТИМУЛИРУЮЩИМИ СВОЙСТВАМИ | 2018 |
|
RU2679616C1 |
| Способ выявления гепарина в крови | 2017 |
|
RU2662171C1 |
| СПОСОБ ОЦЕНКИ ФУНКЦИОНАЛЬНОГО СОСТОЯНИЯ СИСТЕМЫ ГЕМОСТАЗА | 1992 |
|
RU2063037C1 |
Изобретение относится к медицине, а именно к производственной и клинической трансфузиологии, и может быть использовано для оценки гемостатического потенциала концентрата тромбоцитов (КТ). Осуществляют отбор исследуемой пробы КТ. Отбирают образец цельной донорской венозной крови, имеющей аналогичную исследуемому КТ группу крови. Часть образца цельной донорской венозной крови используют в качестве положительного контроля при проведении тромбоэластографии (ТЭГ), часть образца венозной крови без тромбоцитов используют в качестве отрицательного контроля при проведении ТЭГ, часть смешивают с отобранной исследуемой пробой КТ в соотношении 9:1 с последующим добавлением раствора хлористого кальция. Определяют максимальную амплитуду тромбоэластограммы и фазу усиления (k), по которым рассчитывают коэффициент восстановления гемостатической функции HR. При HR > 95% и k < 4 гемостатический потенциал КТ считают высоким, при HR от 75% до 95% и k < 4 – нормальным, при HR < 75% или HR < 95% и k > 4 – низким. Способ обеспечивает эффективную оценку гемостатического потенциала КТ методом тромбоэластографии в среде, аналогичной цельной крови, с возможностью проведения сортировки и отбора КТ с высоким гемостатическим потенциалом тромбоцитов за счет определения коэффициента восстановления гемостатической функции HR. 2 з.п. ф-лы, 2 ил., 2 табл., 11 пр.
1. Способ оценки гемостатического потенциала концентрата тромбоцитов (КТ), включающий отбор исследуемой пробы КТ, подготовку пробы КТ для проведения исследований методом тромбоэластографии (ТЭГ) с последующей регистрацией процесса образования сгустка в образце с помощью ТЭГ, отличающийся тем, что подготовку пробы КТ для проведения исследований методом ТЭГ проводят в несколько этапов: на первом этапе отбирают образец цельной донорской венозной крови, имеющей аналогичную исследуемому КТ группу крови и характеризующейся количественным содержанием тромбоцитов в границах нормы, часть образца цельной донорской венозной крови используют в качестве положительного контроля при проведении ТЭГ, а из оставшейся части цельной донорской венозной крови на следующих этапах сначала получают образец венозной крови без тромбоцитов, часть которого в свою очередь используют в качестве отрицательного контроля при проведении ТЭГ, а затем оставшуюся часть образца венозной крови без тромбоцитов смешивают с отобранной исследуемой пробой КТ в соотношении 9:1 с последующим добавлением раствора хлористого кальция,
после чего в полученных трех образцах донорской венозной крови – для положительного контроля, для отрицательного контроля и содержащего пробу исследуемого КТ методом ТЭГ определяют максимальную амплитуду тромбоэластограммы (МА), мм, фазу усиления (k), мин, по которым рассчитывают коэффициент восстановления гемостатической функции HR,
при получении значения HR > 95% и k < 4 мин гемостатический потенциал КТ считают высоким - характеризующимся высокой способностью тромбоцитов к агрегации и образованию сгустка, при HR от 75% до 95% и k < 4 – нормальным - характеризующимся нормальной способностью тромбоцитов к агрегации и образованию сгустка, при HR < 75% или HR < 95% и k > 4 – низким - характеризующимся низкой способностью тромбоцитов к агрегации и образованию сгустка.
2. Способ по п.1, отличающийся тем, что коэффициент восстановления гемостатической функции HR определяют по формуле
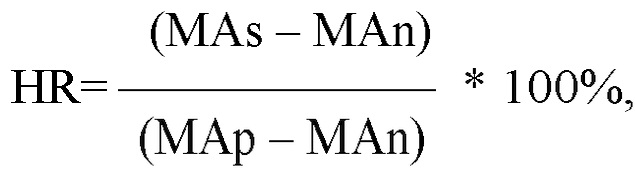
где МАs – максимальная амплитуда образца донорской венозной крови, содержащей пробу КТ; MAn – максимальная амплитуда образца донорской венозной крови для отрицательного контроля, не содержащей тромбоциты; MAp – максимальная амплитуда образца цельной донорской венозной крови для положительного контроля с содержанием тромбоцитов в норме.
3. Способ по п.1, отличающийся тем, что для получения образца донорской венозной крови без тромбоцитов для отрицательного контроля при проведении ТЭГ соответствующую часть образца донорской цельной венозной крови пропускают через лейкоцитарно-тромбоцитарный фильтр.
| СПОСОБ ОЦЕНКИ ГЕМОСТАТИЧЕСКОЙ АКТИВНОСТИ ТРОМБОЦИТОВ | 2015 |
|
RU2601111C1 |
| US 12072310 B2, 27.08.2024 | |||
| ФАНАСКОВА Е.В | |||
| и др | |||
| Низкочастотная пьезотромбоэластография в комплексной оценке гемостаза при операциях коронарного шунтирования в условиях искусственного кровообращения | |||
| Клин | |||
| мед | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
Авторы
Даты
2025-05-19—Публикация
2025-01-18—Подача