Изобретение относится к области биотехнологии и медицины, а именно к способу получения биокомпозита на основе гидрогеля бактериальной целлюлозы с коллагеном, обладающего высокой абсорбционной способностью, а также ранозаживляющим и антибактериальным действием, и может быть использовано в качестве раневого покрытия в медицине и ветеринарии.
Покрытия, применяемые с целью заживления раневых повреждений тканей, становятся более многофункциональными. В настоящее время ведется разработка состава и технологии медицинских материалов, представляющих собой текстильные и полимерные композиции, содержащие субстанции различные по своим фармакологическим свойствам.
Известно достаточно много разнообразных покрытий, предназначенных для лечения ран и ожоговых поверхностей, изготовленных на основе вспомогательных веществ, природного или синтетического происхождения, с введенными в них лекарственными веществами. Перспективным вспомогательным веществом для получения раневых покрытий следует считать целлюлозу бактериального происхождения (бактериальная целлюлоза).
Известны различные способы получения бактериальной целлюлозы, представленные в изобретениях RU 2536973, МПК C12N 1/20, опубл. 27.12.2014, RU 2536257, МПК C12N 1/20, опубл. 20.12.2014, RU 2597291 C1, опубл. 10.09.2016.
Известен способ получения раневого покрытия, обеспечивающего сохранность оптимальной влажности и газопроницаемости, необходимые для создания благоприятных условий процесса заживления и изолирования поврежденной поверхности от воздуха. Покрытие из бактериальной целлюлозы является небиодеградируемым, что позволяет легко отделять его от раны. Способ получения покрытия включает культивирование бактерий Gluconacetobacter sucrofermentans ВКПМ В-11267 на мелассе, получения гидрогеля бактериальной целлюлозы и смешивание с 2% раствором хитозана в 1%-ой уксусной кислоте (соотношение 50:50) или с 2% раствором хитозана в 1%-ой уксусной кислоте, 10% раствором желатина, 20% раствором трансглютаминазы (соотношение 5:5:15:5), добавление фузидина натрия, ферментов, низкомолекулярных пептидов (CA 2632767, МПК А61К 37/715, опубл. 07.06.2007).
Недостатком указанного способа получения раневого покрытия является сложность получения композиции на основе гидрогеля бактериальной целлюлозы, полученной в результате культивирования бактерий Gluconacetobacter sucrofermentans, и однонаправленность действия полученного покрытия за счет введения антибактериального средства фузидина натрия.
Предложен способ получения биокомпозита с антибактериальными свойствами на основе гидрогеля бактериальной целлюлозы, включающий культивирование Komagataeibacter sucrofermentans ВКПМ B-11267 в статических условиях на среде с мелассой, отделение полученной гель-пленки бактериальной целлюлозы от культуральной среды, ее очищение; затем гель-пленку механически измельчают с получением гидрогеля бактериальной целлюлозы с гидромодулем с соотношением 1:3 и вносят антибиотик фузидина натрия или фермент лизоцима в концентрации 7,5 мг/мл и 1 мг/мл гидрогеля соответственно. (RU 2771864 С1, опубл. 13.05.2022).
Указанное средство характеризуется сложностью получения композита на основе гидрогеля бактериальной целлюлозы, полученной в результате культивирования Komagataeibacter sucrofermentans.
Известно биологически активное раневое покрытие с использованием клеточного материала человека, изготовленное путем нанесения на гидратированную микробную целлюлозу коллагенового геля, который содержит десятикратный концентрат ростовой среды M199 и источник ростовых факторов, например, тромбоциты крови и /или клетки мезодермального и эктодермального типа, а также может содержать антибиотики, например, смесь антибиотиков пенициллин от 50 до 100 единиц/мл и стрептомицин от 0,05 до 0,1 мг/мл. (RU 2430743, МПК A61L 15/28, A61F 13/02, A61L 15/44, опубл. 10.10.2011).
Недостатком способа получения раневого покрытия является сложность получения, необходимость введения большого количества ингридиентов, в том числе антибиотиков пенициллина и стрептомицина, к которым быстро развивается устойчивость микроорганизмов.
Известен биоактивный гидрогель для регенерации кожи, полученный посредством химической сшивки желатина глутаровым диальдегидом. Данный гидрогель характеризуется пониженным содержанием и расходом сшивающего агента, пониженной остаточной токсичностью сшивающего агента, повышенной биосовместимостью, повышенной регенеративной активностью. Биоактивный гидрогель дополнительно содержит анионный полимер и бивалентный металл в конечной концентрации не более 50 мМ (RU 2659383, МПК A61K 38/17, опубл. 29.06.2018).
Известен способ получения биокомпозита с регенерационными свойствами на основе гидрогеля бактериальной целлюлозы. Биокомпозит представляет собой гидрогель бактериальная целлюлоза-хитозан в соотношениях 50:50 путем смешения 2%-го раствора хитозана в 1%-ой уксусной кислоте, гидрогеля бактериальной целлюлозы, 25%-го глутарового альдегида, а также получении гидрогеля бактериальная целлюлоза:хитозан:желатин:трансглютаминаза в соотношении 5:5:15:5 соответственно и добавлением фузидина натрия, физиологически активных соединений полифенольной природы в виде дегидрокварцетина или ресвератрола, ферментов в виде трипсина, химотрипсина или лизоцима, низкомолекулярных пептидов (RU 2733137, МПК C12N 1/20, A61L 15/36, опубл. 29.09.2020).
Недостатками известного решения является сложность композиционного состава и сложность технологического процесса.
Наиболее близким решением, взятым в качестве прототипа, является способ получения биокомпозита на основе аэрогеля бактериальной целлюлозы, обладающего кровоостанавливающими свойствами. Получение аэрогеля заключается в получении гель-пленки бактериальной целлюлозы путем культивирования штамма бактерий Gluconacetobacter sucrofermentans ВКПМ В-11267 в статических условиях на среде с мелассой, отделении и ее очищении, измельчении и получения аэрогелей путем лиофильной сушки гидрогелей бактериальной целлюлозы с 2%-ым раствором хитозана в 1%-й уксусной кислоте (в соотношении 80:20) и добавления фузидина натрия (RU 2736061 C1, МПК A61K 35/74, A61K 47/36, A61L 15/28, A61L 15/18, C12N 1/20, A61P 7/04, опубл. 11.11.2020).
Предложенный аэрогель обладает однонаправленностью действия и сложен в техническом исполнении.
Задачей предлагаемого изобретения, является создание нового способа получения раневого покрытия на основе гидрогеля бактериальной целлюлозы.
Технический результат заявленного изобретения заключается в создании способа получения раневого покрытия на основе гидрогеля бактериальной целлюлозы, обладающего высокой абсорбционной способностью, а также ранозаживляющим и антибактериальным действием.
Сущность изобретения заключается в том, что способ получения раневого покрытия в виде биокомпозита на основе гидрогеля бактериальной целлюлозы заключается в получении гель-пленки бактериальной целлюлозы путем культивирования штамма бактерий, ее отделении и очищении, измельчении и лиофильной сушки, в которую внесены следующие новые признаки:
- для получения гель-пленки бактериальной целлюлозы осуществляют культивирование штамма бактерий Medusomyces gisevii в статических условиях на комплексной жидкой питательной среде в течение 7 суток при комнатной температуре;
- комплексная жидкая питательная среда для культивирования биомассы из Medusomyces gisevii содержит следующие ингредиенты, масс.%: глюкоза – 0,99; сахароза – 0,99; дрожжевой экстракт – 0,99; пептон – 0,69; лимонная кислота – 0,02; ледяная уксусная кислота – 0,099 и этанол – 1,32, вода очищенная – до 100; причем для приготовления сначала в воде очищенной растворяют глюкозу, сахарозу, дрожжевой экстракт, пептон и лимонную кислоту, затем полученный раствор автоклавируют при 115°С в течение 30 мин и после охлаждения добавляют при перемешивании этанол и ледяную уксусную кислоту;
- после отделения гель-пленки от питательной среды осуществляют её очищение путем обработки 0,1 Н раствором NaOH при нагревании на водяной бане до 90°C в течение 60 мин, после чего образцы замачивают в 3% растворе перекиси водорода при комнатной температуре в течение 1,5-2 часов, после чего промывают водой очищенной до достижения нейтральной реакции и измельчают с помощью гомогенизатора механического;
- после измельчения гель-плёнку перемешивают до получения гомогенной массы однородной консистенции в соотношении 1:1 с водным раствором активных и вспомогательных ингредиентов, взятых из расчета содержания в граммах на 100 квадратных сантиметров раневого покрытия: коллаген – 0,2, метронидазол – 0,2, бетациклодекстрин – 0,2, декспантенол – 0,5, бензалкония хлорид – 0,05, при этом указанный раствор изготавливают при нагревании до 70°С, путем последовательного растворения в воде очищенной сначала бета-циклодекстрина и метронидазола, а коллаген, декспантенол и бензалкония хлорид растворяют после охлаждения полученного водного раствора;
- полученную массу распределяют на подложку слоем толщиной 8 мм, выдерживают в морозильной камере при температуре минус 40°С в течение суток, после чего высушивают в лиофильной сушилке в течение 24 часов по следующей программе:
1) 5 минут – температура лиофилизации минус 40°С, давление 1 мбар, без нагрева полок;
2) 18 часов – температура лиофилизации минус 40°С, давление 0,2 мбар, температура полок 30°С;
3) 4 часа – температура лиофилизации минус 40°С, давление 0,15 мбар, температура полок 40°С;
4) 2 часа – температура лиофилизации минус 40°С, давление 0,1 мбар, температура полок 50°С.
В качестве продуцента бактериальной целлюлозы в заявленном изобретении использована симбиотическая культура Medusomyces gisevii, положительными характеристиками которой являются высокая адаптивная способность, устойчивость к фагам, способность саморегулировать уровень активной кислотности в процессе ее культивирования, которая формирует матрицу-носитель из тонкой сети нановолокон, обладающая высокой влагосвязывающей и влагоудерживающей способностью, селективной проницаемостью для газов и пара, отсутствием проницаемости для бактерий (интернет-источник: https://cyberleninka.ru/article/n/biosintez-bakterialnoy-tsellyulozy-kulturoy-medusomyces-gisevii/viewer).
Коллаген обеспечивает гемостатическое действие, снижает воспалительные реакции, активизирует репаративные процессы и сокращает сроки заживления ран.
Декспантенол обладает дерматопротективным, противовоспалительным, стимулирующим регенерацию действием. Восполняет дефицит пантотеновой кислоты, обладает противовоспалительным действием, стимулирует процессы регенерации. В организме образует активный метаболит – пантотеновую кислоту, являющуюся субстратным (единственный незаменимый компонент) стимулятором синтеза кофермента A; последний катализирует в организме ацилирование, участвует практически во всех метаболических процессах (цикл трикарбоновых кислот, обмен углеводов, жиров и жирных кислот, фосфолипидов, белков и др.), обеспечивает образование кортикостероидов, ацетилирование холина с образованием ацетилхолина. При местном применении быстро абсорбируется и превращается в пантотеновую кислоту, связывается с белками плазмы (главным образом с бета-глобулином и альбумином). Стимулирует регенерацию кожи.
Метронидазол относится к антибактериальным химиотерапевтическим препаратам, обладает высокой активностью в отношении широкого спектра бактерий и простейших. Механизм действия метронидазола заключается в биохимическом восстановлении 5-нитрогруппы внутриклеточными транспортными протеинами анаэробов и простейших. Восстановленная 5-нитрогруппа взаимодействует с ДНК микроорганизмов и ингибирует ее синтез, приводя к подавлению роста и гибели патогенной микрофлоры.
Бета-циклодекстрин – вспомогательное вещество, обладающее солюбилизирующей активностью, повышает растворимость труднорастворимых в воде препаратов за счет гидрофильной наружной оболочки, увеличивает биодоступность, снижает раздражающее действие веществ на слизистые оболочки.
Бензалкония хлорид – антисептическое средство, как катионный детергент встраивается в клеточную оболочку, взаимодействует с мембранными липопротеидами микроорганизмов, повреждает мембраны и вызывает гибель клеток. Проявляет бактерицидную активность в отношении различных грамположительных (в т.ч. стафилококки, стрептококки) и грамотрицательных (кишечная и синегнойная палочка, протей, клебсиелла и др.) микроорганизмов, фунгицидную – в отношении грибов.
Изложенные характеристики активных и вспомогательных веществ позволяют обеспечить высокую абсорбционную способность, а также ранозаживляющее и антибактериальное действие предлагаемого состава раневого покрытия в виде биокомпозита на основе бактериальной целлюлозы.
Заявленное изобретение обладает новизной и изобретательским уровнем, т.к. из уровня техники неизвестен способ получения раневого покрытия путем культивирования биомассы из Medusomyces gisevii с использованием питательной среды следующего состава, масс.%: глюкоза – 0,99; сахароза – 0,99; дрожжевой экстракт – 0,99; пептон – 0,69; лимонная кислота – 0,02; ледяная уксусная кислота – 0,099 и этанол – 1,32, вода очищенная – до 100; причем для приготовления сначала в воде очищенной растворяют глюкозу, сахарозу, дрожжевой экстракт, пептон и лимонную кислоту, затем полученный раствор автоклавируют при 115°С в течение 30 мин и после охлаждения добавляют при перемешивании этанол и ледяную уксусную кислоту. Использование для культивирования указанного состава позволяет увеличить прирост биомассы на 60%, что значительно превышает прирост на других средах (таблица 1).
Таблица 1
Сравнительная характеристика питательных сред для получения бактериальной целлюлозы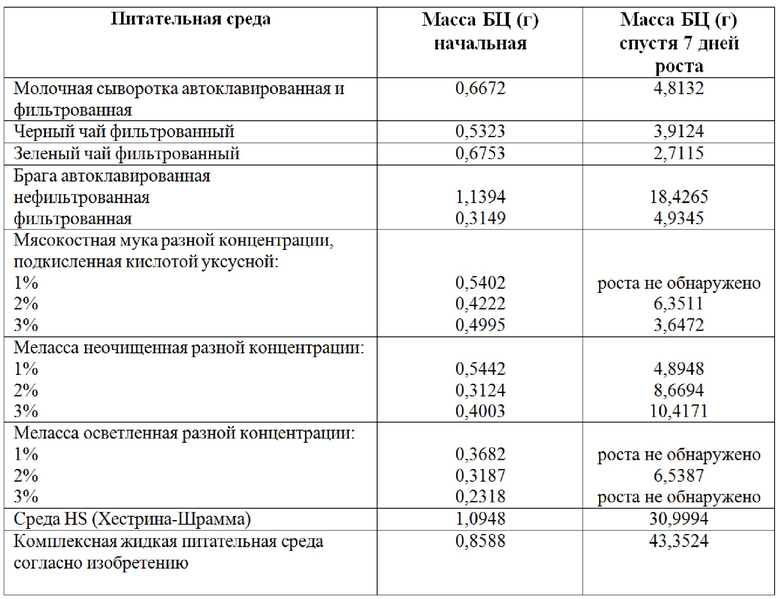
Способ получения раневого покрытия репаративного и антибактериального действия на основе гидрогеля бактериальной целлюлозы с коллагеном осуществляют следующим образом.
Пример 1. Получение гель-пленки бактериальной целлюлозы
Получают гель-пленку бактериальной целлюлозы путем культивирования симбиотической культуры Medusomyces gisevii на комплексной жидкой питательной среде следующего состава: глюкоза – 3,0; сахароза – 3,0; дрожжевой экстракт – 3,0; пептон – 2,1; лимонная кислота – 0,06; вода очищенная – до метки 300 мл; далее раствор автоклавируют при 115°С в течение 30 мин, после автоклавирования добавляют этанол 4 мл и ледяную уксусную кислоту – 300 мкл. В питательную среду добавляют Medusomyces gisevii в количестве 1,0 грамм, культивируют в течение 7 суток при комнатной температуре.
После отделения гель-пленки от питательной среды осуществляют её очищение путем удаления клеток и компонентов культуральной среды, для чего проводят её обработку 0,1 Н раствором NaOH при нагревании на водяной бане до 90°C в течение 60 мин, после чего образцы замачивают в 3% растворе перекиси водорода при комнатной температуре в течение 1,5-2 часов и промывают водой очищенной до достижения нейтральной реакции. Полученные очищенные гель-пленки бактериальной целлюлозы подвергают измельчению до однородной массы с помощью гомогенизатора механического.
Пример 2. Формирование раневого покрытия
Для формирования 100 см2 раневого покрытия изготавливают водный раствор ингридиентов при нагревании до 70°С, путем последовательного растворения в 25 мл воды очищенной 0,2 г бета-циклодекстрина, 0,2 г метронидазола, полученный водный раствор охлаждают и в нем растворяют 0,2 г коллагена, 0,5 г декспантенола и 0,05 г бензалкония хлорида.
Изготавливают гидромодуль измельченной бактериальной целлюлозы с водным раствором ингридиентов в соотношении 1:1 путем перемешивания до получения гомогенной массы однородной консистенции.
Полученную массу распределяют на подложку размером 10×10 см слоем толщиной 8 мм, выдерживают в морозильной камере при температуре минус 40°С в течение суток, после чего высушивают в лиофильной сушилке (модель АК 5-40) в течение 24 часов по следующей программе:
1) 5 минут – температура лиофилизации минус 40°С, давление 1 мбар, без нагрева полок;
2) 18 часов – температура лиофилизации минус 40°С, давление 0,2 мбар, температура полок 30°С;
3) 4 часа – температура лиофилизации минус 40°С, давление 0,15 мбар, температура полок 40°С;
4) 2 часа – температура лиофилизации минус 40°С, давление 0,1 мбар, температура полок 50°С.
Полученное раневое покрытие по внешнему виду представляет собой легкую пористую пластину желтоватого цвета размером 10×10 см.
Пример 3. Изучение ранозаживляющей активности.
Изучение ранозаживляющей активности средства, полученного по примеру №2 проводили в эксперименте на крысах-самцах породы «Вистар» массой 180-200 г, у которых моделировали гнойную рану по методике П.И. Толстых (1976). Экспериментальные животные были разделены на две группы по 36 животных в каждой: в 1-й контрольной группе лечение не проводили, во 2-й опытной группе проводили лечение предлагаемым средством один раз в сутки в течение первых 5 дней течения раневого процесса. Течение раневого процесса у экспериментальных животных оценивали планиметрическим методом Л.И. Поповой по площади заживления раневой поверхности. Применение раневого покрытия повышает скорость заживления раневой поверхности: на 3-и сутки при использовании средства отмечается слабая инфильтрация свежих грануляций лейкоцитами, на 10-е сутки происходит восстановление кожи – наползание эпителиального вала с краев раны, на 14-е сутки рана эпителизирована, наблюдалось практически полное восстановление кожи (таблица 2).
Таблица 2
Ранозаживляющая активность
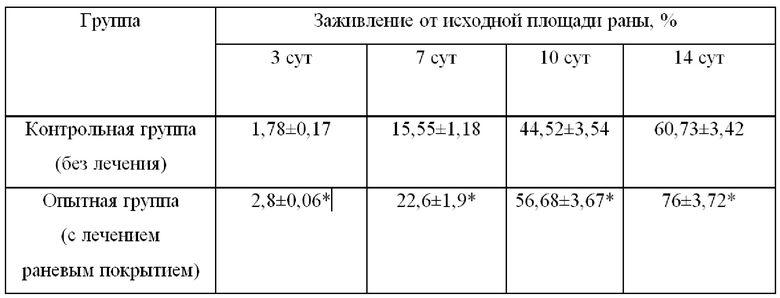
Примечание: – p<0,05 в сравнении с группой контроля на соответствующие сутки.
Пример 4 Изучение антибактериальной активности в отношении Staphylococcus aureus АТСС 6538-Р
Антибактериальные свойства полученного средства по примеру 2 определяли методом, основанным на способности антибактериальных веществ диффундировать в агаровую среду и образовывать зоны задержки роста тест-культуры. В качестве тест-микроорганизма используют бактерии Staphylococcus aureus АТСС 6538-Р. В центр чашки Петри, засеянной тест-культурой, помещают раневое покрытие размером 0,5×0,5 см. Зона отсутствия роста тест-культуры при использовании предложенного раневого покрытия, составила 19,3±2,1 мм. При этом обнаружен рост микроорганизмов при использовании раневого покрытия, полученного путем культивирования штамма бактерий Medusomyces gisevii, без добавления активных и вспомогательных ингредиентов.
Пример 5. Изучение адсорбирующей способности
Образцы раневого покрытия, полученного по примеру 2, с фиксированной массой помещали на фильтровальную бумагу и перемещали в чашки Петри с 10 мл воды очищенной. Затем через 5 мин переносили образец вместе с фильтровальной бумагой в центрифужную пробирку и центрифугировали при 3000 об/мин в течение 10 мин. Поглощение рассчитывали по формуле 1:
Ia = (mt - mo) / mo ⋅ 100%, (1)
где mt – масса образца покрытия после выдержки, г;
mo – начальная масса образца покрытия , г.
Результаты определения абсорбирующей способности представлены в таблице 3. Исходя из полученных результатов, следует, что исследуемые образцы проявляют хорошую влагосвязывающую способность. Соотношение полученного покрытия и поглощенной воды и составляет 1:10.
Таблица 3
Изучение абсорбирующей способности

Таким образом, предложенный способ позволяет получить раневое покрытие на основе бактериальной целлюлозы, обладающее абсорбирующей способностью, ранозаживляющим и антибактериальным действием, которое может применяться в медицине и ветеринарии. При этом, учитывая широкий спектр антибактериального и антимикробного действия, входящих в состав покрытия метронидазола и бензалкония хлорида, можно предполагать наличие соответствующей активности у раневого покрытия, полученного по предложенному способу.
Предлагаемое изобретение позволит расширить ассортимент раневых покрытий полифакторного действия.
| название | год | авторы | номер документа |
|---|---|---|---|
| Раневое покрытие | 2024 |
|
RU2834836C1 |
| Биосовместимая матрица на основе бактериальной целлюлозы и пептидов природного происхождения для активизации репаративных процессов поврежденных тканей | 2023 |
|
RU2824664C1 |
| Способ получения биокомпозиционных материалов с регенеративными и антисептическими свойствами на основе гидрогелей бактериальной целлюлозы | 2023 |
|
RU2814059C1 |
| Способ получения биокомпозита на основе аэрогеля бактериальной целлюлозы, обладающего кровоостанавливающими свойствами | 2019 |
|
RU2736061C1 |
| Способ получения биокомпозита с антибактериальными свойствами на основе гидрогеля бактериальной целлюлозы | 2021 |
|
RU2771864C1 |
| Способ получения биокомпозита с регенерационными свойствами на основе гидрогеля бактериальной целлюлозы | 2019 |
|
RU2733137C1 |
| Способ получения гемостатического препарата в форме аэрогеля на основе бактериальной целлюлозы и альгината кальция | 2022 |
|
RU2798839C1 |
| Способ получения ранозаживляющего геля, содержащего трипсин, для наружного применения | 2021 |
|
RU2778511C1 |
| Способ получения гемостатического пористого композитного материала | 2021 |
|
RU2789327C1 |
| РАНЕВОЕ ПОКРЫТИЕ, ОБЛАДАЮЩЕЕ ГЕМОСТАТИЧЕСКИМ ДЕЙСТВИЕМ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2016 |
|
RU2624242C1 |
Настоящее изобретение относится к способу получения раневого биокомпозита на основе гидрогеля бактериальной целлюлозы, обладающего высокой абсорбирующей способностью, ранозаживляющим и антибактериальным действием, включающему получение гель-пленки бактериальной целлюлозы путем культивирования штамма бактерий, ее отделение и очищение, измельчение и лиофильную сушку, характеризующемуся тем, что для получения гель-пленки бактериальной целлюлозы осуществляют культивирование штамма бактерий Medusomyces gisevii в статических условиях в течение 7 суток при комнатной температуре с использованием комплексной жидкой питательной среды, содержащей следующие ингредиенты, масс.%: глюкоза – 0,99; сахароза – 0,99; дрожжевой экстракт – 0,99; пептон – 0,69; лимонная кислота – 0,02; ледяная уксусная кислота – 0,099 и этанол – 1,32, вода очищенная – до 100 мл; причем для приготовления комплексной жидкой питательной среды сначала в воде очищенной растворяют глюкозу, сахарозу, дрожжевой экстракт, пептон и лимонную кислоту, затем полученный раствор автоклавируют при 115°С в течение 30 мин и после охлаждения добавляют при перемешивании этанол и ледяную уксусную кислоту; после отделения гель-пленки от питательной среды осуществляют её очищение путем обработки 0,1 Н раствором NaOH при нагревании на водяной бане до 90°C в течение 60 мин, после чего образцы замачивают в 3% растворе перекиси водорода при комнатной температуре в течение 1,5-2 часов, затем промывают водой очищенной до достижения нейтральной реакции и измельчают с помощью гомогенизатора механического; измельченную гель-плёнку перемешивают до получения гомогенной массы однородной консистенции в соотношении 1:1 с водным раствором активных и вспомогательных ингредиентов, взятых из расчета содержания в граммах на 100 квадратных сантиметров раневого покрытия: бета-циклодекстрин – 0,2, метронидазол – 0,2, коллаген – 0,2, декспантенол – 0,5, бензалкония хлорид – 0,05, при этом указанный раствор изготавливают путем последовательного растворения в воде очищенной при 70°С сначала бета-циклодекстрина и метронидазола, а коллаген, декспантенол и бензалкония хлорид растворяют после охлаждения полученного водного раствора; полученную массу распределяют на подложку слоем толщиной 8 мм, выдерживают в морозильной камере при температуре минус 40°С в течение суток, после чего высушивают в лиофильной сушилке в течение 24 часов по следующей программе: 5 минут – температура лиофилизации минус 40°С, давление 1 мбар без нагрева полок; 18 часов – температура лиофилизации минус 40°С, давление 0,2 мбар, температура полок 30°С; 4 часа – температура лиофилизации минус 40°С, давление 0,15 мбар температура полок 40°С; 2 часа – температура лиофилизации минус 40°С, давление 0,1 мбар, температура полок 50°С. Настоящее изобретение обеспечивает создание способа получения раневого покрытия на основе гидрогеля бактериальной целлюлозы, обладающего высокой абсорбционной способностью, а также ранозаживляющим и антибактериальным действием. 3 табл., 5 пр.
Способ получения раневого биокомпозита на основе гидрогеля бактериальной целлюлозы, обладающего высокой абсорбирующей способностью, ранозаживляющим и антибактериальным действием, включающий получение гель-пленки бактериальной целлюлозы путем культивирования штамма бактерий, ее отделение и очищение, измельчение и лиофильную сушку, характеризующийся тем, что для получения гель-пленки бактериальной целлюлозы осуществляют культивирование штамма бактерий Medusomyces gisevii в статических условиях в течение 7 суток при комнатной температуре с использованием комплексной жидкой питательной среды, содержащей следующие ингредиенты, масс.%: глюкоза – 0,99; сахароза – 0,99; дрожжевой экстракт – 0,99; пептон – 0,69; лимонная кислота – 0,02; ледяная уксусная кислота – 0,099 и этанол – 1,32, вода очищенная – до 100 мл; причем для приготовления комплексной жидкой питательной среды сначала в воде очищенной растворяют глюкозу, сахарозу, дрожжевой экстракт, пептон и лимонную кислоту, затем полученный раствор автоклавируют при 115°С в течение 30 мин и после охлаждения добавляют при перемешивании этанол и ледяную уксусную кислоту; после отделения гель-пленки от питательной среды осуществляют её очищение путем обработки 0,1 Н раствором NaOH при нагревании на водяной бане до 90°C в течение 60 мин, после чего образцы замачивают в 3% растворе перекиси водорода при комнатной температуре в течение 1,5-2 часов, затем промывают водой очищенной до достижения нейтральной реакции и измельчают с помощью гомогенизатора механического; измельченную гель-плёнку перемешивают до получения гомогенной массы однородной консистенции в соотношении 1:1 с водным раствором активных и вспомогательных ингредиентов, взятых из расчета содержания в граммах на 100 квадратных сантиметров раневого покрытия: бета-циклодекстрин – 0,2, метронидазол – 0,2, коллаген – 0,2, декспантенол – 0,5, бензалкония хлорид – 0,05, при этом указанный раствор изготавливают путем последовательного растворения в воде очищенной при 70°С сначала бета-циклодекстрина и метронидазола, а коллаген, декспантенол и бензалкония хлорид растворяют после охлаждения полученного водного раствора; полученную массу распределяют на подложку слоем толщиной 8 мм, выдерживают в морозильной камере при температуре минус 40°С в течение суток, после чего высушивают в лиофильной сушилке в течение 24 часов по следующей программе:
- 5 минут - температура лиофилизации минус 40°С, давление 1 мбар, без нагрева полок;
- 18 часов - температура лиофилизации минус 40°С, давление 0,2 мбар, температура полок 30°С;
- 4 часа - температура лиофилизации минус 40°С, давление 0,15 мбар, температура полок 40°С;
- 2 часа - температура лиофилизации минус 40°С, давление 0,1 мбар, температура полок 50°С.
| Способ получения биокомпозита на основе аэрогеля бактериальной целлюлозы, обладающего кровоостанавливающими свойствами | 2019 |
|
RU2736061C1 |
| Способ получения биокомпозита с регенерационными свойствами на основе гидрогеля бактериальной целлюлозы | 2019 |
|
RU2733137C1 |
| Rzhepakovsky I | |||
| et al | |||
| Composite of bacterial cellulose and gelatin: A versatile biocompatible scaffold for tissue engineering/ International Journal of Biological Macromolecules, v | |||
| Ножевой прибор к валичной кардочесальной машине | 1923 |
|
SU256A1 |
| СПОСОБ ПОЛУЧЕНИЯ БАКТЕРИАЛЬНОЙ ЦЕЛЛЮЛОЗЫ | 2015 |
|
RU2597291C1 |
Авторы
Даты
2025-06-02—Публикация
2024-07-08—Подача