Изобретение относится к новому соединению производных пиримидиндиона, а именно 3N-амино-6-метил-1Н-пиримидин-2,4-диона и его лекарственной формы для лечения аденокарциномы.
Аденокарциномы легких являются основной причиной смертности от рака в мире, что представляет собой значительную проблему при постановке диагноза на поздних стадиях и ограничивает возможности хирургического лечения [1]. Преобладающим подходом такого лечения является мультимодальная терапия, представляющая собой сочетанное (одновременное) или последовательное, поэтапное, комбинированное применение нескольких методов лечения при лечении одной и той же злокачественной опухоли у одного и того же пациента [2]. Однако прогнозы на выживаемость пациентов все равно остаются неудовлетворительными. Данная ситуация полностью побуждает к созданию новых соединений и лекарственных препаратов на их основе, воздействующих на новые пути реакции организма, измененные при аденокарциноме легких, а также к поиску потенциальных адъювантных стратегий или новых схем лечения данного заболевания [3, 4].
Существующая за рубежом стандартная схема химиотерапии для лечения немелкоклеточного рака легких (НМРЛ) с обработкой рецепторов эпидермальными факторами роста и протеинподобной киназой анапластической лимфомы, ассоциированной с мутацией гена (EML-4-ALK), заключается во внутривенном введении двухкомпонентного препарата платины. В то же время, использование антиметаболитных препаратов, таких как фторпиримидиновый противораковый агент 5-фторурацил, является дополнительным вариантом терапии НМРЛ [5].
Ранее считалось, что использование 5-фторурацила, который относится к классу пиримидиндионов, нецелесообразно для терапии рака легких, поскольку легкие содержат высокие уровни дигидропиримидиндегидрогеназы, которая, как известно, разрушает 5-фторурацил. Однако в настоящее время доступны 2 типа производных 5-фторурацила, которые не имеют проблем деградации дигидропиримидиндегидрогеназой и могут вводиться перорально. Урацил-тегафур, который объединяет урацил и тегафур (пролекарство 5-фторурацила) в молярном соотношении 4:1, был одобрен для лечения пациентов с резецированным НМРЛ в странах, таких как Япония, Корея, Сингапур и Таиланд. Рандомизированные исследования показали, что адъювантная химиотерапия с урацилом-тегафуром улучшает прогноз у пациентов с аденокарциномой I стадии ≥ 2 см, однако это действие не является оптимальным, а требует поиска более эффективных лекарственных препаратов эффективных для лечения аденокарциномы II стадии ≥ 3-5 см [6]. В связи с этим актуальным является поиск новых фармацевтических субстанций на основе пиримидиндионов и создание лекарственных форм на их основе.
Известно использование и фармакологическое действие производных пиримидиндиона, пиримидинтриона, триазиндиона, тетрагидрохиназолиндиона в качестве антагонистов α1 адренергических рецепторов [7] с описанием методов получения производных пиримидиндиона, пиримидинтриона, триазиндиона, тетрагидрохиназолиндиона. При использовании указан только возможный фармакологический эффект для лечения болезни, прямо или косвенно связанной с закупоркой нижних мочевых путей, вызванной доброкачественной гиперплазией простаты.
Известно лекарственное средство с возможной гепатопротекторной активностью [8]. Однако при исследовании средства нет четкого доказательства гепатопротекторной активности.
Также известно применение в качестве лекарственных средств производных гидантоинов, тиогидантоинов, пиримидиндионов и тиоксопиримидинонов, а так же способы их получения [9]. В выводах описано возможное применение данных производных при: акромегалии, гипофизарных аденомах или эндокринных гастро-энтеро-панкреатических опухолях, проявляющихся в виде карциноидного синдрома, и желудочно-кишечных кровотечениях. Однако данные производные были получены в виде химических субстанций, далеких от лекарственных форм, применяемых в фармации. Известно фармакологическое действие производных гидантоинов, тиогидантоинов, пиримидиндионов и тиоксопиримидинонов, способ их получения, промежуточные продукты и фармацевтическая композиция [10]. Описано предположительное фармакологическое действие, которое возможно при следующих заболеваниях: лечении патологических состояний или болезней, акромегалии, гипофизарных аденомах, болезни Кушинга. Недостатком данного патента является предположительное фармакологическое действие. Известен способ получения 5-(метил, 63-н)-2,4-(1н,3н) пиримидиндиона [11]. Однако данный патент несет явную лабораторную направленность.
Технической проблемой, на которую направленно заявляемое изобретение является синтез 3N-амино-6-метил-1H-пиримидин-2,4-диона в качестве нового производного для проведения адъювантной химиотерапии, направленной на повышение выживаемости пациентов и создание лекарственных форм на его основе.
Адъювантная терапия - это терапия, которая назначается после радикальной операции по удалению злокачественной опухоли; Действие адъювантной терапии рассмотрим на примере фторурацила: фторпиримидины в качестве адъювантной терапии значительно увеличивают безрецидивную и общую выживаемость больных раком поджелудочной железы. Предлагаемое изобретение предусматривает производное пиримидин-2,4-диона, а именно 3N-амино-6-метил-1Н-пиримидин-2,4-диона, способ его получения и лекарственную форму в виде аэрозоля на его основе.
Предлагаемое соединение является более эффективным при применении в адъювантной терапии аденомокарциномы легкого вместо 5-фторурацила. Вещество 3N-амино-6-метил-1Н-пиримидин-2,4-диона, имеющего структуру формулы (I),
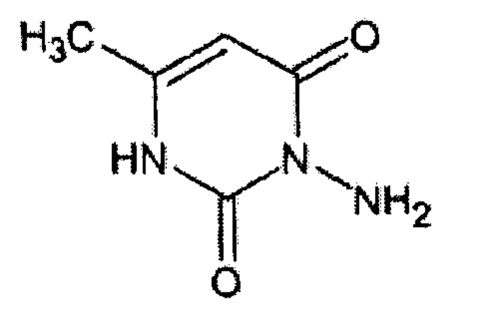
получают следующим образом.
В круглодонную трехгорлую колбу вместимостью 200 мл поместили сернокислого гидразина 14 г (точная навеска) и 4,2 г (точная навеска; мочевины. Затем добавили 130 мл воды и 1 мл аммиачного буферного раствора к данной смеси. После этого раствор нагревали в течение 2 часов с использованием обратного холодильника при температуре 270 градусов. После охлаждения образовался раствор семикарбазида, который был профильтрован через фильтр и помещен на чашку петри до высыхания. Затем, после высыхания, к высохшему веществу массой 8,54 г добавили 15 мл раствора ацетоуксусного эфира (по каплям) и 2 капли раствора соляной кислоты концентрированной. Последним шагом являлось высыхание данного осадка в эксикаторе. Данный синтез представлен согласно реакции 1.
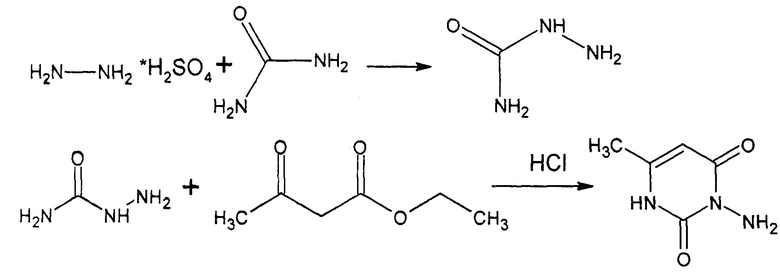
Ингаляционная лекарственная форма для использования при адъювантной терапии совместно с химиотерапевтическими средствами при лечении аденокарциномы легкого содержит 3N-амино-6-метил-1Н-пиримидин-2,4-дион и вспомогательные вещества (табл. 1).

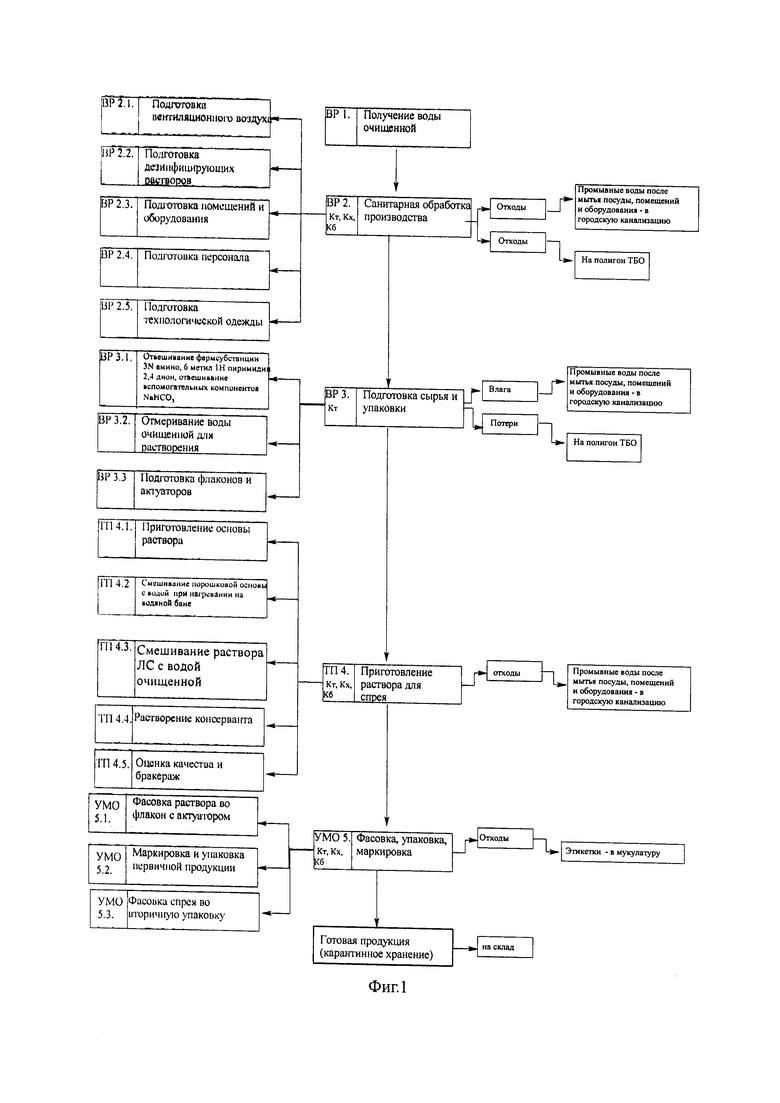
Лекарственную форму в лабораторных условиях готовили следующим образом: взвешивали навеску 3N-амино-6-метил-1Н-пиримидин-2,4-диона 50 мг (точная навеска), навеску натрия гидрокарбоната 35 мг (точная навеска) помещали в мерную колбу на 5 мл и доводили водой до метки. Таким образом, концентрация раствора по действующему веществу составила 1%. На Фиг. 1 представлена Технологическая схема для производства ингаляционной лекарственной формы для лечения аденокарциномы легкого.
Описание технологической схемы
При синтезе нового вещества первой стадией всегда идет получение воды очищенной. Следующей важной стадией является санитарная обработка производства, включающая в себя подготовку: вентиляционного воздуха, дезинфицирующих растворов, помещений и оборудования, персонала и технологической одежды. Третьим важным этапом является подготовка непосредственно сырья, включающая в себя взвешивание всех компонентов и отмеривание воды для растворения веществ. Четвертым шагом является приготовление раствора, включающее в себя непосредственно получение раствора и оценку его качества, и бракераж. Пятым заключительным этапом является фасовка, упаковка, маркировка и хранение готовой продукции.
Для доказательства фармакологической активности разработанной ингаляционной формы 3N-амино-6-метил-1Н-пиримидин-2,4-диона проводили исследования на клеточных культурах в сравнении с 5-фторурацилом в той же концентрации.
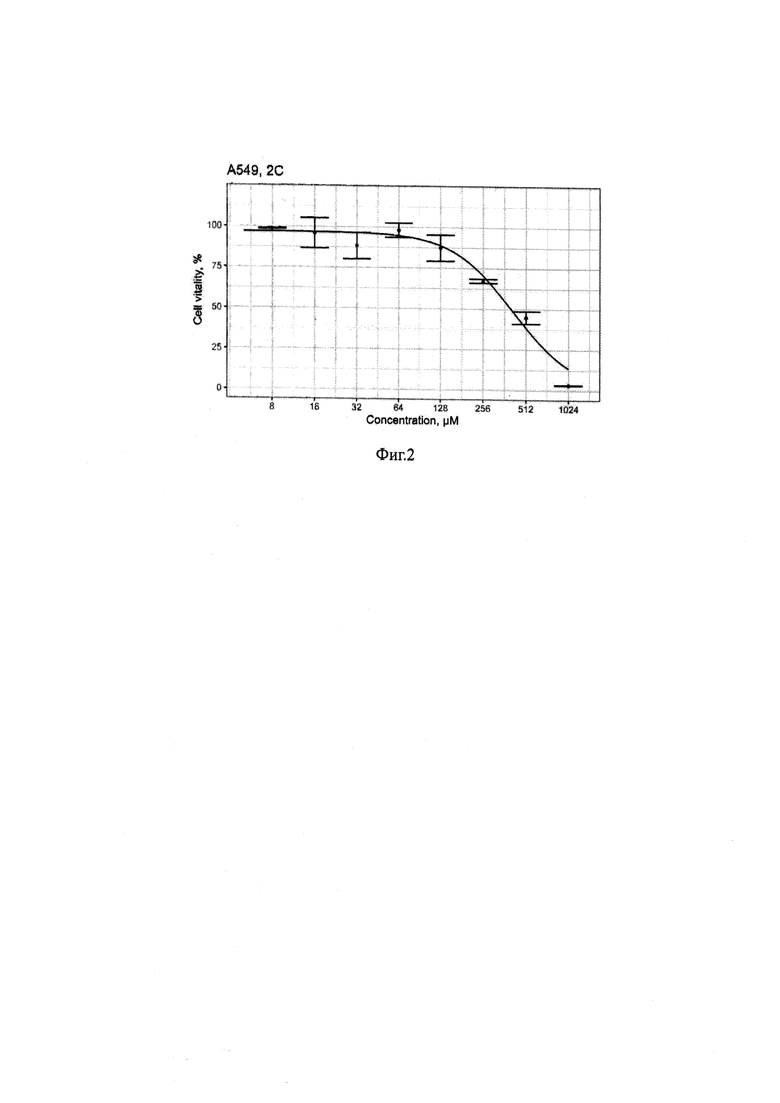
Соединение 3N-амино-6-метил-1Н-пиримидин-2,4-диона проявило большую токсичность на клетках аденокарциномы легкого человека А549. Их жизнедеятельность значительно снизилась при максимальных тестируемых концентрациях, а параметр IC50 ± SE составил 415.974 ± 30.812 μМ.
На Фиг. 2. представлена Кривая «доза-эффект» для 3N-амино-6-метил-1Н-пиримидин-2,4-диона на А549 (mean ± SD, n=3).
Для ингаляционной формы 5-фторурацил в концентрации 50 мг/мл параметр IC50 ± SE составил >1024 μМ, что почти в 2,5 раза хуже, чем для 3N-6-метил-пиримидин-2,4-диона.
Фармакологическое исследование ингаляционной формы на основе 3N-амино-6-метил-1Н-пиримидин-2,4-диона проводили методом открытого поля. Целью данного исследования было изучение значимых поведенческих факторов, происходящих при ингаляционном введении 3N-амино-6-метил-1Н-пиримидин-2,4-диона аэрозоля, на поведение мышей в открытом поле. Исследование проводилось с использованием стандартного протокола открытого поля, который позволяет изучать двигательную активность, исследовательское поведение и тревожность животных.
Также было проведено исследование ингаляционной формы на основе 3N-амино-6-метил-1Н-пиримидин-2,4-диона, в котором была описана острая и хроническая токсичность. В рамках исследований проводились тесты, направленные на определение возможных токсических эффектов при различных дозировках и длительном воздействии. Данные исследования позволяют определить допустимые уровни экспозиции, разработать рекомендации по безопасному применению соединения. Острая и токсическая реакция на препарат отсутствует.
Таким образом, разработанная ингаляционная форма на основе 3N-амино-6-метил-1Н-пиримидин-2,4-диона обладает высокой фармакологической активностью и может быть использована для проведения адъювантной химиотерапии, направленной на повышение выживаемости пациентов, в частности при лечении аденокарциномы, и создания лекарственных форм на его основе.
Список используемой литературы
1. Tsukamoto Y. et al. Recurrence of Lung Adenocarcinoma After an Interval of 15 Years Revealed by Demonstration of the Same Type of EML4-ALK Fusion Gene //Pathology-Research and Practice. - 2014. - T. 210. - №. 12. - C. 1112-1116.
2. Fujimoto K. et al. Favorable treatment response of bevacizumab-combined chemotherapy for advanced or recurrent invasive mucinous adenocarcinoma of the lung: A retrospective observational study // Respiratory Investigation. - 2024. - T. 62. - №. 3. - C. 360-364.
3. Wang X. et al. Survival outcomes of targeted and immune consolidation therapies in locally advanced unresectable lung adenocarcinoma // International Immunopharmacology. - 2024. - T. 129. - C. 111684.
4. Demir T. et al. Efficacy of Systemic Treatments in Patients With Metastatic Lung Invasive Mucinous Adenocarcinoma // Clinical Lung Cancer. - 2024.
5. Ogata S. et al. A pilot study of mRNA expressions of 5-fluorouracil pathway genes in peripheral blood mononuclear cells and tumor tissues in patients with lung adenocarcinoma //Lung Cancer. - 2011. - T. 71. - №. 2. - C. 199-204.
6. Shukuya Т. et al. Efficacy of adjuvant chemotherapy with tegafur-uracil in patients with completely resected, node-negative NSCLC-real-world data in the era of molecularly targeted agents and immunotherapy // JTO Clinical and Research Reports. - 2022. - T. 3. - №. 5. - C. 100320.
7. Заявка RU №96111418 Антивирусные производные пиримидиндиона, способ их получения и фармацевтическая композиция на их основе / Гэри В.Бэнтл, Ангел Гузман, Франсиско Х.Лопес-Тапиа, Артуро Перес-Медрано, Эрик Б.Сьогрен, Тодд Р.Элворси, Саул Хайме-Фигероа, Дэвид Дж.Морганс (младший), Юрг Р.Пфистер, Франсиско Кс.Таламас - Дата публикации заявки: 27.09.1998.
8. Патент RU №2595868 Лекарственное средство с гепатопротекторной активностью / Тец Виктор Вениаминович, Тец Георгий Викторович, Краснов Константин Андреевич - Заявка: 2015111184/15, 27.03.2015; Опубл. 27.08.2016. Бюл. №24.
9. Заявка RU №2002105024 Производные гидантоинов, тиогидантоинов, пиримидиндионов и тиоксопиримидинонов, способы их получения и их применение в качестве лекарственных средств / ПУАТУ Лиди, Кристоф Тюрью, БРО Валери; Дата публикации заявки: 20.09.2003.
10. Патент RU 801505 Способ получения 5-(метил-3Н3)-2,4-(1Н,3Н)-пиримидиндиона / Мясоедов Н.Ф., Сидоров Г.В., Иванькова Е.К., Воронков А.Л. - Заявка: 2786114/04, 29.06.1979; Опубл. 15.03.1994.
11. Патент RU №2203891 Антивирусные производные пиримидиндиона, способ их получения и фармацевтическая композиция на их основе / ЧО Еуи-Хван, ЧУНГ Сун-Ган, ЛИ Сун-Хван, КВОН Хо-Сеок, ЛИ Дзае-Еунг, ДЗОО Дзеонг-Хо - Заявка: 2001101497/04, 08.04.2000; Опубл. 10.05.2003. Бюл. №13.
| название | год | авторы | номер документа |
|---|---|---|---|
| Макрогетероциклические нуклеозидные производные и их аналоги, получение и применение | 2017 |
|
RU2731385C1 |
| НОВЫЕ ДИСПИРО-ИНДОЛИНОНЫ, ИНГИБИТОРЫ MDM2/p53 ВЗАИМОДЕЙСТВИЯ, СПОСОБ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2015 |
|
RU2629750C2 |
| ДИСПИРОИНДОЛИНОНЫ НА ОСНОВЕ РОДАНИНОВ КАК ИНГИБИТОРЫ Р53-MDM2 БЕЛОК-БЕЛКОВОГО ВЗАИМОДЕЙСТВИЯ | 2019 |
|
RU2730286C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ОСНОВЕ 6-[(4-МЕТИЛ-I-1-ПИПЕРАЗИНИЛ)МЕТИЛ]-ИНДОЛО[1',7':1,2,3]ПИРРОЛО[3',4':6,7]АЗЕПИНО[4,5-b]ИНДОЛ-1,3(2Н,10 Н)-ДИОНА В КАЧЕСТВЕ ПРОТИВООПУХОЛЕВОГО СРЕДСТВА | 2013 |
|
RU2523387C1 |
| ПРИМЕНЕНИЕ 3-О-СУЛЬФАМОИЛОКСИ-7β-МЕТИЛ-D-ГОМО-6-ОКСАЭСТРА-1,3,5(10),8(9)-ТЕТРАЕН-17а-ОНА ДЛЯ ЛЕЧЕНИЯ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ, ВКЛЮЧАЯ ТРИЖДЫ НЕГАТИВНУЮ ФОРМУ | 2018 |
|
RU2678845C1 |
| Способ получения производных ксантина или их солей | 1979 |
|
SU952105A3 |
| ЦИКЛИЧЕСКИЕ ДЕЗОКСИРИБОНУКЛЕОТИДНЫЕ СОЕДИНЕНИЯ | 2020 |
|
RU2836016C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2003 |
|
RU2248978C1 |
| НОВОЕ СОЧЕТАНИЕ З-[(3-{ [4-(4-МОРФОЛИНИЛМЕТИЛ)-1Н-ПИРРОЛ-2-ИЛ]МЕТИЛЕН} -2-ОКСО-2,3-ДИГИДРО-1Н-ИНДОЛ-5-ИЛ)МЕТИЛ]-1,3-ТИАЗОЛИДИН-2,4-ДИОНА И ИНГИБИТОРА ТИРОЗИНКИНАЗЫ EGFR | 2016 |
|
RU2695362C2 |
| Нуклеотиды, включающие N-[(S)-1-циклобутоксикарбонил]фосфорамидатный фрагмент, их аналоги и их применение | 2017 |
|
RU2659388C1 |
Изобретение относится к лекарственной форме производного пиримидиндиона 3N-амино-6-метил-1Н-пиримидин-2,4-диона формулы, представленной ниже:
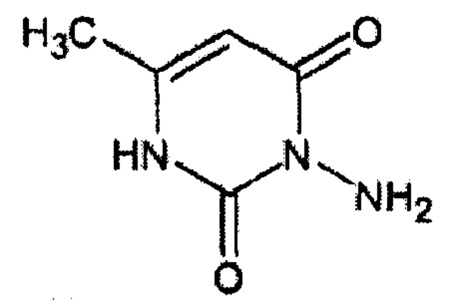
Предложенная ингаляционная лекарственная форма содержит 3N-амино-6-метил-1Н-пиримидин-2,4-диона, натрия гидрокарбонат (NaHCO3), бензалкония хлорид/бромид, воду при определенном соотношении. Ингаляционная лекарственная форма обладает высокой фармакологической активностью и повышает эффективность адъювантной терапии аденокарциномы легкого. 2 ил., 1 табл.
Ингаляционная форма для лечения аденокарциномы, характеризирующаяся тем, что включает вещество 3N-амино-6-метил-1Н-пиримидин-2,4-диона и вспомогательные вещества при следующем соотношении компонентов:
3N-амино-6-метил-1Н-пиримидин-2,4-диона, мг - 50
Натрия гидрокарбонат (NaHCO3), мг - 35
Бензалкония хлорид/бромид, мг - 1,25
Вода объемом, мл - 5
| WO 2020181283 A1, 2020.09.10 | |||
| Gershanovich ML, Filatova LV | |||
| Therapeutic effect of amigluracil aerosol inhalation on radiation- and bleomycin-induced pulmonitis in patients with malignant lymphomas, Vopr Onkol | |||
| Способ и аппарат для получения гидразобензола или его гомологов | 1922 |
|
SU1998A1 |
| WO 2014168986 A1, 2014.10.16 | |||
| МЕЩЕРЯКОВА С.А | |||
| СИНТЕЗ, СВОЙСТВА, СТРУКТУРА И БИОЛОГИЧЕСКАЯ АКТИВНОСТЬ НОВЫХ S И N | |||
Авторы
Даты
2025-06-03—Публикация
2024-12-23—Подача