(54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ КСАНТИНА ИЛИ ИХ СОЛЕЙ




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 2,4-диамино-5-(замещенных) пиримидинов | 1983 |
|
SU1306473A3 |
| Производные оксадиазолилалкилпурина, проявляющие противокашлевую активность | 1988 |
|
SU1602862A1 |
| 2-[(4-ГЕТЕРОЦИКЛ-ФЕНОКСИМЕТИЛ)ФЕНОКСИ]-АЛКАНОАТЫ, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ, СПОСОБ ПОДАВЛЕНИЯ НЕЖЕЛАТЕЛЬНОЙ РАСТИТЕЛЬНОСТИ | 1993 |
|
RU2113434C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИДЕЗОКСИДИДЕГИДРОКАРБОЦИКЛИЧЕСКИХ НУКЛЕОЗИДОВ | 1989 |
|
RU2067097C1 |
| Способ получения N @ -/1,2-цис-2-галогеноциклопропил/-замещенной пиридонкарбоновой кислоты | 1989 |
|
SU1792416A3 |
| Способ получения производных 1,8-нафтиридина или их солей | 1984 |
|
SU1482527A3 |
| ПРОИЗВОДНЫЕ 8-ХИНОЛИНКСАНТИНА И 8-ИЗОХИНОЛИНКСАНТИНА В КАЧЕСТВЕ ИНГИБИТОРОВ ФОСФОЭСТЕРАЗЫ PDE 5 | 2001 |
|
RU2269529C2 |
| СПОСОБ ПОЛУЧЕНИЯ БИС(ГИДРОКСИМЕТИЛ)ЦИКЛОБУТИЛ ПУРИНОВ ИЛИ ПИРИМИДИНОВ | 1989 |
|
RU2041213C1 |
| Способ получения производных арилтиазолов или их хлористоводородных или бромистоводородных солей | 1985 |
|
SU1380614A3 |
| ДИДЕЗОКСИДИДЕГИДРОКАРБОЦИКЛИЧЕСКИЕ НУКЛЕОЗИДЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1989 |
|
RU2114846C1 |

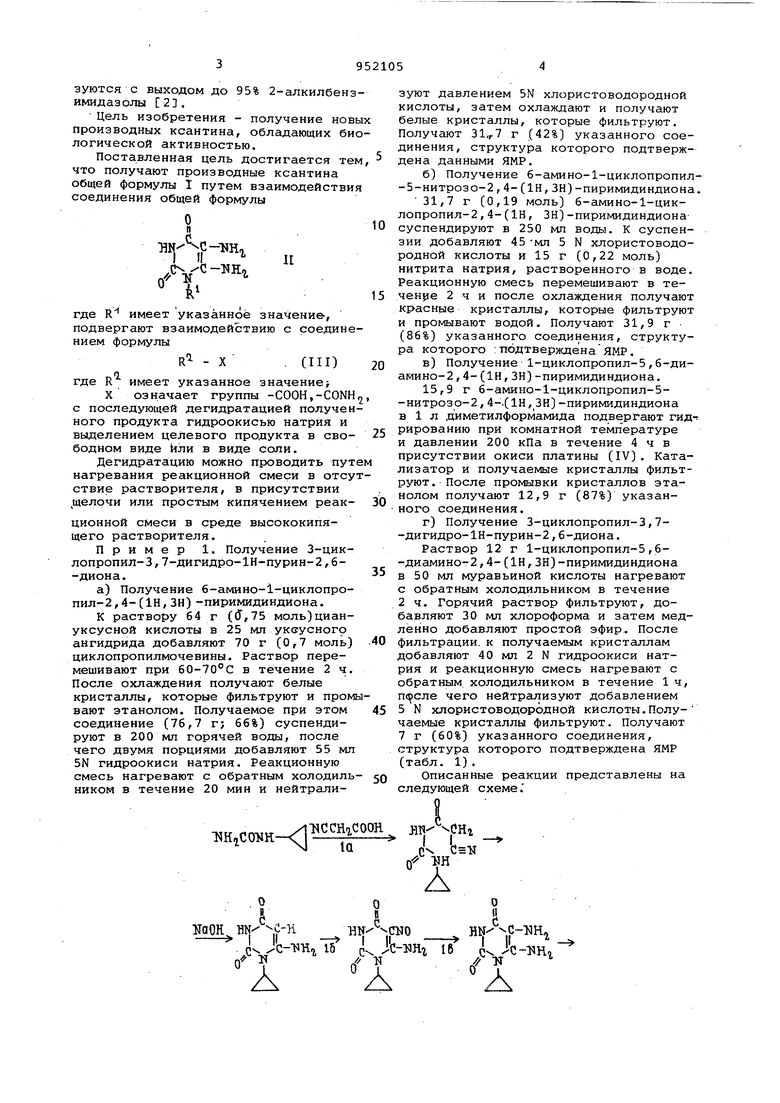
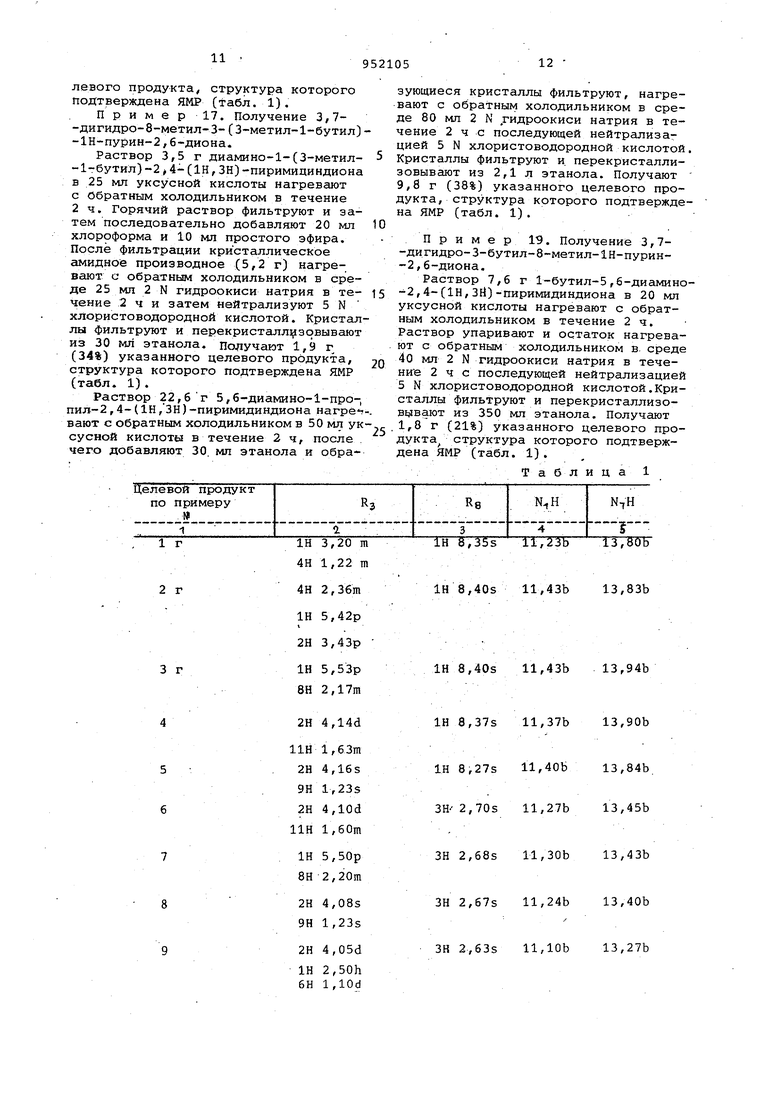
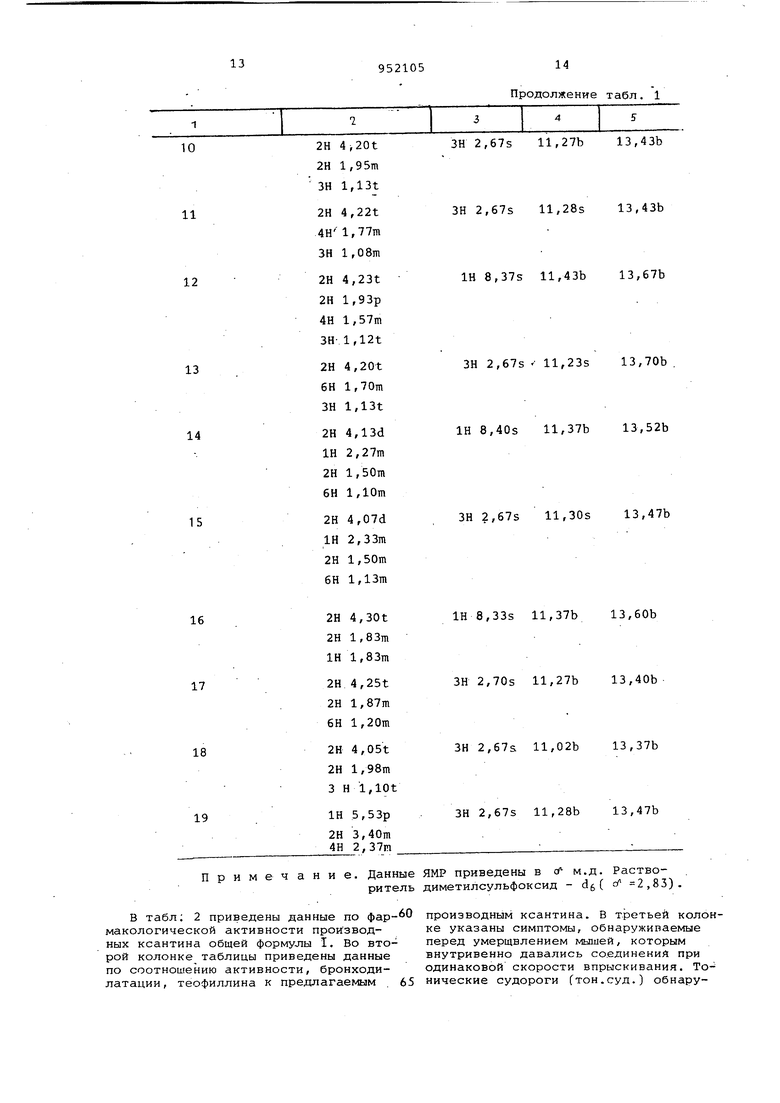
Изобретение относится к органической химии, конкретно к способу получения новых гетероциклических соединений, в частности к способам получения производных ксантина обще формулы С- I, где н-пропил, н-бутйл, н-пентил 2-метилпропил, 2-метилбутил 3-метилбутил, 2,2-диметилпро пил, циклопропил, циклобутил циклопентил, циклогексилметил;R - водород, метил, причем если . R означает н-пропил, н-бутил, 2-метилпропил, то R - означает метил, или их солей Производные ксантина представляют интерес как биологически активные со динения, в частности они могут прояв лять фармакологическую активность и быть использованы при лечении дыхательных путей и заболевания сердца. Известен ксантин-или 2,6-диоксипурин и его производные, встречающиеся в растениях (например, вместе с производным - кофеином и теофиллином он содержится в чае); а также в организме животных (в крови, печени).Производные ксантина применяются, в частности теофиллин и кофеин, для лечения хронических заболеваний дыхательных путей и заболеваний.сердца. Эти соединения обычно выделяют из растений, в частности кофеин выделяют из отходов чайного производства, а также синтетически из мочево кислоты метилированием аминогрупп tl. Фармакологическое действие кофеина и теофиллина в ряде случаев имеет побочное воздействие, они вызывают су- дороги. Известно взаимодействие азотсодержащих соединений с органическими кислотами и их производными, протекающее при нагревании в среде органического растворителя. Так.,в частности, при кипячении о-фенилендиамина с карбоновыми кислотами в течение 0,5 ч образуются с выходом до 95% 2-алкил6ен имидазолы 2, Цель изобретения - получение нов производных ксантина, обладающих би логической активностью. Поставленная цель достигается те что получают производные ксантина общей формулы I путем взаимодействи соединения общей формулы T ir- c-uHi где R имеет указанное значение, подвергают взаимодействию с соедине нием формулы R - X . (Ill) где R имеет указанное значениеj х означает группы -COOH,-CONH с последующей дегидратацией получе ного продукта гидроокисью натрия и выделением целевого продукта в свободном виде или в виде сопи. Дегидратацию можно проводить пут нагревания реакционной смеси в отсу ствие растворителя, в присутствии цeлoчи или простым кипячением реакционной смеси в среде высококипящего растворителя. Пример 1. Получение 3-циклопропил-3,7-дигидро-1Н-пурин-2,б-диона. а) Получение 6-амино-1-циклопропил-2,4-С1Н,ЗН) -пиримидиндиона. К раствору 64 г (ИГ,75 моль)циануксусной кислоты в 25 мл уксусного ангидрида добавляют 70 г (0,7 моль) циклопропилмочевины. Раствор перемешивают при 60-70°С в течение 2ч После охлаждения получают белые кристаллы, которые фильтруют и пром вают этанолом. Получаемое при этом соединение (76,7 г; 66%) суспендируют в 200 мл горячей воды, после чего двумя порциями добавляют 55 мл 5N гидроокиси натрия. Реакционную смесь нагревают с обратным холодил НИКОМ в течение 20 мин и нейтралиусснгСоон
IQ
1
Uv
Г та
л
V
I HN-
А зуют давлением 5N хлористоводородной кислоты, затем охлаждают и получают белые кристаллы, которые фильтруют. Получают 31,г7 г ,(42%) указанного соединения, структура которого подтверждена данными ЯМР. б)Получение 6-амино-1-циклопропил-5-нитроз0-2,4-(1Н,ЗН)-пиримидиндиона. 31,7 г (0,19 моль) 6-амино-1-циклопропил-2,4-(1Н, ЗН)-пиримидиндиона суспендируют в 250 мп воды. К суспензии добавляют 45-мл 5 N хлористоводородной кислоты и 15 г (0,22 моль) нитрита натрия, растворенного в воде. Реакционную смесь перемешивают в теченре 2 ч и после охлаждения получают красные кристаллы, которые фильтруют и промывают водой. Получают 31,9 г (86%) указанного соединения, структура которого :Т1бдтвержденаяМР. в)Получение 1-циклопропил-5,6- диамино-2,4-(1Н,ЗН)-пиримидиндиона. 15,9 г 6-амино-1-циклопропил-5-нитрозо-2, 4-.(1Н,ЗН)-пиримидиндиона в 1 л диметилформамида подвергают гидт рированию при комнатной температуре и давлении 200 кПа в течение 4 ч в присутствии окиси платины (IV). Катализатор и получаемые кристаллы фильтруют. После промывки кристаллов этанолом получают 12,9 г (87%) указанного соединения. г)Получение 3-циклопропил-З,7-дигидро-1Н-пурин-2,6-диона. Раствор 12 г 1-ЦИКЛОПРОПИЛ-5,6-диамино-2,4-(1Н,ЗН)-пиримидиндиона в 50 мл муравьиной кислоты нагревают с обратным холодильником в течение 2 ч. Горячий раствор фильтруют, добавляют 30 мл хлороформа и затем медленно добавляют простой эфир. После фильтрации, к получаемым кристаллам добавляют 40 мл 2 N гидроокиси натрия и реакционную смесь нагревают с обратным холодильником в течение 1 ч, чего нейтргшизуют добавлением 5 N хлористоводородной кислоты.Получаемые кристаллы фильтруют. Получают 7 г (60%) указанного соединения, структура которого подтверждена ЯМР (табл. 1). Описанные реакции представлены на следующей схеме. Пример 2. Получение 3-циклобутил-3,7-дигидро-1н-пурин-2,б-диона. а)Получение 6-амино-1-циклобутил-2,4-(1Н,ЗН -пиримидиндиона. К раствору 30 г (0,35. моль)циануксусной кислоты и 100 мл уксусного ангидрида добавляют 36,1 г (0,32 моль циклобутилмочевины. Раствор перемешивают при 60-70°С в течение 2 ч. После охлаждения получают белые кристаллы, которые фильтруют и промывают этаноло Получаемое при этом промежуточное сое динение (36,4 г; 63%) суспендируют в 100 мл горячей воды, после чего порци ми добавляют 50 мл 2 N гидроокиси натрия. Реакционную смесь нагревают-с обратным холодильником в течение 20 мин. После охлаждения получают белые кристаллы, которые фильтруют.Получают 3,6 г (20%) указанного соедине ния, структура которого подтверждена ЯМР. б)Получение 6-амино-1-:Циклобутил-5-нитрозо-2,4-(1Н,ЗН)-пиримидиндиона 3- г (0,0166 моль) 6-амино-1-циклобутил-2,4-(1Н,ЗН)-пиримидиндиона суспендируют в 25 мл воды. К суспензии добавляют 4 мл 5 N хлористоводородной кислоты и 1,3 г (0,019 моль) нитрита натрия, растворенного в воде. Реакцио ную смесь перемешивают в течение 3 ч. Получаемые красные кристаллы фильтрую и промывают водой. Получают 3,1 г (89%) указанного соединения, структур которого подтверждена ЯМР. в)Получение 1-циклобутил-5,6-диамино-2,4-(1Н,ЗН)-пиримидиндиона. 6,9 г 6-амино-1-циклобутил-5-нитро ЗО-2,4-(1Н,ЗН)-пиримидиндиона в среде 250 мл диметилформамида подвергают гидрированию при комнатной температуре и давлении 200 кПа в течение 2 ч в присутствии 0,1 г окиси платины.Катализатор и получаемые кристаллыфильтруют . После промывки кристаллов этанолом получают 3,5 г (54%) указанного соединения. г).Получение 3-циклобутил-З,7-1Н пурин-2,6-диона. Раствор 3,5 г 1-циклобутил-5,6-диамино-2,4-(1Н,ЗН)-пиримидиндиона в 20 мл муравьиной кислоты нагревают с обратным холодильником в течение 2 ч. После фильтрации горячего раствора добавляют 20 мл хлороформа,затем медленно простой эфир и после фильт- рации к получаемым кристаллам прибавляют 20 мл 2 N гидроокиси натрия.Реак ционную смесь нагревают с обратным
, Н
Г
ВД /Си
/Л
-W
А холодильником в течение 1 ч, затем, нейтрализуют добавлением 5 N хлористоводородной кислоты. Получаемые кристаллы фильтруют и перекристаллизовывают из 150 мл этанола. Получают 1,4 г (38%) указанного соединения, структура которого подтверждена ЯМР (табл. 1). Примерз. Получение 3-циклопентил-3, 7-дигидро-1Н--пури 1-2,6-диона. а)Получение 6-амино-1-циклопентил-2,4-(1Н,ЗН)-пиримидиндиона. К раствору 136 г (1,6 моль) цианоуксусной кислоты и 400 мл уксусного янгидрида добавляют 192 г (1,5 моль циклопентилмочевины.Раствор перемешивают при 60-7(fc в течение 2 ч. После охлаждения получают белые кристаллы, которые фильтруют и промывают этанолом. Получаемое при этом промежуточное соединение (192 г; 66%) суспендируют в горячей воде и порциями добавляют 195 мл 5 N гидроокиси натрия. Реакционную смесь нагревают с обратным холодильником в течение 20 мин и затем нейтрализуют добавлением 5 N хлористоводородной кислоты. После охлаждения 159 г белых кристаллов циклопентилмочевины ее фильтруют. Фильтрат упаривают и остаток нагревают с обратным холодильником в среде 200 мл 1 N гидроокиси натрия. После охлаждения циклoneнтилмочевину фильтруют и фильтрат нейтрализуют добавлением 5 N хлористоводородной кислоты. Получаемые кристаллы фильтруют. Получают 3,8 г (2%) указанного соединения, структура которого подтверждена ЯМР. б)Получение 6-амино-1-циклопентил-5-нитрозо-2,4-(1Н,ЗН)-пиримидиндиона. 12,4 г (0,064 моль) 6-амино-1-циклопентил-2,4-(1Н,ЗН)-пиримидиндиона суспендируют в 200 мл воды, после чего последовательно добавляют 14 мл 5 N хлористоводородной кислоты и 4,8 г (0,07 моль) нитрита натрия, растворенного в воде. Реакционную смесь перемешивают в течение 1 ч и промывают водой. Получают 12,9 г (90%) указанного соединения, структура которого подтверждена ЯМР. в)Получение 1-циклопентил-5,6-диамино-2,4-(1Н,ЗН)-пиримидиндиона. 12,9 г 6-амино-1-циклопентил-5-нитрозо-2,4-(1Н,ЗН)-пиримидиндиона в среде 30 мл 2 N хлористоводородной кислоты подвергают гидрированию при комнатной температуре и давлении 200 кПа в течение 3 ч в присутствии 0,1 г окиси платины. Катализатор фильтруют и фильтрат нейтрализуют до бавлением 5 N гидроокиси натрия. Получае -ше кристаллы фильтруют. Получают 6Д г (50%) указанного соединения. г) Получение 3-циклопентил-З,7-дигидро-1Н-пурин-2,б-диона. Раствор 6,1 г 1-циклопентил-5,6-диамино-2,4-(IH,ЗН)-пиримидиндиона в 25 мл муравьиной кислоты нагревают с обратным холодильником в течение 1 ч. После фильтрадии горячего раствора добавляют 20 мл хлороформа и затем медленно простой эфир. Получаемые кристаллы фильтруют. Получаемое при этом промежуточное соединение в среде 30 мл 2 N гидроокиси нат рия нагревают с обратным холодильником в течение 1 ч и затем нейтрализуют добавлением 5 N хлористоводородной кислоты. Получают 3,4 г С53%) указанного соединения, структура которого подтверждена ЯМР (табл. 1). По аналогичным схемам примеров 1-3 получают и другие соединения общ общей формулы II. Пример 4. Получение 3,7-дигидро-3-циклогексилметил-1Н-пурин-2,6-диона. 2 г 5,б-диамино-1-циклогексилметил-2,4-(1Н,ЗН)-пиримидиндиона в среде 10 мл муравьиной кислоты нагревают с обратным холодильником в течение 1 ч. После добавления 5 мл хлороформа медленно добавляют просто эфир. Получаемые кристаллы фильтруют и.образующееся при этом промежуточно соединение (2,1 г) нагревают с обрат ным холодильником в среде 15 мл 2 N гидроокиси натрия в течение 1 ч после чего смесь нейтрализуют добавлением 5 N хлористоводородной кислоты. Получают 1,7 г указанного соединения, структура которого подтвержде на ЯМР (табл. 1). Пример 5. Получение 3,7-дигидро-3-(2,2-диметилпропил)-1Н-пурин -2fб-диона, 4,0 г 5,6-диамино-1-(2,2-диметилпропил ) -2,4-(1Н,ЗН)-пиримидиндиона .в 20 мл формамида нагревают с обратным холодильником в течение 30 мин. После охлаждения добавляют 30 мл эта НОЛа. Получаемые желтые кристаллы фильтруют и перекристаллизовывают из 15 мл диметилформамида. Получают 2,0 г указанного соединения, структу ра которого подтверждена ЯМР (табл.1 Пример 6. Получение 3,7-дигидро-8-метил-3-циклогексилметил-1Н-пурин-2,б-диона. 1 г5,б-диaминo-l-циклoгeкcилмe тил-2,4-(lH, ЗН)-пиримидиндиона в ере де 5 мл уксусной кислоты нагревают с обратным холодильником в течение 1 ч, затем добавляют 2 мл хлороформа и медленно простой эфир. Образующиеся кристаллы фильтруют. Получаемое при этом промежуточное соединение в среде 10 мл 2 N гидроокиси натрия нагревают с обратным холодильником в течение 1 ч и затем нейтрализуют добавлением 5 N хлористоводородной кислоты. Кристаллы фильтруют и перекристаллизавывают из 80 мл этанола. Получают 0,6 г указанного соединения, структура которого подтверждена ЯМР (табл. 1). Пример 7. Получение 3-циклопентил-З, 7-дигидро-8-метил-1Н-пурин-2,6-диона. 1,6 1-циклопентил-5,6-диамино-2,4-(1Н,ЗН)-пиримидиндиона в среде 10 мл уксусной кислоты нагревают с обратным холодильником в течение 15 мин. После -добавления 10 мл хлороформа медленно добавляют простой эфир.Получаемые кристаллы фильтруют, а промежуточное соединение в среде 5 мл 2 N гидроокиси натрия нагревают с обратным холодильником в течение 1 ч и затем нейтрализуют добавлением 5 N хлористоводородной кислоты, после чего кри.сталлы вновь фильтруют и перекриста;ллизовывают из 25 мл 80%-ного этанола. Получают 0,7 г указанного соединения, структура которого подтверждена ЯМР (табл. 1). Пример 8. Получение 3,7-дигидро-3-(2,2-диметилпропил)-8-метил-1Н-пурин-2,6-диона. 10,4 г 5,6-диамино-1-(2,2-диметилпропил) -2 ,4-(1Н,ЗН)-пиримидиндиона в среде 75 мл уксусной кислоты нагревают с обратным холодильником в течение 1 ч, затем добавляют 50 мя хлороформа и медленно простой эфир. Образующиеся кристаллы фильтруют, после этого нагревают с обратным холодильником в среде 50 мл 1 N гидроокиси натрия в течение 1 ч и затем нейтрализуют добавлением 5 N хлористоводородной кислоты. Получают 7,2 г указанного соединения,структура которого подтверждена ЯМР (табл. 1). П р и м -е р 9. Получение 3,7-дигидро-8-метил-З- (2-.метилпропил) -1Н-пурин-2,б-диона. 10 г-5,б диамино-1-(2-метилпропил)-2,4-(1Н,ЗН)-пиримидиндиона в среде 50 мл уксусной кислоты нагревают с обратным холодильником в течение 1 ч, затем добавляют 30 мл хлороформа и медленно простой эфир. Образующиеся кристаллы фильтруют и это промежуточное соединение нагревают с обратным холодильником в среде 30 мл 2 N гидроокиси натрия в течение 1 ч, после чего его нейтрализуют 5 N хлористоводородной кислоты, кристаллы фильтруют и перекристалли зовывают из 50 мл уксусной кислоты. Получают 3,3 I. указанного соединения .структура которого подтверждена ЯМР (табл. 1), Пример 10. Получение 3-циклопропил-3,7-дигидро-8-метил-1н-пурин-2,6-диона. Раствор 6,4 г 1-циклопропил-5,6-диамино-2,4-(1Н,ЗН)-пиримидиндиона в 20 мл уксусной кислоты нагревают с обратным холодильником в течение 2ч, затем раствор упаривают и остаток нагревают с обратным холодильником в течение 1 ч в среде 40 мл 2 N гидроокиси натрия и 80 мл 5 N гидроокиси натрия, после чего нейтрализуют 5 N хлористоводородной кислотой После фильтрации получают 1,85 г (26%) указанного целевого продукта структура которого подтверждена ЯМР (табл. 1) . Пример 11. Получение 3-цикл бутил-3,7-дигидро-8-метил-1Н-пурин-2,6-диона. Раствор 2,2 г 1-циклобутил-5,б-диам бно-2 ,4- (1Н, ЗН) -пиримидиндиона в 10 мл уксусной кислоты нагревают с обратным холодильником в течение 2 ч, затем раствор упаривают и получаемый остаток нагревают с обратным холодильником в среде 30 мл 5 N гидроокиси натрия в течение 1 ч, после чего-нейтрализуют 5 N хлористоводородной кислотой. Кристаллы фильтруют и перекристаллизовывают из 100 мл этанола. Получают 0,4 г (18%) укаванного целевого продукта, структура которого подтверждена ЯМР (табл. 1) Пример 12. Получение 3,7-дигидро-3-пентил-1Н-пурин-2,б-диона 37,4 г 5,б-диамино-1-пентил-2,4-(1Н,ЗН)-пиримидиндиона в 50 мл муравьиной кислоты нагревают с обратны холодильником в течение 2 ч. Затем последовательно добавляют 50 мл хлороформа и 10 мл простого эфира и фильтруют кристаллы. 36,8 г амидного производного нагревают с обратньлм холодильником в среде 50 мл 5 N гид роокиси натрия в течение. 2 чи нейтрализуют 5 N хлористоводородной кислотой. Кристаллы фильтруют и перекристаллизовывают из 1,8л этанола. Получают 18,3 г указанного целевого продукта, структура которого подтверждена ЯМР (табл. 1). Пример 13. Получение 3,7-дигиДро-8-метил-3-пентил-1Н-пурин-2,6-диона. Раствор 5 г 5,6-диамино-1-пентил-2,4-(1Н,ЗН)-пиримидиндиона в 15 мл уксусной кислоты нагревают с обратным ХОЛОДИЛЬНИКОМ в течение 2 ч. Горячий раствор фильтруют, после чего последовательно добавляют 15 мл хлороформа и 5 мл простого эфира, фильт руют кристаллы 5,5 г амидного произ водного нагревают с обратным холодильником в среде 25 мл 2 N гидроокиси натрия в течение 2 ч и нейтрализуют 5 N хлористоводородной кислотой. Криста 1лы фильтруют и перекристаллизовывают из 225 мл этанола. Получают 2,1 г (37%) указанного целевого продукта, структура которого подтвержде-. на ЯМР (табл. 1). Пример 14. Получение 3,7- . -дигидро-3-(2-метил-1-бутил)-1Н-пурин-2,6-диона. 17,3 г 5,6-диaминo-l-(2-мeтил-l-бyтил) -2,4-(1Н,ЗН)-пиримидиндиона нагревают в 30 мл муравьиной кислоты в течение 2 ч. Затем последовательно добавляют 20 мл хлороформа и 5 мл простого эфира, образующееся амидное . производное (17,0 г) нагревают с обратным холодильником в среде 50 мл 2 N гидроокиси натрия в течение 2 ч и. нейтрализуют 5 N хлористоводородной кислотой. Кристаллы фильтруют и перкристаллизовывают из 400 мл этанола. Получают10 г указанного целевого продукта, структура которого подтверждена ЯМР (табл. 1).. Пример 15. Получение 3,7-дигидро-8-метил-3-(2-метил-1-бутил)-1Н-пурин-2,6-диона. Раствор 3,2 г ,6-диамино-1-(2-метил-1-бутил)-2,4-(1Н,ЗН)-пиримидиндиона в 8 мл уксусной кислоты нагревают с обратным холодильником в течение 2 ч. Горячий раствор фильтруют и затем последовательно добавляют 8 мл хлороформа и 4 мл простого эфира. Остающееся после фильтрации кристаллическое амидное производное нагревают с обратным холодильником в среде 10 мл 2 N гидроокиси натрия в течение 2 ч и затем нейтрализуют 5 N хлористоводородной кислотой. Кристаллы фильтруют и перекристаллизовывают из 75 мл этанола. Получают 2,0 г указанного целевого продукта, структура которого подтверждена ЯМР (табл. 1). Пример 16. Получение 3,7-дигидро-3-(3-метил-1-бутил)-1Н-пурин-2,6-диона. Раствор 21 г 5,6-диамино-1-(3-метил-1-бутил)-1Н-пурин-2,6-диона в 50 мл муравьиной кислоты нагревают с обратным холодильником в течение 2 ч. Горячий раствор фильтруют,после чего последовательно добавляют 50 мл хлороформа и 20 мл простого эфира. Остающееся после фильтрации кристаллическое амидное производное (20,2 г) нагревают с обратным холодильником в среде 25 мл 5 N гидроокиси натрия в течение 2 ч и затем нейтрализуют 5 N хлористоводородной кислотой. Кристаллы фильтруют и перекристаллизовывают из 500 мл этанола. Получают 9,7 г (44%) указанного целевого продукта, структура которого подтверждена ЯМР (табл. 1).
Пример 17. Получение 3,7-дигидро-8-метил-З-(З-метил-1-бутил)-1Н-пурин-2,6-диона.
Раствор 3,5 г диамино-1-(3-метил-1-бутил)-2 4-(IH,ЗН)-пиримидиндиона в 25 мл уксусной кислоты нагревают с Обратным холодильником в течение 2 ч. Горячий раствор фильтруют и затем последовательно добавляют 20 мл хлороформа и 10 мл простого эфира. После фильтрации кристаллическое амидное производное (5,2 г) нагреBcuoT с обратным холодильником в среде 25 мл 2 N гидроокиси натрия в течение 2 ч и затем нейтрализуют 5 N хлористоводородной кислотой. Кристаллы фильтруют и перекристалл1 зсэвывают из 30 мл этанола. Получают 1,9 г (34%) указанного целевого продукта, структура которого подтверждена ЯМР (табл. 1).
Раствор 22, б г 5, б-диамино-1-про-, пил-2,4- (1Н /ЗН) -пиримидиндиона нагре-гвают с обратным холодильником в 50 мл уксусной кислоты в течение 2ч, после . чего добавляют 30. мл этанола и обра4Н 2,36т 1Н 5,42р
t
2Н 3,43р
1Н 5,53р 8Н 2,17т
2Н 4,14d
1,6 Зга
IH 2Н 9Н 2Н 4,16s 1,23s 4,10d 1,60m
1Н
5,50p
1Н 8Н 2,20m
4,08s
2Н 9Н 1,23s
4,05d
2Н
2,50h
1Н бН l,10d
зующиеся кристаллы фильтруют, нагревают с обратным холодильником в среде 80 мл 2 N .гидроокиси натрия в течение 2 ч с последующей нейтрализаг цией 5 N хлористоводородной кислотой Кристаллы фильтруют и. перекристаллизовывают из 2,1 л этанола. Получают 9,8 г (38%) указанного целевого продукта, структура которого подтверждена ЯМР (табл. 1).
Пример 19. Получение 3,7-дигидро-3-бутил-8-метил-1Н-пурин-2,6-диона.
Раствор 7,6 г 1-бутил-5,б-диaминo-2,4-(lH, ЗН) -пиримидиндиона в 20 мл уксусной кислоты нагревают с обратным холодильником в течение 2ч. Раствор упаривают и остаток нагревают с обратным холодильником в- среде 40 мл 2 N гидроокиси натрия в течение 2 ч с последующей нейтрализацией 5 N хлористоводородной кислотой.Кристаллы фильтруют и перекристаллизовывают из 350 мл этанола. Получают .1,8 г (21%) указанного целевого продукта структура которого подтверждена ЯМР (табл. 1).
Таблица
1Н 8,40s ll,43b 13,83b
2Н 2Н 1,95m ЗН l,13t
2Н 4,221
4Н1,77m ЗН 1,08т
2Н 4,23t 2Н 1,93р 4Н 1,57т ЗН- l,12t
2Н 4,20t 6Н 1,70т ЗН l,13t
2Н 4,13d 1Н 2,27т 2Н 1,50т 6Н 1,10т
2Н4,07d
1Н2,33т
2Н1,50т
бН1,13т
2H 4,30t 2H 1,83m IH 1,83m
2H 4,25t 2H 1,87m 6H 1,20m
2H 4,05t 2H 1,98m 3 Hi,lot
IH 5,53p
2H 3,40m 4H 2,37n
Примечание. Данные
В табл; 2 приведены данные по фар-60 макологической активности производных ксантина общей формулы I, Во второй колонке таблицы приведены данные по соотношению активности, бронходилатации, теофиллина к предлагаемым 65
Продолжение табл. l
ЗН 2,67s 11,27Ъ 13,43Ь
ЗН 2,67s 11,28s 13,43b
IH 8,37s ll,43b 13,67b
3H 2,67s 11,23s 13,70b
IH 8,40s ll,37b 13,52b
3H 2,67s 11,30s 13,47b
1Н 8,33s ll,37b 13,60b
ЗН 2,70s ll,27b 13,40b
ЗН 2,67s ll,02b 13,37b
3H 2,67s ll,28b 13,47b
ЯМР приведены в J м.д. Растводиметилсульфоксид - d(,( cf- 2,83).
ритель
производным ксантина. В третьей колонке указаны симптомы, обнаружипаемые перед умерщвлением JvibnueA, которым внутривенно давались соединений при одинаковой скорости впрыскивания. Тонические судороги (тон.суд.) обнаруживались у всех животных после дачи теофиллина и кофеина. Предлагаемые соединёния, активность которых исследовалась на 10 животных, не вызывали тонических судорог. На некоторых животных соединения примеров 1 г, 2 г и 9 вызывали судороги клонического типа или смешанного клонически-тонического типа, интенсивность которых намного ниже интенсивности судорог, вызываемых теофиллином и кофеином. В пятой колонке указана кардиотоническая активность как положительная хроноторпная активность.
Авторы
Даты
1982-08-15—Публикация
1979-10-11—Подача