Изобретение относится к фармацевтической промышленности и включает в себя фармацевтическую композицию, представляющую собой раствор фармацевтически приемлемой соли 6-[(4-метил-1-1-пиперазинил)метил]-индоло[1',7':1,2,3]пирроло[3',4':6,7]азепино [4,5-b]индол-1,3(2H,10H)-диона формулы (I), в частности мезилата 6-[(4-метил-1-1-пиперазинил)метил]-индоло[1',7':1,2,3]пирроло[3',4':6,7]азепино [4,5-b]индол-1,3(2H,10H)-диона в фармацевтически приемлемом полисорбате (твине), в частности в полисорбате-60 (твин-60). Композиция применяется для терапии злокачественных опухолей человека или животных.
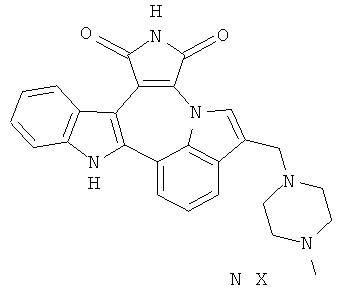
Формула I
где N=1 или 2, а Х представляет собой анион любой фармакологически приемлемой органической или неорганической кислоты.
Уровень техники
Опухолевые заболевания являются одной из основных причин смерти в России и во всем мире. Для раковых клеток характерны быстрое деление и инвазивность, т.е. способность мигрировать и метастазировать. В опухолевых клетках дефектны механизмы клеточной смерти (апоптоза), которые в противном случае могли бы регулировать их уровень, а также пролиферацию и миграцию. Напротив, в опухолевых клетках задействованы механизмы выживания, защищающие их от апоптоза. Фермент Pim-1 (от его viral integration Moloney virus) защищает клетки от апоптоза; этот механизм способствует злокачественной трансформации клеток [Moroy Т., Grzeschiczek A., Petzold S., and Hartmann К. U.1993. Expression of Pim-1 transgene accelerates limphoproliferation and inhibits apoptosis in lpr/lpr mice. Proc. Nat. cad. Sci. 90(22). 1073-4-10738.]. Pim-1 гиперэкспрессирован или активирован в опухолях системы крови (гемобластозах), а также при аденокарциномах предстательной и молочной желез. Для гемобластозов показана роль Pim-1 в развитии В-клеточной неходжкинской лимфомы, диффузной В-клеточной лимфомы, лимфомы Беркитта и мантийно-клеточной лимфомы [Sivertsen E.A., Galtrland Е., Mu D., et al. 2006. Gain of chromosome 6p is an infrequent cause of increased PIM1 expression in B-cell non-Hodgkin's lymphomas. Leykaemia. 20. 539-42.; Deutsch A., Aigelrransreiter A., Behan-Schmid C., Beham A., Linkesch W., Neumeister P.2005. Aberrant somatic hypermutayion in extranodal marginal zone B-cell lymphoma of MALT type. Blood. 106.125a-6a. Abstr 417. Rainio E.M., Ahlfors H., Carter K.L., et al. 2005. PIM kinases enchance EBNA2 activity. Virology. 333. 201-6. de Vos S., Krug U., Hofmann W.K., et al. 2003. Cell cycle alteration in the blastoid variant of mantle cell lymphoma (ML-BV) as detected by gene expression profiling of mantle cell lymphoma (MCL) and MCL-BV. Diagn Mol Pathol. 12. 35-43.18-21].
Итак, протеинкиназа Pim-1 - проонкогенный белок, важный для патогенеза опухолей системы крови и некоторых солидных опухолей (рак предстательной железы, молочной железы). Отсюда следует, что ингибирование активности Pim-1 - необходимый компонент химиотерапии указанных опухолей.
В настоящее время в клинической онкологии используется нескольких десятков противоопухолевых фармакологических препаратов, эффективность большинства из которых недостаточна, а спектр онкологических заболеваний, излечиваемых с помощью химиотерапии, в значительной мере ограничен.
Известен лекарственный препарат «Доксорубицин», противоопухолевый антибиотик антрациклинового ряда. Доксорубицин обладает высокой противоопухолевой и противолейкозной активностью, обладает способностью интеркалировать ДНК клеток. Обладает иммуносупрессивной активностью. Применяют Доксорубицин при раке молочной железы, саркомах мягких тканей, остеогенной саркоме, опухоли Юнга, раке легкого, лимфосаркоме, раке яичников, плоскоклеточных раках различной локализации, раке мочевого пузыря, опухоли Вильямса, раке щитовидной железы, острых лейкозах, лимфогранулематозе. Вводят только внутривенно. Недостатками данного средства является угнетающее влияние на кроветворение, а также очень высокая токсичность LD 50 13-15 мг/кг и кардиотоксическое действие (Машковский М.Д. Лекарственные средства. Москва. - 2001 г.).
Известен лекарственный препарат «Фторурацил», который является одним из широко используемых в клинической онкологии противоопухолевых препаратов и применяется для лечения рака яичников, рака молочной железы, рака печени (гапатомы), меланомы и др. (Safit J.N., Bonavida В. // Cancer Res. - 1992. - Vol.52. - P.6630). Как и все цитостатики, 5-фторурацил очень токсичен - при его применении возникают тошнота, рвота, угнетение костномозгового кроветворения, токсическое поражение почек и др. (Машковский М.Д. Лекарственные средства. Москва. - 2001 г., стр.425).
Наиболее близким по структуре является вещество, описанное в патенте РФ №2011108627 от 09.03.2011 г., в этом патенте также предложено применение производных 6-(4-метил-1-1 -пиперазинил)метил-индоло [1',7':1,2,3] пирроло [3',4':6,7] азепино [4,5-b]индол-1,3(2H,10H)-диона формулы I в качестве противоопухолевых препаратов, но не приведены конкрентные составы фармацевтических композиций. Новизна заключается в том, что нами впервые предложен состав композиции, позволяющий преодолеть плохую растворимость этих веществ в воде и физрастворе, что ранее не позволяло применять их в виде инъекционных форм для терапии опухолей.
Раскрытие изобретения
Данное изобретение относится к фармацевтической композиции, представляющей собой раствор активного ингредиента - производного 6-[(4-метил-1-1-пиперазинил)метил]-индоло[1',7':1,2,3]пирроло[3',4':6,7]азепино[4,5-b]индол-1,3(2H,10H)-диона формулы I, в частности мезилата 6-[(4-метил-1-1-пиперазинил)метил]-индоло[1',7':1,2,3]пирроло[3',4':6,7]азепино[4,5-b]индол-1,3(2H,10H)-диона в неионногенном поверхностно-активном вспомогательнорм веществе - фармацевтически приемлемом полисорбате (твине), в частности в полисорбате-60 (твин-60), из которой можно легко приготовить фармацевтический препарат, путем разбавления водными растворами, например физиологическим раствором.

Формула I
где Х представляет собой анион любой фармацевтически приемлемой органической или неорганической кислоты, например мезилат, а N=1 или 2.
Полисорбат (Твин), предназначенный для применения в данном изобретении, представляет собой, например, полисорбат-60 или другой фармацевтически приемлемый полисорбат.
Термин «Фармацевтически приемлемый» означает материал, который используют при получении фармацевтической композиции и который обычно является безопасным в биологическом или ином отношении, нетоксичным и приемлемым как в ветеринарии, так и в фармацевтике.
Препаративная форма фармацевтической композиции данного изобретения представляет собой жидкость, которая, в частности, является инъекционным раствором, с особенным предпочтением раствора для инъекций (например, для внутривенных, подкожных, внутримышечных и т.д. инъекций) и жидкости для внутривенных вливаний.
Фармацевтическая композиция данного изобретения может использоваться в форме жидкого препарата для терапии злокачественных опухолей.
Пример способа получения фармацевтической композиции:
К 10 г 1%-ного водного раствора Твина-60 при комнатной температуре добаляют 50 мг мезилата 6-[(4-метил-1-1-пиперазинил)метил]-индоло[1',7':1,2,3]пирроло[3',4':6,7]азепино [4,5-b]индол-1,3(2H,10H)-диона и облучают ультразвуком до полного растворения.
Биологическая активность
Тестируемые вещества получены методами, описанными в Патенте РФ №№2011108627 от 09.03.2011 г.
Противоопухолевая активность лекарственной формы пимина на мышах с подкожно перевитой аденокарциномой молочной железы мышей АК 755
Исследование проведено на мышах BDF1 (C57 B1×DBA2) самках, массой 20-22 грамма, полученных из питомника РАМЫ «Андреевка». Животных содержали в условиях вивария ФГБУ «НИИНА» РАМН. Все животные имели ветеринарный паспорт - сертификат качества здоровья животных. Животные содержались в специальных клетках по 10 особей при температуре воздуха 20-23°C и относительной влажности 65% в условиях искусственного освещения и принудительной вентиляции на подстилке из древесных стружек. Для кормления животных использован стандартный промышленный и сертифицированный экстузированный корм для грызунов с установленным сроком годности. Питьевую воду, помещенную в закрытые поилки, животные получали в неограниченном количестве. После двухнедельного карантина клинически здоровых животных вводили в эксперимент. Формировали группы по 10 мышей в каждой.
Аденокарциному молочной железы мышей АК 755 (5 генерация) перевивали по стандартной методике подкожно по 1 млн клеток.
Препарат растворяли в 1%-ном растворе ТВИН 60 в физиологическом растворе хлорида натрия и в виде 2%-ного раствора вводили мышам при помощи пластикового шприца ежедневно в течение 5 дней внутрибрюшинно в разовых дозах 10 и 20 мг/кг, начиная через 48 часов после перевивки опухоли.
Ежедневно наблюдали за состоянием и поведением животных, один раз в неделю измеряли условный объем опухолей (как произведение 3-х диаметров опухоли). ТРО% рассчитывали по общепринятой формуле: 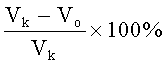
где: Vo - средний объем опухолей в подопытной группе, Vk - средний объем опухолей в контрольной группе.
Противоопухолевая активность соединения представлена в таблице 1.
Из представленных материалов видно, что препарат, примененный в дозе 20 мг/кг ежедневно в течение 5 дней, проявляет выраженную достоверную противоопухолевую активность, которая сохраняется в течение 15 суток после перевивки опухоли. Препарат, введенный в дозе 10 мг/кг, проявляет достоверную противоопухолевую активность только на 11 сутки после перевивки опухоли. К 15 суткам этот эффект отсутствует.
Противоопухолевая активность лекарственной формы пимина на мышах с подкожно перевитой меланомой мышей В-16
Исследование проведено на мышах BDF1 (C57 B1×DBA2) самцах, массой 20-22 грамма, полученных из питомника РАМН «Андреевка». Животных содержали в условиях вивария ФГБУ «НИИНА» РАМН. Все животные имели ветеринарный паспорт - сертификат качества здоровья животных. Животные содержались в специальных клетках по 10 особей при температуре воздуха 20-23°C и относительной влажности 65% в условиях искусственного освещения и принудительной вентиляции на подстилке из древесных стружек. Для кормления животных использован стандартный промышленный и сертифицированный экстузированный корм для грызунов с установленным сроком годности. Питьевую воду, помещенную в закрытые поилки, животные получали в неограниченном количестве.
После двухнедельного карантина клинически здоровых животных вводили в эксперимент. Формировали группы по 10 мышей в каждой.
Меланому мышей В-16 (8 генерация) перевивали по стандартной методике подкожно по 1 млн клеток.
Препарат растворяли в 1%-ном растворе ТВИН 60 в физиологическом растворе хлорида натрия и в виде 2%-ного раствора вводили мышам при помощи пластикового шприца ежедневно в течение 5 дней внутрибрюшинно в разовых дозах 10; 20 и 30 мг/кг, начиная через 72 часа после перевивки опухоли.
Ежедневно наблюдали за состоянием и поведением животных, один раз в неделю измеряли условный объем опухолей (как произведение 3-х диаметров опухоли). ТРО% рассчитывали по общепринятой формуле: 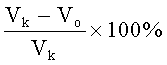
где: Vo - средний объем опухолей в подопытной группе, Vk - средний объем опухолей в контрольной группе.
Противоопухолевая активность соединения представлена в таблице 2.
При ежедневном пятикратном применении в дозах от 10 до 30 мг/кг препарат в лекарственной форме проявляет выраженную противоопухолевую активность в отношении меланомы В-16 мышей, которая сохраняется до 21 суток после перевивки опухоли.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНГИБИТОР PIM1-КИНАЗЫ 6-[(4-МЕТИЛ-1-1-ПИПЕРАЗИНИЛ)МЕТИЛ]-ИНДОЛО[1',7':1,2,3]ПИРРОЛО[3',4':6,7]АЗЕПИНО[4,5-b]ИНДОЛ-1,3(2Н, 10Н)-ДИОН, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ | 2011 |
|
RU2466132C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ОСНОВЕ ПРОИЗВОДНОГО ТРИИНДОЛИЛМЕТАНА В КАЧЕСТВЕ ПРОТИВООПУХОЛЕВОГО СРЕДСТВА | 2012 |
|
RU2549430C2 |
| Способ синтеза индоло[1',7':1,2,3]пирроло[3',4':6,7]азепино[4,5-b]индол-1,3(2Н,10Н)-диона | 2017 |
|
RU2648039C1 |
| ПРОТИВООПУХОЛЕВЫЙ АНТРАФУРАНДИОН И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ЕГО ОСНОВЕ | 2014 |
|
RU2554939C1 |
| 4-(1-(4-(4-МЕТОКСИФЕНИЛТИО)-2,5-ДИОКСО-2,5-ДИГИДРО-1Н-ПИРРО-3-ИЛ)-1Н-ИНДОЛ-3-ИЛ)БУТИЛКАРБАМИМИДОТИОАТ И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2009 |
|
RU2441000C2 |
| НОВОЕ СОЧЕТАНИЕ З-[(3-{ [4-(4-МОРФОЛИНИЛМЕТИЛ)-1Н-ПИРРОЛ-2-ИЛ]МЕТИЛЕН} -2-ОКСО-2,3-ДИГИДРО-1Н-ИНДОЛ-5-ИЛ)МЕТИЛ]-1,3-ТИАЗОЛИДИН-2,4-ДИОНА И ИНГИБИТОРА ТИРОЗИНКИНАЗЫ EGFR | 2016 |
|
RU2695362C2 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ОСНОВЕ ПРОИЗВОДНЫХ 4-ЗАМЕЩЕННЫХ-3-(3-ДИАЛКИЛАМИНОМЕТИЛ-ИНДОЛ-1-ИЛ)МАЛЕИМИДОВ | 2006 |
|
RU2388759C2 |
| ПРОИЗВОДНЫЕ ГЛИКОЗИДОВ ИНДОЛО[2,3-А]ПИРРОЛО[3,4-С]КАРБАЗОЛ-5,7-ДИОНОВ, ОБЛАДАЮЩИЕ ЦИТОТОКСИЧЕСКОЙ И ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2003 |
|
RU2255089C1 |
| N-ГЛИКОЗИДЫ ИНДОЛО[2,3-a]ПИРРОЛО[3,4-c]КАРБАЗОЛОВ, ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2014 |
|
RU2548045C1 |
| Замещенные N-{ 3-[4-(1-метил-1Н-индол-3-ил)пиримидин-2-иламино]-4-метоксифенил} -амиды в качестве модуляторов EGFR, предназначенные для лечения рака | 2015 |
|
RU2606949C9 |
Изобретение относится к фармацевтической промышленности. Предложена фармацевтическая композиция, содержащая как минимум один активный компонент - фармацевтически приемлемую соль 6-[(4-метил-1-1-пиперазинил)метил]-индоло[1',7':1,2,3]пирроло[3',4':6,7]азепино [4,5-b]индол-1,3(2H,10H)-диона формулы (I), в частности мезилата 6-[(4-метил-1-1-пиперазинил)метил]-индоло[1',7':1,2,3]пирро-ло[3',4':6,7]азепино [4,5-b]индол-1,3(2H,10H)-диона формулы (1), и как минимум одно вспомогательное вещество. Технический результат: показано подавление роста опухоли аденокарциномы и меланомы. Композиция применяется для терапии злокачественных опухолей человека или животных. 2 табл.

Формула I
Фармацевтическая композиция для терапии злокачественных опухолей, содержащая как минимум один активный компонент - фармацевтически приемлемую соль 6-[(4-метил-1-1-пиперазинил)метил]-индоло[1′,7′:1,2,3]пирроло[3′,4′:6,7]азепино[4,5-b]индол-1,3(2H,10H)-диона формулы (I),
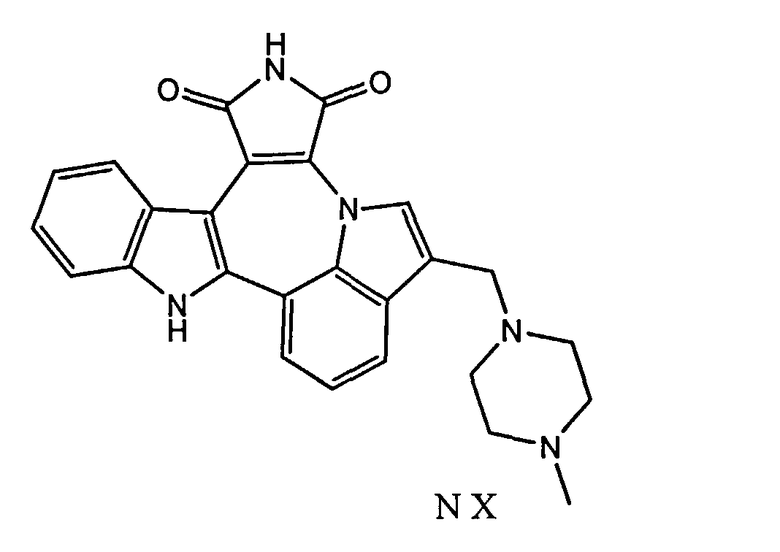
Формула I
где N=1 или 2, а X представляет собой анион любой фармакологически приемлемой органической или неорганической кислоты, в частности мезилат 6-[(4-метил-1-1-пиперазинил)метил]-индоло[1′,7′:1,2,3]пирроло[3′,4′:6,7]азепино[4,5-b]индол-1,3(2H,10H)-диона, и как минимум одно вспомогательное вещество.
| ИНГИБИТОР PIM1-КИНАЗЫ 6-[(4-МЕТИЛ-1-1-ПИПЕРАЗИНИЛ)МЕТИЛ]-ИНДОЛО[1',7':1,2,3]ПИРРОЛО[3',4':6,7]АЗЕПИНО[4,5-b]ИНДОЛ-1,3(2Н, 10Н)-ДИОН, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ | 2011 |
|
RU2466132C1 |
| КАРБОСТИРИЛЬНОЕ СОЕДИНЕНИЕ | 2005 |
|
RU2430920C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭПОКСИДА ДИЦИКЛОПЕНТЕНА (ЭПОКСИДА ТРИЦИКЛО-[5.2.1.0]ДЕЦЕНА-3,9-ОКСАТЕТРАЦИКЛО-[5.3.1.0.0]-УНДЕКАНА) | 2011 |
|
RU2471789C1 |
| ТЕХНОЛОГИЯ ЛЕКАРСТВЕННЫХ ФОРМ Под ред.Т.С.Кондратьевой М., Медицина 1991 т.1 с.105-106 §5.3.3 | |||
Авторы
Даты
2014-07-20—Публикация
2013-03-19—Подача