Объектом изобретения являются рекомбинантная плазмидная ДНК pFUSE 1-68 MAR TSH, кодирующая кДНК генов альфа и бета субъединиц рекомбинантного тиротропина альфа, и клеточная линия rhTSHCHO, полученная трансформацией культуры клеток яичника китайского хомячка CHO DG44 методом нуклеофекции рекомбинантной плазмидной ДНК pFUSE 1-68 MAR TSH.
Тиреотропный гормон (тиротропина альфа, ТТГ, TSH) - это гликопротеин; углеводная часть субъединиц составляет более 10% их массы и необходимы для нормального тиреотропного действия и внутрисосудистой кинетики.
ТТГ связывается со специфическими рецепторами на поверхности эпителиальных клеток щитовидной железы и стимулирует выработку и активацию тироксина. Рецептор ТТГ представляет собой мембранный GPCR-рецептор, сопряженный с G-белком, который, в свою очередь, активирует аденилатциклазу и увеличивает потребление йода клетками железы. Дальнейшее увеличение уровня цАМФ обусловливает действие ТТГ на биосинтез трийодтиронина (Т3) и тироксина (Т4), которые являются важнейшими гормонами, регулирующими рост и развитие.
Ранее в клинической практике использовали ТТГ выделенный из гипофиза крупного рогатого скота. Так бычий ТТГ использовался для проверки функции щитовидной железы и увеличения поглощения радиоактивного йода у пациентов с раком щитовидной железы. Однако он вызывал побочные аллергические реакции, поэтому после развития технологий рекомбинантной ДНК и появлением возможности искусственного получения гормона от использования ТТГ крупного рогатого скота отказались. Рекомбинантный ТТГ человека (рчТТГ) имеет аминокислотную структуру, идентичную человеческому ТТГ гипофиза и производится модифицированными клеточными линиями на основе клеток китайского хомячка CHO.
Одним из самых известных препаратов рекомбинантного ТТГ человека является препарат Тироджин (rhTSH; Thyrogen®). Он был одобрен FDA США для диагностического использования у пациентов с раком щитовидной железы. Альфа и бета субъединицы Thyrogen® идентичны субъединицам ТТГ гипофиза человека. Thyrogen® имеет удельную активность примерно 4 МЕ/мг и является мощным стимулятором секреции T4, T3 и тиреоглобулина (Tg) у здоровых добровольцев. Он также увеличивает поглощение йодида щитовидной железы у пациентов с раком щитовидной железы или многоузловым зобом и у добровольцев, даже тех, кто подвергается воздействию больших количеств стабильного йодида. Пациенты с раком щитовидной железы, которым была проведена тиреоидэктомия и аблация радиоактивным йодом, но которые имеют риск развития остаточного рака щитовидной железы, являются кандидатами для введения рчТТГ для подготовки к сканированию всего тела с помощью йодида и измерению уровня ТГ в сыворотке. У пациентов с тиреоидэктомированным раком щитовидной железы, которые не могут секретировать ТТГ гипофизом после отмены гормонов щитовидной железы, рчТТГ является единственным приемлемым методом подготовки их к этим процедурам. рчТТГ, помимо того, что он полезен при лечении пациентов с раком щитовидной железы, потенциально полезен для проверки резерва щитовидной железы и для помощи в процедурах ядерной медицины, связанных с щитовидной железой.
В патенте US 6455282 (Genzyme Corporation, США) описаны биологически активные гетерополимерные белки, состоящие из множества субъединиц, в том числе ТТГ, и способы их получения. Показано, что обе субъединицы синтезируются в одной клетке, имеющей вектора экспрессии, содержащие гетерологичную ДНК, кодирующую субъединицы как в составе единой плазмидной ДНК, так и в составе разных плазмидных ДНК. Оба варианта предполагают использование последовательности позднего промотора вируса SV40 для экспрессии гена альфа субъединицы и промотора белка металлотионеина мыши. Также упоминается использование промотора BPV вируса папилломы быка. Действие патента завершено в 2019 году.
В патенте US 7479549 описана нуклеиновая кислота, имеющая последовательность, по меньшей мере на 98% гомологичную последовательности, которая кодирует α-субъединицу собачьего тиреотропного гормона. Изобретение в патенте также включает способ получения субъединицы рекомбинантного собачьего тиреотропного гормона (rcTSH) путем экспрессии последовательностей в трансгенной клетке насекомого, модифицированной сиалированными белками, и получения сиалилированной субъединицы rcTSH для использования в диагностике и лечении гипотиреоз у собак.
В патенте US 20110052591 описан чистый рекомбинантный ТТГ, полученный из клона, содержащего полную нуклеотидную последовательность для экспрессии ТТГ. Описаны полинуклеотидные и полипептидные последовательности, которые кодируют новые варианты белков бета-тиреотропного гормона мыши или человека, которые можно использовать в терапевтических, диагностических и фармакогеномных применениях для предотвращения, лечения или снижения тяжести заболеваний, связанных с тиреотропным гормоном-бета. Представлены варианты конструкций с использованием промотора цитомегаловируса человека.
В патенте US 20190062396 представлен способ получения рекомбинантного тиреоидного гормона человека. В патенте представлена генетическая конструкция, содержащая последовательности генов бета и альфа субъединиц ТТГ, разделенные последовательностью IRES (Internal Ribosome Entry Site - участок внутренней посадки рибосомы), под управлением единого промотора цитомегаловируса человека и терминатора гормона роста быка (BGH), а также последовательности селектирующего белка - дегидрофолатредуктазы (DHFR).
Применение классических подходов с использованием гена DHFR требует длительного времени селекции клона продуцента. Для технического решения проблемы длительного времени селекции клона продуцента была избрана стратегия использования нуклеотидной последовательности удлиненного участка внутренней посадки рибосомы и последовательности PEST в составе фьюжн-белка hDHFR-PEST, что обеспечивает пониженный уровень дегидрофолатредуктазы внутри клетки и приводит к более эффективной селекции в присутствии метотрексата, что позволяет получать линии-продуценты с максимальным уровнем секреции рекомбинантного белка.
Изобретение иллюстрируют следующими графическими материалами.
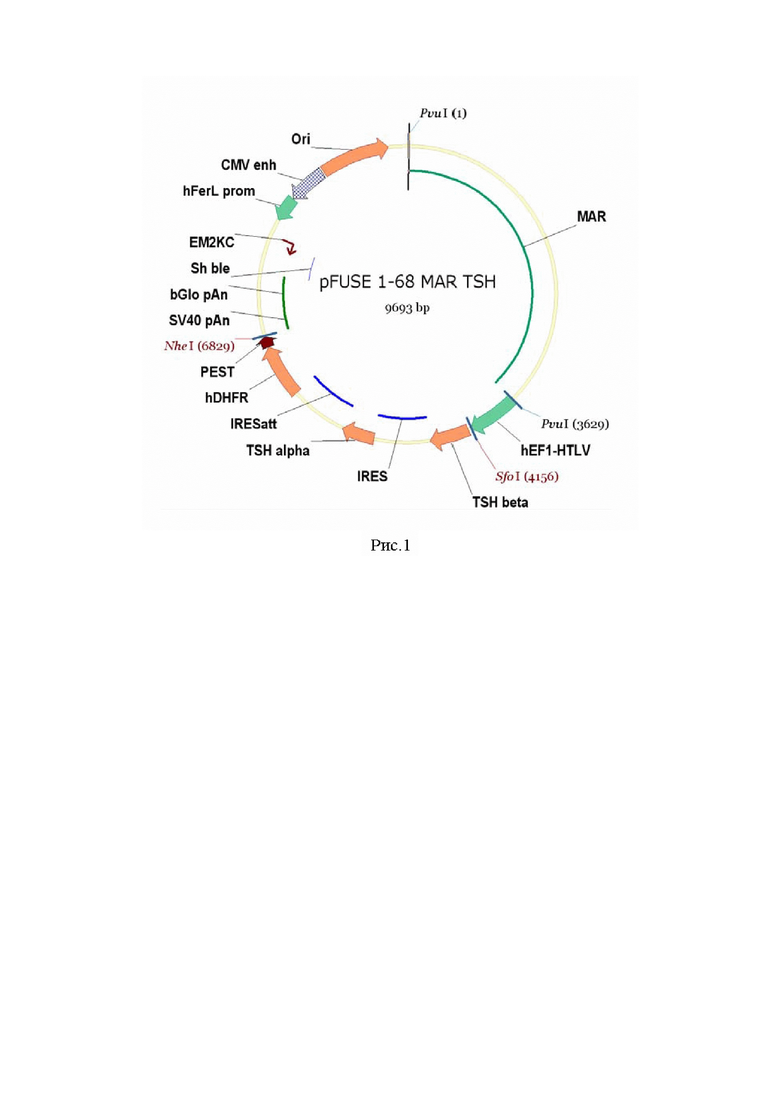
Рис. 1. Схема генетической конструкции - рекомбинантной плазмидной ДНК pFUSE 1-68 MAR TSH, с основными генетическими элементами и ключевыми сайтами гидролиза эндонуклеаз рестрикции.
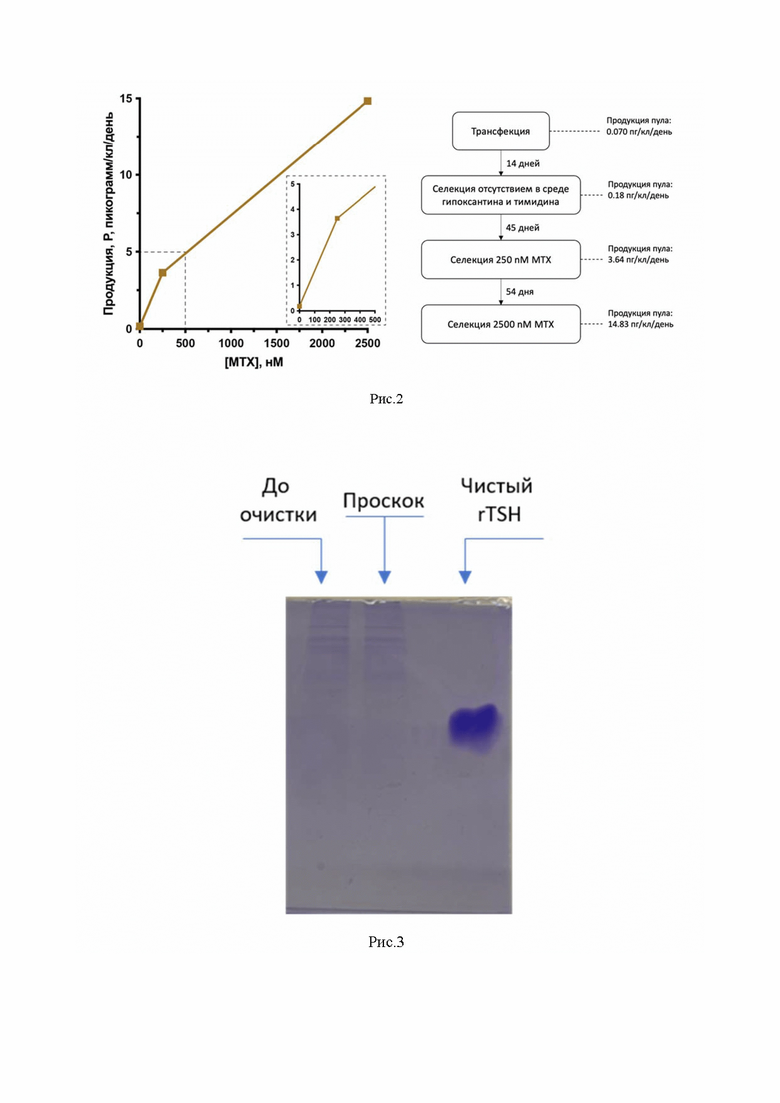
Рис. 2. Схема селекции пула клеток, трансформированных рекомбинантной плазмидной ДНК pFUSE 1-68 MAR TSH.
Рис. 3. Электрофоретический анализ очищенного препарата тиротропина альфа, полученного в результате культивирования клеточной линии rhTSHCHO
В результате решения заявленной технической проблемы получают следующий технический результат:
1. Рекомбинантную плазмидную ДНК pFUSE 1-68 MAR TSH SEQ ID NO: 1, содержащую нуклеотидные последовательности обоих субъединиц тиротропина альфа человека в составе единой мРНК, предпочтительна в настоящем изобретении, т.к. позволяет синтезировать каждой трансформированной единичной клеткой обе субъединицы тиротропина альфа, что уменьшает гетерогенность пула трансформированных клеток, и содержащую:
- нуклеотидную последовательность присоединения к ядерному матриксу MAR1-68, позволяющую повысить продукцию целевого белка за счет как увеличения уровня транскрипции расположенного в непосредственной близости гена, так и за счет большей стабильности комплекса рибосома-транскрипт,
- высокоэффективный синтетический промотор hEF-HTLV,
- нуклеотидную последовательность кДНК гена бета субъединицы тиротропина альфа человека (TSH beta),
- нуклеотидную последовательность участка внутренней посадки рибосомы (IRES), обеспечивающую инициацию трансляции кэп-независимую или внутреннюю инициацию трансляции в эукариотических клетках,
- нуклеотидную последовательность кДНК гена альфа субъединицы тиротропина альфа человека (TSH alpha),
- нуклеотидную последовательность удлиненного участка внутренней посадки рибосомы (IRESatt), обеспечивающую более низкий уровень внутренней инициации трансляции в эукариотических клетках,
- нуклеотидную последовательность кДНК гена дегидрофолатредуктазы человека (hDHFR), обеспечивающей жизнеспособность клеток линии CHO DG44 при росте на синтетических средах, не содержащих гипоксантин и тимидин, и находящуюся в единой рамке считывания с нуклеотидной последовательностью 39 С-концевых аминокислот орнитиндекарбоксилазы мыши (PEST), обеспечивающей быструю деградацию фьюжн-белка hDHFR-PEST.
2. Клеточную линию rhTSHCHO - высокопродуктивную стабильную линию-продуцент рекомбинантного тиреотропный гормона человека (тиротропина альфа), созданную путем трансформации линии CHO DG44 методом нуклеофекции рекомбинантной плазмидной ДНК pFUSE 1-68 MAR TSH, геном которой содержит экспрессионную плазмидную ДНК pFUSE 1-68 MAR TSH, кодирующую кДНК генов альфа и бета субъединиц рекомбинантного тиротропина альфа.
Изобретение иллюстрируют следующими примерами.
ПРИМЕР 1
Создание генетической конструкции pFUSE 1-68 MAR TSH SEQ ID NO: 1
Фрагмент ДНК, содержащий нуклеотидную последовательность MAR1-68, получали методом ПЦР, с использованием в качестве матрицы геномную ДНК клеток НЕК293 и специфических олигонуклеотидов 5- aatacgatcgccctcttgcagatccctgaactgaggag и 5- aatacgatcggcccagtcttgtttctcttaaatcgtccaaacca. Полученный ПЦР-продукт был клонирован в плазмидную ДНК pFuse-hIgG1-Fc2 с использованием эндонуклеазы рестрикции PvuI с получением генетической конструкции pFuse-hIgG1-Fc2-1-68 MAR. Синтетически полученный фрагмент ДНК, содержащий нуклеотидную последовательность, кодирующую кДНК генов альфа и бета субъединиц рекомбинантного тиротропина альфа и нуклеотидную последовательность, кодирующую фьюжн-белок hDHFR-PEST, клонировали в плазмидную ДНК pFuse-hIgG1-Fc2-1-68 MAR с использованием эндонуклеаз рестрикции SfoI и NheI с получением генетической конструкции pFUSE 1-68 MAR TSH (Рис. 1).
ПРИМЕР 2
Получение линии клеток CHO DG44 продуцента рекомбинантного тиротропина альфа человека
Генетической конструкция pFUSE 1-68 MAR TSH были трансформированы клетки CHO DG44 методом нуклеофекции, используя набор реагентов Amaxa Cell Line Nucleofector Kit V (Lonza, Германия) на приборе Nucleofector 2b (Lonza, Германия). Для этого, согласно протоколу производителя, были поставлены 3 реакции нуклеофекции, содержащие 2, 5 и 10 мкг плазмидной ДНК pFUSE 1-68 MAR TSH и по 1 млн клеток DG44. Трансфецированные клетки объединяли в одну 125 мл колбу Эрленмейера (Corning, США), содержащую 30 мл прогретой до 37 °C базовой ростовой среды без добавления гипоксантина и тимидина (ProCHO5, 4 mM глутамин, 4 mM GlutaMAX) и культивировали на орбитальной качалке в инкубаторе (37 °C, 5% CO2, влажность 95%, 125 оборотов/минуту). На 2-е сутки после трансфекции была отобрана проба культуральной жидкости для оценки продукции тиротропина методом ИФА. Продукция пула составила 0.070 пг/кл/день (0.04 мг/л культуры).
Для селекции самых продуктивных клеток и максимальной амплификации генетической кассеты конструкции pFUSE 1-68 MAR TSH в геноме CHO DG44 пул клеток после трансфекции пассировали по схеме, приведённой на Рис. 2. Для этого клетки пассировали в вышеупомянутой среде и условиях в течение 14 дней до восстановления жизнеспособности культуры более 90%. Пересев осуществляли каждые 3-6 дней центрифугированием культуры при 200g, отбором 90% супернатанта и добавлением равного объема свежей среды к оставшейся кондиционной среде с клетками в осадке. По прошествии этого времени жизнеспособность пула клеток составила 93%, продукция пула была 0.18 пг/кл/день (0.504 мг/л культуры).
Затем клетки пассировали вышеописанным способом в такую же среду, но теперь содержащую 250 нМ метотрексата (МТХ, Sigma-Aldrich). Метотрексат является ингибитором дегидрофолатредуктазы человека (hDHFR), что создает дополнительно метаболическое давление на клетки и приводит к накоплению всей генетической кассеты конструкции pFUSE 1-68 MAR TSH. Пассирование при данной концентрации метотрексата осуществляли в течение 45 дней, до достижения жизнеспособности 91%. Продукция пула составила 3.64 пг/кл/день (10.20 мг/л культуры).
Последним этапом клетки пассировали вышеописанным способом в среду, но содержащую 2500 нМ МТХ. Пассирование осуществляли в течение 54 дней, до достижения жизнеспособности 91%. Продукция пула составила 14.83 пг/кл/день (41.52 мг/л культуры).
Полученный высокопродуктивный пул клеток был расклонирован для получения гомогенной линии-продуцента, потомка одной клетки. Для этого клеточная культура была разбавлена до концентрации 3 клетки/мл в базовой среде с добавлением 10% кондиционной среды и раскапана по 100 мкл в лунки десяти 96-ти луночных культуральных планшетов. В тот же день на микроскопе в планшетах были найдены и отмечены лунки, содержащие строго одну клетку на лунку. В таком виде клетки растили в течение 10 дней, после чего содержимое выбранных ранее лунок с единичными клонами переносили для наращивания биомассы в 48-ми и затем в 12-ти луночный планшет. В течение это времени наблюдали относительную скорость роста клонов. Клоны с оптимальной скоростью роста и показателями жизнеспособности были отобраны для оценки продукции методом ИФА. Из 14-ти моноклонов по показателям продукции на клетку в планшете было выбрано 6 лучших для анализа экспрессии в колбах и для заморозки посевного пула клеток. Следующим этапом два лучших по продукции клона были отобраны для исследования стабильности продукции, для чего линии пассировали в течение трех недель и затем их снова использовали для наработки тиротропина. Линия с минимальным изменением показателей экспрессии была использована для получения главного банка клеток.
--->
<?xml version="1.0" encoding="UTF-8"?>
<!DOCTYPE ST26SequenceListing PUBLIC "-//WIPO//DTD Sequence Listing
1.3//EN" "ST26SequenceListing_V1_3.dtd">
<ST26SequenceListing originalFreeTextLanguageCode="ru"
dtdVersion="V1_3" fileName="Рекомбинантная плазмидная ДНК, кодирующая
последовательность белка тиротропина альфа, клеточная линия rhTSHCHO,
трансформированная плазмидной ДНК и секретирующая рекомбинантный
тиреотропный гормон человека.xml" softwareName="WIPO Sequence"
softwareVersion="2.2.0" productionDate="2024-07-03">
<ApplicantFileReference>1</ApplicantFileReference>
<ApplicantName languageCode="ru">ИБХ РАН, ЭНЦ</ApplicantName>
<ApplicantNameLatin>Shemyakin-Ovchinnikov Institute of bioorganic
chemistry, Endocrinology research center</ApplicantNameLatin>
<InventionTitle languageCode="ru">Рекомбинантная плазмидная ДНК,
кодирующая последовательность белка тиротропина альфа, клеточная
линия rhTSHCHO, трансформированная плазмидной ДНК и секретирующая
рекомбинантный тиреотропный гормон человека</InventionTitle>
<SequenceTotalQuantity>1</SequenceTotalQuantity>
<SequenceData sequenceIDNumber="1">
<INSDSeq>
<INSDSeq_length>9693</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..9693</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q2">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>Synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>cgccctcttgcagatccctgaactgaggaggcaagatcagtttggcagt
tgaagcagctggaatctgcaattcagagaatctaagaaaagacaaccctgaagagagagacccagaaacc
tagcaggagtttctccaaacattcaaggctgagggataaatgttacatgcacagggtgagcctccagagg
cttgtccattagcaactgctacagtttcattatctcagggatcacagattgtgctacctattgcctacca
tctgaaaacagttgcttcctatatttcatccagtttaatatttatttaaaccaagaaggttaatctggca
ccagctattccgttgtgagtggatgtgaaagtaccaattccattctgttttactattaactatcctttgc
cttaatatgtatcagtaggtggcttgttgctaggaaatattaaatgaatggcatgtttcataggttgtgt
ttaaagttgttttttgagttaaatctttctttaataatactttctgatgtcaaaaacacttagaagtcat
ggtgttgaacatctatatagggttggatctaaaatagcttcttaacctttcctaaccactgtttttgttt
gtttgtttttaactaagcatccagtttgggaaattctgaattaggggaatcataaaaggtttcattttag
ctgggccacataaggaaagtaagatatcaaattgtaaaaatcgttaagaacttctatcccatctgaagtg
tgggttaggtgcctcttctctgtgctcccttaacatcctattttatctgtatatatatatattcttccaa
atatccatgggaaaaaaaatctgatcataaaaatattttaggctgggagtggtggctcacgcctgtaatc
ccagcactttgggaggctgaggtgggcggatcatgaggtcaagagatcgagaccatcctgaccaatatgg
tgaaaccccatctctactaaagatacaaaactattagctggacgtggtggcacgtgcctgtagtcccagc
tactcgggaggctgaggcaggagaacggcttgaacccaggaggtggaggttgcagtgagctgagatcgcg
ccactgcactccagcctgggcgacagagcgagactctgtctcaaaaaaaaaatatatatatatatatata
tacacatatatatataaaatatatatatatacacacatatatatataaaatatatatatatacacacata
tatataaaatatatatatatacacacatatatataaaatatatatatacacacatatatataaaatatat
atatacacacatatatataaaatatatatatacacacatatatataaaatatatatatacacacatatat
ataaaatatatatatacacacatatatataaaatatatatatacacacatatatataaaatatatatata
cacacatatatataaaatatatatatacacacatatatataaaatatatatatacacacatatatataaa
atatatatatacacacatatataaaatatatatatacacacatatataaaatatatatatacacatatat
ataaaatatatatatacacatatatataaaatatatatacacacatatatataaaatatatatatacaca
catatatataaaatatatatatacacatatatataaaatatatatatacacatatatataaaatatatat
atatacacatatatataaaatatatatacacacatatatataaagtatatatatacacacatatatataa
aatatatatatacacatatatataaaatatatatatacacatatatataaaatatatatatacacatata
tataaaaatatatatatatattttttaaaatattccaattgtctcactttgtggatgagaaaaagaagta
gttagaggtcaagtaacttggcctacatcttttctcaagattgtaaactcctagtgagcaataaccacat
cttcattttctttgtataaaacaagaaagtttagcatgaaaaaggtactcaattacaaatgtgttggatt
gaattgaagacccttggaaggggattttgtacctgaggatctctttcttttggccatattgttcaatgga
caaaatttagccttcgaaggcaggccgatttgaggttaatactacctttaccacttgatagctatgtgac
cttggccatgtggtttcaacagtctgaacctcattttctctgtgtatgtgtggtcctccttacaagtttg
tgaaaaatgtgaagtccttagccatgatagcccaatataacaggctaaatgataataggtttatgttctt
ttcctttatattctcagataagcactgtccaagtttgaggtgttttgaggtctcgcctgatttggattgt
ttgagtttatgctattctttgaattctttgagctgttctgaagcagtgtatcatgaacaaaaacatcccc
agttcagtccaaacccctggttacatatcattcttatgccatgttataaccagtttgagagtgttccctc
tgttattgcatttaagtttcagcctcacacagaaattcagcagccaatttctaagccctaagcataaaat
ctggggtgggggggggggatggcctgaagagcagcattatgaatagcaccattataattaatgatctctc
aggaagatttacaatcacaggtagcagataaaacaaatagtactgcttctgcacttcccctccttttatt
cgctatgaaattttatgggaaatcagtccagtgaaaaatgtaagctcttaatctttcccagaaatcctac
ctcatttgatgaatactttgagggaatgaattagagcatttttttcttttatagtctacttcgcatttac
gaagtgaggacggtagcttaggctgcctggccaactgatgagaaggtcagaggcatttttagagacctct
gttgtctttcattcatgttcattttccacaaggcaagtaatttccaacaaatcagtgtcttcattagtaa
taagattattaacaacaataatagtcatagtaactattcagtgagagtccattatatatcaggcattcta
caaggtactttatatacatctgagtaaacctcacacaattctacagggaggtatttctatccccatttaa
caaataaggaaacgaagtccaagtaaattaacttgcccaaggtcacacagatagtacctggcagaacagg
aatttaaacctaaatttgtccaactccaaaagcagccttctatttgttataaatgctgcctctcattatc
acatattttattattaacaacaacaaacataccaattagcttaagatacaatacaaccagataatcatga
tgacaacagtaattgttatactattataataaaatagatgttttgtatgttactataatcttgaatttga
atagaaatttgcatttctgaaagcatgttcctgtcatctaatatgattctgtatctattaaaatagtact
acatctagagttctactactagatttatttatcactgagaatggtttggacgatttaagagaaacaagac
tgggccgatcgctccggtgcccgtcagtgggcagagcgcacatcgcccacagtccccgagaagttggggg
gaggggtcggcaattgaacgggtgcctagagaaggtggcgcggggtaaactgggaaagtgatgtcgtgta
ctggctccgcctttttcccgagggtgggggagaaccgtatataagtgcagtagtcgccgtgaacgttctt
tttcgcaacgggtttgccgccagaacacagctgaagcttcgaggggctcgcatctctccttcacgcgccc
gccgccctacctgaggccgccatccacgccggttgagtcgcgttctgccgcctcccgcctgtggtgcctc
ctgaactgcgtccgccgtctaggtaagtttaaagctcaggtcgagaccgggcctttgtccggcgctccct
tggagcctacctagactcagccggctctccacgctttgcctgaccctgcttgctcaactctacgtctttg
tttcgttttctgttctgcgccgttacagatccaagctgtgaccggcgcctacctgagatcaccggcgaag
gagggccaccatgactgctctctttctgatgtccatgctttttggccttgcatgtgggcaagcgatgtct
ttttgtattccaactgagtatacaatgcacatcgaaaggagagagtgtgcttattgcctaaccatcaaca
ccaccatctgtgctggatattgtatgacacgggatatcaatggcaaactgtttcttcccaaatatgctct
gtcccaggatgtttgcacatatagagacttcatctacaggactgtagaaataccaggatgcccactccat
gttgctccctatttttcctatcctgttgctttaagctgtaagtgtggcaagtgcaatactgactatagtg
actgcatacatgaagccatcaagacaaactactgtaccaaacctcagaagtcttatctggtaggattttc
tgtctaatagccctcccccccccctaacgttactggccgaagccgcttggaataaggccggtgtgcgttt
gtctatatgttattttccaccatattgccgtcttttggcaatgtgagggcccggaaacctggccctgtct
tcttgacgagcattcctaggggtctttcccctctcgccaaaggaatgcaaggtctgttgaatgtcgtgaa
ggaagcagttcctctggaagcttcttgaagacaaacaacgtctgtagcgaccctttgcaggcagcggaac
cccccacctggcgacaggtgcctctgcggccaaaagccacgtgtataagatacacctgcaaaggcggcac
aaccccagtgccacgttgtgagttggatagttgtggaaagagtcaaatggctctcctcaagcgtattcaa
caaggggctgaaggatgcccagaaggtaccccattgtatgggatctgatctggggcctcggtgcacatgc
tttacatgtgtttagtcgaggttaaaaaaacgtctaggccccccgaaccacggggacgtggttttccttt
gaaaaacacgatgataatatggccacaaccatggattactacagaaaatatgcagctatctttctggtca
cattgtcggtgtttctgcatgttctccattccgctcctgatgtgcaggattgcccagaatgcacgctaca
ggaaaacccattcttctcccagccgggtgccccaatacttcagtgcatgggctgctgcttctctagagca
tatcccactccactaaggtccaagaagacgatgttggtccaaaagaacgtcacctcagagtccacttgct
gtgtagctaaatcatataacagggtcacagtaatggggggtttcaaagtggagaaccacacggcgtgcca
ctgcagtacttgttattatcacaaatcttaatagccctcccccccccctaacgttactggccgaagccgc
ttggaataaggccggtgtgcgtttgtctatatgttattttccaccatattgccgtcttttggcaatgtga
gggcccggaaacctggccctgtcttcttgacgagcattcctaggggtctttcccctctcgccaaaggaat
gcaaggtctgttgaatgtcgtgaaggaagcagttcctctggaagcttcttgaagacaaacaacgtctgta
gcgaccctttgcaggcagcggaaccccccacctggcgacaggtgcctctgcggccaaaagccacgtgtat
aagatacacctgcaaaggcggcacaaccccagtgccacgttgtgagttggatagttgtggaaagagtcaa
atggctctcctcaagcgtattcaacaaggggctgaaggatgcccagaaggtaccccattgtatgggatct
gatctggggcctcggtgcacatgctttacatgtgtttagtcgaggttaaaaaaacgtctaggccccccga
accacggggacgtggttttcctttgaaaaacacgatgataagcttgccacaacccgggatcctctagagt
cgacatggttggttcgctaaactgcatcgtcgctgtgtcccagaacatgggcatcggcaagaacggggac
ctgccctggccaccgctcaggaatgaattcagatatttccagagaatgaccacaacctcttcagtagaag
gtaaacagaatctggtgattatgggtaagaagacctggttctccattcctgagaagaatcgacctttaaa
gggtagaattaatttagttctcagcagagaactcaaggaacctccacaaggagctcattttctttccaga
agtctagatgatgccttaaaacttactgaacaaccagaattagcaaataaagtagacatggtctggatag
ttggtggcagttctgtttataaggaagccatgaatcacccaggccatcttaaactatttgtgacaaggat
catgcaagactttgaaagtgacacgttttttccagaaattgatttggagaaatataaacttctgccagaa
tacccaggtgttctctctgatgtccaggaggagaaaggcattaagtacaaatttgaagtatatgagaaga
atgatcacggcttccctcccgaggtggaggagcaggccgccggcaccctgcccatgagctgcgcccagga
gagcggcatggatagacaccctgctgcttgcgccagcgccaggatcaacgtctaataggctagctggcca
gacatgataagatacattgatgagtttggacaaaccacaactagaatgcagtgaaaaaaatgctttattt
gtgaaatttgtgatgctattgctttatttgtaaccattataagctgcaataaacaagttaacaacaacaa
ttgcattcattttatgtttcaggttcagggggaggtgtgggaggttttttaaagcaagtaaaacctctac
aaatgtggtatggaattaattctaaaatacagcatagcaaaactttaacctccaaatcaagcctctactt
gaatccttttctgagggatgaataaggcataggcatcaggggctgttgccaatgtgcattagctgtttgc
agcctcaccttctttcatggagtttaagatatagtgtattttcccaaggtttgaactagctcttcatttc
tttatgttttaaatgcactgacctcccacattccctttttagtaaaatattcagaaataatttaaataca
tcattgcaatgaaaataaatgttttttattaggcagaatccagatgctcaaggcccttcataatatcccc
cagtttagtagttggacttagggaacaaaggaacctttaatagaaattggacagcaagaaagcgagcttc
tagcttatcctcagtcctgctcctctgccacaaagtgcacgcagttgccggccgggtcgcgcagggcgaa
ctcccgcccccacggctgctcgccgatctcggtcatggccggcccggaggcgtcccggaagttcgtggac
acgacctccgaccactcggcgtacagctcgtccaggccgcgcacccacacccaggccagggtgttgtccg
gcaccacctggtcctggaccgcgctgatgaacagggtcacgtcgtcccggaccacaccggcgaagtcgtc
ctccacgaagtcccgggagaacccgagccggtcggtccagaactcgaccgctccggcgacgtcgcgcgcg
gtgagcaccggaacggcactggtcaacttggccatgatggctcctcctgtcaggagaggaaagagaagaa
ggttagtacaattgctatagtgagttgtattatactatgcagatatactatgccaatgattaattgtcaa
actagggctgcagggttcatagtgccacttttcctgcactgccccatctcctgcccaccctttcccaggc
atagacagtcagtgacttaccaaactcacaggagggagaaggcagaagcttgagacagacccgcgggacc
gccgaactgcgaggggacgtggctagggcggcttcttttatggtgcgccggccctcggaggcagggcgct
cggggaggcctagcggccaatctgcggtggcaggaggcggggccgaaggccgtgcctgaccaatccggag
cacataggagtctcagccccccgccccaaagcaaggggaagtcacgcgcctgtagcgccagcgtgttgtg
aaatgggggcttgggggggttggggccctgactagtcaaaacaaactcccattgacgtcaatggggtgga
gacttggaaatccccgtgagtcaaaccgctatccacgcccattgatgtactgccaaaaccgcatcatcat
ggtaatagcgatgactaatacgtagatgtactgccaagtaggaaagtcccataaggtcatgtactgggca
taatgccaggcgggccatttaccgtcattgacgtcaatagggggcgtacttggcatatgatacacttgat
gtactgccaagtgggcagtttaccgtaaatactccacccattgacgtcaatggaaagtccctattggcgt
tactatgggaacatacgtcattattgacgtcaatgggcgggggtcgttgggcggtcagccaggcgggcca
tttaccgtaagttatgtaacgcctgcaggttaattaagaacatgtgagcaaaaggccagcaaaaggccag
gaaccgtaaaaaggccgcgttgctggcgtttttccataggctccgcccccctgacgagcatcacaaaaat
cgacgctcaagtcagaggtggcgaaacccgacaggactataaagataccaggcgtttccccctggaagct
ccctcgtgcgctctcctgttccgaccctgccgcttaccggatacctgtccgcctttctcccttcgggaag
cgtggcgctttctcatagctcacgctgtaggtatctcagttcggtgtaggtcgttcgctccaagctgggc
tgtgtgcacgaaccccccgttcagcccgaccgctgcgccttatccggtaactatcgtcttgagtccaacc
cggtaagacacgacttatcgccactggcagcagccactggtaacaggattagcagagcgaggtatgtagg
cggtgctacagagttcttgaagtggtggcctaactacggctacactagaagaacagtatttggtatctgc
gctctgctgaagccagttaccttcggaaaaagagttggtagctcttgatccggcaaacaaaccaccgctg
gtagcggtggtttttttgtttgcaagcagcagattacgcgcagaaaaaaaggatctcaagaagatccttt
gatcttttctacggggtctgacgctcagtggaacgaaaactcacgttaagggattttggtcatggctagt
taattaacatttaaatcagcggccgcaataaaatatctttattttcattacatctgtgtgttggtttttt
gtgtgaatcgtaactaacatacgctctccatcaaaacaaaacgaaacaaaacaaactagcaaaataggct
gtccccagtgcaagtgcaggtgccagaacatttctctatcgaaggatctgcgat</INSDSeq_sequen
ce>
</INSDSeq>
</SequenceData>
</ST26SequenceListing>
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pBiPr-ABIgA1FI6-Intht ДЛЯ ПОЛУЧЕНИЯ РЕКОМБИНАНТНОГО ИММУНОГЛОБУЛИНА А ИЗОТИПА IgA1 | 2016 |
|
RU2664184C2 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pBiPr-ABIgA2m1F16-ht ДЛЯ ПОЛУЧЕНИЯ РЕКОМБИНАНТНОГО ИММУНОГЛОБУЛИНА А ИЗОТИПА IGA2m1 | 2016 |
|
RU2671477C2 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pBiPr-ABIgA1FI6-ht ДЛЯ ПОЛУЧЕНИЯ РЕКОМБИНАНТНОГО ИММУНОГЛОБУЛИНА А ИЗОТИПА IGA1 | 2016 |
|
RU2656142C1 |
| СПОСОБ ПОЛУЧЕНИЯ РЕКОМБИНАНТНОГО ИММУНОГЛОБУЛИНА IGA2m1-ИЗОТИПА В КЛЕТКАХ МЛЕКОПИТАЮЩИХ | 2022 |
|
RU2801178C1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК, КОДИРУЮЩАЯ ХИМЕРНОЕ АНТИТЕЛО ПРОТИВ ФАКТОРА НЕКРОЗА ОПУХОЛИ-АЛЬФА ЧЕЛОВЕКА, ЛИНИЯ ЭУКАРИОТИЧЕСКИХ КЛЕТОК-ПРОДУЦЕНТ ХИМЕРНОГО АНТИТЕЛА И СПОСОБ ПОЛУЧЕНИЯ ХИМЕРНОГО АНТИТЕЛА | 2013 |
|
RU2555533C9 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК, КОДИРУЮЩАЯ ПОСЛЕДОВАТЕЛЬНОСТЬ БЕЛКА ФАКТОРА VII ЧЕЛОВЕКА, ЛИНИЯ КЛЕТОК ВНК/F7, ТРАНСФОРМИРОВАННАЯ ПЛАЗМИДНОЙ ДНК | 2006 |
|
RU2337965C2 |
| Плазмида для экспрессии рекомбинантного хорионического гонадотропина человека (ХГЧ), плазмида для экспрессии рекомбинантных альфа- и бета-субъединиц ХГЧ, моноклональная линия клеток млекопитающих - продуцент ХГЧ, способ получения рекомбинантного ХГЧ | 2024 |
|
RU2834784C1 |
| ПЛАЗМИДА ДЛЯ ЭКСПРЕССИИ РЕКОМБИНАНТНОГО ФАКТОРА СВЁРТЫВАЕМОСТИ КРОВИ IX ЧЕЛОВЕКА, КЛЕТКА СНО - ПРОДУЦЕНТ РЕКОМБИНАНТНОГО ФАКТОРА СВЁРТЫВАЕМОСТИ КРОВИ IX ЧЕЛОВЕКА И СПОСОБ ПОЛУЧЕНИЯ УКАЗАННОГО ФАКТОРА | 2014 |
|
RU2585532C2 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pFUSE-MARX-29-PRAD-F2A/BChE-14, СОДЕРЖАЩАЯ ГЕН МОДИФИЦИРОВАННОЙ БУТИРИЛХОЛИНЭСТЕРАЗЫ ЧЕЛОВЕКА, ПРЕДНАЗНАЧЕННАЯ ДЛЯ ЭКСПРЕССИИ ГЕНА БУТИРИЛХОЛИНЭСТЕРАЗЫ В КЛЕТКАХ МЛЕКОПИТАЮЩИХ ДЛЯ ТЕРАПИИ ОТРАВЛЕНИЙ ФОСФОРОРГАНИЧЕСКИМИ ТОКСИНАМИ | 2016 |
|
RU2688729C1 |
| Способ получения димерной формы иммуноглобулина IgA1-изотипа в клетках млекопитающих | 2023 |
|
RU2822890C1 |
Изобретение относится к области генной инженерии и биотехнологии. Предложены рекомбинантная плазмидная ДНК pFUSE 1-68 MAR TSH с SEQ ID NO: 1, кодирующая кДНК генов альфа и бета субъединиц рекомбинантного тиротропина альфа, и клеточная линия клеток яичника китайского хомячка rhTSHCHO, продуцирующая рекомбинантный тиротропин альфа человека и созданная путем трансформации линии CHO DG44 методом нуклеофекции вышеуказанной рекомбинантной плазмидной ДНК. Изобретение позволяет получить высокопродуктивную стабильную линию-продуцент рекомбинантного тиротропина альфа человека, а также синтезировать обе субъединицы тиротропина альфа, что уменьшает гетерогенность пула трансформированных клеток. 2 н.п. ф-лы, 3 ил., 2 пр.
1. Рекомбинантная плазмидная ДНК pFUSE 1-68 MAR TSH SEQ ID NO: 1, кодирующая кДНК генов альфа и бета субъединиц рекомбинантного тиротропина альфа и содержащая нуклеотидную последовательность присоединения к ядерному матриксу MAR1-68, синтетический промотор hEF-HTLV, нуклеотидную последовательность кДНК гена бета субъединицы тиротропина альфа человека (TSH beta), нуклеотидную последовательность участка внутренней посадки рибосомы (IRES), нуклеотидную последовательность кДНК генов альфа субъединицы тиротропина альфа человека (TSH alpha), нуклеотидную последовательность удлиненного участка внутренней посадки рибосомы, нуклеотидную последовательность кДНК гена дегидрофолатредуктазы человека (hDHFR), находящуюся в единой рамке считывания с нуклеотидной последовательностью 39 С-концевых аминокислот орнитиндекарбоксилазы мыши.
2. Клеточная линия клеток яичника китайского хомячка rhTSHCHO - продуцент рекомбинантного тиротропина альфа человека, созданная путем трансформации линии CHO DG44 методом нуклеофекции рекомбинантной плазмидной ДНК pFUSE 1-68 MAR TSH по п.1.
| СМИРНОВ И.В и др | |||
| Получение отечественного препарата рекомбинантного тиреотропного гормона человека для использования в клинической практике | |||
| Инновационные технологии в эндокринологии: Сборник тезисов IV (XXVII) Национального конгресса эндокринологов с международным участием, Москва, 22-25 сентября 2021 года, с | |||
| Русская печь | 1919 |
|
SU240A1 |
| US 20190062396 A1, | |||
Авторы
Даты
2025-06-06—Публикация
2024-07-10—Подача