рого подтверждает его соответствие указанной структуре.
5 г полученного таким образом П0о-. межуточного продукта добавляют к раствору, состоящему из 5 г NaOH в 100 мл 5 воды, и эту операцию проводят при перемешивании и при температуре 60°С. После того, как раствор становится чистым, его подвергают охлаждению до комнатной температуры и Далее до- to бавляют 10 мл концентрированной хлористоводородной кислоты. Образовавшийся в результате остаток отделяют и подвергают экстрагированию хлороформом (три раза по 50-мл)о После вы-15 паривания растворителя получают 2,7 г 1-изопропил-3 хлор-5-оксипиразола (характеризуемого температурой точки плавления, равной 138-1 0С,
Масса, спектр ядерно-магнитного ре-м зонанса и инфракрасный спектр так же, как и элементный анализ,подтверждают соответствие полученного продукта указанной структуре.
Пример 3. Получение 0,0-ди- 25 метил-0-(1-фенил-З-хлорпиразол-5-ил)тиофосфата.
К 5 г 1-фенил-З-хлор-5-оксипиразола б 120 мл ацетона добавляют 5,3 г K. и 4,12 г 0,0-диметилтиофосфо- зо рилхлорида. Полученную реакционную смесь перемешивают в течение 4ч, , а далее фильтруют с тем, чтобы удалить неорганические соли. После выпаривания растворителя получают 8 г 35 0,0-диметил-0-С1-фенил-3-хлорпиразрл-5-ил)тиофосфата, представляющего собой масло (см, табл, 1, соединение О,
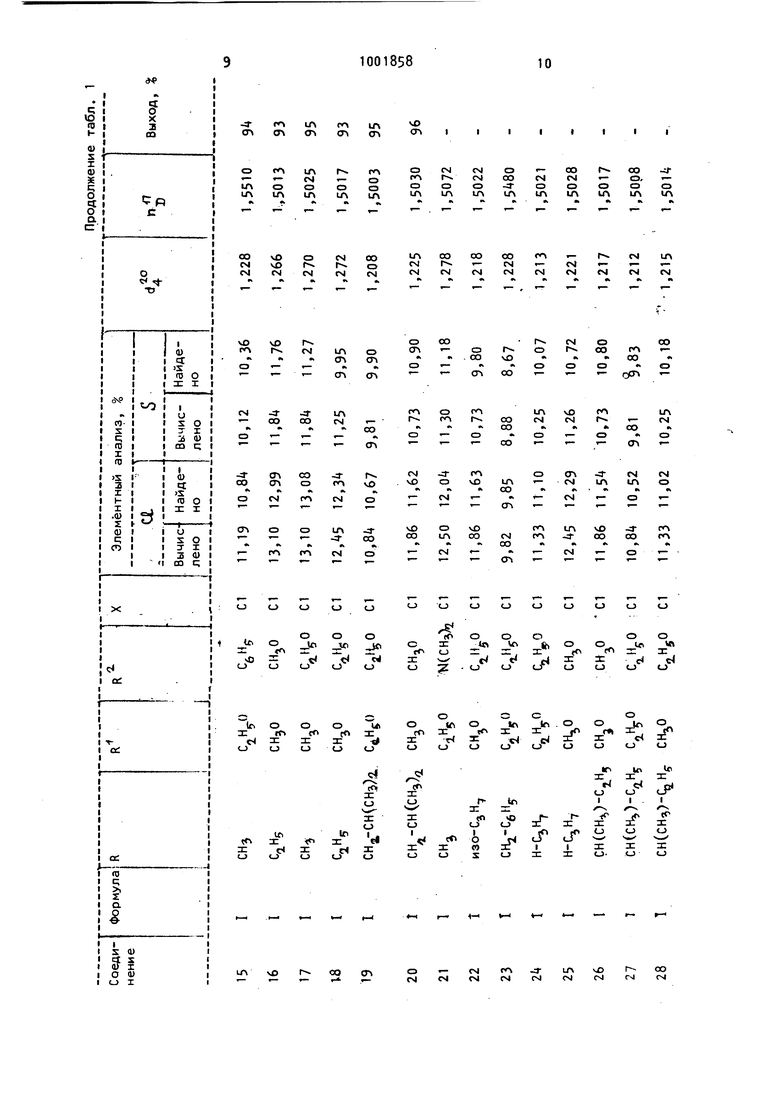
Аналогично получают другие фосфо, рилированные 5(3)окспиразолы, физико-химические характеристики и выход которых представлены в табл, 1.
Соединения, характеризуемые общими формулами 1 и 11, обладают значительной активностью против таких насекомых как lepltoptera, dlptera и coleoptera.
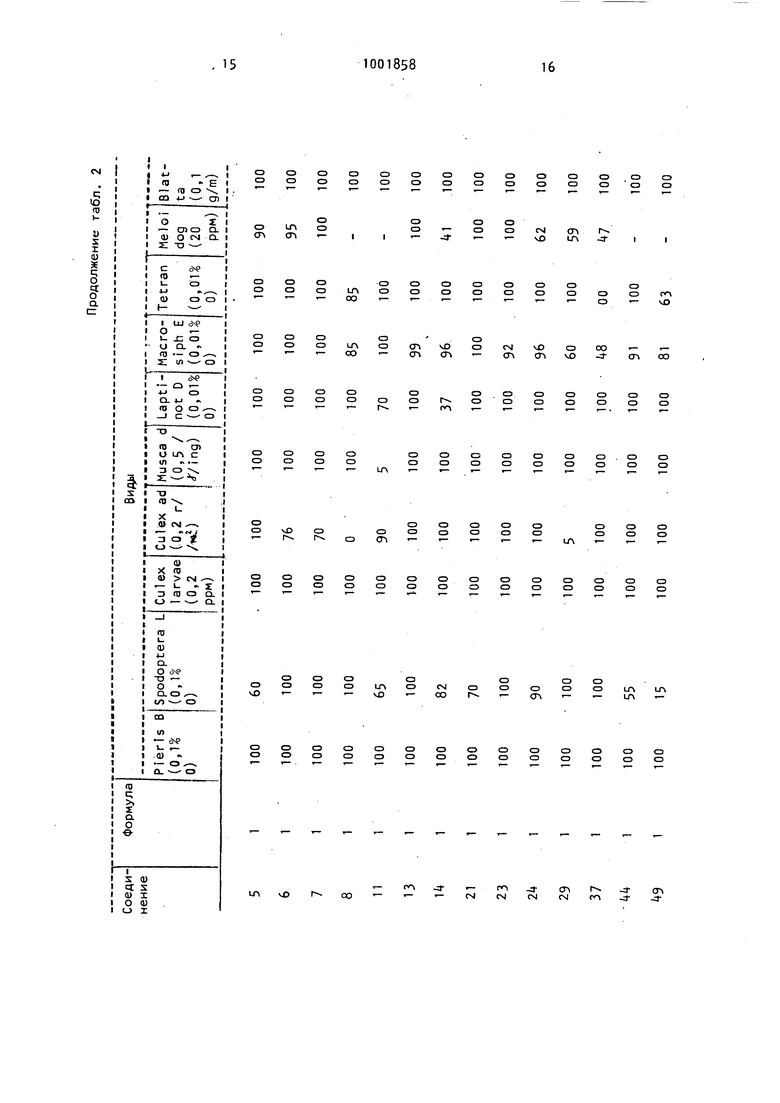
Активность против насекомых представлена в табл, 2 в сравнении с данными для пиразотиона.
Как видно из:табл, 2, полученные соединения обладают превосходной активностью по сравнению с пиразотионом для Blatta и Macrosiphum, но неожиданно и против Spodopteka, , Musca, Zeptinotarsa Meloldogine ncoghita, no отношению к которым пиразотион оказывается неэффективным.
Новые соединега1я обладают другой неожиданной характеристикой, делающей их ценными для использования в качестве инсектицидов. В действительности они обладают относительно низкий токсичностью по отнсшетю к животным. Их токсичность, как указано-ниже значительно меньше, чем токсичность пиразотиона.
Ниже приведена токсичность в опытах на крысах
Соединение Смертельная доза 50(U3)) , мг/кг Живого цеса: 2155
1400
4800
6175
Пиразотион Зб СПР СП00 -J-LTlUnCN)о оил о- оо оо 1Л1Г илил оол ол- оо илил






| название | год | авторы | номер документа |
|---|---|---|---|
| Гербицидная композиция | 1978 |
|
SU1019990A3 |
| Сумматор по модулю пятнадцать | 1989 |
|
SU1603375A1 |
| Способ предварительного нагрева лома в конвертере | 1981 |
|
SU968075A1 |
| Способ определения дипрофена | 1980 |
|
SU930085A1 |
| Способ получения спиртов С @ из побочных продуктов производства бутанолов | 1987 |
|
SU1509349A1 |
| Способ борьбы с нежелательными растениями | 1985 |
|
SU1715190A3 |
| Полиэфирная композиция | 1980 |
|
SU937487A1 |
| Способ борьбы с нежелательной растительностью | 1980 |
|
SU980602A3 |
| Способ получения вяжущего | 1980 |
|
SU947116A1 |
| Сополимер @ , @ -дигидроперфторгептилакрилата,N-диметиламиноэтилметакрилата и N-метилолметакриламида для придания текстильным материалам маслоотталкивающих и грязеудаляющих свойств | 1980 |
|
SU937469A1 |

Г-ГЛООО1ЛСГ иЛООоо
ff rf г- -СМ - - со vO со - t 4CMfMCMCvJC Jrgc JtNCNj
очо
г-CNj
чо
л CD
оо «---
го
г-
ил
СМ
«о
ол -
GOГ
CSI
со
ол
г
см см со
г- см .Зо
о- j 5
о
In
Icl
J
О чО - tN
CNl (SICS
со-
смсм
СП
см -d чоил
-3ол
см «г-«
-со
см
,-о
осз
--
ол .-ол-
оо
гл
ол
ЧО
ил
ил
ил
- гоо
-Чоо
гч
чО со см оо
о
- со
СП-
со
см
СП
га ил
-i-аго о
сэ о
.-
-JчО
-дчО
ол
rg
см
см
СП
го го
vO
- ил
и
ол
ил со оо
Ол
СП
00
ол г
см
о
r
ff
сinо
с
tn
If.
{)
о
m
d cJ
: I
с«-(
л:
ооо о cj
X
z о
()
d
d
л:
СУ-оi:д: (J
о I
rfx
m
со
а: о i:
х I I X (
in (J
о зсз: и
со
ол
чО
2 СО
С
ш ct s
та о з: г
V3
I
и
Sо
тI
ji(1
DOц
ш ct 2:
(D О
з: I
о
Sо
тI
2О
СОс;
«
та , а
31 о 0) I
о о
о о о о
х
СПI
00
оо о
vDI« ОО
о о со -3ол -Л ол o
оо о
о г о о - СП t- о о о о о о о о
о о сэ о
0000
о о сэ о о о о о
о о
оо(Мо
--ОООО
о о о сэ са сз
см го -ата Е - (О о -. ОО 4J -- О) оZ I-СП CDо. ШО CVJО. з:тз - с I-t3 ,-, 0)00
о о
сз
сэ сз
сз
- о т-
о
сэ сз
сэ о
и о
о
СХ 4-1 о
га о сэ ,- | с -- сэ
го о
о о
сэ о
сэ сэ О 1Л с
(П « -
31
ТЭ
о L. X
о сэ
да см х-.
чО
сэ
г
и о г
- -ч
о о
о о
сэ
о
Z
о.
QL
о
о
о
CD
сэ чО
о о
сэ о
о о
ш
а о е
ч
сэ сэ
vD
схэ
D CTv
см
сэ
СП со vO
СП
СП
сэ о
CD
сэ сэ
сэ сэ
сэ
сэ
r
сэ сэ о
о
сэ
ОО
о сэ
о сэ
сэ сэ
о сэ
о о
CD
сэ
о о о
сэ
о
CD CD
сэ
о
о
сэ
сэ
CD
сз
сз о
сз
CD
LAг---
о о
сз
сэ сэ
о сэ
о сз
о о
сэ
сэ о
о
сэ
о
о о
сэ
CM CO
CD
LA LA
сэ
сэ сгч
о о
О
о о
сз
сэ
CD
CD
о о
сэ
CD
сэ
CD
о
г
m
сг
-сг
а
-3-зг -
.- см
Гч|
см
-3ГАCN -3о о сэ сэ см D сэ rf г-чО
n
тI
о.о
SS
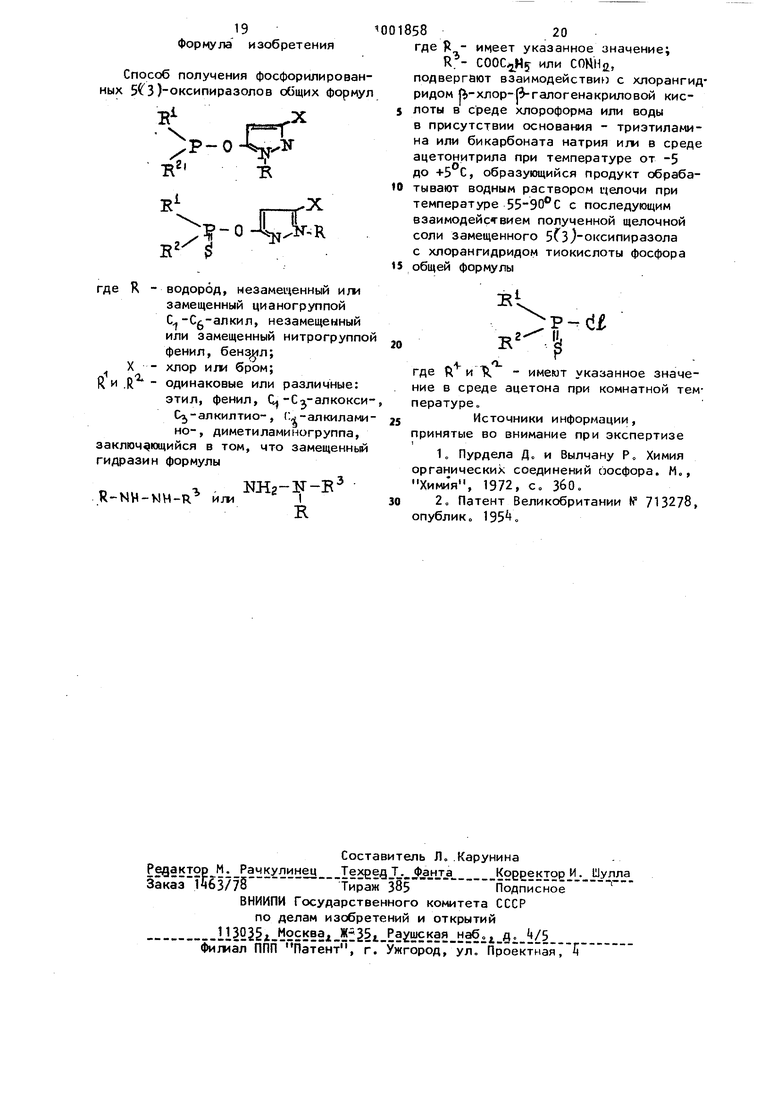
с:ь 19 Формула изобретения Способ получения фосфорилирова ных )оксипиразолов общих форм .цр-0-о К где R водород, незамеченный или замещенный цианогруппой Ц-Сг-алкил, незамещенный или замещенный нитрогруппо фенил, бензол; хлор или бром; одинаковые или различные: этил, фенил, (Ц-Са-алкокси С1,-алкилтио-, C.rf-aлкилa 4 но-, диметиламиногруппа, заключающийся в том, что замещенный гидразин формулы а . NHs-lT-B R-NH-MM-R и/иI sS где Я - имеет указанное значение; или СОНН, подвергают взаимодействию с хлорангидРИДОМ Л-хлор-| -гапогенакриловой кислоты в среде хлороформа или воды в присутствии основания - триэтиламина или бикарбоната натрия или в среде ацетонитрила при температуре от -5 до +5 С, образующийся продукт обрабатывают водным раствором щелочи при температуре 55-90 С с последующим взаимодействием полученной щелочной соли замещенного 5Сз)оксипиразола с хлорангидридом тиокислоты фосфора общей формулы ..4- . где кик имеют указанное значение в среде ацетона при комнатной температуре. Источники информации, принятые во внимание при экспертизе 1„ Пурдела Д„ и Вылчану Р, Химия органических соединений оосфора. М., Химия, 1972, Со 360, 2 Патент Великобритании К° 713278, опублико 
Авторы
Даты
1983-02-28—Публикация
1979-06-18—Подача