О
о:
N0 ГО
ел
4
Изобретение относится к спиртовой про1-1ышленности, а именно к способам определения декстринолитической активности (активности фермента олигоot-1,6-глюкозидаэы, или декстриназы солодов.
Известны способы определения декстриназы солодов .с использованием в качестве субстрата для ферментативного гидролиза полисахарида пуллулуна 1J.
Наиболее близким к предлагаемому по технической сущности является способ количественного определения декстринолитической активности солода, предуйматриваюй1ий выделение декстринов из сброженного сусла, экстракцию декстриназы из солода, ферментативный гидролиз декстринов экстрактом декатриназы и определение редуцирующих углеводов, образующихся при ферментативном гидролизе, с последующим расчетом декстринолитической активности Д2}.
Недостатком данных способов является малая ТОЧНОСТЬ определения.декстриназы, происходящая из-за того, что лекстоины, используемыв в этих способах, гидролйзуйТся сопутствующими о( - и Э-амилазами солодов.
Недостаточная точность указанных способов проистекает также из-за использования таких методов определени редуцирующих углеводо.в, которые способны определять лишь большие их количества, т..е. макрометодовJА .они требуют проведения г губокого ферментативного гидролиза декстринов. При этом нарушается прямо пропорциональная зависимость между количеством фермента, взятого на анализ, временем его действия и KOjm4ecTBOM образованных им редуцирующих углеводов, что мешает последующему количественному расчету декстринолитической активности солода.
Цель изобретения - повыыение точ иости определения декстриназы.
Указанная цель достигается тем, что согласно способу количественного определения декстринолитической активности солода, предусматривающего вьвделение декстринов из сброженного сусла, экстракцию декстриназы из солода, ферментативный гидролиз декстринов экстрактом декстриназы и определение редуцирующих углеводов, образующихся при ферментативном гидролизе, с последующим расчетом дектринолитической активности, выделенные декстрины подвергают ферментативному гидролизу плесневой Ы-амилазой в количестве 20-20,5 ед. АС/г при 29,5-30,5°С в течение 175-180 мин . до получений ot-предельных декстри йов, а количество солода, взятого дл экстракции декстриназы устанавливают равным 0,001-0,02 г/мл ферментативного гидролизата для обеспечения прямо пропорциональной зависимости между количеством декстриназы, временем ее действия :н количеством образующихся редуцирующих углеводов.
Сущность способа заключается в следующем.
Первоначально получают исходные декстрины. Их выделяют осаждением этанолом из сброженного дрожжами сусла, приготовленного из оклейстеризованного картофельного крахмала, рсахаренного ячменним солодом четырех-, пятидневного ращения. Эти исходные декстрины дополнительно обрабатывают плесневой of.-амилазой, например препаратом Аг ииюризин IllOx, внося его в 10%-ный раствор исходных декстринов в количестве 20-20,5 ед. АС/г декстрина, инкубируют при 29,5-30,5°С в течение 175-180 мин, кипятят для инактивации фермента, охлаждают, осаждают этанолом и высушивают на воздухе при комнатной температуре с получением ci-предельных декстринов, которые служат субстратом при определении декстринолитической активности солода. Зс1тем из солода экстрагируют водой декстриназу.
Готовят контроль на субстрат и йнактивированный фермент без ферментативного гидролиза. Д)1Я этого 5-10 м раствора декстриназы из солода инактивируют 10 мин в кипящей водяной бане, охла;Хцают, фильтруют и отбира от 0,5 мл в пробирку. Туда же вносят 1 мл предварительно нагретого до 30°С 2%-ного раствора d -предельных декстринов в 0,15 м ацетатнонатриевом буфере с рН 4 ,.5, перемешивают и отбирают 0,5 в пробирку, в которую предварительно добавляют 5 мл медного реактива для определени редуцирующих углеводов и 4,5 мл воды перемешивают и кипятят на водяной бане 20 ми:н для определения редуцирующих углеводов одним из гликронетодов их определения.
Опыт(ферментативный гидролиз субстрата ферментом ).
0,5 мл раствора декстриназы и 1 KUI раствора d- -предельных декстринов, приготовленного таким же образом, что и: в контроле, инкубируют при ЗО-с в течение tiO мин (при анализе просяного солода ) или 60-120 мин (при анализе ячменного или овсяного солода ). Затем останавливают ферментативную реакцию, добавляя 5 мл медного реактива для определения редуцирующих углеводов и 4,5 мл воды и кипятят 20 мин на водяной бане для определения редуцирующих углеводов тем же методом, что и в контроле.
Разница в содержании редуцирующих углеводов до и после ферментативного гидролиза (в пересчете на глюкозу) соответстЕ1ует количеству прогидролиэованных декстриназой ,б-глюкозид ных связей в декстринах и количественно отражает содержание декстриназы в солоде, взятом на анализ. Это справедливо в том случае, когда гидролиз с.-предельных декстринов не превьлиает 10-11% от взятого на анали количества. При этом разница в содержании углеводов до и после фермен тативного гидролиза пропорциональна количеству декстриназы, взятой на анализ, и времени ее действия на ct-предельные декстрины; Поэтому рас чет декстринолитической активности не требует выведения специальных кор ректировочных формул, а производится по пропорции ме)еду количеством солод взятого на анализ, временем действия фермента и разницей в содержаиии редуцирующих углеводов до и после ферментативного гидролиза. Расчет производится по следующей формуле: « n-180.t- где а - разность в содержании редуцирунхдих углеводов до и после ферментативного гидролиза в 0,5 мл инкубационной смеси взятой на определение редуци рующих углеводов, мкг глюкозы/п - количество солода, взятое на ферментативный гидролиз в 0,5 cA}i инкубационной смеси, отобранных на определение углеводов, г; 180 - молярная масса глюкозы (пересчет с мкг глюкозы в мкэкзивалентны редуцирующих групп ; i - времй ферментативного гидролиза, мин; ДС - декстринолитическая активность солода, ед/ДС/г солода. За единицу дестринолитической акгивности принято количество фермента катализирующее при 3Q°C и рН 4,7 гнд ролиз ot -1,6-глюкозидных связей с освобождением за 1 мин 1 мкэкв. редуцирующих групп, соответствующих количеству прогидролизованных глюкот Iэидных связей. Пример. 10 кг исходных декст ринов раство{5яют в 70-80 л горячей воды, нагревают до кипения, охлаждают до 43°С, добавляют 10 л 1М ацетат но-натриевого буфера с .рН 4,7 и 10 л раствора препарата Л-шлилазы (85,2 г AivIИЛOpизинa и ПЮх с активностью 2350 ед.АС/г препарата) и проводят гидролиз при 40±1С при периодическо перемешивании. Затем фермент иаактив ируют нагреванием (в течение 5 г/шн) ДО кипения, раствор декстринов кипятят при перемешивании 20 мин, охлаждают до 25с и сепарируют. Затем раствор упаривают до концентрации 4% 5°Б при 80-90 0 в вакууме при 0,6-0,7 ати, охладдают и дважды переоса хдают в80%-ном этаноле,обезвоживают ацетоном и высушивают при комнатной температуре на воздухе. Выход d -предельных декстринов составил 25-26% от исходного, количества декстринов. Дня приготовления раствора декст риназы 5 г сухого просяного солода экстрагируют в 50 мл дистиллированной воды и отфидьтровывсиот.- Из фильтрата приготавливают рабочий раствор фермента: 15 мл фильтрата вносят в мерную колбу на 25 мн и объем доводят до метки дистиллированной водой (рабочий раствор). Контроль на субстрат и инаКтивированный фермен - 10 мл рабочего раствора фермента инактивируют в кипящей водяной бане в течение 10 мин, охлаждают и отфильтровывают. Для составления контрольной инку(бационной смеси в пробирку вносят 0,5 1ЛЛ инактивированного раствора фермента и 1 мл 2%-ного раствора Ы-предельных декстринов в 0,15 М ацетатно-натриевом буфере с рН 4,5. При этом получают 1,5 мл контрольной инкубационной смеси с рН 4,7. Для анализа редуцирующих углеводов отбирают 0,5 мл контрольной инкубационной смеси, которую смешивают с 5 мл медного реактива и 4,5 мл дистиллированной воды и кипятят в водяной бане в течение 20 мин с последукяцим титрованием 0,005 м тиосульфатом натрия. Опыт (ферментативный гидролиз субстрата ферментом . Для составления опытной инкубационной смеси отбирают 0,5 мл рабочего раствора фермента и 1 мл того же раствора декстринов, что и в контроле. Опытная инкубационная смесь после перемешивания растворов также имеет рН 4,7 и объем 1,5 wi. Опытную смесь подвергают инкубации при в течение 60 мин. Затем из нее отбирают 0,5 мл для определения редуцирующих углеводов так же, как и в контроле. Определение редуцирующих углеводов, отобранных н$ ансишзе в опыте и в контроле, производится одновременно. Предварительно строят стандартную кривую, отражающую соотношение меходу количеством глюкозы и количеством мл 0,005 н тиосульфата, расходуемых на реакцию с нею. Расчет декстринолитической активности. Содержание солода в 0,5 ми инкубационной смеси, отобранных на определение редуцирующих углеводов в опыте и в контроле, равно:
п ,„ р. 50 мл-25 мл.1,5 М)1
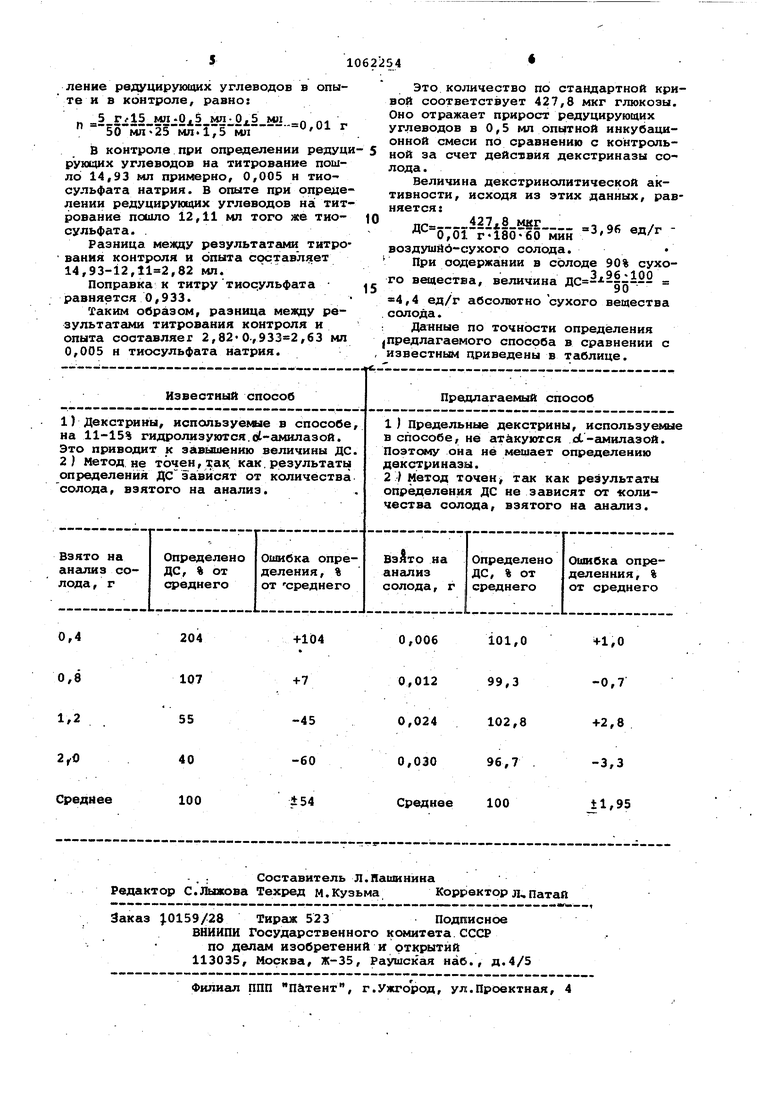
В контроле при определении редуци руихдих углеводов на титрование пошло 14,93 мл примерно, 0,005 н тиосульфата натрия. В опыте при определении редуцирующих углеводов на титрование пошло 12,11 мл того же тиосульфата. .Разница между результатами титрования контроля и опыта составляет 14,93-12,,82 мл.
Поправка к титру тиосульфата равняется 0,933.
Таким образом, разница между результатами титрования контроля и опыта составляет 2,820,,63 мл 0,005 н тиосульфата натрия.
Известный способ
1) Декстрины, используе в11е в способе, на 11-15% гидролизуются.Ы-амилазой. Это приводит к завьаиению величины ДС. 2 ) Метод, не точен, так как, результаты определения ДС зависят от количества солода, взятого на анализ.
Это количество по стандартной кривой cooTB€JTCTByeT 427,Q мкг глюкозы. Оно отражает прирост редуцирующих углеводов в 0,5 мл опытной инкубационной смеси по сравнению с контрольной за счет действия декстриназы солода.
Величина декстринолитической активности, исходя из этих данных, равняется:
o7or tio 5-iS55 3,96 ед/г воздушйд-сухого солода. При содержании в солоде 90% сухого вещестЕ1а, величина ДС ---| -,--
4,4 ед/г абсолютносухого вещества .солода.
: Данные по точности определения Iпредлагаемого спосрба в сравнении с
известным цриведены в таблице.
Пре,цлагаемый способ
1) Предельные декстрины, используемые в способе, не атакуются uL-амилазой. Поэтому она не мешает определению декстриназы.
2) Метод точен так как результаты определения ДС не зависят от «оличества солода, взятого на гшализ.

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПИВОВАРЕНИЯ | 2009 |
|
RU2524118C2 |
| СПОСОБ ЭКСТРАКЦИИ БЕТА-АМИЛАЗЫ ИЗ ЗЕРЕН ЗЛАКА И ЦЕЛЛЮЛАЗА ДЛЯ ЭКСТРАКЦИИ БЕТА-АМИЛАЗЫ ИЗ ЗЕРЕН ЗЛАКА | 2002 |
|
RU2290440C2 |
| СПОСОБ ПОЛУЧЕНИЯ СУСЛА | 2007 |
|
RU2426775C2 |
| СПОСОБ ЗАТИРАНИЯ | 2007 |
|
RU2524413C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПИВНОГО СУСЛА | 2012 |
|
RU2600885C2 |
| Способ получения кормового белка | 1978 |
|
SU718079A1 |
| Способ получения бактериального ферментного препарата | 1989 |
|
SU1708840A1 |
| СПОСОБ ВЫРАЩИВАНИЯ ДРОЖЖЕЙ | 2013 |
|
RU2522006C1 |
| Способ контроля процесса гидролиза крахмалистого сырья | 1977 |
|
SU729508A1 |
| СТАБИЛИЗАТОР ФЕРМЕНТНЫХ БЕЛКОВ | 2010 |
|
RU2441069C2 |
СПОСОБ КОЛИЧЕСРВЕННОГО ОПРБДЕЛБЯ11Я ДЕКСТРИНОЛИТИЧБСКОЙ АКТИВНОСТИ COJlOMA, предусматривсиосций выдел ение декстринов из сброженного Ъуела, экстракцию декстриназы из солода , ферментативный гидролиз декстринов экстрактом декстриназы и определение редуцирукчцих углеводов, образукхцихся при ферментативном гидролизе, с последующим расчетом декстринолитичёской активности, отличающийся тем, что, с целью повьшения точности -определения путем предотвращения действия на декстрины. (JL- и в -амилазы солода, вьщеленные декстрины подвергают ферментативному гищ}олиэу плесневой об-амилазой в количестве 20-20,5 ед КС/г, при 29,5Э0,5с в течение 175-180 мин до получения Ы-предельных декстринов, а количество солода, взятого для экстракции декстриназы, устанавливают paвны L от 0,001 до 0,020 г/мл ферментативно-З 3 го гидролизата для обеспечения прямо пропорциональной зависимости меяоду количеством декстриназы, временем ее действия и количеством образукяцихся редуцирующихся углеводов.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Мэннерс Д | |||
| и Йелшоулис Д | |||
| Предельная декстриназа из проросшего ячменя | |||
| - Крахмал, ФРГ, 1971, п 23т, 7, с | |||
| Приспособление для нагрузки тендеров дровами | 1920 |
|
SU228A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ качественной оценки солода | 1950 |
|
SU91465A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
1983-12-23—Публикация
1982-01-19—Подача