О
со Изобретение относится к медицине и может найти применение в клинической практике для своевременного выявления истинного кардиогенного шока и дифференциации его с инфарктом миокарда. Известен способ диагностики инфаркта миокарда, в основе которого /1ежит клиническая картина, включающая три признака разрыва мыщ сердца: падение артериального давления сочетающегося с периферическими признаками шока, повьшение централь ного венозного давления, сопровождающееся выраженным переполнением шейных вен, маленькое тихое сердце 13. Недостатком описанного способа диагности;си является отсутствие пря.мых признаков диагностики инфаркта миокарда, приведенные признаки харак терны вообще для шоковых состояний. Наиболее близким к изобретению по технической сущности и достигаемому результату является, способ диагности ки разрыва сердца 2. Характернь для больных, впоследствии погибших от разрьшов сердца, считается высокий лейкоцитоз, выраже ная гиперферментймия, в частности высокая активность лактатдегидрогеназы. Недостатком известного способа диагностики является то, что выраже ный лейкоцитоз отмечается как при шоке, так и при отеке легких. Иссле дование для диагностики разрывов сердца лактатдегидрогеназы также им ет возражения. Увеличение ДЦГ носит неспецифический характер, является поздним тестом, так как максимум увеличения лактатдегидрогеназы набл дается к четвертым суткам, а разрыв мьащы сердца обычно возникают в пер вые три дня заболевания. Целью изобретения является диффе ренциальная диагностика кардиогенно го шока и шока от разрьгаа сердечной . мышцы. Эта цель достигается тем, что со ласно способу диагностики инфаркта миокарда .путем определения бибхимических характеристик крови, в крови больных определяют количество общег белка, фибрина и фибриногена и уровень активности аспартатаминотрансферазы (ACT), причем уменьшение об- , щего белка на 5,4-7%, увеличение активности ACT на 16-22%, повьштение содержания фибрина на 76-80% и фибриногена на 59-62% свидетельствует о развитии кардиогенного шока, а уменьшение уровня общего белка на 10-12%, повьшгение активности ACT на 54-67%, содержания фибрина на 127 130% и фибриногена на 113-121% свидетельствует об инфаркте миокарда. Способ осуществляют следующим образом. В первые 30-40 мин после электрокардиографического подтверждения инфаркта миокарда и выявления клинических симптомов кардиогенного шока у больного берут из вены 6 мл крови. Затем для определения фибрина и фибриногена в мерную центрифужную пробирку, содержащую 0,8 ivi 3,8%-ного раствора цитрата натрия, добавляют 3 мл крови больного, центрифугируют при 2000 об/мин в течение 10 мин. Плазму отсасывают и исследуют содержание фибрина и фибриногена по методу Рутберг. Оставшиеся 3 мп крови помещают в центрифужную пробирку с каплей гепарина. Для предотвращения образования сгусткрв содержимое пробирки осторожно перемешивают, после чего центрифугируют в течение 15 мин при 3000 об/мин. Берут О,1 мл сыворотки крови и определяют активность аспартатаминотрансферазы по методу Райтмана и Френкел}. Общий белок определяют р.ефрактометрйчески. П р и м е р 1. Б-ной К,, история болезни № 13240/842, 59 Лет поступил в кардиологическое отделение больницы скорой помощи через 8 ч после возникновения болевого приступа в области сердца в крайне тяжелом состоянии. Стонал от боли Кожные покровы быпи влажнь О1, бледными, холодным на о1цупь« Отмечался вьфаженный 1(ианоз. термальное давление при поступлении 120/90 мм рт.ст. Пульс 87 уд./мин. ЭКстрасистолия. На ЭКГ указания на свежий трансмуральный пер€ дасперегорсдоч{шй инфаркт миокарда с вовлечением верхушки. При исследовании крови в этот Период получены следующие результаты. Общий Уменьшен на 5,6% ACTПовыпен на 17,8% ,
Фибрин Повышен на 78% Фибриноген Повышен на 60,9%. Полученные лабораторные данные указывают на формирование кардиогенного шока. Несмотря на введение наркотических анальгетиков, препаратов нейролептанальгезии, дачи закиси азота, купировать полностью болевой приступ не удалось. Через 35-40 мин после госпитализации развился тяже- лый кардиогенный шок: состояние стало спутанным, артериальное давление снизилось до 60/40 мм рт. ст. Пульс ста нитевидным, 170 уд/мин. При катетеризации моченого пузыря мочи не получено (анурия). Капельное введение норадреналина, поликлюкина, глюкокортикоидов привело к повышению артериального давления, а введение таламонала, оксибутирата натрия способствовало купированию болей и уменьшению клинических проявлений шока: кожные покровы стали теплее, менее влажными, появилось мочеотделение, уменьшился цианоз. Больной был выведен из состояния шока и выписан из отделения на 48-е сутки.
Пример 2. Б-ной П., история болезни № 13481/870, 60 лет доставлен специализированной бригадой скорой медицинской помощи через сут:ки после возникновения болевого
приступа с диагнозом ишемическая болезнь сердца: свежий трансмуральный задне-боковой инфоркт миокарда, кардиогенньм moKj сердечная астма. Б течение 10 лет страдал гипертонической болезнью. При госпитализации состояние тяжелое. Бледность кожных покровов, Потливость, цианоз губ, одышка, эйфоричность боли за грудиной, границы сердца расширены влево, тоны сердца глухие, систолический шум на верхушке. Артериальное давление 80/75 мм рт.ст. Пульс 90 уд/мин. Диурез составлял менее 20 мл/ч Клийи 1еская картина указьшает на развитие кАрдиогенного шока. Однако исследование крови лабораторным путем показало снижение содержания общего белка на 11,7%, повьШ1ение активности ACT на 59,5%, повьш1ения уровня фибрина на 130%, фибриногена на 118%, что свидетельствовало об прединфарктном состоянии. Однако из-за отсутствия кардиохирургического центра было начато консервативное лечение. После внутривенного введения прессорных
аминов, сердечных гликозидов, препаратов нейролептанальгезии, плазмозаменителей сЬстояние больного стабилизировалось при удовлетворительных показателях гемодинамики АД 120/80 м рт.ст. Пульс 84 уд/мин. В течение 20 ч состояние больного оставалось относительно удовлетворительным, отсутствовал болевой синдром, отмечалось стойкое повьш1ение артериального давления, был диурез.
К концу первых суток пребывания в стационаре больной внезапно вскрикнул и потерял сознание. Реанимационные мероприятия были неэффективными, на вскрытии обнаружен трансмуральный инфаркт миокарда левого желудочка, разрыв задней стенки, гемопёрикард.
Пример 3. Под наблюдением находилось 42 пациенте с истинным кардиогенным шоком и 27 больных с наружным разрывом сердца. В 40,7% всех разрывов сердечной мышцы (11 больных) наблюдался кардиогенный шок с медленным наступлением смерти при неуклонном ухудшении состояния. У 16 больных отмечена стабилизация состояния после диквидации симптомов кардиогенного шока и дальнейшим развитием внезапной смерти. В этих случаях отмечена избыточная физическая активность как фактор, способствующий разрыву сердца. Йричем Уг- всех больных с внезапно развивающейся тампонадой полостей перикарда накануне отмечались характерные для разрьша сердца изменения исследуемых показателей,
проведен сравнительный анализ изчаемых показателей у больных с кардиогенным шоком, разрывом миокарда с аналогичными показателями у больных с трансмуральным инфарктом миокарда,
в клинических условиях изучена проницаемость кровеносных сосудов методом артерио-венозной разницы и исследован гематокрит у больных с разными формами кардиогенного шока.
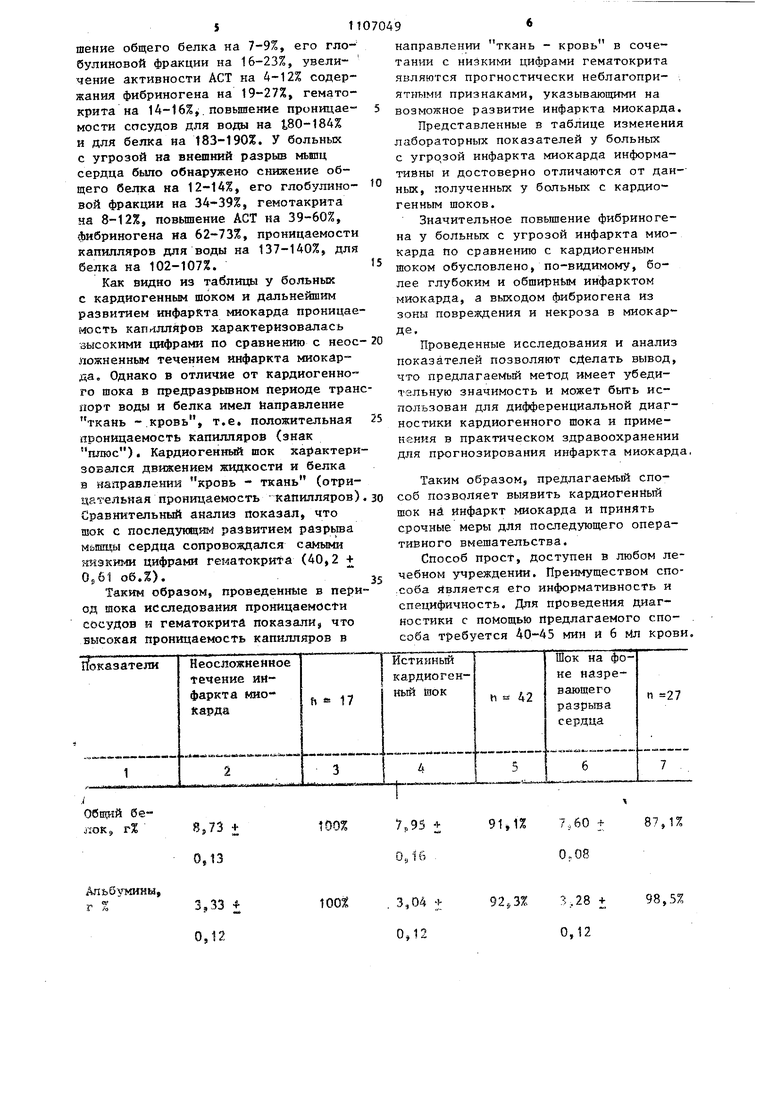
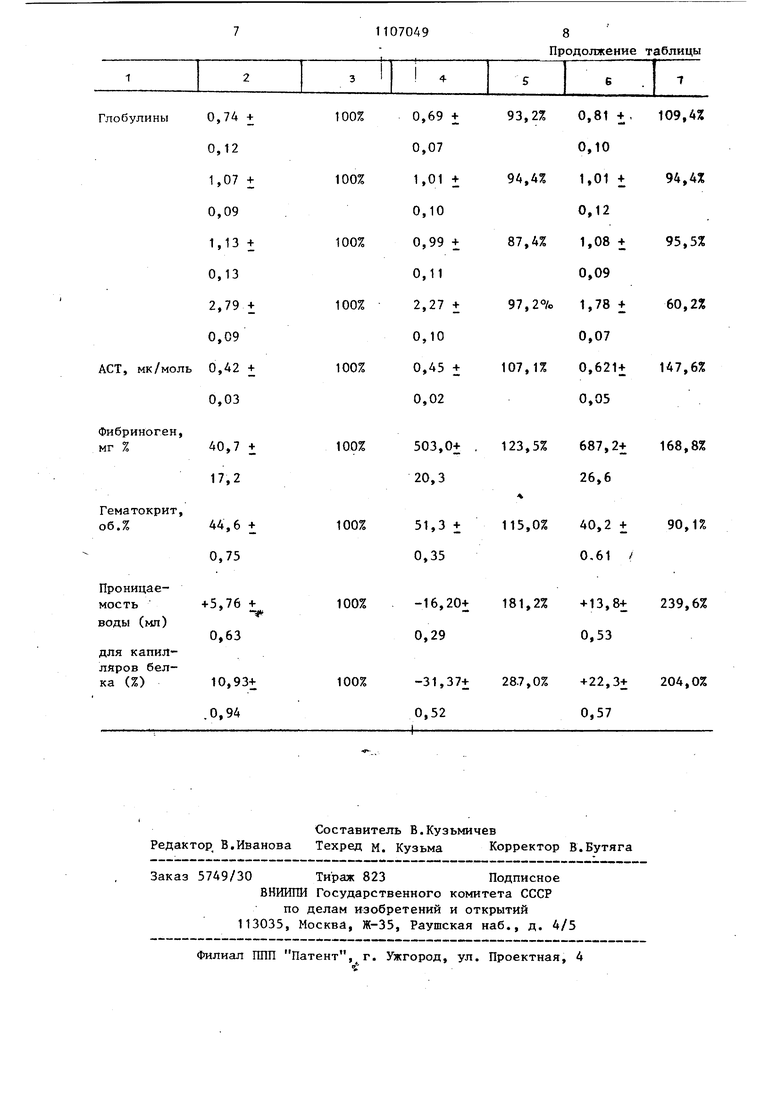
Изменения лабораторных показателей у больных с кардиогенным шоком на фоне назревающего инфаркта миокарда представлены в таблице.
Как видно из представленных данных у больных с кардиогенным шоком по сравнению с несложным течением инфаркта миокарда отмечается умень- шение общего белка на 7-9%, его глобулиновой фракции на 16-23%, увеличение активности ACT на 4-12% содержания фибриногена на 19-27%, гематскрита на 14-16%. повьппенне проницаемости сосудов для воды на 180-184% и для белка на 183-190%. У больных с угрозой на внешний разрыв мьвпц сердца было обнаружено снижение общего белка на 12-14%, его глобулиновой фракции на 34-39%, гемотакрита яа 8-12%, повьшение ACT на 39-60%, фибриногена на 62-73%, проницаемости капилляров для воды на 137-140%, для белка на 102-107%. Как видно из таблицы у больных с кардиогенным шоком и дальнейшим развитием инфарКта миокарда проницае мость капилляров характеризовалась высокими цифрами по сравнению с неос ложненньм течением инфаркта миокарда. Однако в отличие от кардиогенно™ го шока в предразрьшном периоде тран порт воды и белка имел Направление ткань - кровь, т.е. положительная проницаемость капилляров (знак плюс). Кардиогенный шок ха{)актери зовался движением жидкости и белка в направлений кровь - ткань (отрицательная проницаемость -капилляров) Сравнительный анализ показал, что азок с последзпощим развитием разрьта мьшщы сердца сопровождался самыми 5 зкими цифрами гематокритй (40,2 + об.%). Таким образом, проведенные в пери од шока исследования проницаемости сосудов и гематокрита показали, что высокая проницаемость капилляров в направлении ткань - кровь в соче тании с низкими цифрами гематокрита являются прогностически неблагопри- . признаками, указывающими на возможное развитие инфаркта миокарда. Представленные в таблице изменения лабораторных показателей у больных с угрозой инфаркта миокарда информативны и достоверно отличаются от дан-ных, полученных у больных с кардиогенным шоков. Значительное повьш1ение фибриногена у больных с угрозой инфаркта миокарда по сравнению с кардиогенным шоком обусловлено, по-видимому, более глубоким и обширн{ 1М инфарктом миокарда, а выходом фибриогена из зоны повреждения и некроза в миокарде. Проведенные исследования и анализ показателей позволяют сделать вывод, что предлагаемый метод имеет убедительную значимость и может быть использован для дифференциальной диагностики кардиогенного шока и применения в практическом здравоохранении для прогнозирования инфаркта миокарда, Таким образом, предлагаемый способ позволяет выявить кардиогенйый шок нА инфаркт миокарда и принять срочные меры для последующего оператийного вмешательства. Способ прост, доступен в любом лечебном учреждении. Преимуществом спо.соба Является его информативность и специфичность. Для проведения диагностики с помощью предлагаемого способа требуется 40-45 мин И 6 Мл крови.

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения формы кардиогенного шока у больных острым инфарктом миокарда | 1989 |
|
SU1774264A1 |
| Способ диагностики кардиогенного шока | 1980 |
|
SU1139413A1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ОСЛОЖНЕНИЙ ИНФАРКТА МИОКАРДА | 2008 |
|
RU2373542C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ЖИЗНЕУГРОЖАЮЩИХ ОСЛОЖНЕНИЙ У ПАЦИЕНТОВ В ОСТРОМ ПЕРИОДЕ ИНФАРКТА МИОКАРДА | 2021 |
|
RU2767914C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗРЫВА СЕРДЕЧНОЙ СТЕНКИ В ОСТРОМ ПЕРИОДЕ ИНФАРКТА МИОКАРДА | 2007 |
|
RU2335237C1 |
| Способ прогнозирования осложнения при инфаркте миокарда | 1984 |
|
SU1264078A1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ПОВТОРНОГО ИНФАРКТА МИОКАРДА | 2010 |
|
RU2424531C1 |
| СПОСОБ ЛЕЧЕНИЯ ЖЕЛУДОЧКОВОЙ ЭКСТРАСИСТОЛИИ ПРИ ИНФАРКТЕ МИОКАРДА | 2000 |
|
RU2197241C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ОСЛОЖНЕНИЙ БОЛЬНОГО ИНФАРКТОМ МИОКАРДА | 2000 |
|
RU2197173C2 |
| СПОСОБ РАННЕЙ ДИАГНОСТИКИ ОСЛОЖНЕННОГО СИСТЕМНОГО ВОСПАЛИТЕЛЬНОГО ОТВЕТА У ПАЦИЕНТОВ, ОПЕРИРОВАННЫХ В УСЛОВИЯХ ИСКУССТВЕННОГО КРОВООБРАЩЕНИЯ | 2011 |
|
RU2463606C1 |
СПОСОБ ДИАГНОСТИКИ ИНФАРКТА МИОКАРДА путем определения биохимических характеристик крови, отличающийся, тем, что, с целью дифференциальной диагностики кардиогенного шока и шока от разрыва сердечной мышцы, в крови ббльных определяют количество общего белка, фибрина и фибриногена и уровень активности аспартатаминотрансферазы, причем уменьшение об1цего белка на 5,4-7%, Увеличение активности аспартатаминотрансферазы на 16-22%, повы шение содержания фибрина на 76-80% и фибриногена на 59-62% Свидетельствует о развитии кардиогенного шока,а уменьшение Уровня общего белка на 10-12%, повышение активности аспартатаминотрансфераэы на 54-67%, содержания фибрина на 127-130% и фибриногена на 113-121% cвидeтeльctвует об инфаркте миокарда.
100%
8j73 + 0,13
,
100
3,33 f 0,12
7,93 +
9Ы%
87,1%
7,60 j0,08
0,16 .
98,5%
3,28 j
3,04 f
92,3% 0,12 0,12
1007,
0,74 +
ины 0,12
100% 1,07 + 0,09
100% 1,13 + 0,13
100% 2,79 i 0,09
100%
к/моль 0,42 + 0,03
оген,
100%
40,7 i 17,2
крит,
44,6 +
100% 0,75 Проницае100%+5,76 + мость -jff воды (мл) для капилляров белка (%) 100% 10,93+ .0,94
109,4%
0,81 +.
93,2%
0,10
94,4%
1,01 ±
94,4%
0,12
95,5%
87,4%
1,08 +
0,09
60,2%
1,78 +
97,2°/o
0,07
147,6%
0,621+
107,1%
0,05
687,2+ 168,8%
123,5%
, 26,6
40,2 + 90,1%
115,0%
+ 0.61 / -16,20+ 181,2% +13,8+ 239,6% 0,290,53 -31,37+ 28.7,0% +22,3+ 204,0% 0,520,57 1.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Гольдберг Э., Вит М | |||
| Лечение больных с тяжелыми заболеваниями сердца | |||
| М., 1979 (аналог) | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Гороховский Б.И | |||
| ПРИБОР ДЛЯ ЗАПИСИ И ВОСПРОИЗВЕДЕНИЯ ЗВУКОВ | 1923 |
|
SU1974A1 |
Авторы
Даты
1984-08-07—Публикация
1980-04-17—Подача