Изобретение относится к новьи биологически активным соединениям конъюгатам тиреоидных гормонов с альбумином общей формулы
Со - NH - uAbSyiWH
х-сн J ин-со-снз
где X;
НО
для выработки антител к тиреоидным гормонам у животных.
Известны аналоги описываемых сое динений:конън)га1ы формул II и III соответственно
СО -ОСНз
СН
11
I
иН со fl/ib /yww
СО-OCHj
- Cfs,
TJH-со-СН -Н-СЯу CO-llH-iM J|pwM
Конъюгаты формулы II имеют низкую степень конъюгирования (11-1 молекул тиреоидного гормона на I молекулу альбумина), что приводит к недостаточно эффективной наработке антител. Кроме того, при получении II и III на 1-й стадии может происходить частичиое деиодирование исходного соединения, что приводит к образованию в конъюгате тироксина с альбумином примеси трииодтиронина с альбумином. В связи с этим известные конъюгаты II и III не могут обеспечить выработку высокоспецифических антител.
Цель изобретения - новые конъюгат тиреоидных гормонов с альбумином с высокой степенью конъюгирования и обеспечивающие выработку антител к тиреоидным гормонам с высокой специфичностью.
Поставленная цель достигается описываемыми конъюгатами тиреоидных гормонов с альбумином общей формулы 1 для выработки антител к тиреоидным гормонам у животных.
Конъюгаты получают по следунмцей
схеме
I
соон
х-сн CHj-CO- ОI«l2
соон I
miK -х-сн
IV
рЩ-СО-СНз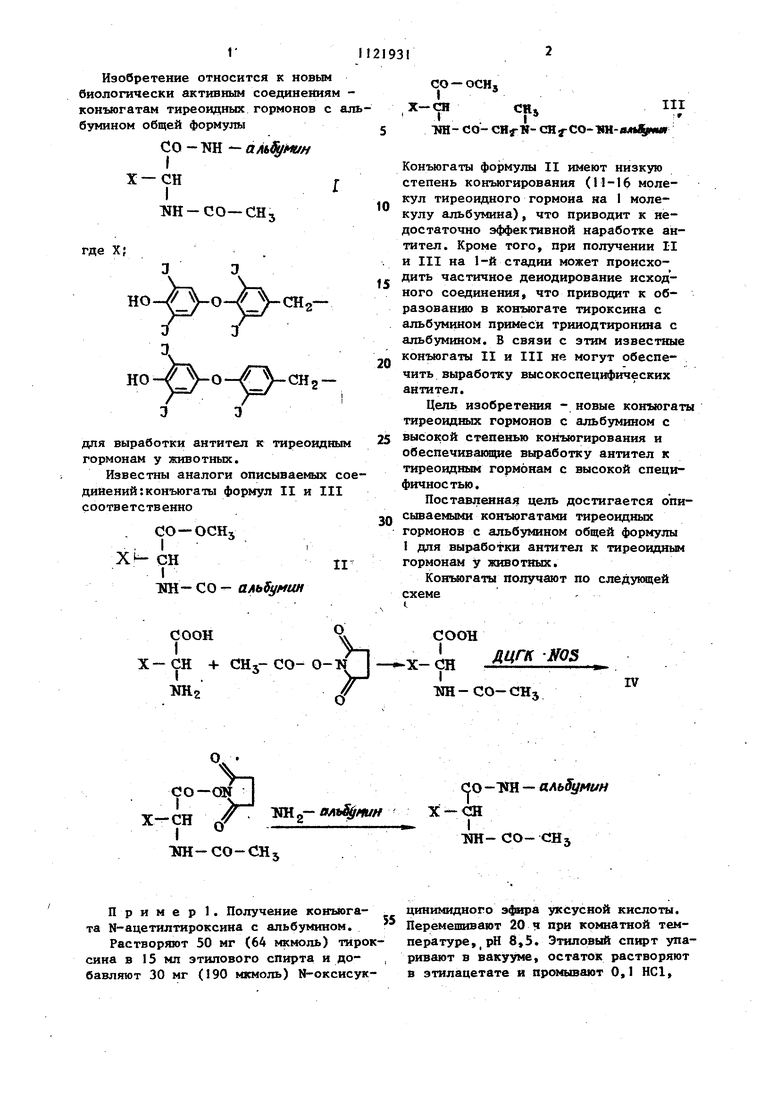


| название | год | авторы | номер документа |
|---|---|---|---|
| N-ОКСИСУКЦИНИМИДНЫЕ ЭФИРЫ N-АЦЕТИЛТИРОНИНОВ В КАЧЕСТВЕ ПОЛУПРОДУКТОВ ДЛЯ СИНТЕЗА КОНЪЮГАТОВ ТИРЕОИДНЫХ ГОРМОНОВ С АЛЬБУМИНОМ | 1983 |
|
SU1100846A1 |
| ШТАММ ГИБРИДНЫХ КУЛЬТИВИРУЕМЫХ КЛЕТОК МЫШИ MUS MUSCULUS L., ИСПОЛЬЗУЕМЫЙ ДЛЯ ПОЛУЧЕНИЯ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ К ТИРОКСИНУ | 1993 |
|
RU2049816C1 |
| СПОСОБ ОЧИСТКИ КРОВИ ОТ АНТИТЕЛ К ТИРЕОИДНЫМ ГОРМОНАМ С ПОМОЩЬЮ ИММОБИЛИЗИРОВАННОГО ГРАНУЛИРОВАННОГО МАГНИТОУПРАВЛЯЕМОГО ПРЕПАРАТА | 2007 |
|
RU2366958C2 |
| СПОСОБ ОЧИСТКИ АНТИТЕЛ К ТИРЕОИДНЫМ ГОРМОНАМ | 1987 |
|
SU1484094A1 |
| СПОСОБ ПОЛУЧЕНИЯ КОНЪЮГАТА АЙМАЛИНА С БЫЧЬИМ СЫВОРОТОЧНЫМ АЛЬБУМИНОМ | 1993 |
|
RU2088230C1 |
| СРЕДСТВО, СТИМУЛИРУЮЩЕЕ ПРОДУКЦИЮ ТИРЕОТРОПНОГО И ТИРЕОИДНЫХ ГОРМОНОВ | 2006 |
|
RU2325397C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОНЪЮГАТА КАТЕХОЛАМИНОВ | 1991 |
|
RU2027443C1 |
| НОВЫЙ АГОНИСТ β-РЕЦЕПТОРА ТИРЕОИДНЫХ ГОРМОНОВ | 2021 |
|
RU2839610C1 |
| Способ получения моноспецифических антител к лактоферрицину человека | 2022 |
|
RU2795322C1 |
| КОНЬЮГАТЫ ДЛЯ ПРЕДУПРЕЖДЕНИЯ ИЛИ ЛЕЧЕНИЯ НИКОТИНОВОЙ ЗАВИСИМОСТИ | 2011 |
|
RU2574032C2 |
КонЫогаты тиреоидных гормонов с альбумином формулы GO -IW - oMSyMUM lIH-CO-CHj где X: СН,- (Л для вьфаботки антител к тиреоидным СО гормонам у животных. 00
Приме р 1. Получение конъюга- ,цинимидного эфира уксусной кислоты,
та N-ацетилтироксина с альбумином. Перемешивают 20 ч при комнатной темРастворяют 50 мг (64 мкмоль) тирок-пературе,,рН 8,5. Этиловый сп1фт упасина в 15 нл этипового спирта и до- ,ривают в вакууме, остаток растворяют
бавляют 30 мг (190 мкмоль) N-оксисук-в этилацетате и промывают 0,1 НС1,
со -ТШ -аль5уиин СН
I тт-со- снз
водой, высушивают , упаривают в вакууме. Получают 50 мг (95%) аморфного N-ацетилтироксина.
Растворяют 50 мг (61 мкмоль) N-ацетилтироксина в А мл этилацетата, добавляют 10 мг (87 мкмоль) N-оксисукцинимида. Раствор охлаждают до ОС и по каплям добавляют 14 мг (67 мкмоль) дициклогексилкарбодиимида в 2 мл Q этилацетата. Перемешивают 1 ч при и 20 ч при комнатной температуре. Выпавшую дициклогексилмочевину отфильтровывают, этилацетатный раствор промывают последовательно в 1 н NaHCOj, 5 водой, высушивают ,, упаривают в вакууме. Получают 50 мг (90%) М-оксисукцинимидного эфира N-ацетилтироксина. Т.пл. 188-189°С (этилацетат/гек -. сан).20
Ж-спектр, см : 1680, 17А8, 1795, 1825, 3400.
М.вес.916,0 Cj, H,607N2l4 Найдено,%: С 27,53; Н 1,68; N 3,01 Вычислено,%: С 27,51; Н 1,75; 25 N 3,06.
Растворяют 50 мг (64,2 мкмоль) Nоксисукцинимидного эфира Н-ацетилтироксина в 5 мл дноксана и прибавля- JQ т 50 мг (0,72 мкмоль) бычьего сывороточного альбумина (EGA) в 5 мл воы (рН 8,35; 0,1 М р-р NaHCO,). Перемешивают в течение 20 ч при комнатной температуре. Реакционную смесь подвергают диализу против дистиллированной воды в течение 36 ч, лйофилизуют. Определение степени конъюгирования тиреоидного гаптена с EGA проводят спектрофотометрическим . методом. Для этого измеряют поглощение конъюгата в области 300 нм, обусловленное в основном поглощением гаптена и вычитают вклад поглощения белка в эту спектральную область. На ос- 5 новании предварительно найденного коэффициента экстинкции тиреондного гаптена рассчитывают концентрацию гаптена в растворе и относят ее к известной концентрации белка. Для про- en верки достоверности расчета,степени конъюгирования с БСА были использованы радиоактивномеченные гаптены с известной удельной радиоактивностью. Разница в определении по двум мето- . дам не превышала 5-8%. По данным спектрометрических измерешШ на t молекулу БСА приходится 48 молекул № ацетилтироксина.
Пример. Получение конъюгата N-ацетилтрийодтиронина с альбумином .
Растворяют 250 мг (0,406 мкмоль) трийодтиронина в 6Q мл этилового спирта и добавляют 78,5 мг (0,5 мкмоль) N-оксисукцинимидного эфира уксусной кислоты. Проведение реакции и выделение продукта, как в примере 1. Получают 250 мг (94%) аморфного N-ацетилтрийодтиронина.
Растворяют 250 мг (0,360 мкмоль) N-ац етилтрийодтиронина в 10 мл этилацет та, добавляют 57,5 мг (0,5мкмоль N-оксисукцинимида. Раствор охлаждают до.О°С и по каплям добавляют 84,2 мг (0,4 мкмоль) дициклогексилкарбодиимида в 4 мл этилацетата. Проведение реакции и выделение продукта, как в примере 1. Получают 250 мг (87,7%) N-оксисукцинимидного эфира N-ацетилтрийодтиронина. Т.пл. 152-154 С абс. этиловый спирт.
ИК-спектр, : 1670, 1748, 1795, 1825, 3400.
М.вес. 790,0; C,i,H,,, .
Найдено,%: С 31,87; Н 2,07; N 3,51.
Вычислено,%: С 31,90; Н 2,15; N 3,54.
Растворяют 50 мг (76,2 мкмоль) Nоксисукцинимидного N-ацетнптрийодтиронина в 5 мл диоксана и прибавляют 50 мл (0,72 мкмоль) БСА в 5 мл 0,1 М раствора NaHCO, рН 8,35. Условия проведения реакции и выделения целевого продукта описаны в примере 1 .
По данным спектрофотометрии на 1 молекулу БСА приходится 46 молекул N-ацетилтрийодтиронина.
Проведены биологические испытания описываемых конъюгатов общей формулы . Для сравне1шя взяты известные конъюгаты общей формулы - лучшие из применяемых для радиоиммунологического анализа тиреоидных гормонов.
Б ходе испытаний определялись иммунргенные свойства конъюгатов тиреоидных гормонов с альбумином, т.е. способность oпиcывae вdx соединений вызывать при введении в организм живого образование за определенный промежуток времени антител к тиреоидным гормонам и изучались характеристики полученных антител.
Иммунизация кроликов конъюгатом N-ацетилтироксина с альбумином. Конъюгат (1 мг), содержащий 48 мо лекул тироксина на молекулу альбумина, растворяли в 0,5 мл физиологичес кого раствора и прибавляли 0,5 мл полного адъюванта Фрейнда. Смесь тщательно гомогенизировали и с помощью медицинского шприца вводили кролику. Процесс иммунизации состоял из нескольких циклов. Первь цикл включал трехкратное введение конъюга та подкожно во множество точек спины животного. Второй и последующие циклы состояли из однократного введения ан тигенного материала в той же дозе, что и в первом цикле. Взятие крови дпя тестирования антител проводили на 8-10 день после введения конъюгата. После дефибринирования и отделения форменных элементов крови получали сьгаоротку, содержащую антитела к тироксину (антисыворотку). Имм п11изация кроликов конъюгатом №-ацетилтрийодтиронина с альбумином. Антйсыворотку к трийодтиронину получали как описано выше, но вместо конъюгата «псроксина с альбумином использовали конъюгат трийодтиронина с альб яданом, имеюсций 46 молекул трийодтиронина на молекулу альбумина. Определение характеристик полученных антител. С помощью стандартных методик определялись следунщие характеристики антител: титр - (величина, характери9унщая концентрацию антител в сыворотке -и определяемая наибольшим разве дением антисыворотки, при котором свя зывается 50% меченого антигена)j специфичность - (относительная реакциейная способность тироксиновых антител К трийодтиронину и трийодтирониновых антител к тироксину). Нашпи, что уже через 1 месяц после, начала иммунизации достигается активность антител, достаточная для целей радиоиммунного определения тироксина и трийодтиронина. После второго цикла иммунизации достигались титры 1 : : 15.000 и 1:12.000 дпя тироксиновых и трийодтирониновых антител соответственно., При использовании известных конъюгатов формулы II максимальный титр тироксиновых антител составлял 1:4.000, а трийодтирониновых - 1: :2.000. Относительная реакционная способность тироксиновых антител к трийодтиронину составила 0,8%, а относи- : тельная реакционная способность трийодтирониновых антител к тироксину 0,02%. Для конъюгата II эти величины равны 2-3% и 0,2-0,4% соответственно. , . Проведенные испытания позволяют сделать вывод, что иммунизацию животных описывае№1ми соединениями I уменьшает время образования антител (усиливает динамику их продуцирования) и у величивает значение их максимальной концентрации (ТИТР) по сравнению с аналогичными соединениями (П). Получаемые антитела обладают высокой степенью конъюгирования (46-48 вместо для II) и специфичностью и могут использоваться для радиоиммуиологического определения тироксина или трийодтирокина. Описываемые конъюгаты могут быть использованы для наработки высокоспецифических антител, являющихся компонентом радиодиагностаческих наборов для определения тироксина и трийодтиронина.
| Резников А.Г | |||
| Методы определения гормонов | |||
| Киев | |||
| Наукова думка, 1980, 182 | |||
| , Uljnan E.F., Yoshida R.А., Blakemore J.I., .Moggio E., Leute B | |||
| Mechanism of inhibition of malate dehydirogenase by thyyokine derivatives and reactivation by antibodies Biochem Biophys Acta, 1979, 567, 66-74 | |||
| Carrett E.R | |||
| Suzuki Т., Weber D.J, The acidic solvolytic transf ormatipns | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Chem | |||
| Soc | |||
| Прибор для заливки свинцом стыковых рельсовых зазоров | 1925 |
|
SU1964A1 |
Авторы
Даты
1988-04-15—Публикация
1983-01-10—Подача