4;
00
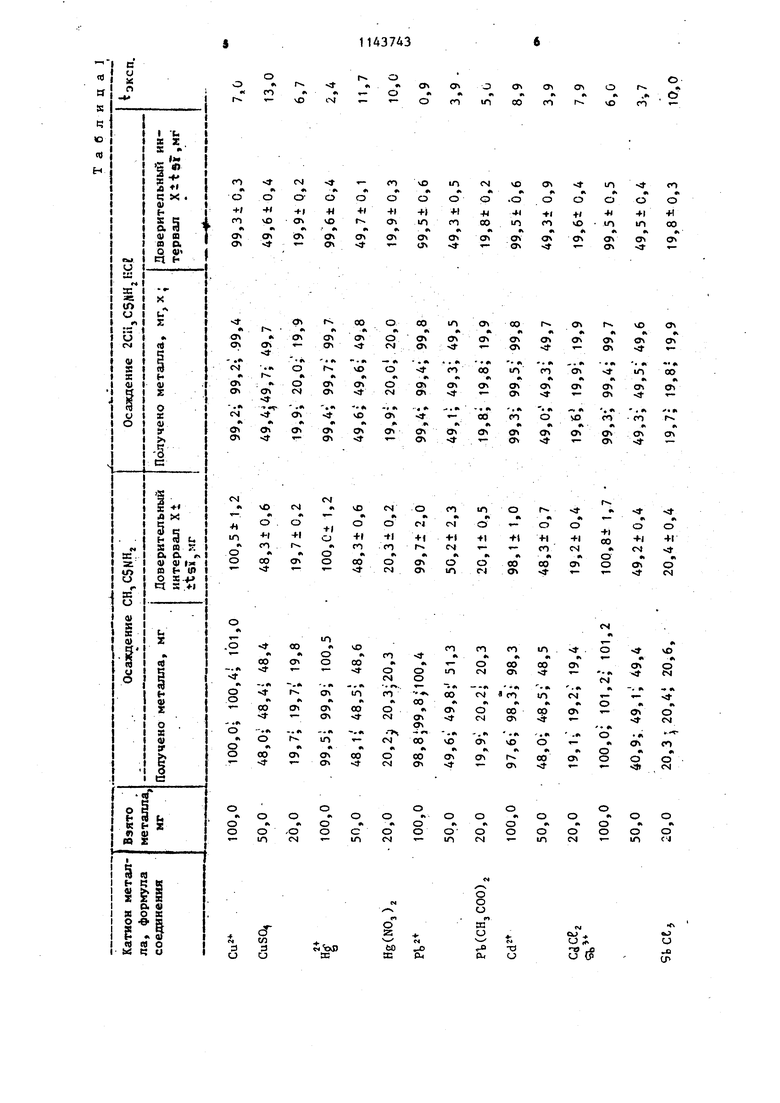
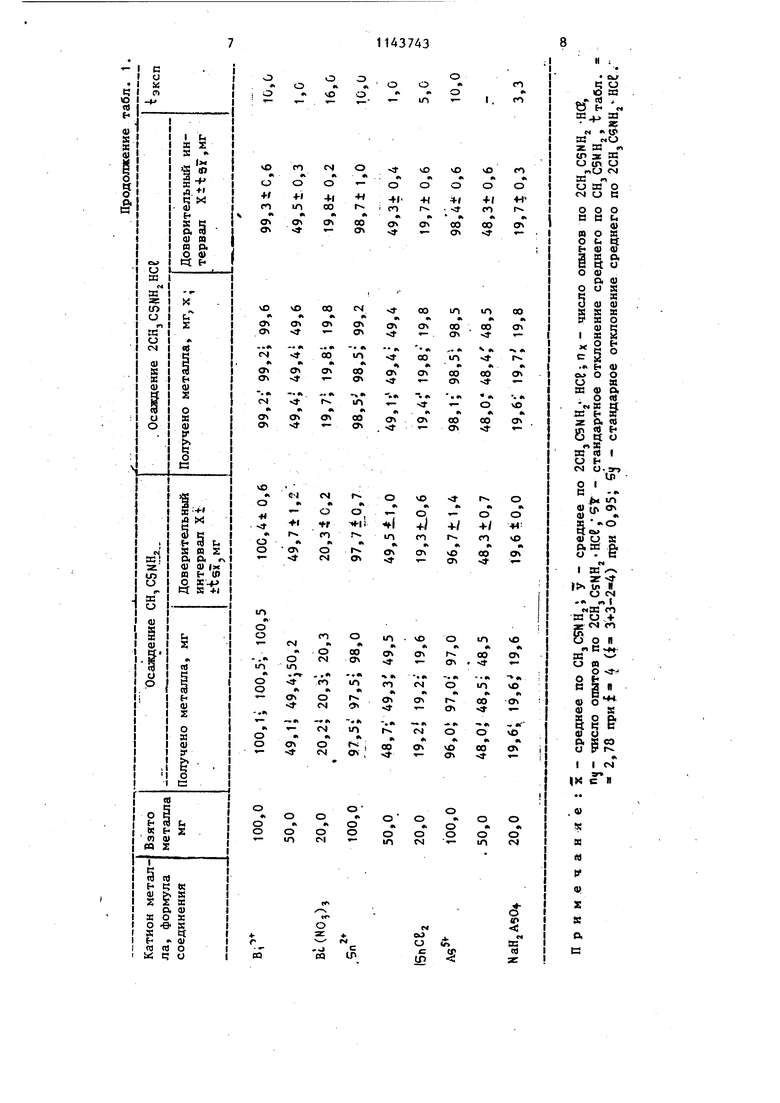
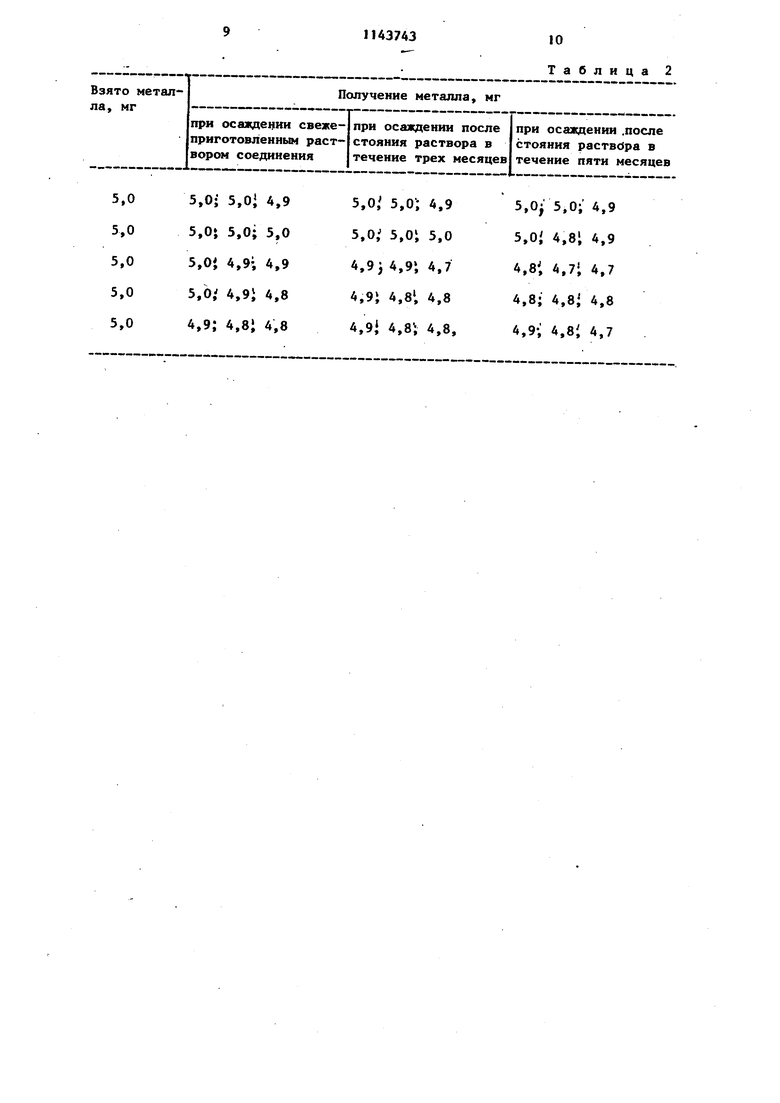
00 Изобретение относится к новым хи мическим соединениям, а именно к гидрохлориду дитиоацетамида формулы 2CH3C5MHj.HCE. Гидрохлорид дич иоацетамида может быть использован в качестве осадите ля тяжелых металлов (Си, С, Htf, 5Ь, Bi.,5n, АЧ, РЪ) при определении важнейших тяжелых металлов в фармацевтических препаратах, в массовом качественном и количествеином анали зе. Известно соединение, используемо в качестве осадителя тяжелых металлов (Си, Cd, Hg, 6Ь, BI , Sn , As, Pb) - тиоацетамид l . Осаждение тиоацетамидом катионов 11,.налитическдй группы (jCUt, Cj : 51П9г 5п ;АГ ,, ВГ ) происходит из 2-4 н. растворов по нес сульфиды металлов выпадайт при кипячении растворов. Метод с применением тиоацетамида 25 имеет ряд недостатков: завьппение результатов анализа из-за адсорбции посторонних ионов (С6 , ) вследствие сильнокислой среды при осаждении и образовании устойчивых ком- 30 иьгх плексных соединений осаждаемого металла с тиоацетамидом, реакции осаж дения идут только при кипячении раствораi недостаточная быстрота анализа. Целью изобретения является кание соединений с более высокой осаждаюи1ей способностью. Полезные свойства определяются хи мической структурой гидрохлорида ди тиоацетамида, которая выражается формулой (1). Соединёние формулы (t) получают путем взаимодействия тиоацетамида газообразным хлороводородом в среде дизтилового зфира. Структура подтверждена данными элементного анализа и ИК-спектроскопического исследования. Пример 1.К5,Ог тиоацета мида приливают 25-30 мл диэтилового эфира. В полученную смесь пропускаю сухой газообразный хлороводород в течение 20-25 мин до образования творожистого осадка бледно-желтого цвета, который фильтруют, промывают эфиром. Получают 6,11 г соединения (98,40%). Полученный продукт анализируют на содержание С, Н,5, М , СЕ по методикам рГ, количественное содержание Н определяют алкапиметрическим титрованием 0,05 н.раствором щелочи. Кислород определяют по разности. При этом получают следующий состав вещества, %: С 25,81; 5 34,22; N 15,12; ее 18,80; Н 5,63. Полученный состав соответствует формуле соединения гидрохлорида дитиоацетамида 2CH3CSNIIjнеб , для которого вычислено, %: С 25,79, 5 34,31, N15,01; се 19,03- Н 5,89. Температура плавления гидрохлорида дитиоацетамида . Новое соединение испытывают в качестве осадителя следующих катионов: СиП 5Ъ ,5ЬГ, Bi с-З с.4+ т,, г „,2 Аб РЬ 5п, Зп f т , L и , проведено качественное и количественное осаждение названных катионов в виде сульфидов. Исследовано влияние рН, времени осаждения, избытка реактивов, температуры на осаждение металлов. В качестве стандартного осадителя используют тиоацетамид . s Осаждение проводят из 0,05-0,5 н.водрастворов соответствующих солей. не имеющих осадка, а именно из водных растворов Cu50,)2, Pb(CHjCOO)j SdCl,,5T се,, В,ЧКО,,)з, 5г,Се2,, StCBy, (N03)2,Na,jHA50j, , катионы металлов осаждаются из любых солей тяжелых металлов. Природа аниона не влияет на процесс осаждения. Осаждение катионов при сравнительном испытании проводят 1-2%-ным раствором гидрохлорида дитиоац тамида при 20 С. Условия осаждения оставляют такими же, как и при тиоацетамидном осаждении. Осадитель прибавляют в полуторном количестве, избыток реактива не влия результаты осаждения. Фильтрование осадков проводят на фильтр ах Шотта № 2 и 3. Осадки сульФВДов высушивают в сушильном ШкаФУ «P« 105°С. Анализ можно заканчи ать весовым, объемным (комштексонометрическим), спектральным и другими методами. Результаты испытаний приведены в сравнительной табл. 1. Как видно из табл. 1, использование осадителя гидрохлорида дитиоацетамида обеспечивает по сравнению с известным осадителем тиоацетамидо следующие преимущества: реакции осаждения протекают в 3 раза быстрее, чем с тиоацетамидом обеспечение более высокой воспроизводимости анализа (табл. 4)j использование при осаждении одно реактива, так как раствор осадителя содержит хлороводородную кислоту, необходимую для прохождения процессов образования .сульфидов; отсутствие явлений образования комплексов металлов с избытком тиоацетамида, например при определении ртути, сурьмы, свинца, висмута с помощью тиоацетамида возможно образование нерастворимых комплексных соединений общей формулы MeCC,CHjCHH получение крупнокристаллических, легкофильтрующихся осадков, не требующих дополнительных операций промывания . Новое соединение может найти практическое применение в массовом качественном и количественном анали зах. Проведена статистическая обработ ка результатов осаждения металлов тиоацетамидок и гидрохлоридом дитио ацетамида. Из табл. 1 видно, что согласно величине iSy воспроизводимости мето осаждения катионов металлов гидрохл ридом дитиоацетамида лучше, чем при осаждении тиоацетамидом. Величина 4; зксп. почти во всех случаях боль шей табл. (при Р 0,95-2,78). Водные растворы гидрохлорида дитиоацетамида устойчивы и сохраняют реакционную способность в течение 4-5 мес, что показано в табл. 2. Новый осадитель может быть использован и в качественном анализе катионов. Ход анализа смеси катионов И аналитической группы приведен в табл. 3. При использовании в качестве группового реактива гидрохлорида ди тиоацетамида значительно ускоряется 7434 анализ (в 3 разабыстрее), используется один реактив, не требуется кипячения смеси. Качественный анализ катионов проводят при в соляно-кислой среде, создаваемой гидролизом соединения . табл. 4 даны результаты осаждения некоторых элементов 2%-ным раст-, вором 2CHjC5NH,jHCe при . Полное осаждение катионов И аналитической группы при использовании соединения формулы (|) происходит и при использовании 1-2%-ных водных растворов 2CHj CSHHj HCt. При необходимости возможно использование более концентрированных растворов и повышение температуры смеси до 50 С, что значительно ускоряет образование осадков сульфидов (осадки выпадают сразу). Как видно, из приведенных данных, реакции осаждения с применением гидрохлорида дитиоацетамида 2CHj C5NHj НС протекают в 3 раза быстрее, чем с тиоацетамидом, при осаждении ис- . пользуется один реактив, раствор осадителя содержит хлороводородную кислоту, необходимую для прохождения процессов образования сульфидов. При использовании осадителя формулы (I) отсутствуют явления образования комплексов металлов с тиоацетамидом, что приводит к завышению результатов при осаждении тиоацетамидом (например, при определении ртути, сурьмы, .свинца, висмута с помощью тиоацетамида возможно образование нерастворимых комплексных соединений общей формулы MeCKjCHjCSKHj). При .использовании осадителя формулы (|) образуются крупнокристаллические, легко фильтруюощеся осадки, не требую1ф{едополнительных операций промывания, обеспечивается высокая точность анализа. Соединение формулы (f) может найти практическое применение в массовом качественном и количественном анализах.
S S a tf
4
z
s a
fS
Таблица 2



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения сурьмы и мышьяка в ферровольфраме и ферромолибдене | 2018 |
|
RU2684730C1 |
| СПОСОБ ПОЛУЧЕНИЯ КООРДИНАЦИОННЫХ СОЕДИНЕНИЙ ОЛИГОГАЛАКТУРОНОВОЙ КИСЛОТЫ С БИОГЕННЫМИ МЕТАЛЛАМИ (II), КАК СИСТЕМ ДОСТАВКИ БИОГЕННЫХ МЕТАЛЛОВ (II) И СИСТЕМ ВЫВЕДЕНИЯ ТЯЖЕЛЫХ МЕТАЛЛОВ (II) | 2015 |
|
RU2599494C1 |
| ТРАВИЛЬНЫЙ РАСТВОР ДЛЯ СЛОЕВ СУЛЬФИДА ИНДИЯ | 1993 |
|
RU2046451C1 |
| Способ получения двойных сульфидов редкоземельных металлов | 1987 |
|
SU1456365A1 |
| СПОСОБ ОЧИСТКИ ВОДНЫХ РАСТВОРОВ ОТ ЖЕЛЕЗА (III) | 2014 |
|
RU2565214C1 |
| СПОСОБ ПОЛУЧЕНИЯ 6-АМИНОКАПРОНОВОЙ КИСЛОТЫ | 2021 |
|
RU2786162C2 |
| ПОЛУЧЕНИЕ ФОСФАТНЫХ СОЕДИНЕНИЙ ИЗ МАТЕРИАЛОВ, СОДЕРЖАЩИХ ФОСФОР И ПО МЕНЬШЕЙ МЕРЕ ОДИН МЕТАЛЛ, ВЫБРАННЫЙ ИЗ ЖЕЛЕЗА И АЛЮМИНИЯ | 2014 |
|
RU2766116C2 |
| ПОЛУЧЕНИЕ ФОСФАТНЫХ СОЕДИНЕНИЙ ИЗ МАТЕРИАЛОВ, СОДЕРЖАЩИХ ФОСФОР И ПО МЕНЬШЕЙ МЕРЕ ОДИН МЕТАЛЛ, ВЫБРАННЫЙ ИЗ ЖЕЛЕЗА И АЛЮМИНИЯ | 2014 |
|
RU2663034C2 |
| Инверсионно-вольтамперометрический способ определения тиоацетамида в водных растворах | 1985 |
|
SU1270668A1 |
| СПОСОБ ОЧИСТКИ СТОЧНЫХ ВОД ОТ ИОНОВ РТУТИ И ЦИНКА | 2011 |
|
RU2487086C2 |
Гидрохлорид дитиоацетамида формулы 2CHjC5NHjHCE в качестве осадителя тяжелых металлов .
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Яковлев П.Я и Разумова Г.П | |||
| Тиоацетамид - заменитель сероводорода | |||
| М., Металлургиздат, 1963 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Климова В.А | |||
| Основные микрометоды анализа органических соединений, М., Химия, 1975. | |||
Авторы
Даты
1985-03-07—Публикация
1983-07-21—Подача