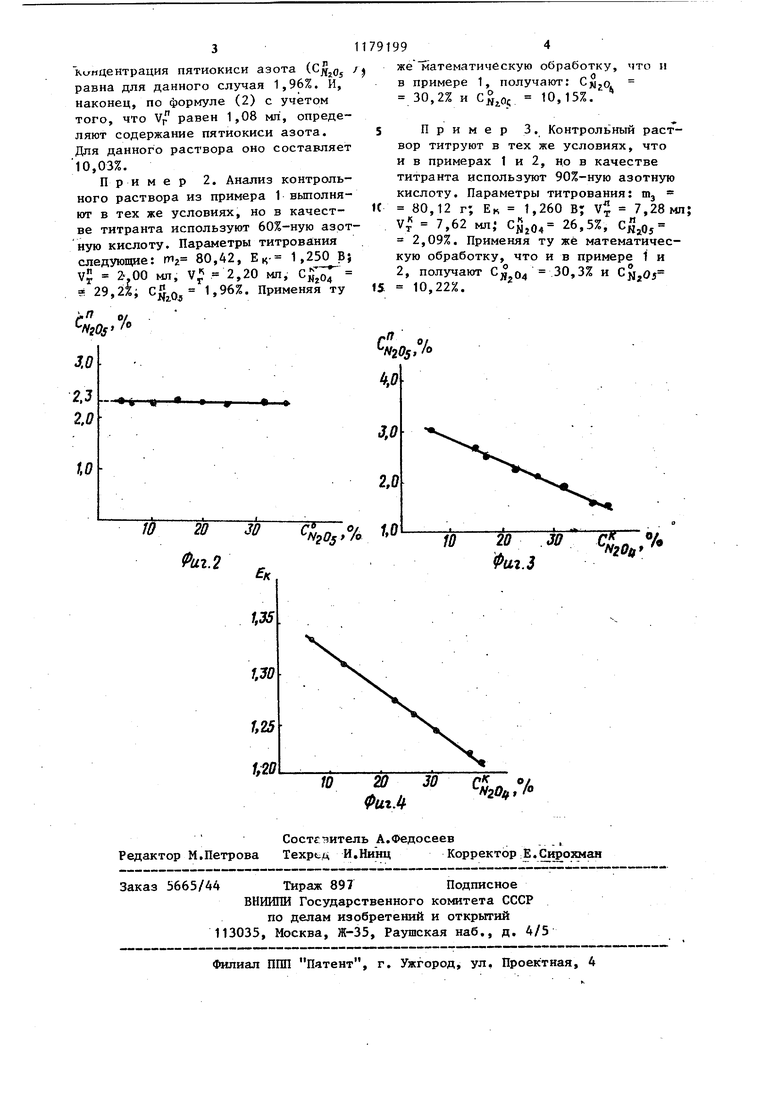
1 Изобретение относится к аналитической химии и может быть использовано в различных отраслях химическо промышленности. Цель изобретения - упрощение спо соба и повьяиение точности анализа. На фиг. 1 представлены кривая 1 потенциометрического титрования и дифференциальная кривая 2 титрования (ЛЕ/ДУ), тде ДЕ - изменение потенциала, а ЛУ - изменение объема титранта; на фиг. 2 - положение точ ки перегиба (пика) в зависимости от концентрации пятиокиси азота в исходном титруемом растворе концен ращ1я четырекокиси азота в растворах данной серии вблизи точки перегиба 22 вес. % (с учетом разбавления по четырехокиси азота), где HiOs концентрация пятиокиси азота, соответствующая точке перегиба, а , начальная концентрация пятиокиси азота в титруемом растворе); на фиг. 3 - положение точки перегиба (пика) в зависимости от концентрации четырехокиси азота в исходном, исследуемом растворе вблизи точки окончания скачка (с учетом разбавления раствора по четырекокиси азота)i содержание пятиокиси азота в растворах данной серчи 5 вес.%, на фиг. 4 - зависимость окислительно-восстановительного пот.енциала в конце скачка (Ен) от содержания четырехокиси азота в раств ре вблизи точки ЕЯ. Пример. Проводится титрование исследуемого раствора и строится кривая E-Vt (для более точного нахождения точки перегиба можно дос роить .дифференциальную кривую ЛЕ/ДУ - V). Из графика на фиг. 4 определяетс содержание четырехокиси азота в рас воре, вблизи точки, соответствующей Eii(Cwi04) и по приведенной формуле определяется концентрация в ис ходном растворе
- (ту + УТ Яг )
(1)
Шо
содержание в исходном растворе, вес.%;
Cjv.oJ)- содержание N;0 в
растворе вблизи точки, соответствунлцей Ец, вес. %;
ную кривые титрования и находят величины EKS ЕП v. и yj. Значение ЕК равно 1,250 В. Находят (фиг. 4), что содержание четырехокиси азота, определенное в растворе в конце скачка (C|5jq4 равно 29,2% и по формуле (1) с учетом того, что объем равен
1,18 мл,- рассчитывают содержание четырехокиси азота в исходном растворе. .4 составляет 29,6%.Поправочная 92 Шо масса исходного раст вора. Г , VT - объем добавленного титранта, мл, РТ плотность титранта, г/см . Далее по графику (фиг. 3), связываюв(ему положение точки перегиба (%) с содержанием четырехокиси азота в растворе, находим поправочную концентрацию пятиокиси азота (. ), а затем по формуле определяют содержание NjO в исходном растворе. УГ- РТ Сн;,о -108 NzOj где содержание NjOj в исходном растворе, вес.%; y,j, - объем титранта в точке перегиба, мп; РТ - плотность титранта, содержание воды в титруемом растворе, %/100j 108 и 18 - молекулярные веса NjOj и H,jO. Содержание азотной кислоты в исходном растворе (Сцдоз .находится по разности CH.NO} 100 - Cjj.05 - Сд,о, (3) Таким образом, предлагаемый способ позволяет определять содержание всех компонентов, используя одно титрование. Пример 1. Контрольный раствор пятиокиси и четырехокиси азота В азотной кислоте готовят путем растворения навесок пятиокиси и четырехокиси азота в 100%-ной азотной кислоте. Состав контрольного раствора 10,20% и 30,16% .Пробу контрольного раствор.а, имеющую вес nij 80,24 г, титруют дистиллированной водой и условиях, описанных выше. По результатам титрования строят интегральную и дифференциаль ki/fiaeHTpauHH пятиокиси азота .jOj равна для данного случая 1,96%. И, наконец, по формуле (2) с учетом того, что v равен 1,08 мл, определяют содержание пятиокиси азота. Для данного раствора оно составляет 10,03%. Пример 2. Анализ контрольного раствора из примера 1 вьшолняют в тех же условиях, но в качестве титранта используют 60%-ную азот ную кислоту. Параметры титрования следующие: т2 80,42, ЕК- 1,250 В; V5 2-00 мл, v;j 2,20 мл, С 5 29,2%; ,, 1,96%. Применяя ту
.П
,%
NyOs 99 же математическую обработку, что и в примере 1, получают: C.Q 30,2% и ,. 10,15%. Пример 3. Контрольный раствор титруют в тех же условиях, что и в примерах 1 и 2, но в качестве титранта используют 90%-кую азотную кислоту. Параметры титрования: т 80,12 г; ЕК 1,260 в; VT 7,28мл V 7,62 мл 26,5%, 2,09%. Применяя ту же математическую обработку, что и в примере 1 и 2, получают Сд «4 0,3% и С,05 10,22%.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ анализа системы азотная кислота-вода (пятиокись азота)-четырехокись азота | 1984 |
|
SU1224682A1 |
| Способ выделения азотного ангидрида из его раствора в азотной кислоте | 1985 |
|
SU1279956A1 |
| Способ получения пятиокиси азота | 1982 |
|
SU1089047A1 |
| Способ определения азотной кислоты и нитратов | 1976 |
|
SU658083A1 |
| Способ определения состава реагентного аммиачно-карбонатного раствора | 1991 |
|
SU1784910A1 |
| Способ определения @ , @ -дихлор- @ -формилакриловой кислоты в водной среде | 1983 |
|
SU1132229A1 |
| СПОСОБ ИДЕНТИФИКАЦИИ ПОДЛИННОСТИ ВИНА | 2008 |
|
RU2384841C1 |
| Способ определения ароматических сульфокислот | 1980 |
|
SU924566A1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ АСКОРБИНОВОЙ КИСЛОТЫ В ЛЕКАРСТВЕННЫХ СРЕДСТВАХ | 2018 |
|
RU2696865C1 |
| Способ определения сложных эфиров нитрофенолов | 1987 |
|
SU1483359A1 |

СПОСОБ АНАЛИЗА СМЕСИ АЗОТНАЯ КИСЛОТА - ПЯТИОКИСЬ АЗОТА - ЧЕТЫРЕХОКИСЬ АЗОТА, отличающийся тем, что, с целью упрощения способа и повышения точности анализа, проводят потенциометричес- кое титрование анализируемой смеси водой или водным раствором азотной кислоты с концентрацией не более 90 мас.% и по характеристическим точкам кривой титрования рассчитывают содержание компонентов смеси. В СО со СО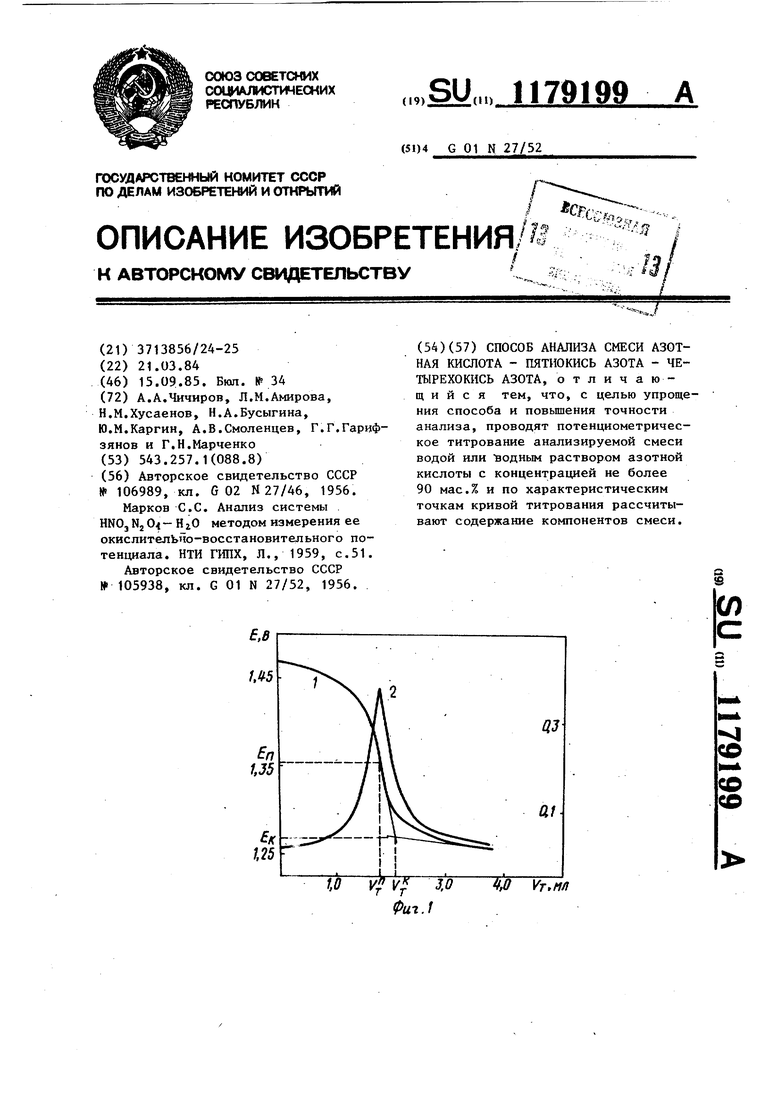
| Метод анализа системы НПО3-П2О4-Н2О | 1956 |
|
SU106989A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Марков С.С | |||
| Анализ системы HNOj Nj Оч - Н гО методом измерения ее окислителЬйо-восстановительного потенциала | |||
| НТИ ГШХ, Л., 1959, с.51 | |||
| Способ измерения окислительно-восстановительного потенциала | 1956 |
|
SU105938A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
1985-09-15—Публикация
1984-03-21—Подача