Изобретение относится к экспериментальной биологии и медицине и может быть использовано в целях выяснения механизмов динамического нарушения равновесия компонентов системы, регулирующей агрегатное состояние крови, а также установления возможностей фармакологической коррекции изменений тромбоцитарного и плаз- менно-коагуляционного гемостаза в условиях патологии инфекционной природы.
Цель изобретения - воспроизведение пролонгированного течения гиперкоагуляции за счет того, что экспериментальным животным внутримышечно вводят однократно бо- тулинический токсин типа С в дозе 2,2- 2,5 мышиных LD 50/кг массы тела.
Пример 1. У контрольной крысы массой 220 г показатели системы гемостаза харак теризовались следуюшими показателями: время свертывания крови 120 с, силиконовое время свертывания крови 120 с. индекс диапазона контактной активации 33,33%, антитромбин 111 - 14 с, гепарин 4 ед.
Опытной крысе массой 230 г внутримышечно вводят однократно в икроножные мышцы обеих задних конечностей ботулини- ческий токсин типа С в дозе 2,2 мышиных Ш50/кг массы тела.
Через 1 ч после введения ботулиничес- кого токсина при отсутствии клинических проявлений интоксикации в показателях системы гемостаза произошли следуюш,ие изменения: время свертывания крови 90 с, силиконовое время свертывания крови 90 с, индекс диапазона контактной активации , антитромбин 111 - 10 с, гепарин 3 ед.
Через 72 ч после инъекции токсина развились параличи задних конечностей. Наблюдаются следующие изменения в показателях системы гемостаза: время свертывания крови 240 с, силиконовое время свертывания крови 480 с, индекс диапазона контактной активации 50%, антитромбин 111 - 33 с, гепарин 9 ед.
Таким образом, через 1 ч после введения экзотоксина у экспериментального животного развилась гиперкоагуляционная фаза диссеминированного внутрисосудистого свертывания крови (ДВС-синдрома)., связанная с усилением контактной и фосфолипидной активации процесса свертывания крови, а через 3 сут - гипокоагуляционная фаза с возникновением дефицита плазменных факторов свертывания крови.
Пример 2. У контрольной крысы массой 220 г определяют наличие в крови комплексов фибрин-мономера с продуктами деградации фибриногена и состояние системы фиб- ринолиза: этаноловый тест отрицательный, протамин - сульфатный тест отрицательный, фибриноген Б отрицательный, суммарная фибринолитическая активность крови 113 мм, плазминовая активность 60 мм.
активаторы плазминогена 53 мм, антиплаз- миновая активность 158 мм.
Опытной крысе массой 200 г однократно внутримышечно вводят в икроножные мышцы обеих задних конечностей ботулиничес- кий токсин типа С в дозе 2,5 мышиных Ш50кг массы тела.
Через 1 ч после введения ботулиническо- го токсина при отсутствии клинических проявлений интоксикации определение продук0 тов паракоагуляции и показателей системы фибринолиза дало следующие результаты: этаноловый тест положительный, протамин - сульфатный тест положительный, фибриноген Б положительный, суммарная фибрино5 литическая активность 141 мм, плазминовая активность 86 мм, активаторы плазминогена 55 мм, антиплазминовая активность 108 мм2.
Через 72 ч после инъекции токсина разви0 лись параличи задних конечностей. Определение продуктов паракоагуляции и показателей системы фибринолиза дало следующие результаты: этаноловый тест положительный, протамин-сульфатный тест положитель5 ный,фибриноген Б положительный, суммарная фибринолитическая активность 154 мм, плазминовая активность 78 мм2, активаторы плазминогена 76 мм, антиплазминовая активность 99 мм.
Таким образом, через 1 ч и в течение
0 3 сут после инъекции животному ботулини- ческого экзотоксина в крови отмечается появление комплексов фибрин-мономера с продуктами деградации фибриногена, усиливается фибринолитическая активность крови, обусловленная повышением активности плаз5 мина и активаторов плазминогена и снижением антиплазминовой активности, характерных для ДВС-синдрома.
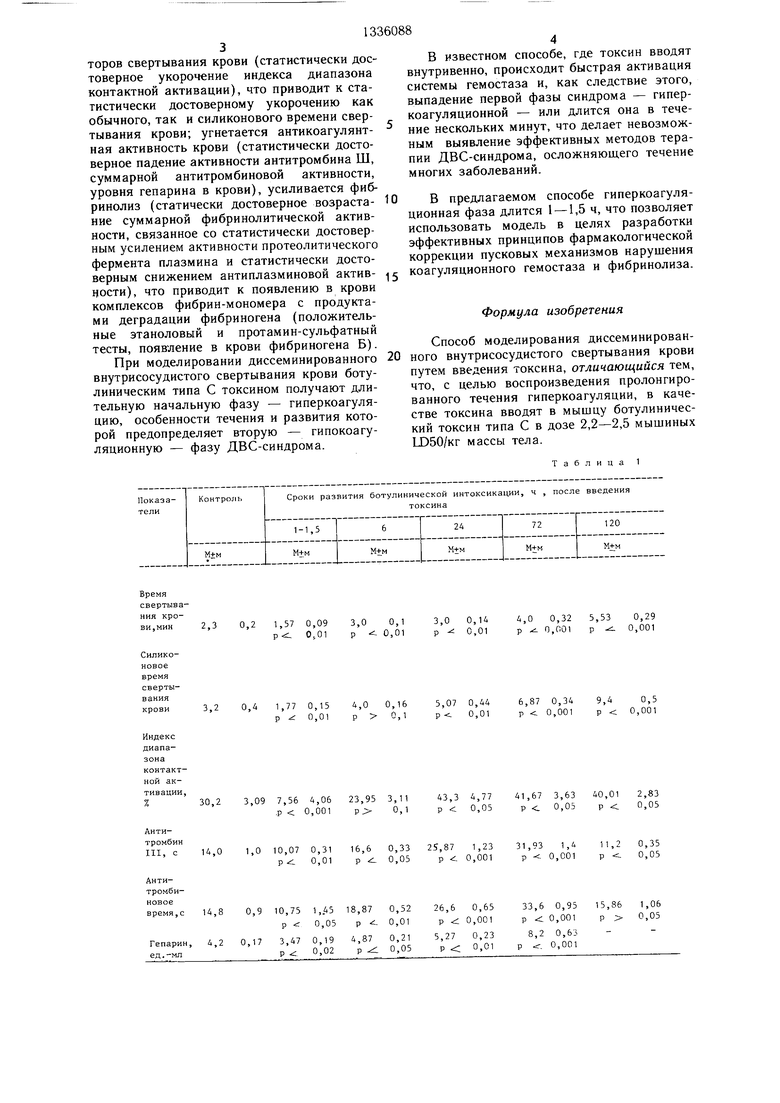
В табл. 1 приведены показатели коагу- ляционного гемостаза в динамике ботули0 нической типа С интоксикации у белых крыс. В табл. 2 приведены показатели, характеризующие появления комплексов фибрин-мономера с продуктами деградации фибриногена у белых крыс в динамике ботулинической интоксикации (/о положительных проб).
5 В табл. 3 приведены показатели фибрино- литической системы крови в динамике ботулинической типа С интоксикации у белых крыс.
В табл. 1 и 3 р - рассчитано к контроQ лю, в каждой серии опытов использовано в среднем по 15 животных.
В табл. 1-3 приводятся сравнительные данные, подтверждающие, что в течение 1-1,5 ч после инъекции ботулинического токсина в дозах 2,2-2,5 Ш50/кг развивает5 ся начальная фаза (гиперкоагуляция) диссеминированного внутрисосудистого свертывания крови, в течение которой происходит контактная и фосфолипидная активация факторов свертывания крови (статистически достоверное укорочение индекса диапазона контактной активации), что приводит к статистически достоверному укорочению как обычного, так и силиконового времени свертывания крови; угнетается антикоагулянт- ная активность крови (статистически достоверное падение активности антитромбина Ш, суммарной антитромбиновой активности, уровня гепарина в крови), усиливается фиб- ринолиз (статически достоверное возраста- ние суммарной фибринолитической активности, связанное со статистически достоверным усилением активности протеолитического фермента плазмина и статистически достоверным снижением антиплазминовой активности), что приводит к появлению в крови комплексов фибрин-мономера с продуктами деградации фибриногена (положительные этаноловый и протамин-сульфатный тесты, появление в крови фибриногена Б).
При моделировании диссеминированного внутрисосудистого свертывания крови боту- линическим типа С токсином получают длительную начальную фазу - гиперкоагуляцию, особенности течения и развития которой предопределяет вторую - гипокоагу- ляционную - фазу ДВС-синдрома.
0
В известном способе, где токсин вводят внутривенно, происходит быстрая активация системы гемостаза и, как следствие этого, выпадение первой фазы синдрома - гипер- коагуляционной - или длится она в течение нескольких минут, что делает невозможным выявление эффективных методов терапии ДВС-синдрома, осложняющего течение многих заболеваний.
В предлагаемом способе гиперкоагуля- ционная фаза длится 1 -1,5 ч, что позволяет использовать модель в целях разработки эффективных принципов фармакологической коррекции пусковых механизмов нарушения г коагуляционного гемостаза и фибринолиза.
Формула изобретения
Способ моделирования диссеминированного внутрисосудистого свертывания крови путем введения токсина, отличающийся тем, что, с целью воспроизведения пролонгированного течения гиперкоагуляции, в качестве токсина вводят в мышцу ботулиничес- кий токсин типа С в дозе 2,2-2,5 мышиных LD50/Kr массы тела.
Таблица 1
-
О О
60,0
66,777,
63,2
60,053,363,247,4
100,0100,0100,0100,0
Суммарная
фибринолитическая
актив- 110,3
ность,мм
1,07 141,2 2,27 191,45 12,21 227,65 10,67 156,39 3,53 146,69 4,34 р -0,001 ,001 р 0,001 0,001 ,001
Плазмино- вая активность,мм 2,04 84,85 3,0 84,23 4,6 82,32 1,75 79,88 3.66 106,26 3,29
,001 р.0,001 р . 0,001 р -0,01 ,001
Активаторы плазми- 49,08 ногена,мм1,64 56,35 2,84 107,0 10,34 145,33 10,92 76,52 5,88 40,43 5,44 ,,001р 0,001 р.0,001р 0.01
154,0 4,1 118,8 3,79 112,17 4,22 110,16 3.78 89,76 2.52
р л 0,001р, 0,001р, 0,001р 0,001
Таблица 2
66,777,
63,2
Таблица 3
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ СТЕНОКАРДИЕЙ | 1994 |
|
RU2086269C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ФАКТОРОВ ПРОГНОЗА ТЯЖЕЛЫХ ГЕМОРРАГИЧЕСКИХ ОСЛОЖНЕНИЙ У БОЛЬНЫХ ОСТРЫМ ПРОМИЕЛОЦИТАРНЫМ ЛЕЙКОЗОМ ПРИ ДИАГНОСТИКЕ | 2009 |
|
RU2400750C1 |
| СПОСОБ ОПТИМИЗАЦИИ ДИАГНОСТИКИ СТАДИЙ ОСТРОГО СИНДРОМА ДИССЕМИНИРОВАННОГО ВНУТРИСОСУДИСТОГО СВЕРТЫВАНИЯ КРОВИ | 2009 |
|
RU2402277C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ РАННИХ КРИТЕРИЕВ РАЗВИТИЯ ГИПЕРКОАГУЛЯЦИИ В ПРОЦЕССЕ ЛЕЧЕНИЯ БОЛЬНЫХ ОСТРЫМ ЛЕЙКОЗОМ | 2002 |
|
RU2227301C2 |
| СПОСОБ ВЫЯВЛЕНИЯ ГИПЕРКОАГУЛЯЦИИ И АКТИВАЦИИ ВНУТРИСОСУДИСТОГО СВЕРТЫВАНИЯ У БОЛЬНЫХ ОСТРЫМ ЛИМФОБЛАСТНЫМ ЛЕЙКОЗОМ ПРИ МАНИФЕСТАЦИИ ЗАБОЛЕВАНИЯ | 2012 |
|
RU2497127C1 |
| Способ профилактики хронической свинцовой коагулопатии у экспериментальных животных | 2019 |
|
RU2706386C1 |
| СПОСОБ ПРОФИЛАКТИКИ ХРОНИЧЕСКОЙ МОЛИБДЕНОВОЙ КОАГУЛОПАТИИ | 2020 |
|
RU2739690C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ХРОМ-ИНДУЦИРОВАННОЙ КОАГУЛОПАТИИ У КРЫС В ЭКСПЕРИМЕНТЕ | 2020 |
|
RU2743812C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГЕМОСТАЗИОЛОГИЧЕСКИХ КРИТЕРИЕВ НЕБЛАГОПРИЯТНОГО ИСХОДА СЕПСИСА У БОЛЬНЫХ ОСТРЫМ МИЕЛОБЛАСТНЫМ ЛЕЙКОЗОМ | 2006 |
|
RU2320996C1 |
| Способ количественного определения фибриногена в плазме крови | 1983 |
|
SU1146002A1 |


Авторы
Даты
1987-09-07—Публикация
1985-06-05—Подача