Изобретение относится к области медицины и биологии, в частности к энзимологии системы комплемента и количественной характеристики биопрепаратов.
Цель изобретения - повышение точности способа.
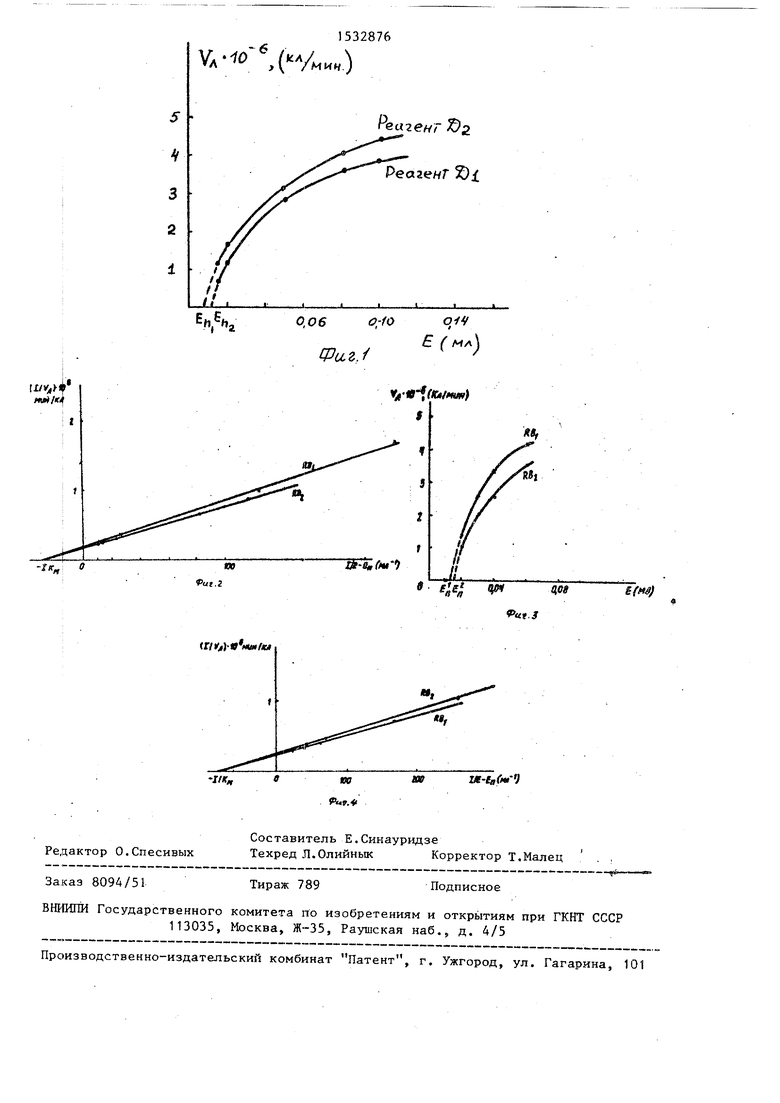
На фиг.1 представлена зависимость скорости лизиса от количества фактора D в пробе, полученная для разных реагентов; на фиг.2 - зависимость величины обратной скорости лизиса от величины обратной ргзности общего и порогового количества фактора D в пробе, полученная для разных реагентов; на фиг.З - зависимость скорости лизиса от количества фактора В в пробе, полученная для разных реагентов; на фиг.4 - зависимость величины обратной скорости лизиса от величины обратной разности общего и порогового количества фактора В в пробе, полученная для разных реагентов.
Повышение точности способа достигается за счет использования зависимости I/VA от I/E-ЕГ,, где Ул - ско
рость лизиса эритроцитов, определяемая тангенсом угла наклона касательной к кривой лизиса на участке наибольшего наклона; Е - полное количество исследуемого фактора в инкубационной среде; Еп - пороговое количество данного фактора, при котором лизис эритроцитов в системе еще не происходит .
Учет порогового количества фактора позволяет получить в указанных координатах прямую, которая пересекает ось абсцисс в точке, соответствующей величине - 1/Км, где Kw - эффективное Количество исследуемого фактора в инкубационной среде, при котором скорость лизиса в системе составляет половину от максимально возможной. Величина К., в данных координатах одиЛп
Какова для всех реагентов, полученных из разных сывороток.
За единицу активности препарата принимают величину, обратную KM
Пример 1. Определение гемолитической активности фактора D.
Состав инкубационной среды и порядок смешивания реагентов.
В кварцевые кюветы вносят препарат фактора D (в фосфатном буфере 0,02 М, рН 7,4, приготовленном на 0,15 М Nad) в количествах 0,15 0,08; 0,05; 0,02 и 0,0165 мл; фосфатный буфер (0,02 М, рН 7,4, приготовленный на 0,15 М NaCl) в количестве, соответственно 0; 0,02; 0,05; 0,08 или 0,0835 мл, т.е. дополняющем пробу до 0,1 мл; реагент для определения фактора D, т.е. сыворотку, истощенную по фактору D (RD) в количестве 0,2 мл; вероналовый буфер, рН 7,4, содержащий 10 мМ ЭГТА и 0,1% желатину, в количестве 0,4 мл.
После смешивания перечисленных компонентов кювета прогревается в тече- ние .3 мин при 37°С в проточной термо- статируемой ячейке спектрофотометра. Затем в каждую кювету вносят по 0,1 мл стандартной суспензии эритроцитов кро лика, приготовленной на вероналовом буфере (рН 7,4), содержащем 0,1% желатины, таким образом, чтобы концентрация клеток в кювете была около 1,2-107 кл/мл. Лизис эритроцитов регистрируется спектро ют ометрически при 800 нм. Результаты измерений активности одного и того же препарата фактора D с двумя реагентами по прототипу приведены в табл. 1.
0
5
0
5
45
0
5
40
55
Из лопученных данных строят зависимость VA -от Е (мл) (фиг.), из которых находят пороговые количества фактора (Е ), при добавлении которых в системе еще не происходит лизис эритроцитов. Из приведенных данных Еп для реагента D( составляет 0,012 мл, а для реагента DZ 0,008мл (на общий объем инкубационной смеси). Зависимость 1/VA от 1/Е нелинейны и не дают возможности определить величину Км.
Затем строят зависимость 1/V от 1/Е-Еп (фиг.2), которая линейна и для всех реагентов пересекают ось абсцисс в одной и той же точке, соответствующей величине -1/Км -28 мл.
Рассчитывают величину К сначала в мл, а затем, зная общую концентрацию белка в препарате фактора D, в мкг. Она равна 0,036 мл или 3,96 мкг (при концентрации белка в препарате фактора 0,11 мг/мл).
Гемолитическую активность исследуемого препарата характеризуют величиной 1/ KM, которая составила в данном случае 0,253 ед/мкг.
График на фиг.2 позволяет также количественно охарактеризовать реагенты, используемые в опыте, по максимальным скоростям лизиса, которые могут быть достигнуты в системе с применением данного реагента при фиксированной концентрации эритроцитов. Прямые, полученные для разных реагентов, отсекают на оси ординат отрезки, численно равные 1/VMOKC. Таким образом, из полученных данных VMaHC для KD 5,56-Ю6 кл/мин, a V для Ю3г 6,25106 кл/мин.
Пример 2. Определение гемолитической активности фактора В.
Состав инкубационной смеси и порядок смешивания реагентов аналогичен примеру 1. Вместо фактора D вносят различные количества фактора В (от 0,01 до 0,06 мл) и соответствующие количества буфера - для доведения объема до 0,1 мл. Затем вносят реагент для определения фактора В (RB) в количестве 0,2 мл. Все остальные действия и расчеты производят аналогично примеру 1. Результаты измерений приведены в табл.2 и представлены на фиг.З и 4.
Из графика на фиг.З определены пороговые количества для каждого реагента. Для RB, ,014 мл, что при кон центрации белка в препарате фактора В, раиной 1,2 мг/мл, соответствует 16,8 мкг, для RBZ , мл, или 19,2 мкг препарата фактора В в инкубационной смеси. С учетом полученных в каждом опыте пороговых значений количества фактора В построены графики в обратных координатах на фиг.А. Из этого графика находят величину Км которая в обоих случаях независимо от реагента составляет 0,013 мл, т.е. 15,6 мкг фактора В. Гемолитическая активность исследуемого препарата фактора В составляет 1:15,6 0,064 ед/мкг. Максимальная скорость лизиса для реагента RB, 4,76-10 кл/ /мин, для реагента ,1710 кл/ /мин.
Формула изобретения
Способ определения гемолитической активности протеолитических компо- нентов альтернативного пути комплемента путем измерения скорости лизиса эритроцитов кролика в присутствии анализируемого фактора и сыворотки крови, истощенной по данному фактору, в качестве реагента, отличающийся тем, что, с целью повышения точности способа, измеряют скорость лизиса эритроцитов при уменьшающихся концентрациях фактора в системе, определяют пороговое количество фактора, добавление которого в систему еще не вызывает лизиса эритроцитов, а затем строят зависимость
1/VA от 1/Е-Е„,
где VA - скорость лизиса эритроцитов; Е - общее количество добавленного в систему препарата исследуемого фактора; Еп - пороговое количество фактора, и по этой зависимости определяют величину гемолитической активности, соответствующую концентрации исследуемого фактора, при которой скорость лизиса в системе равна половине максимальной.
Таблица 1

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ РЕАКТИВНОГО ЛИЗИСА КЛЕТОК | 1995 |
|
RU2101702C1 |
| Скрининг-тест для определения функциональной активности классического пути системы комплемента | 2018 |
|
RU2704121C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ФУНКЦИОНАЛЬНОЙ АКТИВНОСТИ КОМПОНЕНТА C2 КОМПЛЕМЕНТА ЧЕЛОВЕКА | 2001 |
|
RU2195670C1 |
| Способ определения тромбинового пути активации системы комплемента | 2019 |
|
RU2717946C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ФУНКЦИОНАЛЬНОЙ АКТИВНОСТИ С3-КОНВЕРТАЗЫ АЛЬТЕРНАТИВНОГО ПУТИ АКТИВАЦИИ КОМПЛЕМЕНТА ЧЕЛОВЕКА | 2017 |
|
RU2666957C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ИНГИБИРУЮЩЕГО ДЕЙСТВИЯ ВЕЩЕСТВ НА КОМПЛЕМЕНТ | 2000 |
|
RU2195665C2 |
| Определение циркулирующего тромбина в тесте активации системы комплемента | 2019 |
|
RU2709341C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ФУНКЦИОНАЛЬНОЙ АКТИВНОСТИ ФАКТОРА D КОМПЛЕМЕНТА ЧЕЛОВЕКА | 2003 |
|
RU2232991C1 |
| Скрининг-тест для определения функциональной активности системы комплемента крысы | 2022 |
|
RU2786208C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ФУНКЦИОНАЛЬНОЙ АКТИВНОСТИ ФАКТОРА В КОМПЛЕМЕНТА ЧЕЛОВЕКА | 2013 |
|
RU2550946C1 |
Изобретение относится к области медицины и биологии, в частности к способам определения гемолитической активности протеолитических компонентов альтернативного пути комплемента. Способ обеспечивает повышение точности определения гемолитической активности факторов комплемента за счет исключения искажающих влияний со стороны применяемого реагента. Для этого с помощью ряда измерений скорости лизиса при уменьшающихся концентрациях исследуемого фактора, определяют его пороговое количество, ниже которого лизис эритроцитов не происходит, а затем по зависимости 1/Vл от 1/E-Eп, где Vл - скорость лизиса, определяемая из тангенса угла наклона касательной к кривой лизиса на участке наибольшего наклона, E - общее количество препарата исследуемого фактора, внесенное в инкубационную смесь, Eп - пороговое количество препарата исследуемого фактора, определяют такую эффективную концентрацию фактора, при которой скорость лизиса в данной системе составляет половину от максимальной. Способ может быть применен в научных и клинических исследованиях протеолитических компонентов комплемента, а также в производстве реагентов и препаратов факторов комплемента.
15 30 45 60 90
Таблица 2
О
31,8
46,4
42,0
39,7
1532876
, (,,)
s
1
3 2
Е„,Ч
0,O6
Фиг.1/
i/v4
Put 2
VI ,)« « fK
ItK,
Редактор О.Спесивых
Составитель Е.Синауридзе
Техред Л.Олийнык Корректор Т.Малец
Заказ 8094/51
Тираж 789
ВНИИПИ Государственного комитета по изобретениям и открытиям при ГКНТ СССР 113035, Москва, Ж-35, Раушская наб.9 д. 4/5
0-10014
Ј (мл)
S№)
ae-tafm-1}
Подписное
| Иммунология, 1986, № 3, с | |||
| Приспособление для соединения пучка кисти с трубкою или втулкою, служащей для прикрепления ручки | 1915 |
|
SU66A1 |
Авторы
Даты
1989-12-30—Публикация
1988-02-10—Подача