Для соединения (I) электрод обладает прямолинейной электродной функцией в интервале концентраций ионов кальция 1-10 - I - 10-1 моль/л.Крутизна электродной функции составляет 22±3 мВ/рС. Время отклика электрода в растворах кальция с концентрациями - 1 моль/л составляет. 2-5 мин и для концентрации 1 х х 10 моль/л менее 1 мин. Между измерениями электрод хранят в сухом виде. Перед работой электрод вымачивают в растворе хлорида кадьция с концентрацией 1 10 3моль/л в течение 1 ч,затем отмывают 5-10 мин в дистиллированной воде до постоянного значения хлорида кальция с концентрацией 1 х х Ю моль/л в течение 1 ч, затем отмывают 5-10 мин в дистиллированной воде до постоянного значения потенциала. При ежедневном использовании электрода электродная функция сохраняется не менее 1Э5 мес.
Мембрана обратима к ионам кальция в интервале рН 5,5-13,0. Коэффициенты селективности, определенные методом непрерывных растворов и постоянной концентрации мешающих ионов, совпадают (табл.1). При комплексонометрическом титровании ионов кальция 0,1 моль/л раствором ЭДТА определение проводят как в среде аммиачного буфферного раствора с рН 10, так и
в растворах с рН 12-13. Для создания рН 12-13 в анализируемый раствор вводят 5 моль/л раствора КОН. Объем анализируемого раствора составляет 20 мл.
Для нахождения конечной точки титрования результаты титрования представляют графически в виде кривых трех типов :интегральной (EM6- V дифференциальной (-ЛЕ/dV - VM6) и в виде
кривой по методу Грана. По данным кривых титрования строят градуировоч- ный графит в координатах: количество миллимолей титранта - количество мил- лимолей кальция.
В табл. 1 представлены сравнительные характеристики кальцийселектив- ных электродов на основе соединения (l) и амидопроизводных полиоксиэти- леновый (прототип).
Из табл.1 следует, что при рН
5,5-10 методом прямой потенциометрии можно определять сумму ионов кальция и магния, а при рН 12-13 методом по- тенциометрического титрования раствором ЭДТА можно селективно определять кальций в присутствии магния, натрия и кальция.
На фиг.1 представлены результаты титрования- раствором ЭДТА растворов СаС12 в среде аммиачного буферного раствора при рН 10 в интегральной и дифференциальной формах: 1-4 в интегральной форме, 1-4- в дифференциальной форме, МСо)2+моль: 1-0,081, 2-0,244, 3-0,407, 4-0,507. СЭАГ/, 0,1 моль/л.
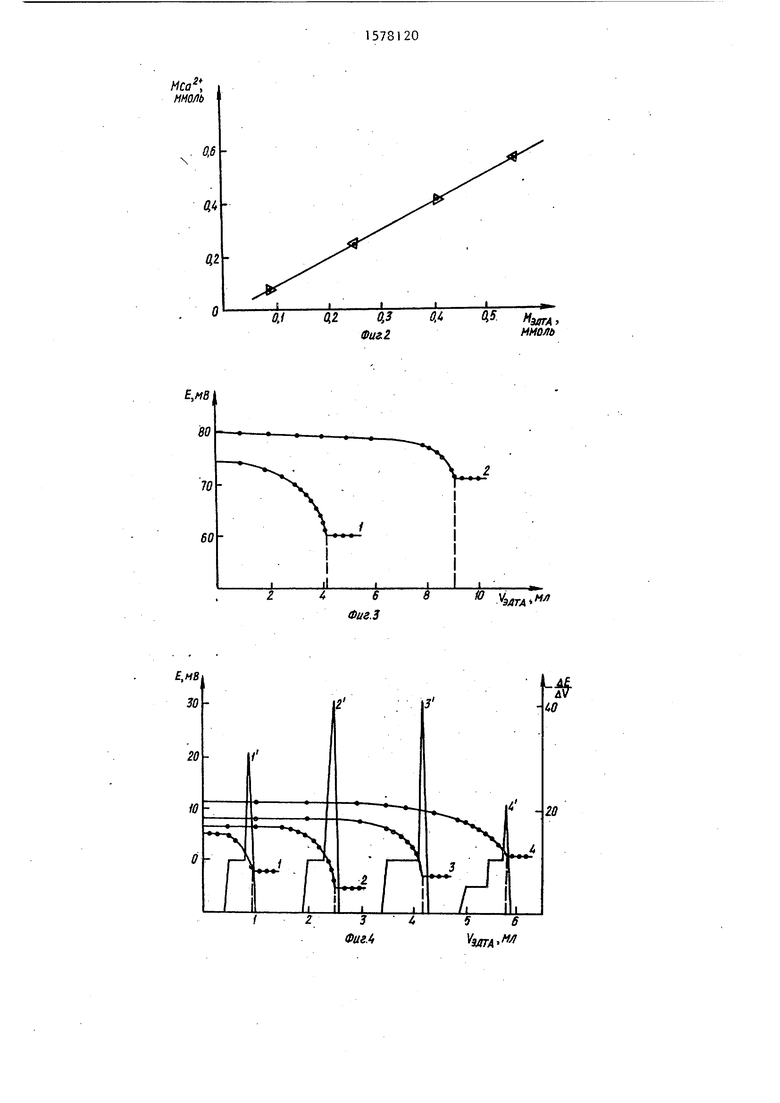
На фиг.2 представлен градуировоч- ный график для определения кальция методом лотенциометрического титрования раствором ЭДТА при рН 10. Из данных фиг.1 и 2 следует, что количемодельных растворах, имитирующих составу сыворотку крови,содержащи фоновый электролит состава: 0,150 моль/л NaCl, 0,005 моль/л К и 0,001 моль/л MgCli, проводят в растворах при рН 12. Результаты т рования, полученные при обработке кривых титрования разными методам IQ совпадают.
Данные по определению кальция растворах фонового электролита пр тавлены в табл.2.
15Как видно из табл.2, кальций м
|НО определять в составах,имитирую щих сыворотку крови.
Таким образом,синтезированное
ство ммолей ЭДТА, затраченное на тит- 2° соединение (I) при использовании
рование, равно количеству ммолей ионов кальция, взятому для титрования, т.е. отношение Сз.:ЭДТА 1: 1.
На фиг о 3 представлены результаты титрования раствором ЭДТА при рН 10:1 - раствора кальция; 2 - модельного раствора Mg lf 1:1. С Эдтл 0,1 ммоль/л. Из фиг.З следует, что при рН 10 титруется сумма ионов кальция и магния.
На фиг.4 представлены кривые титрования кальция раствором ЭДТА при рН 12: 1-4 - в интегральной форме, 1 -4 в дифференциальной форме. МСм« ммоль: 1-0,081; 2-0,24i; 3- 0,407; 4-0,570. Сэдтл 0,1 моль/л.
На фиг.5 представлен градуировоч- ный график для определения ионов кальция методом потенциометрическо- го титрования раствором ЭДТА: 1 - при рН 12; 2 - при рН 13,
На фиг, 6 представлены кривые титрования раствором ЭДТА при рН 12: 1 - ионов кальция; 2 - модельного раствора Са4 : Mg г 1:1, 3 - fMg 1:10; С ЭАТА 0,1 моль/л.
Из данных фиг.4 - 6 видно, что наличие ионов магния не оказывает влияния на определение ионов кальция.
При рН 12-13 с ЭДТА взаимодействует только кальций, магний при этом значении рН выпадает в виде гидрок- сида и не взаимодействует с ЭДТА.
Определение ионов кальция электродом на основе соединения (I) в
модельных растворах, имитирующих по составу сыворотку крови,содержащих фоновый электролит состава: 0,150 моль/л NaCl, 0,005 моль/л КС1 и 0,001 моль/л MgCli, проводят в растворах при рН 12. Результаты титрования, полученные при обработке кривых титрования разными методами, Q совпадают.
Данные по определению кальция в растворах фонового электролита представлены в табл.2.
5Как видно из табл.2, кальций мож|НО определять в составах,имитирующих сыворотку крови.
Таким образом,синтезированное
его в качестве электродноактивного вещества кальцийселективного электрода расширяет область рН работы электрода до 13, что позволяет при рН 12-13 селективно определять активность ионов кальция в присутствии ионов магния, натрия, калия, в частности в сыворотке крови.
Таким образом, предложенное новое химическое соединение 1,8-бисС2-(пи- перидиниминометин)феноксиЗ-3,6-диок- саоктана формулы () позволяет расширить области рН работы кальцийселек- тивного электрода при потенциометри- ческом титровании ионов кальция раствором ЭТДА и определять их активность в присутствии в водном растворе ионов магния, калия, натрия.
Формула изобретения
1,8-Бис- 2-(пиперидиниминометин)- . феноксиЗ 3,6-диоксаоктан формулы
ПГЬ
50
55 в качестве электродноактивного вещест- ва кальцийселективного электрода.
Таблица 1



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ потенционметрического определения концентрации ионов кальция в воде | 1982 |
|
SU1081518A1 |
| Состав мембраны ионоселективного электрода для определения активности ионов стронция | 1981 |
|
SU987499A1 |
| 1,8-Бис-[2-(4-антипирилиминометин)фенокси]-3,6-диоксаоктан в качестве электродноактивного вещества ионоселективного электрода для определения активности ионов свинца в водных растворах | 1988 |
|
SU1546459A1 |
| СПОСОБ АМПЕРОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ МОЛОЧНОЙ КИСЛОТЫ НА ПЛАТИНОВОМ ЭЛЕКТРОДЕ | 2015 |
|
RU2612000C1 |
| Тест-система для скрининга нарушений минерального гомеостаза крови | 2023 |
|
RU2829335C2 |
| ПРОИЗВОДНОЕ БИСАМИДОВ ДИКАРБОНОВЫХ КИСЛОТ, ЕГО ПРИМЕНЕНИЕ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ, СПОСОБЫ ЕГО ПОЛУЧЕНИЯ | 2018 |
|
RU2719464C2 |
| ПРОИЗВОДНОЕ БИСАМИДОВ ДИКАРБОНОВЫХ КИСЛОТ, ЕГО ПРИМЕНЕНИЕ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ, СПОСОБЫ ЕГО ПОЛУЧЕНИЯ | 2020 |
|
RU2815401C2 |
| Способ определения неионогенных поверхностно-активных веществ | 1982 |
|
SU1078325A1 |
| ПРОИЗВОДНОЕ БИСАМИДОВ ДИКАРБОНОВЫХ КИСЛОТ, ЕГО ПРИМЕНЕНИЕ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ, СПОСОБЫ ЕГО ПОЛУЧЕНИЯ | 2018 |
|
RU2725881C2 |
| ПРОИЗВОДНОЕ БИСАМИДОВ ДИКАРБОНОВЫХ КИСЛОТ, ЕГО ПРИМЕНЕНИЕ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ, СПОСОБЫ ЕГО ПОЛУЧЕНИЯ | 2018 |
|
RU2721421C2 |

Изобретение касается химии азотсодержащих гетероциклических соединений, в частности 1,8-бис-[2 - (пиперидиниминометин) фенокси] - 3,6 - диоксаоктана в качестве электродноактивного вещества кальцийселективного электрода. Цель - выявление соединения, позволяющего селективно определять активность ионов кальция в присутствии ионов MG, NA, K в водном растворе. Получение ведут из аминопиперидина и 1,8-бис-(бензальдегидокси)-3,6-диоксаоктана при нагревании при 50-60°С. т.пл. 65-66°С. Брутто-ф-ла C 30H 42O 4N 4. Новое соединение расширяет область PH работы электрода до 13. 6 ил., 2 табл.
Прототип 1 -Ю- -l -10-4 28
4-10
Na - 1,7-КГ, K+-4,5-10-f, Mg44 - 2,6-1 -lO 4
He работает
Таблица2
40
6 VWM
НСа ммоль
0,1
О.
0,2.0,3
Фиг
Е,МВ 80
70
60
04
V Мм, ммо/н
МСаК
MMO/lb
0,6
0,4
0,2
0,1
0,2
ZQ
0,4
Of
MM, ммоль
| Тиоуреидопроизводные дибензополиоксиэтиленов в качестве электродно-активных веществ ионоселективных электродов для определения активности ионов свинца в водных растворах | 1984 |
|
SU1183502A1 |
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| Дзиолеко Вг.М | |||
| Высокоселективный кальциевый электрод на основе лиганда | |||
| - Электрохимия, 1982, т.18, № 10, с | |||
| Способ включения микрофона в цепь накала катодной лампы | 1922 |
|
SU1435A1 |
Авторы
Даты
1990-07-15—Публикация
1988-09-23—Подача