Изобретение относится к химической технологии, в частности к промьш- лечному получению гидроксиламинсуль- фата (ГАС) для производства кяпролак- тама, и быть использовано при получении ГАС каталитическим восстановлением монооксида азота водородом.
Цель изобретения - повышение степени использования монооксида азота и водорода на получение гидроксиламин- сульфата и уменьшение {соличества отходящих газов.
Поставленная цель достигается тем, что в реакционный объем с циркулирующим в нем суспендированным нанесенным платиновым катализатором непрерывно подают газообразные водород и монооксид азота и водный раствор серной кислоты. При этом в реакционном объеме поддерживают давление 0,15-2 МПа и мог.рное отношение водорода к монооксиду азота, равное 10-20. Степень превращения монооксида азота и водорода в ГАС составляет соответственно 92-93 и 71-81,5% (по прототипу при Н : N0 3,5-6 и давлении, несколько превьшающем атмосферное, степени превращения N0 и Hj в ГАС соответственно равны 71,6-89 и 51-78%).
Изобретение позволяет, кроме того, снизить скорость побочной реакции образования оксида диазота (в 1,7-10 раз) и уменьшить количество выбросных газов (в 1,3-2,1 раза).
Пример. Синтез ГАС проводили в качаю цемся реакторе общим объемом 0,4 дм при давлении 0,15 - 2 МПа. В реактор заливали 0,15 дм
исходного раствора 19%-ной серной кислоты и загружали 0,8 г платинового катализатора, представляющего собой платину, нанесенную на электродный графит с размером частиц 25-90 мкм. Перед началом опыта реактор продували водородом до отсутст- ВИЯ кислорода в продувочном газе и поднимали температуру до , после чего включали устройство, обеспечивающее интенсивность перемешивания, нообзсодимую для осуществления процесса в кинетической областиj чтобы скорость реакции была прямо пропорциональна количеству катали aTopai
Для поддержания в объеме реактора молярного отношения Н : N0, равного 10-20, на в реактор подавали газовую смесь с молярным отноше- нием Н : Ш, равным 1,7-2,0.
В качестве сыроя использовали водород (чистотой 99,9%) и оксид азота, содержащий 5% азота. При рекомендуемом отношении Н : N0 в газовой фазе реактора содержится,мае.%: Н 65-83; N0 3-6,2; 0,5-1,2; азот остальное. Такая смесь невзрыво опасна даже при высоких давлениях.
В опытах измеряли расходомерами количество газовой смеси на входе в реактор и количествр выходящих из реактора газов. Хроматографическим анализом определяли состав (содержание водорода, монооксида азота,оксида диазота, азота) в подаваемом в реактор газе и в газовой фазе геак- тора.
Результаты серий опытов представлны на графике и в таблш е.
...
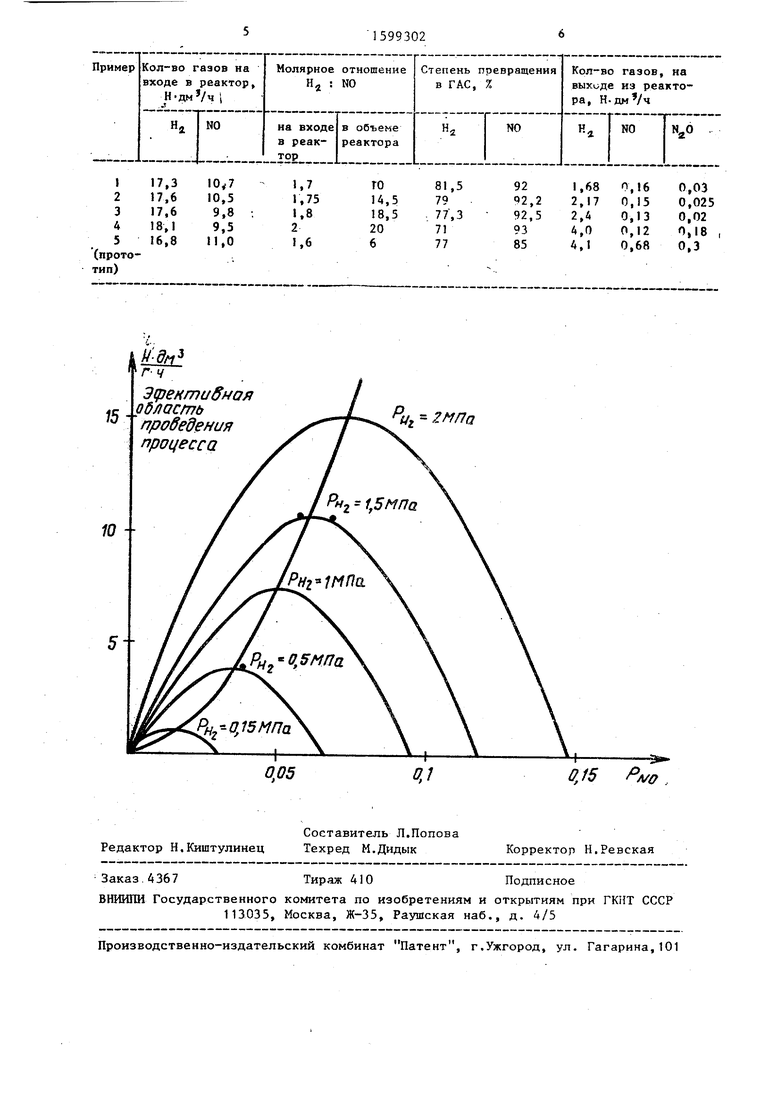
па графике показана скорость переработки (,ч) N0 в ГАС на 1 г катализатора в зависимости от парциального давления N0 и Н.
Кап видно из графика, оптимальной скорости переработки N0 в ГАС соответствует вполне определенное отношение Hg : N0, причем, чем вьше обще
0
5
0
давление в реакторе, тем больще это оптимальное отношение.
Опыт ным путем установлено, что оптимальным отношением Hg : N0 в газовой фазе реактора является 10-20 (преимущественно 10-15). В зтих условиях достигается наиболее высокая степень переработки исходных газообразных компонентов в ГАС.
В таблице представлены конкретные примеры для общего давления 0,4 Ша, поясняющие зависимости степени переработки N0 и Н в ГАС и состава газовой смеси на выходе из реактора от молярного отношения HjiNO в реакционном объеме. Для сравнения показаны данные по прототипу.
Изобретение по сравнению с .прототипом имеет следующие преимущества: степень превращения оксида азота и водорода в гидроксиламинсульфат возрастает соответственно на 4-1I и 255-20%; в 1,3-2,1 раза уменьшается количество выбросных газов, что способствует решению экологических проблем.
5
30 Формула изобретения
0
Способ получения гидроксиламин- сульфата, включающий непрерывную подачу в реактор монооксида азота и водорода, восстановление монооксида азота водородом на нанесенном платиновом катализаторе в растворе серной кислоты при повьшенных температуре и давлении и отвод продукционного раствора и отходящих газов, о т л и- ч а ющий;С я тем, что, с целью повьш1ения степени использования мо- ноо;ссида азота и водорода н а получение гидроксиламинсульфата и уменьшения количества отходящих газов, процесс ведут при молярном отношении водорода к монооксиду азота,равном 10-20, и давлении 0,15-2 МПа.
5
5
г V
Э(рентибиоя ,с Лобласшь проведения
процесса
10 -
005
1 2мпа
-эв.
ff.fS РА/О

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОИЗВОДСТВА ГИДРОКСИЛАМИНСУЛЬФАТА | 2008 |
|
RU2364570C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОКСИЛАМИНСУЛЬФАТА | 2003 |
|
RU2257340C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОКСИЛАМИНСУЛЬФАТА | 2006 |
|
RU2327633C2 |
| Способ получения гидроксиламинсульфата | 1987 |
|
SU1495289A1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОКСИЛАМИНСУЛЬФАТА | 2019 |
|
RU2717515C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОКСИЛАМИНСУЛЬФАТА | 2003 |
|
RU2259940C1 |
| СПОСОБ УПРАВЛЕНИЯ ПРОЦЕССОМ ПОЛУЧЕНИЯ ГИДРОКСИЛАМИНСУЛЬФАТА | 2006 |
|
RU2305657C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОКСИЛАМИНСУЛЬФАТА | 2005 |
|
RU2287481C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОКСИЛАМИНСУЛЬФАТА | 2005 |
|
RU2287482C1 |
| Способ получения гидроксиламинсульфата в барботажном колонном реакторе | 1988 |
|
SU1627508A1 |
Изобретение относится к химической технологии, в частности к промышленному получению гидроксиламинсульфата (ГАС), и может быть использовано при получении ГАС каталитическим восстановлением монооксида азота водородом. Цель изобретения - повышение степени использования монооксида азота и водорода на получение гидроксиламинсульфата и уменьшение количества отходящих газов. В реакционный объем с циркулирующим в нем нанесенным платиновым катализатором непрерывно подают газообразные водород и монооксид азота, водный раствор серной кислоты и процесс ведут при молярном отношении H2 к NO, равном 10-20, и давлении 0,15-2 МПа. Степень превращения монооксида азота и водорода в ГАС составляет соответственно 92-93 и 71-81,5% (по прототипу 71,6-89 и 51-78%). Кроме того скорость побочной реакции образования оксида диазота снижается в 1,7-10 раз, а количество выбросных газов уменьшается в 1,3-2,1 раза. 1 табл.

| Система теплоснабжения | 1985 |
|
SU1257363A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
1990-10-15—Публикация
1988-06-14—Подача