Изобретение относится к новым биологически активным химическим соединениям, а именно к ацилированным производным 1,5,5-триметилбицик- ,2,1 гепт-2-ил-экзо-аминам, являющимся производными ряда изофенхола, содержащим, кроме терпенового фрагмента, амидную группу и проявляющим гипно- седативную активность, что позволяет предполагать возможность их использования в медицине.
Целью изобретения является изыскание соединений с гипноседативной активностью и малой токсичностью в ряду амидов, содержащих терпеновый фрагмент.
Изобретение иллюстрируется следующими примерами.
П р и м е р 1. Ы-пропионил-1,5.5-триме- тилбицикло(2,2,1)гепт-2-ил-экзо-амин (I) получают при взаимодействии 15.4 г 1,5.5- триметилбицикло(2,2.1)гептан-2-экзо-ола (изофенхола) и 17,9 г пропионитрила в присутствии 15 мл концентрированной серной кислоты, при комнатной температуре (25° С). Перемешивание продолжают 24 ч. Затем реакционную смесь выливают на лед и нейтрализуют водным раствором аммиака. Амид (I) экстрагируют из водного раствора эфиром, сушат поташом и после удаления раствориVJ
О СП Ю XI О
теля перекристаллизовывают из этанола. Выход 13 г (63%). Т.пл. 166° С.
Найдено, %: С 74.50; Н 11,05; N 6,72.
C13H2DON
Вычислено. %: С 74, Н 11,07; О 7.64; N 6.69.
ИК-спектр (см 1): 3348 с, 2960 с. 2885 с. 1645с, 1540с. 1457ср, 1390ср. ШОср, 1238 ср, 1070 ел.
Масс-спектр (м/е): 209 (М), 194, 180, 166.149.136, 121,100.95(100), 93.57,44,43, 41,32.
ПМР (б. м.д.): 0.84 с (2СН3), 0,93 с(СН3). 1,17 т (СНз), 2,19 дд (СН2), 3,90 м (С2-Н-эндо), 5.55 с (NH).
П р и м е р 2. М-Бензоил-1,5,5-триметия- бицикло{2.2,1 )гепт-2-ил-экзо-амин(11) пол- учают при взаимодействии 15,4 г изофенхола и 20,6 г бензонитрила в присутствии 15мл концентрированной серной кислоты, при комнатной температуре. Перемешивание продолжают 24 ч. Затем реакционную смесь выливают на лед и нейтрализуют водным раствором аммиака. Амид (II) экстрагируют из водного раствора эфиром, сушат поташом и после удаления растворителя перекристаллизовывают из этанола. Выход 18,6 г (72%). Т.пл. 141° С.
Найдено, %: С 79,41; Н 9.15; N5.50:
C17H250N (257,378)
Вычислено, %: С 79.33: Н 9.01; О 6,22; N5.44
ИК-спектр (см 1): 3340 с. 3065 ел. 3030 ел, 2970 с. 2930 С, 2870 с, 1635 с. 1605 ел, 1580 ср, 1490 ср, 1450 ср. 1365 ср, 1325 ср, 1295 ел. 1285 ел, 1160 ср. 750 ср, 695 с.
Масс-спектр (М/е): 257 (М4): 242, 200. 177, 161. 152. 148. 136(100), 121, 109. 105. 93,77,62.51.46.41.
ПМР-спектр(5. м.д.у. 0,99 с(2СНз), 1,05 С (СНз). 1.20 м (4Н), 1.60 м (2Н). 2.34 м (С3-Н- эндо). 3,90 м (С2-н-эндо). 6,30 с (NH), 7.44 м (ЗН) и 7.77 м (2Н) ароматика.
Биологические испытания проведены на беспородных белых мышах обоего пола массой от 17 до 22 г. Группы состояли из 6 животных. Препараты вводили подкожно в дозах, соответствующих 1/8 ЛДдо. Острую суточную токсичность определяли по методике Buchby (1963). Новые соединения в дозах 1000; 1400; 1600 мг/кг вызывали у мышей наркотический сон, а в дозах 2000 мг/кг и более - гибель.
Гипноседативное действие изучаемых препаратов исследовали во взаимодействии с хлоралгидратом и гексеналом. Хлоралгидрат (350 мг/кг) и гексенал (80 мг/кг) инъецировали внутрибрюшинно через 30
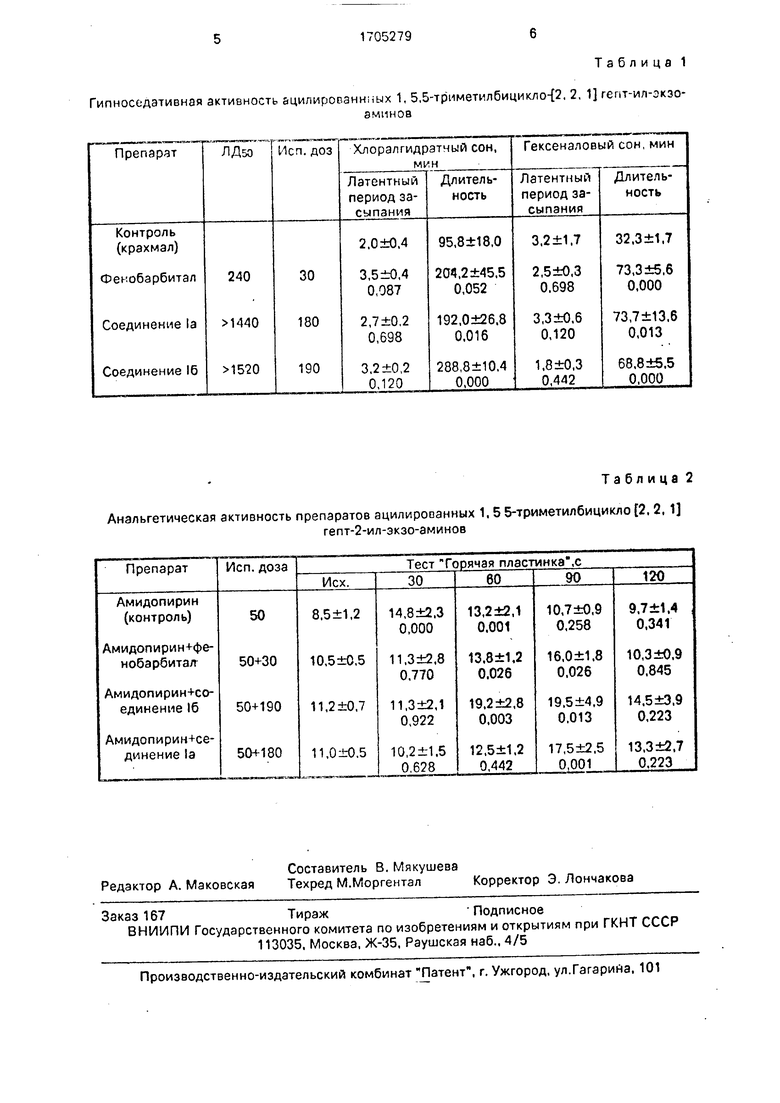
мин после введения исследуемых препаратов. Вычисляли латентный период засыпания и среднюю продолжительность сна - время с момента утраты животными рефлекса переворачивания до его восстановления (табл. 1). Потенцирующее влияние новых соединений на аналыетический эффект амидопирина оценивали по латентному периоду возникновения болевой реакции у мышей при термическом раздражений, которое осуществляли помещением животных на пластину, нагретую до 54 ±0,2° С. Для сравнения использовали фенобарбитал в зоне 30 мг/кг (1/8 ЛДбо). Результаты сведены в табл. 2.
Как видно из табл. 1 и 2, нбвые соединения в дозах 180-190 мг/кг (1 /8 ЛДзд) достоверно пролонгируют длительность сна. вызванного хлоралгидратом и гексеналом. а также повышают латентный период болевой
реакции при термическом раздражении, причем по продолжительности хлррэлгид- ратного сна и степени потенцирования анальгетического эффекта амидопирина (на 60 и 90 мин) соединение (б превосходит
действие фенобарбитала. Таким образом, новые соединения малотоксичны и в экаи- токсических дозах (1 /8 ЛДэд) по активности не уступают базовому препарату фенобарбиталу, а соединение la в некоторых случаях
превосходит его.
Ф о р м у л а и з о б р е т е н и я Ацилированные 1,5,5-триметилбицик- ,2,1 гепт-2-ил-экзоамины формулы
.NH-C-R
О
где R-CaHs или CeHs, проявляющие гипноседативную активность.
Таблица 1 Гипноседативная активность ацилированнных 1, 5,5-триметилбицикло-{2, 2, 1 гепт-ил-зкзоЭМИН08

| название | год | авторы | номер документа |
|---|---|---|---|
| Аммонийная соль 5,5,6-триметилбицикло(2,2,1)-гептан-2-он-3-экзо-сульфокислоты в качестве реагента-собирателя и антислеживателя хлористого калия и способ ее получения | 1986 |
|
SU1361137A1 |
| ПРОТИВОСУДОРОЖНОЕ СРЕДСТВО | 2008 |
|
RU2370260C1 |
| Способ получения амидов ряда 1,4,7,7-тетраметилбицикло[2.2.11]гептана | 1988 |
|
SU1631058A1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ НЕЙРОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ | 2018 |
|
RU2701739C1 |
| Средство, увеличивающее мозговой кровоток | 2016 |
|
RU2655810C2 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ СЕРДЕЧНО-СОСУДИСТЫХ ЗАБОЛЕВАНИЙ | 2014 |
|
RU2555335C9 |
| 5-АМИНО-ЭКЗО-3-АЗАТРИЦИКЛО[5.2.1.0]ДЕКАН-4-ОН, ПРОЯВЛЯЮЩИЙ АНТИАРИТМИЧЕСКУЮ, ПРОТИВОВОСПАЛИТЕЛЬНУЮ, АНАЛЬГЕТИЧЕСКУЮ И НООТРОПНУЮ АКТИВНОСТЬ | 2005 |
|
RU2281938C1 |
| Средство с комплексным фармакологическим эффектом для лечения сердечно-сосудистых заболеваний, коррекции нарушений мозгового кровообращения, лечения последствий цереброваскулярных болезней (варианты) | 2019 |
|
RU2757874C1 |
| БРОМИСТОВОДОРОДНАЯ СОЛЬ ЭЛИМОКЛАВИНА, ОБЛАДАЮЩАЯ НЕЙРОЛЕПТИЧЕСКИМИ СВОЙСТВАМИ, АНТИСЕРОТОНИНОВОЙ АКТИВНОСТЬЮ, ВЛИЯНИЕМ НА СЕРДЕЧНО-СОСУДИСТУЮ СИСТЕМУ И СИСТЕМУ СВЕРТЫВАНИЯ КРОВИ | 1984 |
|
SU1274267A1 |
| ПРОИЗВОДНЫЕ БЕНЗОТИАЗОЛА И ИХ ПРИМЕНЕНИЕ ПРИ ЛЕЧЕНИИ ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С АДЕНОЗИНОВЫМИ A-РЕЦЕПТОРАМИ | 2004 |
|
RU2348629C2 |
Изобретение касается ацилированных аминов, в частности М пропионил-или бен- , зоил)-1.5,5-триметилбицикло 2,2.1 гепт-2-ил- экзо-аминов(1а-б). проявляющих гипносе- дативную активность, что может быть использовано в медицине. Цель - создание новых веществ с низкой токсичностью и новым видом активности. Синтез 1 а-б ведут из изофенхола и пропио- или бензонитрила в присутствии конц. H2S04 при 25° С. Выход, %: т.пл.. °С; брутго-ф-ла; токсичность; ЛДзо мг/кг; активная доза, мг/кг. вызывающая наркотический сон и его длительность, мин: а) 63: 166; Ci3H230N: 1440: 180; 192; б) 72, 141; CntosON; 190. 288 (хлоргидратный сон). Совместно с известным амидопири- ; ном 1 а-б проявляют анальгетическую активность против термического раздражения 
Таблица 2
Анальгетическая активность препаратов ацилированных 1. 55-триметилбицикло 2, 2. 1
гепт-2-ил-экзо-аминов
| Кочетков Н.К., Хорлин А.Л | |||
| и др | |||
| ЖОХ, 1959, т | |||
| Солесос | 1922 |
|
SU29A1 |
| с | |||
| Фальцовая черепица | 0 |
|
SU75A1 |
| Машковский М.Д | |||
| Лекарственные средства | |||
| Ч | |||
| I | |||
| - М.: Медицина | |||
| Приспособление для установки двигателя в топках с получающими возвратно-поступательное перемещение колосниками | 1917 |
|
SU1985A1 |
| Прибор с двумя призмами | 1917 |
|
SU27A1 |
Авторы
Даты
1992-01-15—Публикация
1985-10-29—Подача