11,65 г (10 мМ) соединение V растворяют в 100 мл диметилформамида, добавляют 4,0 г (10 мМ) дипентафторфенилкарбоната (Ilia) и перемешивают при 18-20°С в течение 1 ч, Затем к реакционной массе приливают раствор 5,2 г (10 мМ) трифторацетата L-ала- нил-0-изоглутаминовой кислоты дибензи- лового эфира (VI) и 2 г (20 мМ) триэтиламина в 15 мл диметилформамида. Перемешивают в течение 5 ч, растворитель упаривают, к оставшемуся маслу приливают 200 мл диминерализованной воды, раствор экстрагируют 2x50 мл гексана, к водному слою добавляют 5 г палладиевой черни, 4 мл муравьиной кислоты и пропускают в течение 1,5 ч ток газообразного водорода. После отделения катализатора фильтрат упаривают до половины объема и наносят на колонку объемом 1 л, содержащую анионит сефа- декс А-25 в ацетатной форме. Колонку промывают 2,5 л деминерализованной воды, затем элюируют гликопептид градиентом вода - 0,15М уксусная кислота. После упа- ривания фракций, содержащих гликопептид IV, и лиофилизации остатке получают 7,5 г IV (61.3%, считая на тетрасахарид II (п-2).
Пример 2. Получение N-ацетилглюко- заминил-м -ацетилмурамил-Ьаланил-О- изоглутамина: (ГМДП) (VII).
5 г (10,0 мМ) дисахэрида И (п-1) растворяют в 100мл перегнанного диметилформамида, добавляют 4,4 г (11,0 ОмМ) соединения (Паи 1,2мл(11,ОмМ)М-метмл- морфолина. Перемешивают при 18-20° 30 мин и приливают раствор 4,6 г (11,0 мМ) трифторацетата L-аланил-О-изогяутамина у-бензилового эфира (VIII) и 2,4 мл (22.0 иМ) N-метилморфолина в 20мл i диметилформамида. Через 4,5 ч растворитель упаривают. Обработку далее проводят, как описано в примере 1. После упаривания фракций, содержащих ГМДП. и лиофилизации остатка получают 4,27 г (57,0%) ГМДП VH с содержанием основного вещества99,5% (поданным ВЭЖХ).
Пример 3. Получение соединения VII.
1,5 г р.О мм) соединения И (п-1) растворяют в 30 мл перегнанного диметияформа- мида, добавляют 1,3 г (3,0 мМ) ди-(4 -хлор-2,3.5,6-тетрафторфе н и л)-карбо - ната (1Мб) и 0,45 мл (3,0 мМ) триэтиламина. Через 2 ч приливают раствор 1.3 г (3 мМ) соединения VIII и 0,9 мл (6 мМ) триэтиламина и 5 мл диметилформамида. Перемешивают 8 ч. растворитель упаривают и дальнейшую обработку проводят, как описано в примере 1. Получают 1,4 г (62.2%) ГМДП с содержанием основного вещества 99,1% (по ВЭЖХ).
Пример 4. Получение соединения VII. 1,2 г (20 мМ) N-метилморфолиниевой соли дисахарида II () растворяют в 250 мл диметилформамида, добавляют 8,0 г (20 мМ)
соединения Ilia и перемешивают в течение 30 мин. К реакционной массе добавляют раствор 8.5 г (20 мМ) соединения VIII и 4 мл (40 мМ) N-метилморфолина в 20 мл диметилформамида. Через 5 ч растворитель упаривают. Дальнейшую обработку проводят, как описано в примере 1. Получают 9,7 г (64,7%) ГМДП с содержанием основного вещества 98,9% (по ВЭЖХ).
Пример 5. Получение соединения VII.
60 г (0,1М) N-метилморфолиниевой соли II (п-1) загружают в реактор емкостью 15 л с рубашкой и механической мешалкой и растворяют при перемешивании в 10 л смеси растворителей диметилформамид-ацетонитрил 1:4. Реакционную массу охлаждают до 5-10°С и при перемешивании из мерника добавляют раствор 48 г (0.12М) соединения Ilia в 0,2 л диметилформамида в течение 30 мин,
Охлаждение снимают, перемешивание продолжают 1 ч, затем к реакционной смеси из мерника медленно приливают в течение 30 мин раствор 51 г (0,12 М) трифторацетата VIII в 0,2 л ацетонитрила, содержащий 26 мл
(0,24 М) N-метилморфолина. Перемешивание продолжают 5 ч, растворитель упаривают, смолообразный остаток растворяют в 1 л дименерализованной воды и экстрагируют этилацетатом 2x400 мл. Далее обработку
проводят, как описано в примере 1, учитывая масштабирование синтеза. Получают 48.7 г (62%) гликопептида VII.
Пример 6. Получение N-ацетилглю- козаминил-N -ацетилмурамил-Ь-аланина
(IX).
Аналогично опыту, описанному в примере 3, из 0,5 г (1 мМ) дисахарида II (п-1), 0,43 г (1 мМ) соединения II16, 0,45 мл (3 мМ) триэтиламина и 0,35 г (1 мМ) п-толуолсульфоната бензилоеого эфира L-аланина (Х) получают 0,31 г (55%) N-эцетил-глюкозами- нил-N -ацетилмурамил-1 -аланина (IX).
П р и м е р. 7. Получение соединения VII. Аналогично опыту, описанному в примере 2, из 5 г (10 мМ) соединения II (п-1), 5,2 г (1,3 мМ)соединения Ilia, 1,4мл (13 мМ) N-метилморфолина и 4,2 г (10 мМ) соединения VIII с 2,2 мл (20 мМ) N-метилмормолина получают 3,8 г (50,6%) ГМДП.
Примере, Получение соединения VII, Аналогично опыту, описанному в примере 2, из 5 г (10 мМ) соединения II (п-1), 5.2 г (13 мМ) соединения Ilia, 1,4 мл (13 мМ) N-метилморфолина, 5,5 г (13 мМ) соединения VIII
с 2,8 мл (26 мМ) N-метилморфолина получают 3,4 г (45,3%) ГМДП.
Пример 9. Получение соединения VII.
Аналогично опыту, описанному в примере 2, из 1.0 г (2 мМ) соединения II (п-1), 0,72 г (1.8 мМ) соединения Ilia. 0,2 мл (1,8 мМ) N-метилморфолина и 0.76 г (1,8 мМ) соединения VIII с 0.4 мл (3,6 мМ) N-метилморфолина получают 0,7 г (46.6%, считая на II; 52%, считая на УП)ГМДП.
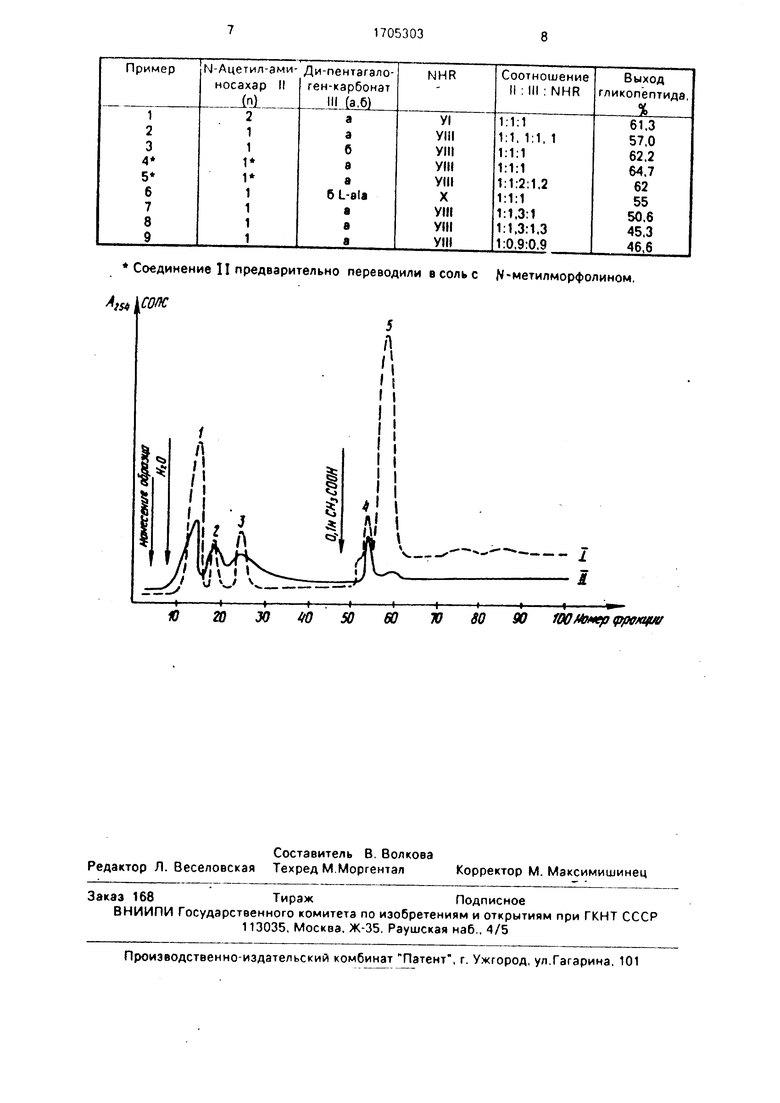
Соотношения реагентов и выход целевых продуктов в примерах 1-9 приведены в таблице.
Все образцы гликопептидов анализировались ВЭЖХ (содержание основного вещества Ј99%, см. чертеж). Температуры плавления, удельное вращение и хроматог- рафическая подвижность в тонком слое соответствуют константам для веществ полученных по способу-прототипу.
Таким образом, разработан новый способ синтеза гликопептидов формулы I, отли- чающийся от способа-прототипа использованием в качестве конденсирующего агента более доступных симметричных карбонатов пентагалогенфенолов Формулы II, обеспечивающий охрану окружающей среды благодаря простому отделе- нию конденсирующего реагента от продукта реакции экстракцией из водного раствора органическим растворителем.
Осуществление предлагаемого способа позволяет повысить выход гликопептидов на 10-25% и упростить процесс их получения за счет уменьшения его продолжительности с 28 ч по способу-прототипу до 5-10 ч и сокращении числа хроматографических очного.
Формула изобретения
Способ получения гликопептидов общей формулы I -г
С1ЦОН- ОЦОН
НО
ИНАс ОШе СНЈН-Ш-Ш
где п-1;
NHR - остаток аминокислоты или пепти- да формулы
LAIa-Dlglu, LAIa-Dlgln или LAIa. взаимодействием N-ацетиламиносахара общей формулы II
Н
СН,ОН
СНЛН 1 О-
frvtf
NHAc 0 NHAe . . СН,СНСООН
где п-1 или 2,
с защищенной аминокислотой или пепти- дом в органическом растворителе в присутствии конденсирующего агента и органического основания при 0-20°С с отщеплением защитных групп и хроматогра- фической очисткой целевого продукта, отличающийся тем, что, с целью повышения выхода и упрощения процесса, в качестве конденсирующего агента используют симметричные карбонаты пентагалогенфенолов формулы III
30
35
где а) х - F; б)х-С1, а в качестве N-ацетиламиносахара - непосредственно N-ацетиламиносахар или его соль с органическим основанием и при молярном соотношении N-ацетиламиносахар или его соли: симметричный карбонат пен- тагалогенфенола : защищенная аминокислота или пептид равном ,2)1-1,2), при этом отщепление защитных групп ведут непосредственно после взаимодействия.
Соединение 11 предварительно переводили в соль с N-метилморфолином.


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ N-АЦЕТИЛГЛЮКОЗАМИНИЛ-N-АЦЕТИЛМУРАМИЛ-L-АЛАНИЛ-D-ГЛУТАМИНОВОЙ КИСЛОТЫ | 2015 |
|
RU2573991C1 |
| ФУЛЛЕРЕНОВОЕ ПРОИЗВОДНОЕ ГЛИКОПЕПТИДА, ОБЛАДАЮЩЕЕ АДЪЮВАНТНОЙ АКТИВНОСТЬЮ | 1997 |
|
RU2124022C1 |
| СПОСОБ ПОЛУЧЕНИЯ МУРАМИЛПЕПТИДОВ | 1995 |
|
RU2083588C1 |
| Способ получения N-ацетилмурамилпептидов | 1979 |
|
SU1326197A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕПТИДА δ СНА | 1995 |
|
RU2111972C1 |
| ЗАЩИЩЕННЫЕ ПЕПТИДЫ КАЛЬЦИТОНИНА | 2000 |
|
RU2193567C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕПТИДА δ- СНА | 1995 |
|
RU2111215C1 |
| Способ получения ариламидов N @ -защищенного аргинина | 1986 |
|
SU1432983A1 |
| СПОСОБ ПОЛУЧЕНИЯ БУСЕРЕЛИНА И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ ДЛЯ ЕГО ПОЛУЧЕНИЯ | 2010 |
|
RU2442791C1 |
| ПЕПТИДЫ, ОБЛАДАЮЩИЕ РЕГЕНЕРАТИВНО-РЕПАРАТИВНЫМ ДЕЙСТВИЕМ | 1994 |
|
RU2065445C1 |
Изобретение касается гликопептидов. в частности получения соединений общей ф- лы: СН,ОН «v. НО NHAc UNHAc CHjCH-СЮЬШ Изобретение относится к синтезу гликопептидов, которые могут найти применение в медицине, иммунологии и ветеринарии в качестве иммуномодуляторов. Цель изобретения - повышение выхода и упрощение процесса. На чертеже представлена диаграмма, поясняющая способ. Пример 1. Получение М-ацетил- глюкозаминил- 1 -4)-м -ацетилмура- мил-(/9 1-4)-М-ацетилглюкозаминил- (ft где л 1 или 2; NHR - остаток аминокислоты или пептида ф-лы L-Ala-Dei-Glu;L-Ala-Del-Gln или L-Ala, применяемых в иммунологии и ветеринарии в качестве иммуномодуляторов. Цель - повышение выхода целевого продукта и упрощение процесса. Его ведут реакцией N-ацетилсахара (или его соли с органическим основанием) с защищенной аминокислотой или пептидом в присутствии конденсирующего агента - акпентафторфе- нилкарбоната или ди(4-хлор-2,3.5,6-тетрах- лорфенил)карбоната при их молярном соотношении (М,3):(1-1.2):1 при 0-20°С с последующим отщеплением защитных групп и хроматографической очисткой целевого продукта. Конденсацию ведут в присутствии основания в среде растворителя (циметилформамида). Эти условия позволяют использовать более доступные вещества, обеспечивают лучшую экологию процесса, повышают выход целевого продукта на 10-25%, снижают продолжительность процесса с 28 до 5-10 ч и сокращают число хроматографических очисток. 1 табл., 1 ил. 1-4)-м -ацетилмурамил-1-аланил-0-изо- глутаминовой кислоты (IV). 9,74 г (10 мМ) тетрасахарида II. () растворяют в 25,0 мл перегнанного диме- тилформамида, добавляют 4 мл М-метил- морфолина, перемешивают 10-15 мин и выливают раствор в 200 мл этилацетата. Выпавший осадок отфильтровывают, промывают 4x50 мл этилацетата, 2x50 мл гексана, высушивают и получают 11,65 г (99%) М-ме- тилморфолиниеаой соли тетрасахарида (V). ч| О СП W о СА
V5
СОК
80 90 100tto ep ppcxtfw
| Биоорганическая химия, 1981, ТЭ, № 12 | |||
| с | |||
| Зрительная с переменным увеличением труба для самолетов | 1924 |
|
SU1813A1 |
Авторы
Даты
1992-01-15—Публикация
1987-09-01—Подача