Изобретение относится к новому классу гетероциклических соединений - ди-{фура- зано 314:51611,4 диоксино} 2,3-Ь; 5, разину формулы
я о к о к
s у Ч
°vW Г °
о-У
(I)
и может быть применено в качестве комплексообразующего реагента, например, в аналитической химии.
Ди-{фуразано 3,4:5,611,4 дмоксиноЯ2, 3-Ь: 5.6-е пиразин (I) является представителем соединений с одновременной последовательностью атомов и связей в аннелиро- ванной пентациклической системе, включающей два фуразановых, два диокси- новых и пиразиновый циклы.
Известны соединения, в которых фура- зановый цикл аннелирован с пиразиновым; такие соединения получают конденсаций 3,4-диаминофуразана с о. -дикарбонильны- ми соединениями
т
о 1 2-f°TR ин
N
R
Н
N О I 1
сл
00
о
Ю
Олммко способом нельзя полу- и f ь Щ-.МУНОНИЯ формулы (I). так как ом позволяет сi-iи гсзиоовать лишь соединения, в кото рыл фупа амоиый цикл непосредственно сп з-ч и с пи рази новым.
1/1 з я е с т н ы соединения, о к о т о р к-: х п и р а з и н о в ы и ц и к л а н н е л и р о в а н с диоксинов ь; м , и способ их получения, заключающийся во взаимодействии 2,3,5,6-тетрахлорпиразина с 0-ди- г и д р о к с и б е н з о л о м в п р и су т с т в и и основания, приводящего к образованию 2.3-дихлор-р-бензодиокс,,3 о ПИра-- ЗИНар
HCux ЯаОКсш ж
сние
С1,-ЛГС НСО-ч BOOK с,
I
С С Щ
С1
К О
ПД А Д
Ci N о
Гфоведен.ие реакции в ДМ ФА (при 78°С) или ДМСО (при 80- 106°С) также при- родит к образованию целевого продукта с хорошим выходом.
В аналогичных условиях реакция с 3,4- дигидроксифуразаном не приводит к получению соединения (I).
Цель изобретения - новая гетероцик20
ОН ,Br,3,HS04l
лическая система, включающая в свои со став два фуразановых. два диоксиновых и пиразинос ый цикл, аннелированных в единую систему, и разработка способ ее получения.
Поставленная цель достигается новым соединением - ди-{фуразано 3,4:5,, оксино} 2.3- о: 5,6-е пиразином формулы ()-. имеющим строение конденсированного пентэциклического соединения, не содержащего заместителей, и способом его пол- учения, заключающимся во взаимодействии 3.4-дигидроксиФуразэна (II) с солью тетра- алкиламмония в присутствии гидроокиси натрия в время с последующей обработкой образующейся при этом бис-тетрэалкилам- мониевой соли (III) с тетрахлорпиразииом (IV) в растворе абсолютного ацетонитрила при 40--82°С и молярном соотношении (/):(н 1:(1,1-1.9)
АуОН .,+NQOH
J- .V
(АШ4)
С1 ,С1
аД Д-И-е
,-г 2-33% от теор. в
:.гм Ч оифу разам. Максима л . достигается при соот5
0
ношении (IV);(I); 1:1,4 температуре процесса ПО С, времени 1 ч и использовании в качестве тетраалкиламмониевых солей тет- рябучиламмоний гидросульфата и триэтил- бен зил аммоний хлорида.
Прогзедение реакции (Н) с (IV) при температурах ниже 50°С и выше 60°С приводит к снижению выхода (I) (см. табл.1). Так. при температуре ниже 40°С реакция протекает очень медленно и продукт образуется в следовых количествах. Повышение температуры выше 80°С приводит к снижению выхода целевого продукта за счет протекания по- Ьочиых процессов.
Для получения (I) важно соотношение и о - од н ы х с о е д и н е н и и.
Так. при соотношении (iV):(l) 1:1,1 единственным продуктом реакции является соединение
Ґ О Я „.
ji
1гч Д
5
0
5 0 5
0
5
При соотношении (IV):(H) 1:1,9 образования (1) также не наблюдается; получается сложная смесь продуктов не установленного строения.
(1 р и м е р 1. К раствору 0.51 г (5 ммоль) 3 Фдигидроксифуразана (П) и 3,4 г (10 ммоль) гидросульфата тетрабутиламмония в 20 мл воды добавляют раствор 0,7 г (20 ммоль) МаОН в 5 мл воды, разбавляют 50 мл спирта и охлаждают до 10°С. Осадок Na2SO отфильтровывают и промывают спиртом. Фильтрат упаривают досуха в вакууме. Оставшееся масло растворяют в 30 мл абс. ацетонитрила и фильтруют от остатков 1ч.). Фильтрат упаривают досуха. Оставшееся масло сушат в вакууме (50°С/1 мм. рт.ст.). Получают 3,3 г ди-тетра- бутиламмониевой соли в виде густого жел- того масла. Полученную соль растворяют в 40 мл збс. ацетонитрила, добавляют 0,78 г (3,57-ммоль) 2,3,5,6-тетрахлорпиразина (IV) и перемешивают при 60°С в течение 1 ч. Реакционную смесь упаривают на роторе досуха, остаток заливают 20 мл воды, выпавший осадок отфильтровывают, промывают водой и высушивают. Остаток перемешивают 10 мин в 50 мл смеси ССЦ 1;1, сырой продукт отфильтровывают, промывают и сушат.
Получают 0,23 г (I) (33% на дигидрокси- фуразан)т.пл. 154-155°С(из СНСЬ).
Масс-спектр, т/г. 276 (М4), 246 (М+ - N0). 208 (М+- 68), 202, 199,
Для CeNeOs М+ -- 276.
ИК-спектр(КВМ), см-1: 1570, 1480, 1400, 1860, 1200, 1035, 985.
Найдено, %: С 34,67; N 30,07.
CsNeOe
Вычислено, %: М 34,80; N 30,44.
П p и м е р 2-16. Процесс ведут аналогично примеру 1,
Условия и результаты опытов приведены в табл.1.
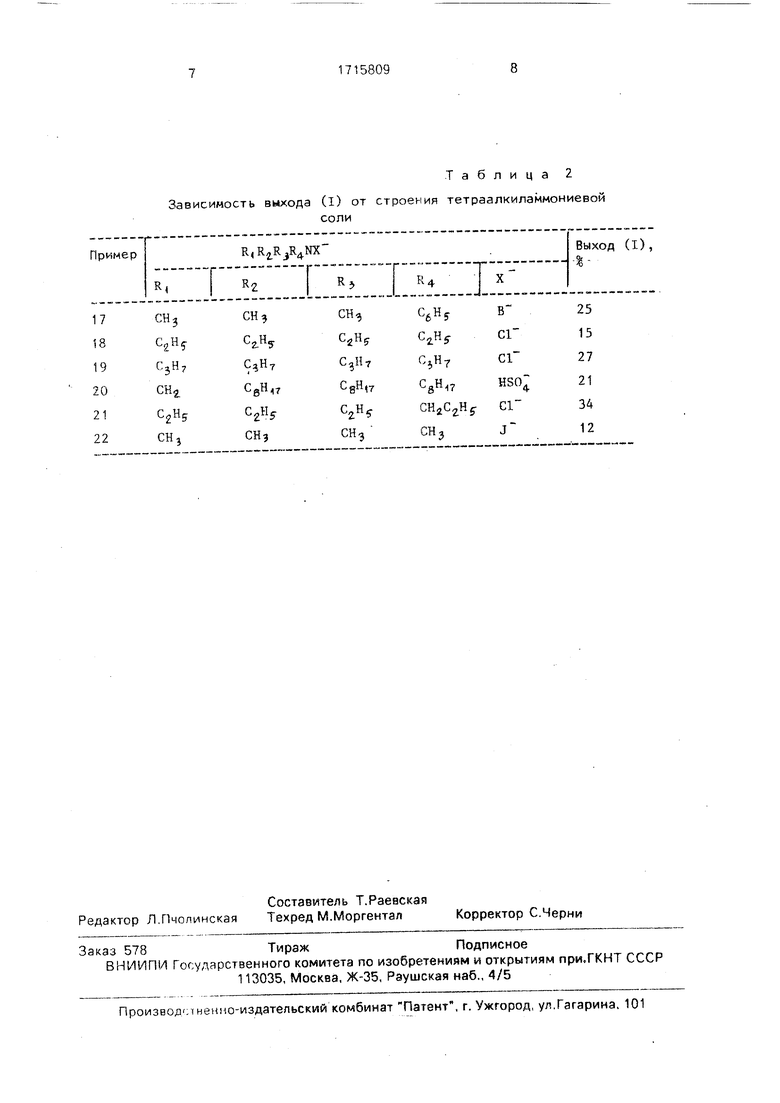
Примеры 17-22. Процесс ведут аналогично примеру 1 при использовании различных тетраалкиаммониевых солей..
Выходы вещества (I) приведены в табл.2.
Таким .образом, применения тетраалки- ламмониевых солей 3,4-дигидроксифураза- на (II) и проведения процесса в ацетонитриле при нагревании при соотношении (IV):(II) 1:(1,1:1,9) обеспечивает получение новой пентэциклической гетеро- системы - ди-{фуразано 3,4:5,,4 диокси- ,3-Ь; 5,6-е пиразин.
Формула изобретения
1. Ди-{фуразано 3,4:5,,4 диокси- ноН2,3-Ь; 5,6-е пиразин формулы
КОКОН
111 Х
N О N
2 Способ получения ди-{фураза- ,4:5,,4 диоксино} 2,3-Ь; 5,6-е пиразина, отличающийс я тем, что 3,4-дигидроксифуразан подвергают взаимодействию с солью тетраалкиламмония в присутствии гидроокиси натрия в воде с последующей обработкой образующейся при этом ди-тетразлкиламмониевой соли 3,4-ди- гидроксифуразана тетрахлорпиразином в растворе абсолютного ацетонитрила при 40-82°С и соотношении тетрахлорпира- зин - 3,4-дигидроксифураэан 1:(1,1-1,9).
3. Способ по п.2, отличающийся тем, что, с целью повышения выхода, процесс ведут при соотношении тетрахлорпи- разин - 3,4-дигидроксифуразан 1:1,4 при 60°С, в качестве тетраалкиаммониевой соли используют тетрабутиламмония гидросульфат или триэтилбензиламмония хлорид.


| название | год | авторы | номер документа |
|---|---|---|---|
| 2,3-Дихлорфуразано[3,4:5,6][1,4]диоксино[2,3-в]пиразин и способ его получения | 1990 |
|
SU1715808A1 |
| Способ получения 2,5-дигидро-1,2-тиазино (5,6-в) индол-3-карбоксамид-1,1-диоксидов или их солей | 1978 |
|
SU654173A3 |
| ПРОИЗВОДНЫЕ ТЕТРАФУРАЗАНО[3,4-b:3',4'-f:3",4"-j:3'",4'"-N][1,4,5,8,9,12,13,16]ОКТААЗАБ ИЦИКЛО[14.2.2]ЭЙКОЗА-4,8,12-ТРИЕНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2000 |
|
RU2167161C1 |
| Замещенные (циано-NNO-азокси)фуразаны и способ их получения | 2021 |
|
RU2775006C1 |
| Соли 3-амино-4-(1Н-тетразол-5-ил-NNO-азокси)фуразана и способы их получения | 2023 |
|
RU2804394C1 |
| ПРОИЗВОДНЫЕ 5,6-ДИГИДРОПИРОНА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1994 |
|
RU2140917C1 |
| СПИРО-5,6-ДИГИДРО-4Н-2,3,5,10В-ТЕТРААЗА-БЕНЗО[Е]АЗУЛЕНЫ | 2009 |
|
RU2514429C2 |
| Замещенные [(3-нитро-1Н-1,2,4-триазол-1-ил)-NNO-азокси]фуразаны и способ их получения | 2020 |
|
RU2747110C1 |
| Замещенные [(3,4-динитро-1H-пиразол-1-ил)-NNO-азокси]фуразаны и способ их получения | 2020 |
|
RU2756321C1 |
| Способ получения производных нафтиридина или их солей | 1975 |
|
SU589916A3 |
Изобретение касается гетероциклических веществ, в частности получения ди-{фу- разано 3,4:5,,4 диоксино} 2,3-Ь; 5,6-е пиразина, который может быть использован в качестве комплексообразующего реагента, например в аналитической химии. Цель - создание нового способа получения новой гетероциклической системы. Синтез ведут реакцией 3,4-дигидроксифуразана с солью тетраалкиламмония (лучше с гид- росу ль фа том тетрабутиламмония-или хлоридом три этилбензиламмонием) с последующей обработкой полученной соли тетрахлорпиразином, взятым в 1,1-1,9-мо- лярном избытке по отношению к 3,4-дигид- рофуразану (лучше в 1,4-молярном избытке) при 40-82°С (лучше при 60°С) в среде абсолютного а-цетонитрила. Выход 33%, т.пл. 154-Т55°С, брутто-ф-ла CeN eOe. 2 с. и 1 з.п. ф-лы, 2 табл, сл С
Таблица 1
/ ч «
Влияние соотношения реагентов и температуры на выход (L)
Примечани я.Для всех опытов содержание вещества II - 5 ммоль;
Bu4NHS04 10 ммоль; NaOH - 20 ммоль. При увеличении времени содержание.(I) в реакционной смеси не увеличивается. Температура кипения ацетонитрила.
Таблица 2
Зависимость выхода (I) от строения тетраалкиламмониевой
соли
сн3
С3Н7 С%
С2% СИ
СНз
С2.% С,Н7
с2%
СН9
С6Н,
сгну
С5Н7
С8НН7
В С1
с Г
HSO
CH2C2Hf С1
сн2515 27
21 34 12
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Прибор для периодического прерывания электрической цепи в случае ее перегрузки | 1921 |
|
SU260A1 |
| Патент США ISfc 3746707, кл | |||
| Прибор для периодического прерывания электрической цепи в случае ее перегрузки | 1921 |
|
SU260A1 |
| ХГС, 1981 | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| .ХГС | |||
| Приспособление для изготовления в грунте бетонных свай с употреблением обсадных труб | 1915 |
|
SU1981A1 |
| Обогреваемый отработавшими газами карбюратор для двигателей внутреннего горения | 1921 |
|
SU321A1 |
| Органическая химия | |||
| - .М,; с | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| , с | |||
| Кард-машина для обработки льняных очесов | 1924 |
|
SU1155A1 |
| Марч Дж | |||
| Мир, 1987, т.З , ХГС, 1984, | |||
Авторы
Даты
1992-02-28—Публикация
1990-06-29—Подача