Изобретение относится к биотехнологии и может быть использовано для определения нитрифицирующей активности ила в процессе биологической очистки сточных вод.
Цель изобретения - упрощение и ускорение способа.
Способ осуществляют следующим образом.
Тщательно перемешанную иловую суспензию помещают в две пробирки. Первую (контрольную) пробирку помещают на 15 мин в кипящую водяную баню, затем обе
пробирки центрифугируют для отделения ила от надиловой жидкости. К полученному осадку добавляют смесь фосфатного буфера с гидроксиламином в соотношении 10:(1.0- 1.2). а затем приливают трифенилтетразо- лий хлористый. Полученную суспензию инкубируют в течение 10-60 мин при т1 30°С. Экстракцию образовавшегося формазана осуществляют этанолом. После центрифугирования надосадочную жидкость колометрируют и по калибровочной кривой определяют дегидрогеназную активность, выраженную в мкг формазана, образуемого
Ч
СО
о
со со
1 г беззольного вещества биомассы в мин. Количество нитрифицирующих бактерий 1 фазы определяют по формуле
In г--И А
.зТ
где С - количество нитрифицирующих бактерий, мл/кг беззольного вещества ила;
А - дегидрогеназная активность, мкг формазана/г беззольного вещества, мин.
П р и м е р 1. Иловую суспензию в количестве 5 мл (концентрация ила по бензольному веществу 0,16-1,5 г/л) помещали в часть пробирок и в течение 3 мин центрифугировали при 2 тыс, об./мин. Затем надсадочную жидкость сливали. К полученному осадку приливали 5,5 мл смеси М/15 фосфатного буфера с 5%-ным раствором гидроксиламина. Объемное соотношение фосфатного буфера к гидроксиламину составило: в первой пробирке: 10:0,4; во второй: 10:1,0; в третьей: 10:1,1; в четвертой: 10:1,2 и в пятой: 10:1,6. рН смеси доводили до .значения 8,0 раствором NaOH. К полученной в каждой из пяти пробирок суспензии приливали 1 мл 10%-ного раствора трифенилтетразолия хлористого, перемешивали и помещали пробирки в водяную баню при т° 30°С.
Инкубацию вели в течение 35 мин. Пробирки центрифугировали, надосадочную жидкость сливали, а к осадку приливали 5 мл этанола для экстракции образовавшегося формазана. Содержимое пробирок перемешивали, встряхивали, после этого пробирки вновь центрифугировали в течение 3 мин и надосадочную жидкость колори- метрировали в кюветах толщиной 0,5 см с зеленым светофильтром.
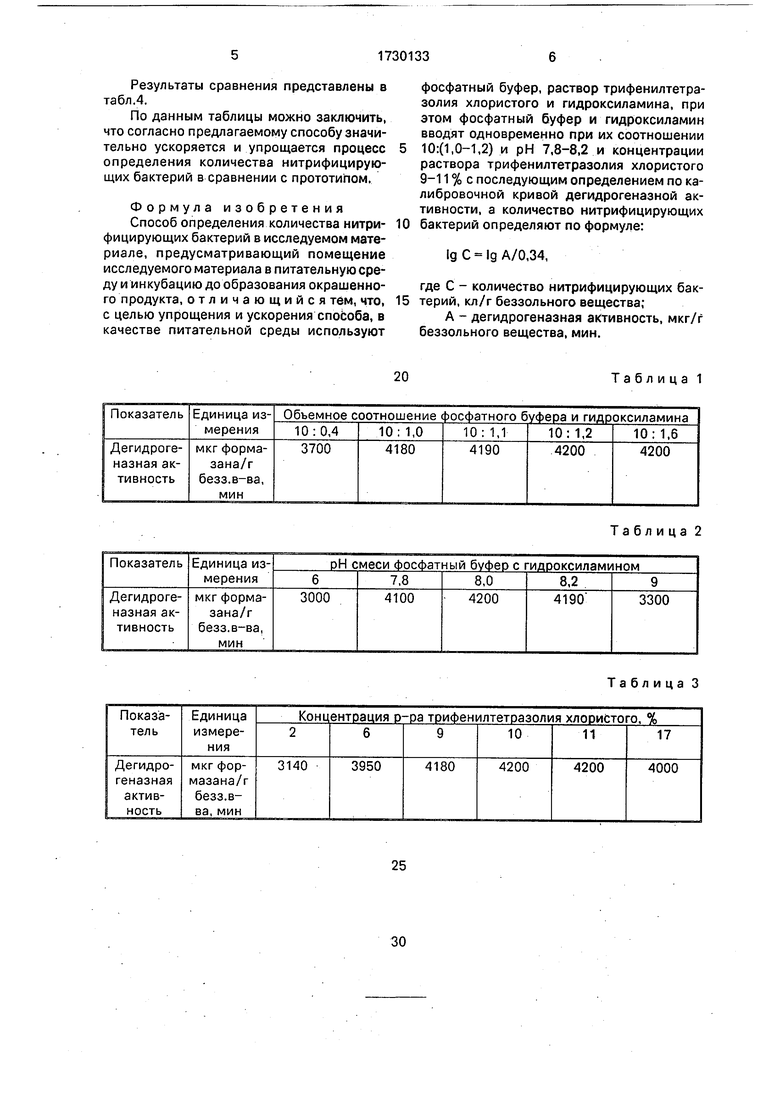
Затем по результатам определения относительной плотности ряда спиртовых растворов формазана с концентрацией от 1 до 25 мкг/мл, строили калибровочную кривую, откладывая по оси абсцисс концентрации растворов формазана. а по оси ординат - значения экстинкций этих растворов. По калибровочной кривой определяли количество выделившегося формазана. Дегидрогеназную активность выражают в мкг восстановленного формазана, обазованного 1 г беззольного вещества ила в 1 мин (см. табл.1).
Результаты опыта представлены в табл.1.
Как видно из табл.1, с увеличением количества гидроксиламина увеличивается количество выделившегося формазана. В четвертой и шестой пробирках при отношении фосфатного буфера к гидроксиламину,
0
5
равном 10:1,0 и 10:1,6, соответственно, количество накапливаемого формазана практически не меняется, т.е. становится стабильным. Это свидетельствует о том, что в этом интервале взятого соотношения компонентов наступает зона устойчивой реакции. Поэтому дальнейшее увеличение количества гидроксиламина нецелесообразно. Таким образом, из приведенных данных видно, что соотношением, при котором достигается поставленная цель, является интервал 10:(1,0-1,2). Количество нитрифицирующих бактерий определяли по формуле
--ЈЈ- «
Предлагаемая формула была проверена
на большом числе объектов и показала вы: сокую достоверность. Коэффициент корре- ляции составляет от 0,84 до 0,92 в зависимости от биоценоза. Нитрифицирующая способность активного ила является
низкой при IgC 7, наблюдаемая при этом скорость окисления азота аммонийного 2 мг/г безз.ч; средняя при 7 |дС 9 (скорость окисления азота аммонийного составляет 2-9 мг/безз.ч.); высокая при
IgC 9 (скорость окисления азота аммонийного составляет 9 мг/г безз.ч).
П р и м е р 2. Определение значения рН смеси фосфатного буфера с гидроксилами- ном. при котором достигается максимальное выделение формазана, проводили в условиях, аналогичных примеру 1. Соотношение фосфатного буфера и гидроксиламина было оптимальным и составило 10:1,1. Результаты опыта приведены в табл.2.
Как видно из табл.2, максимальное количество формазана выделилось при значениях рН смеси, равных 7,8-8,2.
П р и м е р 3. Определение интервала концентраций раствора трифенилтетразолия хлористого, при котором достигается поставленная цель, проводили в условиях, аналогичных примеру 1. Соотношение фосфатного буфера и гидроксиламина составля- ло 10:1,1, рН смеси 8.
Результаты опыта приведены в табл.3.
Из табл.3 видно, что эффект достигается при значениях концентрации трифенилтетразолия хлористого в воде, равных 9-11%, т.е. в этом интервале находится зона устойчивой реакции. Дальнейшее увеличение концентрации трифенилтетразолия хлористого в воде нецелесообразно.
Предлагаемый способ сравнивали с прототопим.
Результаты сравнения представлены в табл.4.
По данным таблицы можно заключить, что согласно предлагаемому способу значительно ускоряется и упрощается процесс определения количества нитрифицирующих бактерий в сравнении с прототипом.
Формула изобретения Способ определения количества нитрифицирующих бактерий в исследуемом материале, предусматривающий помещение исследуемого материала в питательную среду и инкубацию до образования окрашенного продукта, отличающийся тем, что, с целью упрощения и ускорения способа, в качестве питательной среды используют
фосфатный буфер, раствор трифенилтетра- золия хлористого и гидроксиламина, при этом фосфатный буфер и гидроксиламин вводят одновременно при их соотношении
10:(1,0-1,2) и рН 7,8-8,2 и концентрации раствора трифенилтетразолия хлористого 9-11 % с последующим определением по калибровочной кривой дегидрогеназной активности, а количество нитрифицирующих
бактерий определяют по формуле:
Ig С Ig А/0,34,
где С - количество нитрифицирующих бак- терий, кл/г беззольного вещества;
А - дегидрогеназная активность, мкг/г беззольного вещества, мин.


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения токсичности сточных вод | 1981 |
|
SU1008245A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АКТИВНОСТИ ФЕРМЕНТА СУКЦИНАТДЕГИДРОГЕНАЗЫ В КРОВИ | 2002 |
|
RU2236011C2 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ДЕГИДРОГЕНАЗНОЙ АКТИВНОСТИ МИКРООРГАНИЗМОВ | 2011 |
|
RU2476598C2 |
| Способ контроля качества биохимической очистки сточных вод | 1976 |
|
SU654548A1 |
| СПОСОБ СРАВНИТЕЛЬНОЙ ОЦЕНКИ СТОЙКОСТИ СТАЛЕЙ К МИКРОБИОЛОГИЧЕСКОЙ КОРРОЗИИ | 2009 |
|
RU2393459C1 |
| Способ подготовки сточных вод для биологической очистки активным илом | 1984 |
|
SU1265152A1 |
| ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ МЫШЕЧНЫХ ДИСТОНИЙ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2002 |
|
RU2206337C1 |
| Способ оценки гемолитического действия полимеров, полимерных материалов и изделий из них ин витро в статических условиях | 2023 |
|
RU2818010C1 |
| Способ определения бактерицидности производственных сточных вод | 1980 |
|
SU934323A1 |
| Способ определения антистафилококковой активности препарата | 1988 |
|
SU1571069A1 |
Изобретение относится к технологическому контролю состояния ила в очистных сооружениях и биологической очистке сточных вод и может быть использовано для оперативной оценки его нитрифицирующей активности, т.е. способности ила окислять аммиак и азотистую кислоту. Цель изобретения - упрощение и ускорение способа. Тщательно перемешанную иловую суспензию помещают в пробирки, центрифугируют для отделения ила от надиловой жидкости. К полученному осадку добавляют смесь фосфатного буфера с гидроксилами- ном в соотношении 10:(1,0-1,2), рН смеси составляет 7,8-8,2. Затем приливают 1 мл хлористого трифенилтетразолия, концентрация которого составляет 9-11 %. Полученную суспензию инкубируют 10-60 мин при 30°С. Экстракцию образовавшегося форма- зана осуществляют этанолом. После центрифугирования надосадочную жидкость колориметрируют и по калибровочной кривой определяют дегидрогеназную активность, выраженную в мкг восстановленного формазана. Количество нитрифицирующих бактерий определяют по формуле Ig С Ig А/0.34, где С - количество нитрифицирующих бактерий; А - дегидрогеназная активность. 4 табл. (/ С
20
Таблица 1
Таблица 2
Таблица 3
Показатели
Предлагаемый способ
Технологические операии и время их проведения, ч -стерилизация посуды, инструментов
-разведение
-помещение в питательную среду
-центрифугирование
-инкубация
-оценка цветной реакции
-обработка результатов ИТОГО:
Таблица 4
Прототип
тсутствует тсутствует
0,02
0,1 0,68
0,1
0,1 1
4 0,3
0,5
Отсутствует 720 0,1 0,1 725
| SorianoS | |||
| Walker N | |||
| Isolation of ammonia oxiding bacteria. | |||
| Appl, Bacterial, 1969, 31, Ns 3, p.493-497. |
Авторы
Даты
1992-04-30—Публикация
1990-05-24—Подача