Изобретение относится к получению солей многоосновных оксикислот, в частности к усовершенствованному способу получения тартратов щелочных металлов или их смесей, и может быть использовано в процессах их синтеза в промышленном масштабе. Целевые продукты находят применение в электротехнике и в качестве стабилизаторов пищевых продуктов.
Цель изобретения - повышение выхода целевого продукта и интенсификация процесса за счет сокращения времени синтеза.
Поставленная цель достигаэтся тем, что в способе получения тартратов щелочных
металлов или их смесей (а также гидротарт- ратов как частного случая тартратов) взаимодействием малеинового ангидрида с пероксидом водорода в присутствии щелочи, фольфрамата натрия, винной кислоты и гидрохинона или фосфорного соединения щелочного металла, выбранного из группы, включающей фосфат или пиро-, или гидро-, или дигидрофосфат щелочного металла при молярном соотношении малеинового ангидрида, пероксида водорода, щелочи, вольфрамата натрия, винной кислоты, фосфорного соединения щелочного металла или гидрохинона, равном 1.0 : 1,0-1 2 1,000 N3 00 00 СП
XI
1,05:0,002-0,004:0,005-0,01 :0,0005-0,001, при 65-75° С в течение 4-5 ч с последующим повышением температуры до 80-100° С и одновременным введением в реакционную массу растворимой в воде соли железа (111) при молярном соотношении малеинового ангидрида и железа (III), равном 1,0 : 0,001- 0,005, и введением в реакционную массу после завершения реакции дополнительного количества щелочи при молярном соотношении щелочи м малеинового ангидрида, равном 0,002-1,0 : 1,0. Выделение и очистку целевого продукта ведут известными методами.
При уменьшении количества щелочи на первом этапе синтеза резко уменьшается скорость процесса. При увеличении же этого количества на первом этапе синтеза снижается выход и резко увеличивается продолжительность процесса. Уменьшение соотношения малеинового ангидрида, винной кислоты и фосфорного соединения или гидрохинона ведут к снижению выхода, увеличение же этих соотношений приводит к торможению реакции и увеличению времени процесса. Снижение соотношения малеинового ангидрида железа (lit) увеличивает продолжительность процесса и снижает выход, увеличение же не приводит к улучшению характеристик способа и может служить источником загрязнений. Уменьшение времени и температуры синтеза на первой стадии приводят к снижению выхода, увеличение времени не приводит к повышению выхода, а увеличение температуры его снижает. К снижению выхода приводит также выход за пределы температур на второй стадии синтеза или применение нерастворимой соли железа. Увеличение количества щелочи на последнем этапе синтеза экономически неоправдано, а уменьшение ведет к потерям целевого продукта на стадии выделения.,
Способ иллюстрируется следующим примерами.
Пример 1. В реактор с мешалкой внутренним обьемом 1 л заливают 280 мл воды, загружают 160 г малеинового ангидрида (1,63 моль), включают мешалку, доводя температуру до 70° С и при перемешивании добавляют 92 г (1,63 моль) КОН в 250 мл.воды, засыпают 1,4 г NaaWCM 2НзО (0,00424 моль) и начинают подавать 180 мл 30 % раствора Н202(1,75 моль), содержащего 1.83 г d, 1-винной кислоты и 0,147 г NaH2P04. Соотношение малеиновый ангидрид : H2U2 КОН : вольфрамат натрия : винная кислота : NaH2P04 1,0 : 1,07 : 1,0 : 0.0026 : 0,0075 : 0,00075. Время подачи 40 мин. По истечении 4,5 ч с момента начала
реакции температуру реакционной массы поднимают до 90° С, добавляют 0,978 г Рв2(504)з. Эквивалентное соотношение малеиновый ангидрид: Fe (III) 1 : 0,003. Реакцию ведут еще 2,5 ч. затем в полученную реакционную массу прибавляют 0,20 г КОН (молярное соотношение малеиновый ангидрид : КОН на последнем этапе составляет 1 : 0,002) при 45-50° С, упаривают ее под
вакуумом с остаточным давлением 35 мм рт. ст. до удельного веса 1.25 г/см3. Удельный вес измеряют ореометром. Затем раствор охлаждают до 10° С, при этом выпадают кристаллы гидротартрата калия. После кристаллизации кристаллы отфильтровывают от маточного раствора, промывают 2 раза по 10 мл холодной воды и сушат в вакууме при 100° С. выход гидротартрата калия за вычетом введенной в реакцию винной кислоты
81 % (250,5 г), Общее время синтеза 7 ч.
Примеры 1-37 введены в таблицу. Пример 38. Способ осуществляют по примеру 1, за исключением того, что на по
следнем этапе синтеза после завершения
реакции смесь охлаждают и прибавляют еще 50 % раствор КОН при соотношении малеиновый ангидрид : щелочь 1,0 : 1,0. В результате разделения по примеру 1 получают81 % (301,5 г) дикалиевой соли винной кислоты.
Пример 39. Способ ведут по примеру 2 и 38, за исключением того, что прибавляют NaOH. Получают 82 % динатриевой соли
винной кислоты (261,7 г).
Пример 40. Способ ведут по примеру 38, но прибавляют такое же количество NaOH. В результате получают 80 % (276,4 г) натрий-калиевой соли винной кислоты.
Пример 41. Способ осуществляют по
примеру 38, но прибавляют КОН при молярном соотношении на последнем этапе синтеза малеиновый ангидрид: КОН 1 : 0,5. В результате получают 276,4 г смеси калиевой
и дикалиевой соли винной кислоты (81 %), содержащей 125,4 г калиевой соли и 150,7 г дикалиевой соли.
Пример 42. Способ ведут по примеру 40, но прибавляют NaOH из расчета малеиновый ангидрид: NaOH на последнем этапе синтеза в соотношении равном 1 : 0,5. В результате получают 262,1 г и 138,3 г натрий-калиевой соли винной кислоты.
Пример 43. Способ осуществляют по
примеру 1. за исключением того, что на последнем этапе синтеза прибавляют не 0.20 г КОН, а 0,05 г КОН. В результате выход продукта после выделения падает до 64 %, причем продукт получается в виде эморфной комковатой массы, плохо подлежащей осушке.
Пример 44. Осуществляют синтез мононатриевой соли эпоксиянтэрной кислоты по известной модифицированной методике. Растворяют 1 моль малеинового ангидрида в 300 мл воды и добавляют 40 г NaOH в 100 мл воды. Затем в реакционную массу добавляют 6,6 г Na2WC 4 2H20, нагревают до 65° С и дозируют 1,2 моль 30 % H2U2 за 20 мин, после чего выдерживают 1,5 ч. Затем из раствора под вакуумом отгоняют 250 мл воды, остаток отделяют и сушат. Пол- fнают 136 г (95 %) мононатриевой соли эпок- сисукцината.
Полученный продукт делят на 3 равные части по 45,3 г. Первую часть смешивают с 200 мл воды и нагревают при 100° С 5 ч. Вторую часть смешивают с 200 мл воды и нагревают при 100° С 15 ч. Третью часть смешивают с 200 мл воды, добавляют 5 г Ре2(5См)з и нагревают при 100° С 5 ч, В результате гидролиза получают в первом случае 59% выход мононатриевой соли винной кислоты, во втором случае - 63 % выход, в третьем - 64 % выхода. Таким образом, данный пример иллюстрирует очень малую эффективность применения только соли железа при гидролизе, Суммарный выход продукта не превышает 61 % по обеим стадиям.
Пример 45. Способ осуществляют по примеру 1, но в реакционную массу не вводят ни фосфат, ни гидрохинон, ни винную кислоту.
Время реакции по обеим стадиям синтеза определяют по результатам анализа титриметрически (соль малеиновой кислоты на первой стадии синтеза) и фотокалоримет- рически (целевой продукт) по прекращению расходования исходного вещества и прекращению накопления конечного продукта.
В результате общее время синтеза за счет увеличения времени для обеих стадий составляет 15 ч, выход целевого продукта падает до 63 %. Таким образом, отсутствие указанных добавок не позволяет достичь цели изобретения даже в присутствии соединений железа на второй стадии синтеза.
П р и м е р ы 44 и 45 иллюстрируют неочевидный факт увеличения каталитической активности по обеим стадиям синтеза.
Как следует из таблицы и примеров 36- 40, 38-43, соблюдение заявленных условий позволяет повысить выход продукта до 74- 83 % и сократить общее время процесса до 6,0-11 ч (примеры 1 10. 12, 14, 15, 17, 19, 21-24, 26, 28. 30. 32, 34, 36-42). Снижение температурь и уполичение времени на первой стадии синюза (пример 11), повышение темперлтуры и ,и ныирние времени на
этой стадии (пример 13) снижает выход продукта. Применение нераство : мой соли железа (пример позволяет гокрэппк время и снижает выход продукта 5Уменьшение температуры нг. второй
стадии синтеза (пример 18) уврличиваег время процесса и снижает выход, увеличение же температуры (пример 20) снижает выход за счет осмоления. Снижение соотно0 шения малеиновый ангмдрид : винная кислота ( пример 25) снижает выход продукта. К такому же результату приводит повышение содержания винной кис/.оты (пример 27). Снижение содержания фосфорного со5 единения щелочного металла или гидрохинона (пример 29) уменьшает выход, а увеличение приводит, кроМетого, к увеличению продолжительности процесса (пример 31). Уменьшение содержания соли железа
0 (III) не позволяет увеличить выход (пример 33), а увеличение экономически не оправдано, так как не улучшает показатели процесса (пример 35).
Уменьшение количества щелочи на пео5 вом этапе синтеза (пример 36) приводит к резкому замедлению скорости оеакции на первой стадии, что увеличивает продолжительность всего процесса. Увеличение же этого количества (пример 37) резко умень0 шает скорость на второй стадии и снижает выход продукта.
Уменьшение количества щелочи на последнем этапе синтеза снижает выход и ухудшает качество продукта (пример 43).
5 Таким образом, только совокупность всех заявленных условий позволяет повысить выход продукта и интенсифицировать процесс за счетснижения времени реакции. Дополнительным преимуществом спо0 соба является возможность получать по же- ланию как чистые тартраты или гидротартраты, так и их смеси, в том числе и дойные соли, например калий-натриевую соль. Это легко регулируется количество
5 введенной щелочи на втором этапе синтеза
Формула изобретения Способ получения тартратов щелочных металлов или их смесей путем взаимодейст0 вия малеинового ангидрида с пероксидом водорода в водном растворе в присутствии щелочи и фольфрамета натрия в качестве катализатора при ступенчатом повышении температуры и последующим выделением
5 целевого продукта, отличающийся тем. что, с целью повышения выхода целевого продукта и интенсификации процесса катализатор дополнительно содерхит винную кислоту и гидрохинон или фосфорсодержащее соединение щелочного метялга РЫбранное из группы : фосфат, пиро-, гидро-, дигидрофосфат щелочного металла, и процесс ведут при молярном соотношении малеиновый ангидрид: пероксид водооопа ; вольфрамат натрия :щелочь : винная кислота : гидрохинон или фосфорсодержащее соединение щелочного металла, равном 1 : 1,0-1,2 : 0,002-0,004 : 1,0-1,05 : 0,005-0,01 : ОДЮ05-0.001, при температуре 65-75° С в течение 4-5 ч с последующим повышением
температуры до 80-100° С и одновременным введением в реакционную массу растворимой в воде соли железа (III) при молярном соотношении малеиновый ангидрид : соль железа (III), равном 1 : 0,001- 0,005, и добавлением в реакционную массу после завершения реакции дополнительного количества щелочи при молярном соотношении малеиновый ангидрид : щелочь 1 : 0.002-1,0.


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ СИНТЕЗА 1,6-ГЕКСАМЕТИЛЕНДИАМИН-N, N'-ДИЯНТАРНОЙ КИСЛОТЫ | 2013 |
|
RU2527271C1 |
| СПОСОБ ПОЛУЧЕНИЯ СОЛЕЙ МЕДИ (II) С ДИКАРБОНОВЫМИ КИСЛОТАМИ | 2004 |
|
RU2256648C1 |
| СПОСОБ ПОЛУЧЕНИЯ МЕЛКОКРИСТАЛЛИЧЕСКОЙ ФОРМЫ ЦИС-2,3-ЭПОКСИСУКЦИНАТА КАЛЬЦИЯ | 2020 |
|
RU2762326C2 |
| СПОСОБ ПОЛУЧЕНИЯ КРИСТАЛЛИЧЕСКОЙ ФОРМЫ ЦИС-2,3-ЭПОКСИСУКЦИНАТА КАЛЬЦИЯ | 2020 |
|
RU2763329C2 |
| СПОСОБ ПОЛУЧЕНИЯ КРИСТАЛЛИЧЕСКОЙ ФОРМЫ ЦИС-2,3-ЭПОКСИСУКЦИНАТА КАЛЬЦИЯ | 2020 |
|
RU2741870C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОМЕЖУТОЧНЫХ ПРОДУКТОВ ДЛЯ СИНТЕЗА АНАЭРОБНЫХ ГЕРМЕТИКОВ | 1986 |
|
SU1413912A1 |
| КРИСТАЛЛИЧЕСКАЯ ФОРМА ЭПОКСИСУКЦИНАТА КАЛЬЦИЯ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ ДЛЯ ПОЛУЧЕНИЯ ВИННОЙ КИСЛОТЫ | 2020 |
|
RU2787475C2 |
| СПОСОБ ПОЛУЧЕНИЯ КРИСТАЛЛИЧЕСКОЙ ФОРМЫ ЦИС-2,3-ЭПОКСИСУКЦИНАТА КАЛЬЦИЯ | 2020 |
|
RU2757039C2 |
| СЛОЖНЫЙ КАРБОКСИЛАТНЫЙ ЭФИР ПОЛИСАХАРИДА | 2015 |
|
RU2654031C2 |
| СПОСОБ ПОЛУЧЕНИЯ КРИСТАЛЛИЧЕСКОЙ ФОРМЫ ЦИС-2,3-ЭПОКСИСУКЦИНАТА КАЛЬЦИЯ | 2020 |
|
RU2756956C2 |
Сущность изобретения: Продукт - гид- ротартрат БФ С4 Н6 05 Li, или гидротартрат натрия БФ С4 Н6 05Na, или гидротартрат калия БФ С4 Н605К. Реагент 1: малеиновый ангидрид. Реагент 2: 15 %-ный раствор гид- роксида щелочного металла в воде. Реагент 3: 30 %-ный водный раствор пероксида водорода. Условия реакции: в присутствии вольфрамата натрия, виннЪй кислоты БФ 04 Р4 06 и гидрохинона или фосфорсодержащего соединения щелочного металла при молярном соотношении малеиновый ангидрид : пероксид водорода : воль- фрамат натрия : щелочь : винная кислота : гидрохинон или фосфорсодержащее соединение щелочного металла 1 :1.0-1,2 : 0,002- 0,004 : 1,0-1,05 : 0,005-0,01 : 0,0005-0,001 при 65-75° С с последующим повышением температуры до 80-100° С и одновременным введением в реакционную массу после завершения реакции дополнительного количества при молярном соотношении малеиновый ангидрид : щелочь 1 : 0,002-1,0. 1 табл. (Л С
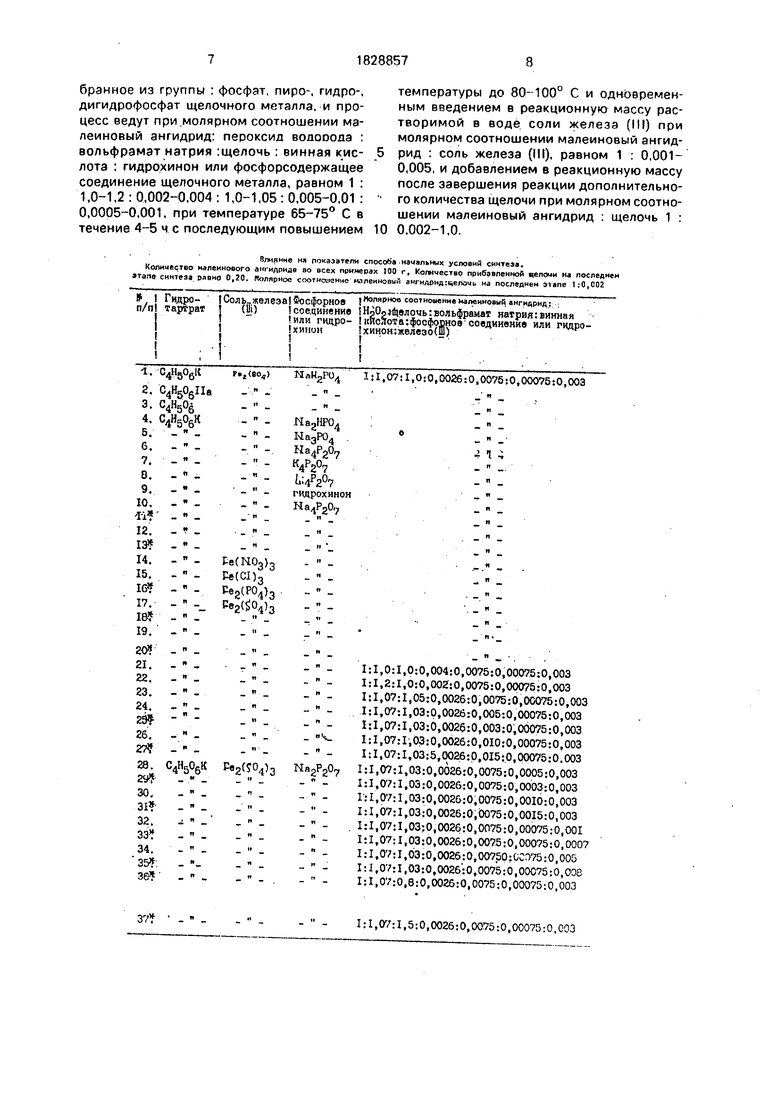
Влияние на показатели способа начальных условий синтеза.
Количество малейнового ангидриде во всех примерах 100 г. Количество прибавленной щелочи на последнем этапе синтеза равно 0,20. Р олярнос соотношение малеиновый а «гидрид гцелочь на последнем 1;0,С02
37
1:1,07:1,5:0,0026:0,0075:0,00075:0,003
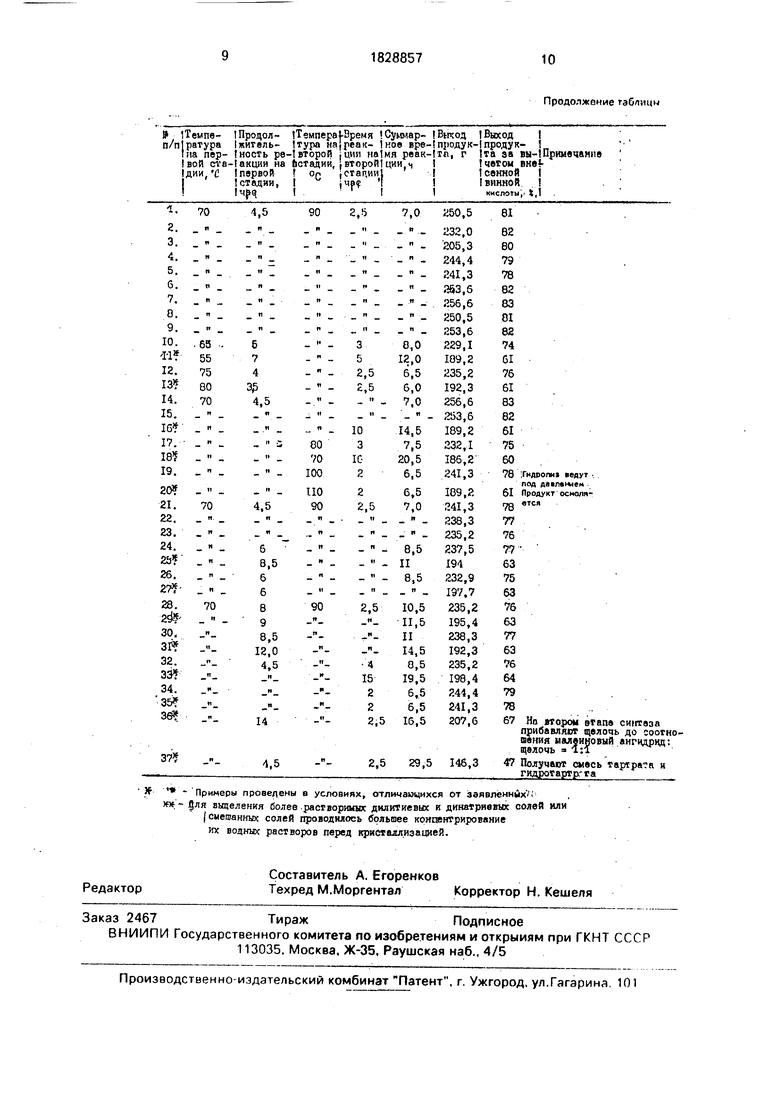
Продолжение таблиц
| Выписка из постоянного технологического регламента производства Калия d, I- гидротартрата квалификации чистый цеха N 1 Ереванского завода химических реактивов. |
Авторы
Даты
1993-07-23—Публикация
1990-02-26—Подача