Изобретение относится к новым борорганическим соединениям, а именно к (4- циано-3-галогенфенилоксикарбонил)-3-гало генфенил}-5-алкил-1, 3, 2-диоксаборинанам общей формулы
.0
cnH2ntV
4I4 B iyCQChQ-CN 0 XУ
где или 5; х - Н, F, CI;
у - F или CI; - Н или F;
у- F или CI;
или 7.
x-y-F,
которые могут найти применение в качестве компонентов жидкокристаллических композиций, предназначенных для электрооптических устройств отображения информации.
Целью изобретения является поиск новых соединений, характеризующихся более низкими температурами образования нема- тической фазы, более высокой положительной диэлектрической анизотропией по сравнению с известными аналогами.
Пример 1. (4-Циано-3-хлорфени- локсикарбонил)-3-фторфенил -5-пропил-1, 3, 2-диоксаборинан. Смесь 1 г (0,004 моль) 2-{4-карбокси-3-фторфенил)-5-пропил-1, 3, 2- диоксаборинана, 0,32 мл пиридина, 0,32 мл тионила хлористого в 50 мл безводного диэ- тилового эфира перемешивали 1 ч, Затем добавляли 0,5 г (0,004 моль) 4-окси-2-хлорбензонитрила и 1 мл пиридина. Смесь оставляли на ночь, затем фильтровали. Остаток, полученный после отгонки растворителя, кристаллизовали из гексана, этилового спирта. Выход 1,3 г, 86%, т. пл. Ш°С.
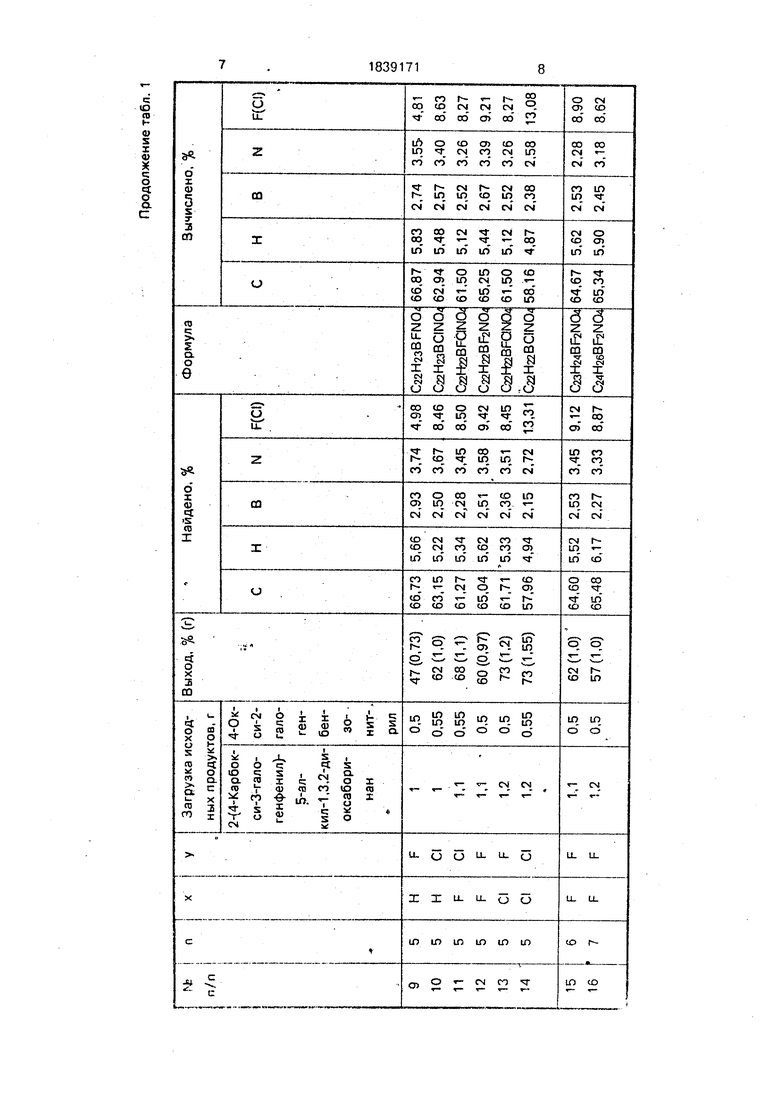
Аналогично были получены и другие эфиры, выход и температуры фазовых переходов которых представлены в табл. 1 и 2.
Состав и строение эфиров подтверждены результатами элементного анализа (табл. Т), данными ИК-, ПМР-спектрое.
Так, в спектрах ПМР предлагаемых соединений (10%-й раствор в дейтероацетоне, эталон-гексаметилдисилоксан, прибор Tesla BS - 467, д м. д.), сигналы атомов водорода боринанового фрагмента наблюдаются в области 3.4-4.3 (центры при 3.54,
3.70, 3.86, 4.00, 4.10, 4.16, 4.26). Сигналы атомов водорода бензольных колец наблюдаются в области 7.10-8.06 м. R. в ПК-спектрах соединений (0,1 молярные растворы с
ССЦ хлороформе) интенсивные пики 1715, 2215 см соответствуют валентным колебаниям карбонила сложноэфирного фрагмента, нитрильной группы.
Синтезированные соединения при комнатной температуре белые, без запаха кристаллы.
Для дополнительного подтверждения преимущества заявляемых соединений по сравнению с аналогом были приготовлены
смеси, содержащие 15 вес. ч. (4-циано, 4-галогенфенилоксикарбонил)-3-галогенфе
нил-5-алкил -1, 3, 2-диоксаборинана и 85
вес. ч. состава (А), состоящего из 2 вес. ч,
4-бутил-4-метоксианизола и 1 вес. ч. 4-бутил-4-гексилкарбоксиазоксибензола, а также смеси, содержащие) фенил 15 вес. ч. 2-{4-(4-цианофенилок.сикарбонил)-5-алкил -1, 3, 2диоксаборинаны и 85 вес. ч. состава (А) Результаты изменений диэлектрической
анизотропии полученных смесей подтвердили преимущество данных соединений по сравнению с аналогом (табл. 3).
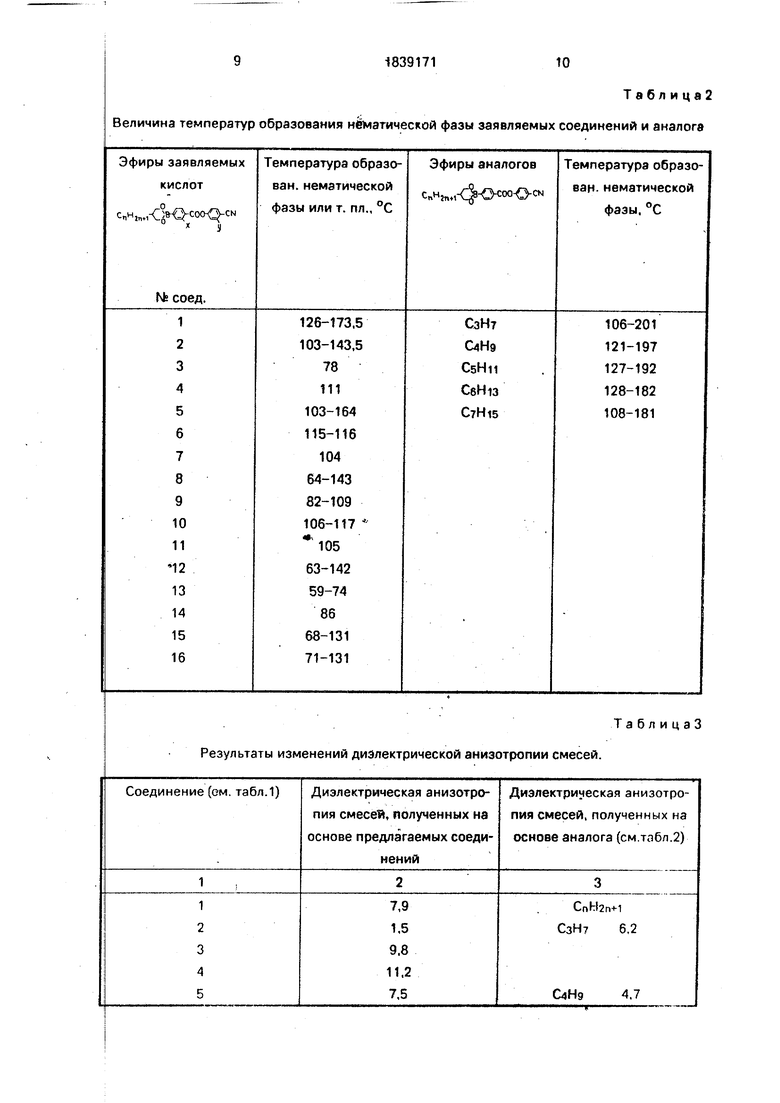
Измерение положительной диэлектрической анизотропии заявляемых соединений, смесей, полученных на основе этих соединений, и сопоставление, приведенное в табл.3, этих данных с результатами аналогичных измерений смесей, полученных с добавлением соединений аналога, показало,
что предлагаемые соединения, смеси на их основе характеризуются более высокими значениями положительной диэлектрической анизотропии, чем те же производные аналога. .
Таким образом, предлагаемые соединения по сравнению с аналогом характеризуются более высокими значениями положительной диэлектрической анизотропией и могут найти широкое применение в
качестве компонентов жидкокристаллических композиций, предназначенных для электрооптических устройств отображения информации.
(56) Авторское свидетельство СССР № 1793726, кй. С 09 К 19/52, 1985.
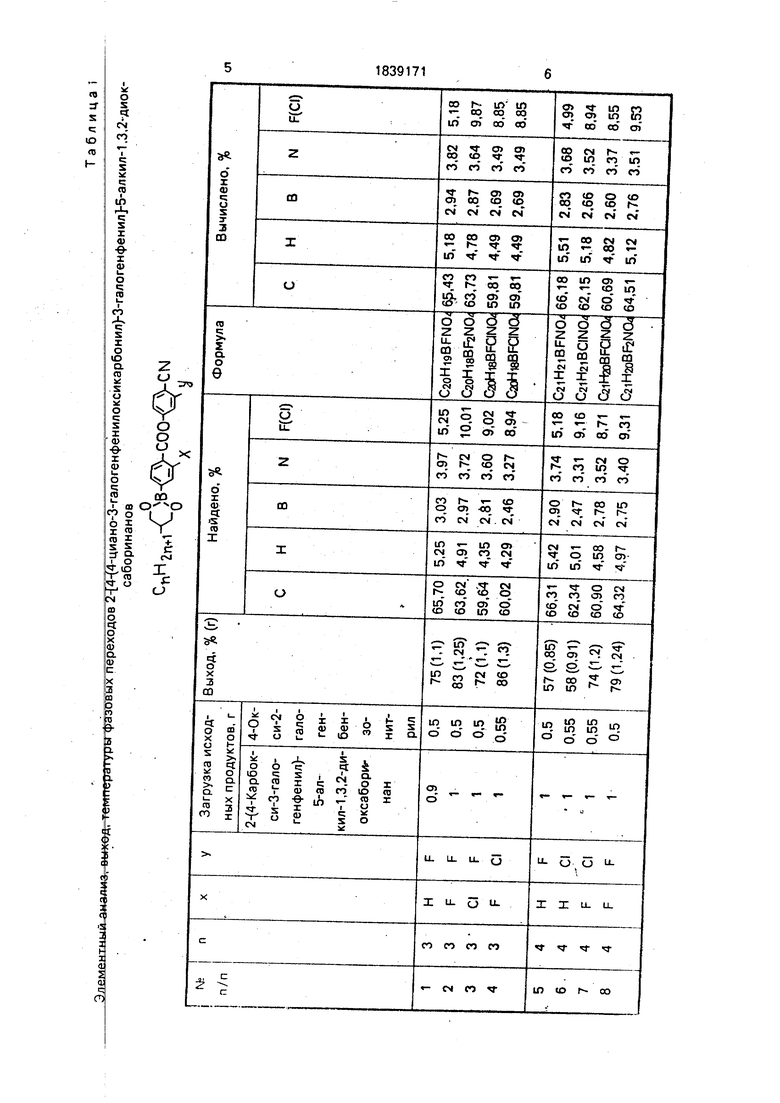
Элементццм а циила
ryp
переходов Й -циано-З-галогенфенилоксикарбонил З-галогенфенил б-алкил-Т.З -диок- саборинанов
, -O-COO-fVCN
-nn Zn+1
Таблица2 Величина температур образования нёматической фазы заявляемых соединений и аналога

| название | год | авторы | номер документа |
|---|---|---|---|
| 2-(4-Карбокси-3-галогенфенил)-5-алкил-1,3,2-диоксаборинаны в качестве полупродуктов синтеза жидкокристаллических производных галогенфенил-5-алкил-1,3,2-диоксаборинанов | 1986 |
|
SU1766922A1 |
| 5-(4-Алкил- или алкоксифенил)-2-(4-цианофенил)-пиридины,обладающие жидкокристаллическими свойствами | 1978 |
|
SU713153A1 |
| Жидкокристаллический материал для электрооптических устройств | 1982 |
|
SU1069413A1 |
| Жидкокристаллический материал для электрооптических устройств | 1985 |
|
SU1302684A1 |
| 6-(ПОЛИЗАМЕЩЕННЫЙ АРИЛ)-4-АМИНОПИКОЛИНАТЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ГЕРБИЦИДОВ | 2007 |
|
RU2428416C2 |
| Жидкокристаллический материал для электрооптических устройств | 1982 |
|
SU1063101A1 |
| ПРОИЗВОДНЫЕ ХЛОРДИФТОРМЕТОКСИФЕНИЛА И ЖИДКОКРИСТАЛЛИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЭЛЕКТРООПТИЧЕСКИХ УСТРОЙСТВ НА ИХ ОСНОВЕ | 1993 |
|
RU2070191C1 |
| 2-[4-(4-Транс-алкил-3-метилциклогексил)-фенил]5-(4-транс-алкилциклогексил)пиридины в качестве компонентов жидкокристаллического материала и жидкокристаллический материал для электрооптических устройств | 1988 |
|
SU1781214A1 |
| 5-Алкил-2-(4-цианофенил)-пиридины в качестве жидких кристаллов | 1977 |
|
SU675800A1 |
| Жидкокристаллический диэлектрик | 1978 |
|
SU938745A3 |
Изобретение относится к элементоорганичес- ким соединениям, в частности к 2-{4- (4-циано-З- галопенфенилоксикарбонил ) -3-галогенфенил -б-апкил-1,3,2- диоксаборинанам ф-лы СН п 2ГМ-1 --) Y где п 3 или 5; х - Н, F или С1;у - F или CI; п 4; х - Н или F; у - F или Ct п 6 или 7; х у - F, которые могут найти применение в качестве компонентов жидкокристаллических композиций, предназначенных для электрооптических устройств отображения информации. Получение 2-{4- (4-циано- 3-хпорфенилоксикарбонил)-3-фторфе- нил}-5-пропил-1Д2 -диоксаборинана ведут реакцией смеси 2-{4-карбокси-Э-фторфенил}-5- пропил-1Д2-ДИОксабЬринана. пиридина, тионила хлориаого с 4-окси-2-хлорбензонитрилом в пиридине. Выхйд86%. Тлл. 111°С. 2табп.
Результаты изменений диэлектрической анизотропии смесей.
ТаблицаЗ
Формула изобретения 2-{4-(4-Циано-3 -галогенфенилоксикар- бонил) -3-галогенфенил -5-алкил-1,3,2-ди- оксаборинаны общей формулы /-Ох
Продолжение таб. 3
где п. - 3 или 5; х Н, F или CI; у F или CI;
п 4; х Н или F; у F или CI;
п 6 или 7; х у F.
в качестве компонентов жидкокристаллических композиций.
Авторы
Даты
1993-12-30—Публикация
1986-12-17—Подача