1
Известные способы определения катионов металлов фотометрическим (фотоколориметрическим), объемным, амперометрическим методами с использованием аналитического реагента - производного дитиокарбаминовой кислоты - сопряжены с рядом осложнений из-за образования труднорастворимых осадков этими производными с катионами тяжелых металлов. В процессе анализа приходится применять защитный коллоид или органический растворитель.
Предлагаемый способ отличается тем, что в качестве пронзводного дитиокарбаминовой кислоты используют дикарбоксиметилтиокарбаминат калия. Это дает возможность проводить анализ неносредственно в водных растворах, что упрощает данный процесс.
Дикарбоксиметилдитиокарбаминат калкя получают следующим образом:
)
КООС-ОНзи НООС- СН2.
NH(,o+3KOH
коос-ен/ к
нооС-снз
ла, охлаждают и при постоянном перемешивании добавляют сероутерод. Раствор подогревают до 30°С на водяной бане, выдерживают в течение 20-25 мин и охлаждают до 0°С.
По охлаждении выпадает обильный осадок дикарбоксиметилдитиокарбамината калия. Осадок отсасывают, промывают несколько раз метанолом с добавлением серного эфира и высушивают до постоянного веса в эксикаторе. Полученный Дикарбоксиметилдитиокарбаминат калия представляет собой белое мелкокристаллическое вещество, хорошо растворимое в воде и ночти не растворимое в спирте. Вещество, не плавясь, разрушается ирн
235°С. Полученный продукт подвергают элеAieHTapHOMy анализу на азот, серу и углерод. Дикарбоксиметилдитиокарбаминат калия можно нрименять для фотометрического (фотоколориметрического) определения металлов
иеиосредственно в водном растворе. Псиользование для этих целей диэтилдитиокарбамината натрия сопряжено с применеиием защитного коллоида или органического растворителя.
л
N-C Кроме того, возможно исиользоваиие дикарбоксиметилдитиокарбамината калия для объемного определения металлов с нрименением в качестве индикаторов оргаиических краст :телей, образующих с определяемыми ионамн окрашенные комплексные соединения, менее
наты соответствующих металлов. В случае, когда для титрования металлов берут известные производные дитиокарбаминовой кислоты, выпадают осадки, и фиксирование эквивалентной точки при помощи металлоиндикаторов становится затруднительным. Дикарбоксиметилдитиокарбаминатом калия можно также маскировать в водных растворах многие ионы. При использовании для этой цели диэтилдитиокарбамината натрия образующиеся труднорастворимые дитиокарбаминаты необходимо экстрагировать органическими растворителями. Дикарбоксиметилдитиокарбаминат калия образует с ионами меди, никеля, кобальта окрашенные комплексные соединения.
Пример 1. Фотометрическое онределенис кобальта в сталях.
Навеску стали в 0,1 г растворяют при нагревании в 15 мл П25О4 (1 :4). Содержимое колбы кипятят до побеления остатка. Осадок кремниевой кислоты и неразлол ;ивщихся карбидов отфильтровывают через плотный фильтр и промывают несколько раз горячей разбавленной HgSOi (1 : 10). Фильтрат переносят в мерную колбу емкостью 250-500 лгл, доводят до метки водой и перемешивают. Для определения отбирают в мерную колбу емкостью 50 мл аликвотную часть раствора, добавляют 10 мл буферного раствора с рН 5,1, 0,05- 0,1 г аскорбиновой кислоты, 2 мл 0,01 М раствора дикарбоксиметилдитиокарбамината калия, тщательно перемещивают и доводят до метки 2 нормальной соляной кислотой. Полученный раствор фотометрируют при 320 мла-с и содержание кобальта находят по калибровочной кривой. Калибровочную кривую строят по стандартным образцам стали (фиг. 1).
Удовлетворительные результаты получают при содержании кобальта от 0,2 до 10у в I мл. Часть результатов определения кобальта в сталях представлена в табл. 1.
Таблица 1
Прямолинейная зависимость между оптической плотностью и концентрацией металлов соблюдается также для никеля и меди. Дикарбоксиметилдитиокарбаминат калия можно использовать и для фотометрического определения никеля и меди в различных материалах.
Пример 2. Объемное определение металлов.
Берут раствор реагента
KOOC-te,
X.
KooC-te/ ,1,
в качестве титрованного при объемном определении висмута, свинца, кадмия в присутствии ксиленолового оранжевого, играющего роль металлоиндикатора. Эквивалентная точка фиксируется при молярном отношении Me : R 1 ; 2.
Между количеством взятого металла и расходом реагента сохраняется пропорциональность. Полученные результаты определения висмута, кадмия и свинца (см. табл. 2) свидетельствуют о надежности метода и возможности его применения для определения указанных металлов в различных материалах.
Таблица 2


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ спектрофотометрического опреде-лЕНия СВиНцА | 1978 |
|
SU833531A1 |
| Способ определения свинца ( @ ) | 1983 |
|
SU1161871A1 |
| Способ фотометрического определения титана | 1961 |
|
SU148584A1 |
| Способ определения железа в водных растворах | 1989 |
|
SU1709195A1 |
| Метилбензтиазолилазокетоксим в качестве избирательного аналитического реагента на ионы кобальта в биологических объектах и способ фотометрического определения кобальта в биологических объектах | 1979 |
|
SU891667A1 |
| Способ определения висмута | 1990 |
|
SU1797053A1 |
| Способ переведения висмута в окрашенное комплексное соединение | 1973 |
|
SU482648A1 |
| Способ определения ртути ( @ ) | 1983 |
|
SU1153287A1 |
| Способ экстракционно-фотометричес-КОгО ОпРЕдЕлЕНия КОбАльТА | 1977 |
|
SU798045A1 |
| Способ экстракционно-фотометрического определения молибдена | 1975 |
|
SU585124A1 |


Пример 3. Амперометрическое определение металлов.
вом электроде. Это свойство было использовано для амперометрического определения ртути, висмута, меди, свинца. Эквивалентная точка фиксируется для металлов одной и той
же валентности при разном молярном отношении реагента к металлу. Так, нри титровании ртути анодный ток возрастает при молярном отношении Hg : R 1 : 2, а при титровании меди и свинца эквивалентная точка наблюдается при отношении Me : R 1:1. Висмут титруется дикарбоксиметилдитиокарбаминатом калия в соотношении Bi : R 1 : 2. Эти факты говорят об участии в комплексообразовании и карбоксильных групп, причем их комплексообразуюш,ая способность увеличивается для тех катионов, у которых прочность связи с серой дитиокарбоксильной группы уменьшается. При амперометрическом тлтровании ртути, меди, висмута, свинца дикарбоксиметилдитиокарбаминатом по анодному току реагента были получены удовлетворительные результаты.
Растворы дикарбоксиметилдитиокарбамината калия поглош,ают свет в дальнем ультрафиолете (фиг. 2). Максимумы светоноглоп;ения в нейтральной среде находятся при 260 и 290 ммк. В пделочной они несколько сдвинуты в более ультрафиолетовую область, а в кислой среде ввиду разложения реагента на исходный амин и сероуглерод поглош,епия света почти не происходит.
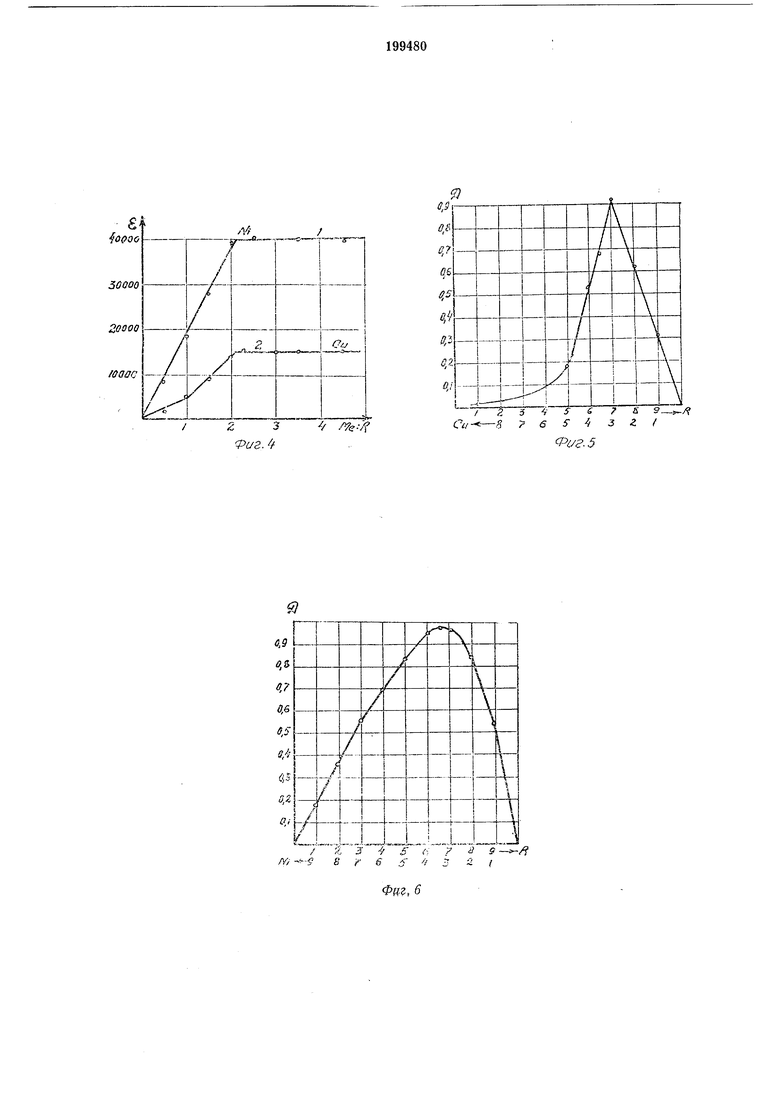
Дикарбоксиметилдитиокарбаминат калия образует с ионами меди, никеля, кобальта окрашенные комплексные соединения с максимумами светопоглощения, лежаш,ими соответственно при 430, 320 и 315 ммк (фиг. 3). Молярные коэффициенты погашения для дикарбоксиметилдитиокарбаминатов меди, никеля и кобальта равны 15250, 40000 и 25000. Методами насьщения и изомолярных серий установлен состав образуюшихся комплексов меди и никеля (фиг. 4 - 6). Для меди наблюдается образование двух комплексных соединений: одного - при молярном отношении Си : R -- 1:1 с максимумом светопоглощения при 390 ммк и второго - при отношении Cu:R 1 :2 с максимумом при 430 ммк.
Для комплексных соединений меди, никеля и кобальта выяснено влияние кислотности на
условия образования и устойчивость комплексов. Опыты показали, что дитиокарбаминаты никеля и кобальта образуются и на протяжении длительного времени не разрушаются при
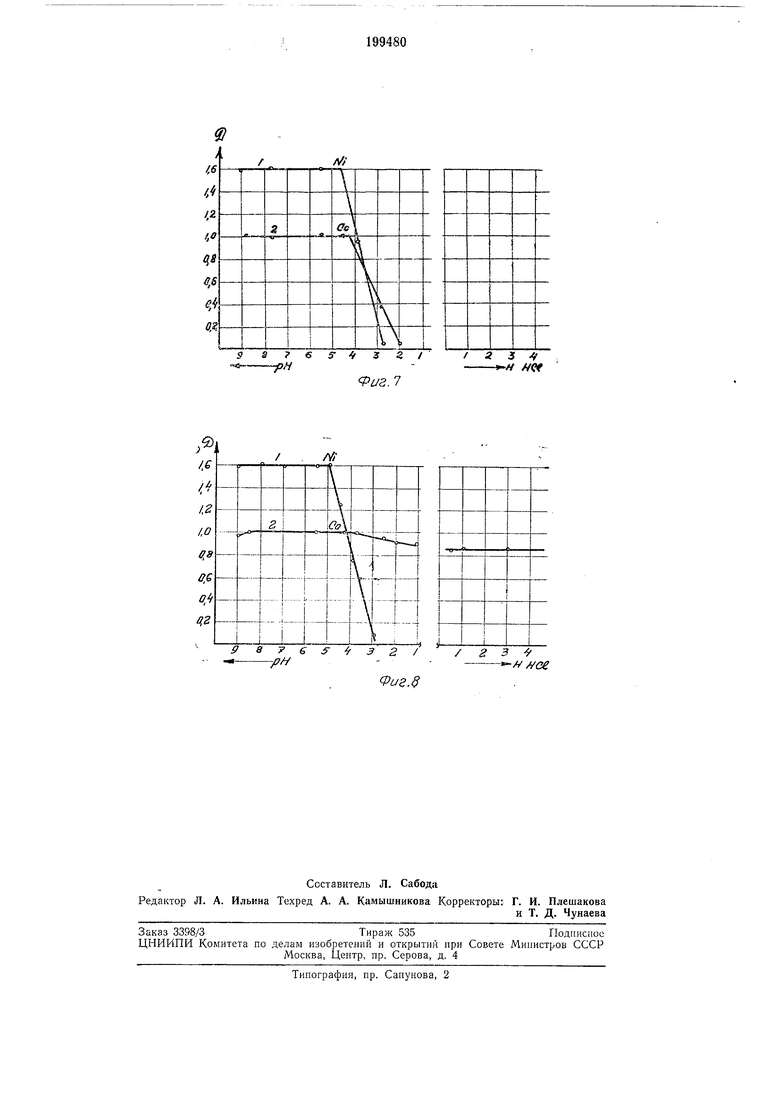
рН 9-5, меди - при рН 9-3 (фиг. 7). В более кислых средах (рН 3) образование окрашенных дикарбоксиметилдптиокарбаминатов никеля и кобальта не нроисходит вследствие малой скорости образования комплексов
и неустойчивости дитиокарбаминовых кислот.
Образование дитиокарбамината меди в этих
условиях наблюдается по выходу комплекса
меньше 100%.
Пределы рН образования дикарбоксиметилдитиокарбаминатов никеля и меди остаются практически постоянными независимо от норядка приливания реактива и буферного раствора. Для комплексного соединения кобальта последовательность прибавления реактивов
играет существенную роль. Если образование дикарбоксиметцлдитиокарбамината кобальта нроисходит при рН 9 - 4,5 (дитиокарбаминат добавляют после создания соответствующей среды), то полученное соединение не удается
разрушить даже 4 н. НС1 (фиг. 8). Такая аномальная устойчивость дикарбоксиметилдитиокарбамината кобальта может быть использована для фотометрического определения никеля и кобальта из двух параллельпых
проб, условия подготовки которых отличаются только введением в одну из них кислоты определенной концентрации.
Предмет изобретения
35
Способ определения катионов металлов фотометрическим(фотоколориметрическим), объемным, амперометрпческим методами с использовапием аналитического реагента - нрсизводного дитиокарбаминовой кислоты, отличающийся тем, что, с целью возможности проведения анализа непосредственно в водных растворах, в качестве производного дитиокарбаминовой кислоты применяют дикарбоксиметилдитиокарбаминат калия.
( sflZ оез ff,f- f,S5 ff ff 0, (Риг.1
i-A -V
-,:, $S/ i.v.- -,( .«/5 ,jj
T.-,- 9
V..,:;. л
.foo SiO 33O jSO 3fO S 39O i-ffs 4.Ч 4гс 4Sff iifff-/f
P(/3- л. : -
loaaa
иа.$
Даты
1967-01-01—Публикация