Изобретение относится к аналитической химии, в 4actHocTM к определению общей концентрации железа в вод« ных растворах . солей и водах, и может быть использован для контроля воды и солей.
Среди фотометрических методов наиболее чувствительный и широко применяемый ,метод с хромйзуролом-S. Комплекс железа (ill) с данным реактивом характеризуется спектром поглощения с опт 575 нм и молярным коэффициентом светопоглощения б ,3«10, рН о&р , О.
Недостатками этого метода являются невысокая чувствительность (13 мкг/л) и низкая избирательность. Определению мешают Си,. Со, Ni, Zn, Pb, Ti, Cr, Al, Ga, In и Ce.
Известен фотометрический метод определения железа в природной воде с 4-(2-пиридилазо)-резорцином (ПАР). При рН 8,0 - 3,3 образуется комплексное соединение 530, нм и 6. 6,04 «10. Предел обнаружения железа 9,3 мкг/л.
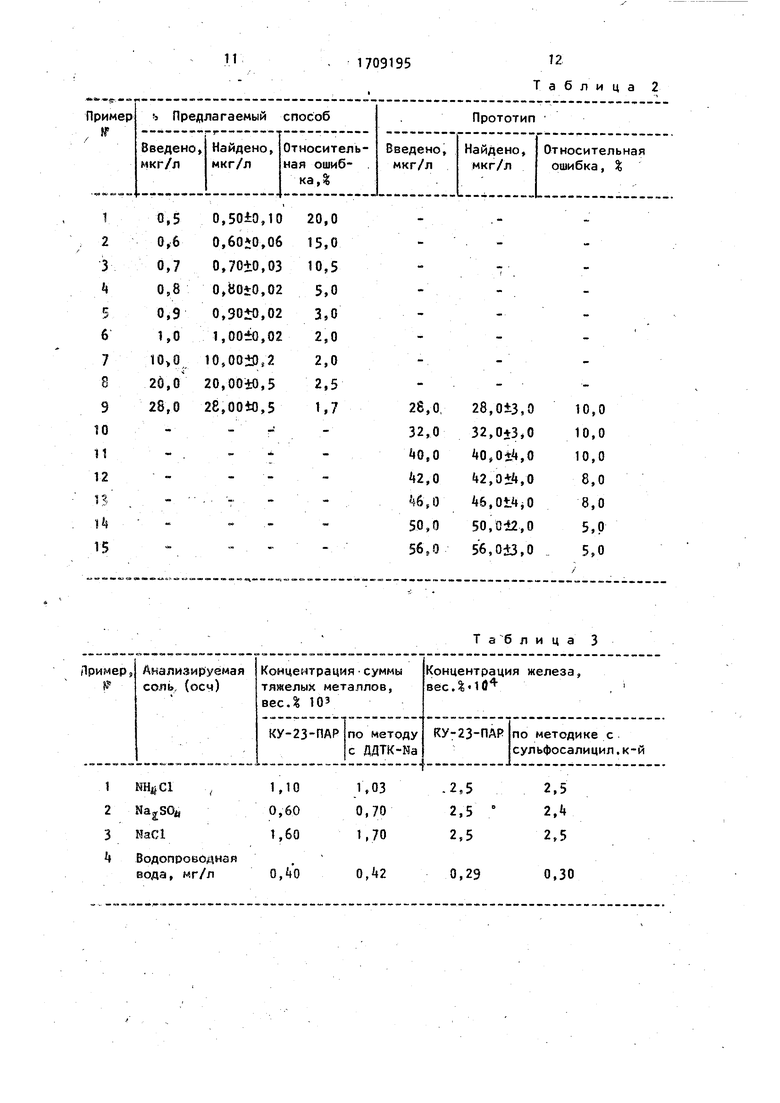
Но данный метод отличается низкой избирательностью, определению мешают Си, Ag, Zn, Cd, Hg, Al, Ga, In, , Tl, Sc, J, La, Ce (III), P3E, Sn (IV) и для устранения их влияния следует добавлять в исследуемый раствор мае-: кирующие реагенты, что снижает точность и чувствительность анализа. Для повышения селективности метода исV пользуют экстракционно-фотометрический вариант, который применен для определения железа в морской воде: 100 мл воды подкис ляют до рН 2,5, выдерживают 15 мин и вводят 1,5 мл М этанольного раствора ПАР и экстрагируют 20 см раствора диентипирилметана 8 хлороформе, массовая доля которого составляет 10%. Измере ние оптической плотности экстракта I проводят на фотоэлектроколориметре, при 500 им, предел обнаружения Ю мкг/л. Определению не мешают в со измеримых количествах элементы морской воды А., Ga и In. Общими нeдoctaткaми всех описанны методов являются невысокая чувствительность и .низкая селективность. Наиболее близким к изобретению является способ определения железаj заключающийся в том, что в исследуемый раствор, содержащий Ре (II) и Fe (III), вводят гидроксиламин для восстановления железа, раствор 1,10-фенантролина, добавляют ацетатный буфер (рН 5jOy. Полученный .раствор 30 мин В|стряхивают с катионообманником Dowex 50W, после чего твердую фазу, содержащую комплекс, отделяют - измеряют светопоглощение тзер дого слоя в специальный кюветах с зеркальными боковыми стенками при 51 им на спектрофотометре Hitachi, модель EPS-3T. - : Недостатки известного метода состоят S следующем.. Низкая чувствительность определе ния железа 20 мкг/л, связаннач с ден ситометрическ.им измерением в тонких кюветах (1 0,1 см). Недостаточно высокая селективност метода. Определению мешают Сг и Zn ; 10-кратный избыток; Со и Си -З мг/л NX мг/л. Нешают определению и ор.ганические вещества. Измерение светопоглощения твердого слоя требует дополнительных приспособлений - специальных кювет. Вос производимость полученных данных пон жается 8 связи ,с трудностью отсеивания зерен катионообменника абсолютно одинакового размера и различной степени упаковки их в кювете. Кроме того, низкая селективность метода требует применения маскирующих реагентов - для восстановления железа необходимо вводить в раствор гидроксил амик, а для создания необходимой кислотности - буферный раствор. Все это способствует загрязнению ионами железа исследуемого раствора. Существует трудность приобретения катионообменника, выпускаемого за рубежом. Цель изобретения - повы.шениё чувствительности и избирательности анализа. Для достижения поставленной цели предложен способ определения железа в воде и растворах солей, . состоящий в том, что в анализируемую пробу вводят сорбент - макропористый катионообменник КУ-23 предварительно модифицированный (2-пиридилазо)-резорцином в количестве 50-62,5 мае.. Окрашенный комплекс железа с ПАР элюируют раствором щелочи при рН среды 11,8-12,3 с последующим фотометрированием элюата. Сравнительный анализ изобретения с прототипом показывает, что предлагаемый способ отличается от известного тем, что окрашенный комплекс получают концентрированием ионов железа на катионообменнике, предварительно модифицированным ПАР (0,5-0,625 г реактива на 1 г сорбента), и регист рацию интенсивности поглощения комплекса ведут а элюате, полученном обработкой сорбента, содержащего комплекс железа с ПАР, раствором щелочи при рН 11,. 8 прототипе сорбцию осуще.ствляют катионообмеиником Дayэкc-50W. При этом сорбируется комплекс, предварительно полученный в растворе. Установлено, что использование такого приема при сорбции отечественным катионообменником не обеспечивает полноты извлечения железа из анализируемого раствора, так как при этом образуется не поглощаемый катионообменником нейтральный комплекс железа с ПАР. Поэтому макропористый катионообменник КУ-23 был предварительно промодифицирован ПАР и использован для сорбции железа- из раствора. Использование отечественного сорбента другой структуры, например гелевого КУ-2, невозможно, так как данный сорбент только модифицируется реактивом, но сорбция железа на нем не осуществляется. Макропористый катионообменник КУ-23 был промодифицироваи брлее 20 органическими реагентами, .широко используемыми в фотометрическом методе анализа. Полученные ионообменники использовались для концентрирования ионов металлов из растворов раз личной степени минерализации. ЛуМшими сорбционными характеристиками обладает КУ-23, модифицированный ПАР {КУ-23-ПАР). Преимуществом КУ-23-ПАР по сравнению с другими изученными модифицированными катионообменниками является также возможность элюирования с его поверхности комплексов . металлов с ПАР в ще-лочной среде. Эт позволяет использовать простой фотометрический метод, не требующий специалйных кювет и обладающий лучшей воспроизводимостью по сравнению с твердофазной спектрофотометрией. Кро ме того, ПАР образуют со многими кат онами металлов ярко окрашенные комплексы с высоким молярным коэффициентом светопоглощения. Установлено, что при элюировании в щелочной среде возможно фотометрическое определение суммы катионов тяжелых металлов и селективное опре деление железа. Для определений сумм тяжелых металлов необходимо фотометрировать раствор при SlO нм, так как при этой длине волны элюаты всех комплексов металлов, в том числе и железа, обладают одинаковым молярным коэффициентом поглощения л/3« 10. Селективное определение железа обусловлено возможностью фотометрирования элюата при / 750 нм так как спектр поглощения комплекса железа с ПАР в отличие от других катионов металлов характеризуется двум максимумами: /{ нм и Д/г. 750 нм. При q комплексные соединения меди, кобальта, кадмия, никеля,; свинца, цинка, хрома, марганца и алюминия с ПАР не влияют на количест венное и селективное определение микр количеств железа в природных водах и растворах солей. Таким образом, высокая чувствительность и селективность определени железа достигается количественной сорбцией ионов железа модифицированным сорбентом и количественным элюированием железа, с ПАР с пбследующим фотометрированием элюата. При этом количество ПАР на сорбенте и рН элюирования комплекса выбраны из услови обеспечивающих высокую чувствительность определения железа (табл.1, примеры 1-9). . Запредельное снижение содержания ПАР на сорбенте приводит к снижению чувствительности определения. Ниж няя грзница обнаружения железа повышается вследствие того, что при меньшем содержании ПАР происходит не количественное взаимодействие ионов железа с реактивом, в результате понижается оптическая плотность элюата (табл.1 ,примеры-1 О, 11.). Предложенное верхнее граничное количество модификатора (ПАР) ограничено стерическим фактором и емкостью катионообменника, так как происходит эквивалентное замещение ионов водорода в катионообменнике на молекулы реактива. Запредельное снижение рН элюата -не обеспечивает чувствительность определения на уровне 0,5 мкг/л. Незначительное изменение рН приводит к резкому изменению чувствительности определения железа (примеры 12, 13). Это связано с тем, что происходит не полное извлечение комплекса железа с с поверхности сорбента Запредельное повышение рН элюата приводит к частичному разрушению элюируемого комплекса,, в результате чего -снижается оптическая плотность элюата и, следовательно, понижается чувствительность определения железа (табл.1, примеры 14, 15). На основании полученных дайных разработан сорбциоино-фотометрический метод определения общего железа и суммы катионов металлов (Си, Со, Cd, Сг, Мп, А1, РЬ, Ki, Zn и Fe) с помощью модифицированного катионо- обменника КУ-23-ПАР в питьевой воде и солях квалификации осч. Применяемые реактивы и аппаратура. Азотная кислота, концентрированная. ГОСТ 461-77 хч О - 10. Хлористоводородная кислота, концентрированная, ГОСТ ЗПЬ-77 хч 0-1t. Растворы металлов: Fe; Со, Си, Cd,« Мп, Сг, Zn, Al; Ni; Pb готовят растворением спектрально чистых металлов в азотной кислоте. Макропористый катионообменник КУ-23 очищают с помощью 5Я хлористоводородной кислоты, промывая в колон ке до бесцветных промывных вод (тща-. тельно промывали бидистиллятом и насыщали при рН 5,0-10,0 раствором ПАР ( М раствор в воде) в расчете на 1 г КУ-23 необходимо 0,5-0,625 г реактива}.. Модифицированный катионобменник промывают бидистиллятом и сушат на воздухе. 71 Натрия гидроокись, ГОСТ 432877 хч 0-26. Фотометрирование по РСТ-29 39-787 Оптическую плотность растворов измеряли на ФЭК-56 М npH-Ji tfip нм, 1 2 см и СФ-5 при / j-pffj 750 нм, 1 5 см. Предложенный способ иллюстрируется следующими примерами. П р и м 6 р t. Определение железа .в дистиллированной воде. 100 смЗ дистиллированной воды под кисляют 0,2 см5 концентрированной азотной кислоты (рН 3,0), вводят железо Б количестве 0,8 мкг/л, добавляют 0,3 г КУ-23-ПАР (50% модификато ра) и встряхивают в колбе с притерто пробкой в темение 30 мин. Раствор, декантируютс,катионообменника и добавляют к последнему 25 смЗ 0,01 М .раствора гидроксидз натрия (рН 12,0) После кипячения в течение 3 мин раст воря встряхивают 15 мин и измеряют оптическую плотность по отношению к раствору сравнения (элюату реактива) при 750 нм на СФ-З, 1 5 см. Калибровочные графики строят а интер вале концентраций 0,5-28,0 мкг/л железа. Проведено 5 параллельных опыто (р О,95)о Найдено0,82 мкг/л желез ошибка определения 5,% (табл.2 при мер ). Данная таблица иллюстрирует оысокуа чунствительность предложенно го метода. При .определении железа- в концентрациях, близких к пределу обн ружения, точность метода ниже, чем при определении железа з концентраци ях, больши,ч 1C мкг/л. Однако, если сравнивать точность опрелеления боль ших концентраций , железа предложенно го способа с прототипом, видно явное преимущество предложенного способа (табл.2). П р и м е р 2. Определение концентрации ионов железа и суммы кати онов тяжелых металлов в некоторых солях. Навеску соям около 0,.8 г, взвешенную с погрешностью не более 0,0002 г, растворяют ;в 100 смз дистиллированной воды. Полученный раствор помещали в колбу с притертой пробкой, создавали рН раствора равное 3,0 с помощью азотной кислоты, добавляли 0,3 г модифицированного сорбента. Колбу закрывали пробкой и ,смесь перемешивали 30 мин, после чего раствор декантировали с .катионообменника. Последний промывали дистиллированной водой. Катионы металлов элюировали 25 см раствора NaOIi (рН 12,0) при нагревании в течение 3 мин на водяной бане и встряхивали 15 мин. После охлаждения раствора измеряли его опт1/ ческую плотность на ФЭК-56 М, .9 нм, 1 5 см. Таким путем возможно определение суммы катионов металлов в солях. При определении концентрации железа в солях оптическую плотность раствора измеряли на спектрофотометре СФ-5 при ,ф 750 им и 1 5 см. Для построения калибровочного графика брали раствор смеси катионов металлов 2-30 мкг/л, где содериание каждого элемента, в том числе и железа, 0,2-0,3 мкг/л. Полученные данные о содержании железа и суммы катионов металлов представлены в табл.З (пример 2) . Определение суммы тяжелых металлов и селективное определение железа возможно в ряде других солей (примеры 1,3 в табл.3). Концентрацию железа во всех пробах контролировали методом добавок и фотометрически с сульфсэсалицилог вой кислотой, а концентрацию суммы катионов металлов - по экстракции с диэтилдитиокарбаминатом с последующим вытеснением катионов металлов медью и фотометрированием экстракта. Для сравнения полученные данные приведены также в табл.3. Примерз. Определение концентрации ионов железа и суммы катионов металлов в водопроводной воде. Питьевую &ОДУ (100 смЗ) подкисляют 0,2 смЗ концентрированной азотной кислоты, кипятят 3 мин. К остывшей воде добавляют 0,3 г КУ-23-ПАР (60% модификатора) и встряхивают в колбе с притертой пробкой э течение 30 мин. Раствор декантируют с катионообменника и добавляют к последнему 25 смз КаЪн (рН 12,0), смесь нагревают до кипения и осторожно кипятят 5 мин. После остывания встряхивают 5 мин и измеряют оптическую плотность по отношению к раствору сравнения (элюату реактива) на ФЭК-56 М,. см. Для определения концентрации железа оптическую плотность измеряют при 750 нм на СФ-5, 1 5см.
Калибровочный график строят в интервале концентраций 0,2-0,5 мкг/л как суммы катионов металлов, так и железа, (табл.3, пример ). Контроль полноты извлечения осуществляли теми же методами, что и при опре.делении металлов в.солях.
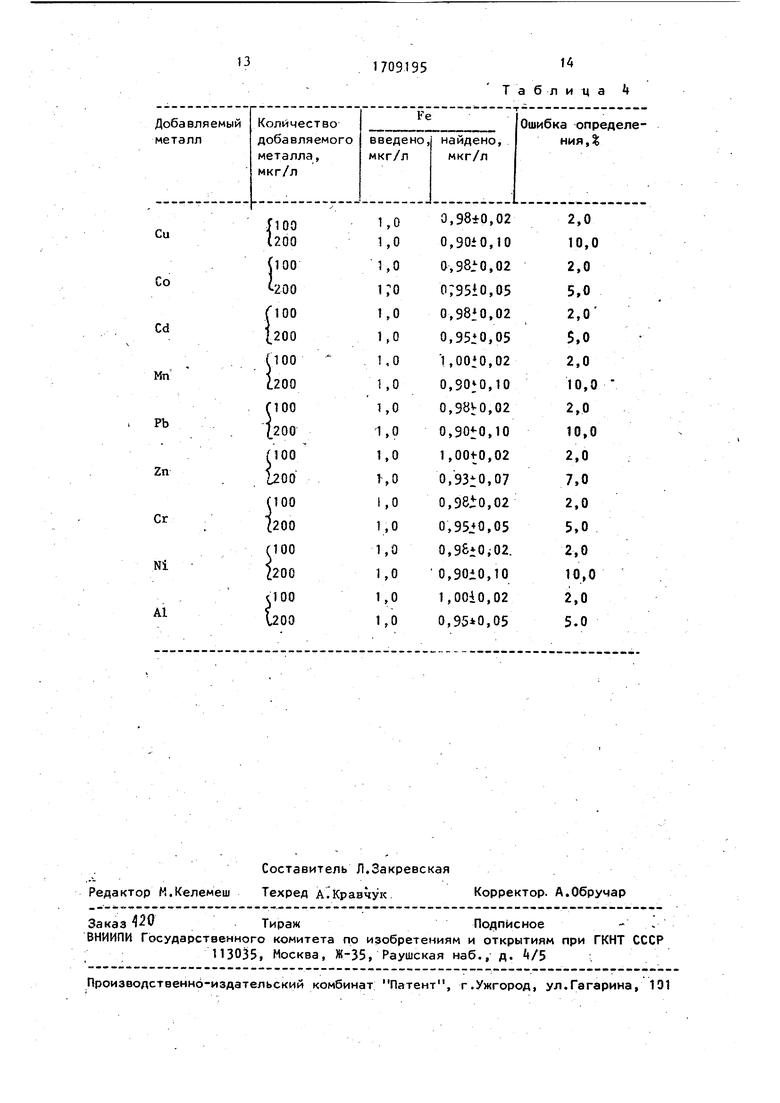
Предлагаемый метод определения железа является высокоселективным. При сутствие в растворе 100-кратного избытка Си, Со, Cd, Мп, Zn, А1, Ni, Pb, Cr не оказывает влияния на селетивное определение делеха в водах и солях.
Увеличение содержания ионов тяжелых металлов до.200-кратного избытка по отношению к железу обуславливает ошибку определения железа до 10 (табл.4).
Предлагаемый способ позволяет повысить чувствительность определения железа по сравнению с прототипри в 50 раз. Способ является в.ысокоселективным. Значительный избыток ионов тяжелых металлов Ht оказывает влияния на чувствительность и точность определения железа данным способой. Высокоточное и селективное
определение железа возможно в водах различной степени минерализации и ряде солей. Разработанный способ отличается простотой в исполнении,, быстрый, обладает хорошей воспроизводимостью, низким пределом обнаружения и высокой(Селективностью определения железа. Формула изобретения
Способ определения железа в водных растворах, включающий его перевод в комплексное соединение с органическим реагентом, концентрирование полученного комплекса на сорбенте и фотометрирование, отличаю щи йс я тем, что, с целью повышения чувствительность и избирательности анализа, перевод в комплексное соединение и концентрирование.осуществляют одновременно на сорбенте, в качестве Которого используют макропорис тый катионит, предварительно модифицированный органическим реагентом до его содержания 0,5-0,625 г/г, в качестве которого применяют -(2-пиридилазо)-резорцин, полученное комплексное соединение элюируют с сорбента раствором щелочи при рН 11, и фотометрированию подвергают элюат.
Таблица




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения меди в воде | 1989 |
|
SU1682866A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЖЕЛЕЗА (II) | 2008 |
|
RU2374639C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ МИКРОКОНЦЕНТРАЦИИ МЕДИ | 1992 |
|
RU2013766C1 |
| Способ фотометрического определения хрома /ш/ | 1975 |
|
SU610795A1 |
| Способ определения железа в цветных металлах и сплавах | 1981 |
|
SU1000401A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЖЕЛЕЗА (II) | 2014 |
|
RU2557980C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПАЛЛАДИЯ (II) | 2008 |
|
RU2374640C1 |
| Способ определения железа в деионированной воде | 1988 |
|
SU1539616A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЖЕЛЕЗА (II) | 2014 |
|
RU2555483C1 |
| Способ экстракционно-фотометрического определения железа | 1979 |
|
SU791604A1 |
Изобретение относится к способам фотометрического определения железав водных растворах и может быть использовано при анализе растворов сложного состава. Цель изобретения - повышение чувствительности.и избирательности анализа. Сущность изобретения заключается в обработке пробы макропористым катионитом, ^модифицированным А-
Запредельные значения
11
0,0
вода, мг/л
12
1709195 Таблица 2
Т а б л и ц а 3
0,42
0.30
0,29
13
14
1709195 Т а б л и 14 а k
| К.Joshimura et.al., jon-exchan- ger phase absorptiometry for trace analysis, Talanta, v.32, 1985,№5,: P | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
Авторы
Даты
1992-01-30—Публикация
1989-06-29—Подача