Изобретение относится к области получения веществ, которые могут найти применение в препаративной органической химии.
Предлагаемый способ получения 2-(5-тетразолил)-N-(замещенный фенил)анилинов общей формулы

где R′ - хлор, бром, йод, фтор, трифторметил, окисленный или сернистый трифторметил, (низший)алкил, (низший)окисленный алкил, нитро-, метилсульфонил, ди(низший)алкиламино- или (низший)сернистый алкил;
R2 и R3 - водород, хлор, бром, йод, фтор, трифторметил, окисленный или сернистый трифторметил, (низший)алкил, (низший)окисленный алкил, нитро-, метилсульфонил, ди(низший)алкиламино- или (низший)сернистый алкил, но R2 водород только тогда, когда R3 также водород,
заключается в том, что 2-циано-N-(замещенный фенил)анилины обрабатывают азидом натрия в присутствии хлорида аммония при 120-127°С в жидкой среде, например в среде диметилформамида. Вместо азида натрия можно применять азид калия, лития, алюминия, аммония, замещенного аммония, например азид тетраметиламмония и азотоводородную кислоту.
В качестве катализатора можно использовать хлорид аммония или какую-нибудь другую кислоту по Льюису, например эфират трехфтористого бора, хлориды тетраалкиламмония, хлоргидрат анилина или хлорид лития. Предпочтительно, чтобы время реакции было около 12 час и температурный интервал - примерно между 80 и 140°С, а жидкая среда реакции была бы безводной. Лучше, если жидкая среда будет содержать монометиловый и этиловый эфиры этилен- и диэтиленгликоля, тетрагидрофуран, формамид, диметилформамид, ацетамиддиметил, диоксан, N-метил-2-пирролидон, этиленгликоль, диэтиленгликоль, диметилсульфоксид, диметилсульфон, алканолы, имеющие от 4 до 6 атомов углерода, например n-бутанол и гексаметилфосфорный триамид.
Исходные соединения получают известными способами из соответствующих антраниловых кислот, которые, в свою очередь, приготовляют также известным способом перегруппировкой Чэпмена из замещенных анилинов или фенолов.
Пример 1. 2-(5-тетразолил)-N-(3-трифторметил фенил)анилин.
0,33 г (0,00508 моль) азида натрия и 0,265 г (0,00495 моль) хлорида аммония прибавляют к раствору 1 г (0,00382 моль) 2-циано-N-(3-трифторметилфенил)анилина в 8 мл диметилформамида. Реакционную смесь нагревают и перемешивают при 120°С 16 час. Диметилформамид удаляют в ротационном выпарном аппарате. Остаток обрабатывают холодной водой, а полученную смесь фильтруют. Фильтрат подкисляют концентрированной соляной кислотой. Осадок кристаллизуют из водного этанола и получают почти белые кристаллы (0,5 г). Продукт дважды перекристаллизовывают из водного этанола и получают бесцветные кристаллы с т. пл. 205-207°С.
C14H10N5F3.
Вычислено, %: С 55,07; Н 30,30; N 22,94.
Найдено, %: С 55,30; Н 3,25; N 22,92.
Пример 2. 2-(5-тетразолил)-N-(2,3-ксилил)анилин.
Смесь 0,644 г (0,00988 моль) азида натрия, 0,53 г (0,00988 моль) хлористого аммония и 2 г (0,00988 моль) 2-циано-N-(2,3-ксилил)анилина в 18 мл диметилформамида нагревают при перемешивании 18 час при 125°С. Диметилформамид удаляют в ротационном выпарном аппарате. Остаток обрабатывают 40 мл воды и подкисляют смесь концентрированной соляной кислотой. Полученный осадок кристаллизуют из водного этанола (с обработкой углем) и получают 2 г 2-(5-тетразолил)-N-(2,3-ксилил)анилина в виде очень бледно-желтых кристаллов. Продукт перекристаллизовывают из водного этанола и получают бесцветные игольчатые кристаллы с т. пл. 203,5-205,5°С.
C15H15N5.
Вычислено, %: С 67,90; Н 5,70; N 26,40.
Найдено, %: С 68,01; Н 5,72; N 26,43.
Пример 3. 2-(5-тетразолил)-N-(2,6-дихлор-3-метилфенил)анилин.
Смесь 9 г (0,0325 моль) 2-циано-N-(2,6-дихлор-3-метилфенил)анилина, 2,535 г (0,039 моль) азида натрия и 2,085 г (0,039 моль) хлористого аммония в 65 мл диметилформамида нагревают при перемешивании при ~127°С 17 час. Диметилформамид удаляют в ротационном выпарном аппарате. Из остатка образуют суспензию в 300 мл холодной воды, которую подкисляют до рН 2 концентрированной соляной кислотой. Твердый продукт собирают и выкристаллизовывают из водного метанола (с обработкой углем) и получают 8,6 г 2-(5-тетразолил)-N-(2,6-дихлор-3-метилфенил) анилина в виде желтых игольчатых кристаллов. Затем продукт перекристаллизовывают из водного метанола и получают желтые игольчатые кристаллы с т. пл. 207-208,5°С (разл.).
C14H11Cl2N5.
Вычислено, %: С 52,52; Н 3,46; Сl 22,15; N 21,88.
Найдено, %: С 52,60; Н 3,73; Сl 22,38; N 21,88.
Пример 4. Аналогично примеру 1 получают:
2-(5-тетразолил)-N-(2,6-дихлор-3-трифторометилфенил)анилин;
2-(5-тетразолил)-N-(2,3,6-триметилфенил)анилин;
2-(5-тетразолил)-N-(нитрофенил)анилин;
2-(5-тетразолил)-N-(2-хлор-3-метилфенил)анилин;
2-(5-тетразолил)-N-(3-хлор-2-метилфенил)анилин;
2-(5-тетразолил)-N-(6-хлор-2,3-диметилфенил)анилин;
2-(5-тетразолил)-N-(3-трифторометоксифенил)анилин;
2-(5-тетразолил)-N-(2,6-дибром-3-трифторометилфенил)анилин;
2-(5-тетразолил)-N-(2-бром-3-метилфенил)анилин;
2-(5-тетразолил)-N-(3-бром-2-метилфенил)анилин;
2-(5-тетразолил)-N-(6-бром-2,3-диметилфенил)анилин;
2-(5-тетразолил)-N- (2,6-дихлор-3-трифторометилфенил)анилин;
2-(5-тетразолил)-N-(2,6-дибром-3-трифторометилфенил)анилин;
2-(5-тетразолил)-N-(2,3,6-триметилфенил)анилин;
2-(5-тетразолил)-N-(6-хлор-2,3-диметилфенил)анилин;
2-(5-тетразолил)-N-(6-бром-2,3-диметилфенил)анилин.
Пример 5. Аналогично примеру 3 получают:
2-(5-тетразолил)-N-(2,6-дихлор-3-трифторметилфенил)анилин;
2-(5-тетразолил)-N-(2,6-дибром-3-трифторометилфенил)анилин;
2-(5-тетразолил)-N-(2,3,6-триметилфенил)анилин;
2-(5-тетразолил)-N-(6-хлор-2,3-диметилфенил)анилин;
2-(5-тетразолил)-N-(6-бром-2,3-диметилфенил)анилин.
Пример 6. 2-(5-тетразолил)-N-(3-трифторметилфенил)анилин.
К раствору 0,0038 моль 2-циан-N-(3-трифторметилфенил)анилина в 10 мл диметилформамида добавляют 0,005 моль азида аммония и реакционную смесь нагревают при перемешивании 16 час при 95°С. Диметилформамид отгоняют во вращающемся испарителе, остаток обрабатывают холодной водой и полученную смесь фильтруют. Фильтрат подкисляют концентрированной соляной кислотой и выпавший осадок собирают и перекристаллизовывают из водного спирта с получением почти белых кристаллов 2-(5-тетразолил)-N-(3-трифторметилфенил) анилина. После двукратной перекристаллизации из водного спирта продукт плавится при 205-207°С.
Пример 7. 2-(5-тетразолил)-N-(2,3-ксилил)анилин.
Нагревают смесь 0,01 моль азида натрия, 0,01 моль хлористого лития и 0,009 моль 2-циан-N-(2,3-ксилил)анилина в 30 мл диметилсульфоксида. Эту смесь при перемешивании выдерживают 24 час при 105°С, отгоняют диметилсульфоксид в вакууме во вращающемся испарителе, остаток обрабатывают 50 мл воды и смесь подкисляют концентрированной соляной кислотой. Полученный осадок собирают и перекристаллизовывают из водного спирта в присутствии активированного угля с получением желтых кристаллов 2-(5-тетразолил)-N-(2,3-ксилил)анилина. После перекристаллизации из водного спирта продукт плавится при 203,5-205,5°С.
Пример 8. 2-(5-тетразолил)-N-(2,6-дихлор-3-метилфенил)анилин.
Смесь 0,03 моль 2-циан-N-(2,6-дихлор-3-метилфенил)анилина, 0,039 моль тетраметиламмонийазида и 0,039 моль тетраметиламмонийхлорида в 75 мл моноэтилового эфира этиленгликоля нагревают при перемешивании с обратным холодильником (135°С) в течение 18 час. Отгоняют растворитель в вакууме во вращающемся испарителе и остаток взмучивают 300 мл холодной воды, подкисленной до рН 2 концентрированной соляной кислотой. Твердый остаток собирают и перекристаллизовывают из водного метанола с обработкой активированным углем. Получают желтые иглы 2-(5-тетразолил)-N-(2,6-дихлор-3-метилфенил)анилина. Этот продукт после перекристаллизации из водного метанола плавится при 207-208,5°С (с разд.).
Пример 9. 2-(5-тетразолил)-N-(2,3-ксилил)анилин.
Смесь 0,03 моль азида алюминия и 2-циан-N-(2,3-ксилил)анилина в 80 мл тетрагидрофурана нагревают при перемешивании в течение 20 час при 115°С. Тетрагидрофуран отгоняют в вакууме во вращающемся испарителе и к остатку добавляют 60 мл воды. После подкисления концентрированной соляной кислотой продукт, а именно 2-(5-тетразолил)-N-(2,3-ксилил)анилин, выпадает в осадок, его отфильтровывают и перекристаллизовывают из водного спирта. Он плавится при 203,5-205,5°С.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных тетразола | 1970 |
|
SU497775A3 |
| СПОСОБ ПОЛУЧЕНИЯ АРИЛОКСИОКСИПРОПИЛЕН-ПИПЕРАЗИНИЛАЦЕТАНИЛИДОВ, ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫХ СЛОЖНЫХ ЭФИРОВ, ИЛИ КИСЛОТНОАДДИТИВНЫХ СОЛЕЙ | 1984 |
|
RU2071471C1 |
| ПРОИЗВОДНЫЕ ПИПЕРАЗИНА И ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СЛОЖНЫЕ ЭФИРЫ И КИСЛОТНО-АДДИТИВНЫЕ СОЛИ | 1991 |
|
RU2083570C1 |
| ПРОИЗВОДНЫЕ 1-АРИЛПИРРОЛОВ, ИНСЕКТОАКАРИЦИДОНЕМАТОЦИДНАЯ КОМПОЗИЦИЯ И СПОСОБ БОРЬБЫ С НАСЕКОМЫМИ | 1991 |
|
RU2092479C1 |
| ПРОИЗВОДНЫЕ САХАРИНА ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМАЯ АДДИТИВНАЯ СОЛЬ КИСЛОТЫ ИЛИ ОСНОВАНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ПРОЯВЛЯЮЩАЯ АКТИВНОСТЬ ИНГИБИТОРА ЭЛАСТАЗЫ | 1992 |
|
RU2114835C1 |
| СПОСОБ ЛЕЧЕНИЯ ВОСПАЛЕНИЯ ИЛИ СВЯЗАННОГО С ВОСПАЛЕНИЕМ ЗАБОЛЕВАНИЯ У СОБАК | 1996 |
|
RU2253456C2 |
| ПИРАЗОЛИЛЗАМЕЩЕННЫЙ БЕНЗОЛСУЛЬФОНАМИД ИЛИ ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМАЯ СОЛЬ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЛЕЧЕНИЯ ОТ ВОСПАЛЕНИЯ ИЛИ СВЯЗАННОГО С ВОСПАЛЕНИЕМ ЗАБОЛЕВАНИЯ | 1994 |
|
RU2139281C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕНИЦИЛЛИНОВ | 1971 |
|
SU307568A1 |
| АМИДЫ ИЗОТИАЗОЛКАРБОНОВОЙ КИСЛОТЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1998 |
|
RU2214403C2 |
| ПИРАЗОЛЬНЫЕ КАРБОКСАНИЛИДЫ И СРЕДСТВА ДЛЯ БОРЬБЫ С БАКТЕРИЯМИ И ГРИБАМИ НА ИХ ОСНОВЕ | 1999 |
|
RU2240314C2 |
1. Способ получения 2-(5-тетразолил)-N-(замещенный фенил)анилинов общей формулы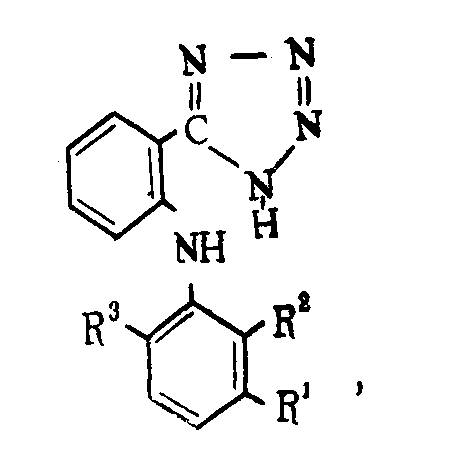
где R1 - хлор, бром, йод, фтор, трифторметил, окисленный или сернистый трифторметил, (низший)алкил, (низший)окисленный алкил, нитро-, метилсульфонил, ди(низший)алкил-амино- или (низший)сернистый алкил; R2 и R3 - водород, хлор, бром, йод, фтор, трифторметил, окисленный или сернистый трифторметил, (низший)-алкил, (низший)окисленный алкил, нитро-, метилсульфонил ди(низший)алкиламино- или (низший)сернистый алкил, но R2 водород только тогда, когда R3 также водород, отличающийся тем, что, 2-циано-N-(замещенный фенил)анилины обрабатывают азидом натрия, калия, лития, алюминия, аммония или замещенного аммония в среде инертного органического растворителя при 80-140°С.
2. Способ по п. 1, отличающийся тем, что процесс ведут в присутствии в качестве катализатора кислоты Льюиса, например хлорида аммония или лития.
Авторы
Даты
1968-07-03—Публикация
1966-06-14—Подача