Изобретение относится к новому способу получения N-1,1,1-замещенных метилазолов, которые обладают биологически активным действием и могут найти применение в качестве лекарственных .препаратов. Описывается способ получения N-1,1,1-замещенных метилазолов общей формулы I A-C-D А, где А означает неразветвленный или разветвленный алкил с числом атомов углерода от 1 до 5, циклопропил, адамант-1-ил, фенил, нафтил, которые отнократно или многократно могут быть замещены галогеном, алкилом с числам атомов углерода от 1 до 4, алкоксигрулпой с одним или двумя атомами углерода, метилтиогруппой, трифторметилом, окси-, фенилоксигруппой, метилсульфонилом , карбоксилом, метоксикарбонилом, циано-, нитро-, амино- и диметиламиногруппой; В - фенил, который может быть замещен галогеном, метилом, метоксилом, метилтио-, диметиламино-, нитро-, фенилоксигруппой, а так же означает 2-фурил, 2-тиенил, 1-метилимидазолил-(2), 3-метил-1,2-оксазолш -(5), 5метил-1,2-оксазолил-(3) или 2-пиридинил, 3пиридинил,4-пиридинил; А и В вместе означают циклическую систему формулы II где Y означает -(СН2)2, , О, S, D-фенил, который может быть замещен галогеном, метилом, метилтиогруппой, трифторметилом, алкоксикарбонил, содержащий в алкоксильной группе 1-2 атома углерода, алкоксикарбонилалкил, имеющий в алкоксильной и алкильной группе от 1 до 2 атомов углерода, Е - атом азота, -СИ-группа, G - атом азота, -СИ-группа; М - метил, фенил, атом водорода; /и - 1, 2, заключающийся в том, что тионилазолид обП1,ей формулы III где Е, G, Л и т имеют вышеприведенные значения подвергают взаимодейетвию с карбинолом общей формулы IV л-(;-в . ОН i где А, В и D имеют вышеприведенные значения, с поеледуюш,им выделением целевого продукта извеетным снособом. Тионилазолиды общей формулы III очень чувствительны к влаге, поэтому их целесообразно не выделять, а сразу использовать для реакции с карбинолами общей формулы IV. В качестве разбавителя могут быть применены хорошо высушенные, инертные для реакции органические растворители. ПодходящиМИ являются, например, алифатические или ароматические углеводороды, имеющие темпсратуру кипения приблизительно 60-120С, например петролейный эфир, бензол, толуол, а также нитрилы, например ацетонитрил, низшие алифатические кетоны, например ацетон, и диалкилэфир, например диэтилэфир. Так}ке могут быть использованы нитрометан, диметилформамид и тетрагидрофуран. Особенно предпочтительным растворителем является ацетонитрил. Температура реакции может быть варьирована в пределах от -20 до + 150°С, лучше всего от О до 80°С, особенно от О до 50°С. При проведении нроцесса предлагаемым способом исходные материалы применяют предпочтительно в молярных соотношениях 1:1. Последовательность введения реакционных компонентов не играет никакой роли для проведения реакции. Продолжительность реакции составляет приблизительно от 3 до 25 час. Продукт реакции выпадает - в зависимости от выбора растворителя - носле закончившейся реакции, и может быть выделен обычными методами. Пример 1. К-1,1,1-трифенилметил-1,2,4триазол. 27,6 г (0,4 моль) 1,2,4-триазола суспендируют в 300 мл ацетонитрила и каплями добавляют 11,9 г (0,1 моль) тионилхлорида, выделившийся триазолгидрохлорид удаляют фильтрованием. Фильтрат разбавляют раствором из 25 г (0,1 моль) тритилкарбинола в 200 мл ацетонитрила, и реакционную смесь нагревают с обратным холодильником. Введением в воду охлажденного до 20°С раствора получают 28,7 г (92% от теоретического) N1,1,1-трифенилметил-1,2,4-триазола с т. пл. 208-21 ГС. Пример 2. (2-Н-мет-илимидазолил1-(2 -метилфенил)-1-фенил -метилимидазол. 27,2 г (0,4 моль) имидазола растворяют в 300 мл ацетонитрила и каплями добавляют 11,9 г (0,1 моль) тионилхлорида, выделившийся имидазолгидрохлорид удаляют фильтрованием. Фильтрат разбавляют раствором нз 1-(2-1 -метилимидазол)-1 - (2 - метилфенил)-бензилового снирта в 300 мл ацетонитрила, и реакционную смесь нагревают с обратным холодильником до окончания выделения SO2. Посредством сгущения раствора нрнблизительпо до 1/10 первоначального объема получают 15,2 г (50% от теоретического). (2-N-мeтилимидaзoлил) - 1-(2 - метилфенил)- -фенил -метилимидазола с т. пл. 186°С. П р и м е р 3. Фенил-2-изопропилфепил-2-пиридилимидазол-1-метан. 15,0 г (0,05 моль) фенил-2-изопропилфенил2-пиридил-карбинола (т. пл. ) разбавляют раствором из 0,06 моль тионилдиимидазола в 100 мл ацетонитрила и нагревают с обратным холодильником в течение 2 час. Затем сгущают, поглощают остаток метилхлоридом, встряхивают многократно с водой, высушивают органическую фазу и сгущают раствор метиленхлорида. Остаток кристаллизуют носле растирания с эфиром. Получают таким образом 14,5 г (82% от теоретического) фенил-2-изопропилфенил - 2 - пиридилимидазол1-илметана с т. пл. 162-165°С. Пример 4. Циклопропилдифенилимидазол1-илметан. 22,4 г (0,1 моль) циклопропилдифепилкарбинола разбавляют раствором из 0,15 моль свежеполученного тионилдиимидазола в 200 мл абсолютного ацетонитрила и в течение 2 час нагревают с обратным холодильником. Затем сгущают, поглощают остаток метиленхлоридом многократно извлекают встряхиванием с водой, высушивают органическую фазу сульфатом натрия и сгущают раствор метиленхлорида. Остаток растирают с эфиром и кристаллизируют. Получают таким образом 19,4 г (71% теоретического) циклопропилдифенилимидазол-1-илметапа с т. пл. 107- 109°С. Пример 5. Фенил-З-нитрофенил-2-ииридилимидазол-1-ил метан. Из 32,5 г (0,48 моль) имидазола, 14,3 г (0,12 моль) тионилхлорида в 150 мл абсолютного тетрагидрофурана при температуре -5°С приготовляют раствор 0,12 моль тионилдиимидазола, отсасывают выпавший .имидазолгидрохлорид и добавляют в фильтрат 30,6 г (0,1 моль) фенил-З-нитрофеиил-2-ниридилкарбинола. Образовавшийся раствор нагревают с обратным холодильником в течение 3- 4 час, сгущают, разбавляют остаток водой и отсасывают. Получают 35,1 г (98% от теоретического) фенил-З-нитрофенил-2-пиридилимидазол-1-илметапа с т. пл. 145-150°С. Перекристаллизация из ацетонитрила дает 30,8 г чистого продукта е т. пл. 166°С. Аналогичным образом могут быть получепы соединения, приведенные ниже. СоединениеТочка плавления, °С 1-(Трифенилметил) - 2-метилимидазол225
1 - (Трифенилметил) - 2,4диметилимидазол
1 - (Трифенилметил) - 4,5дифенилимидазол
-(п - Хлорфенилдифенил|метил)-имидазол
-(п - ФторфенилДифенилметил)-имидазол
1 - (и Толилдифеыилметил)-имидазол
1 - о - Хлорфенилдифенилметил-имидазол
1-{м - Хлорфенилдифенилметил)-имидазол
1-(п - Бромфенилдифенилметил)-имидазол
1-(о - Фторфенилдифенилметил)-имидазол
1-(м - Фторфенилдифенилметил)-имидазол
1-(п - Нитрофенилдифенилметил)-имидазол
-(м - Трифторметилфенилдифенилметил) - имидазол
1-(п - Цианфенилдифенилметил)-имидазол
1-(о - МетоксифеНИлдифенилметил)-имидазол
-(п - Метилтиофенилдифенилметил)-нмидазол
1-(п - Фторфепилдифенилметил) -2-метилимидазол
1-(п-Фторфенил - п - хлорфенилфенилметил)-ймидазол
1-(я-Хлорфенил - м - фторфенил фенил метил)-имидазол
1-(л-Хлор - м - нитрофенилдифеиилметил) - имидазол
1-(я-Бромфенил - п - хлорфенилфенилметил)-имидазол
1-(л( - Цианфенилдифенилметил)-имидазол
-{м - Нитрофенилдифенилметил)--имидазол
- (м - Аминофенилдифенилметил)-имидазол
1-(п-Фторфенил - п - диметиламинофенилфенилметил)-имидазол
1-(п - Диметиламинодифенилметил)-имидазол
1-(«-Хлорфенил - п - нитрофенилфенилмети л ) имядазол
1 - (Трисфенилметил)-1,2,4триазол
1-(о - Хлорфенилдифеиилметил)-1,2,4-триазол
- Метилтиофенил-5 (3 - метил) - изоксазо6
лилфсннлметнл - 1,2,4триазол94-97
1- 4-Метилтиофенил - (5 - метил) - изоксазолилфенил.метил - 1,2,4триазол116-117
1- 4-Хлорфеиил - 3 - (5 метил) - изоксазолилфенилметил - 1,2,4 - триазол104-106
1- 4-Фторфенил - (3 метил) - изоксазолилфенилметил - 1,2,4 - триазол127-128
- 4-трет - Бутилфенил-2(1 -метил) - имидазолилфенилметил -имидазол130
1- 3-Л етилфенил - (1 метил) - имидазолилфеиилметил -имидазол120
1 - (.1/ - Толилдифенилметил) -нмилазолМасло
1 - (о - Толилдифенилметнл)-имидазол128-129
1-(4 - Карбометоксифенилдифеинлметил) - имидазол164
1-(2 - Этилфенилдифенилметил)-имидазол137-140
1-(2 - Изопроиилфенилдифеиил.метил) -имидазол.Масло
1-(2,6 - Дихлорфеинлдифеиилметил) -имидазол168-169
1-(3 - Карбометоксифеиилдифенилметил) -имидазол90
(гидрохлорид)
1-(3 - Карбоксифеиилдифеи и л м е т и л) - и м и д а з о л
1-(4 - Карбоксифеиилдифенилметил) -имидазол87-96
1-(Бис - 4 - метоксифеинлкарбометоксиметил) -имидазол130-131
1 - (Дифеинлкарбометоксиметил)-имидазол35
3- (З-Феиил-4-карбэтокси) -пеит-3-илимидазолМасло
1 - (2 - Тиеиилдифенилметил) -имидазол178-179
1- Дифеинл - 3 - (5-метил) - изоксазолилметил -имидазол149-150
1- Дифеиил - 2 - (1-метил) - имидазолилметил -имидазол200
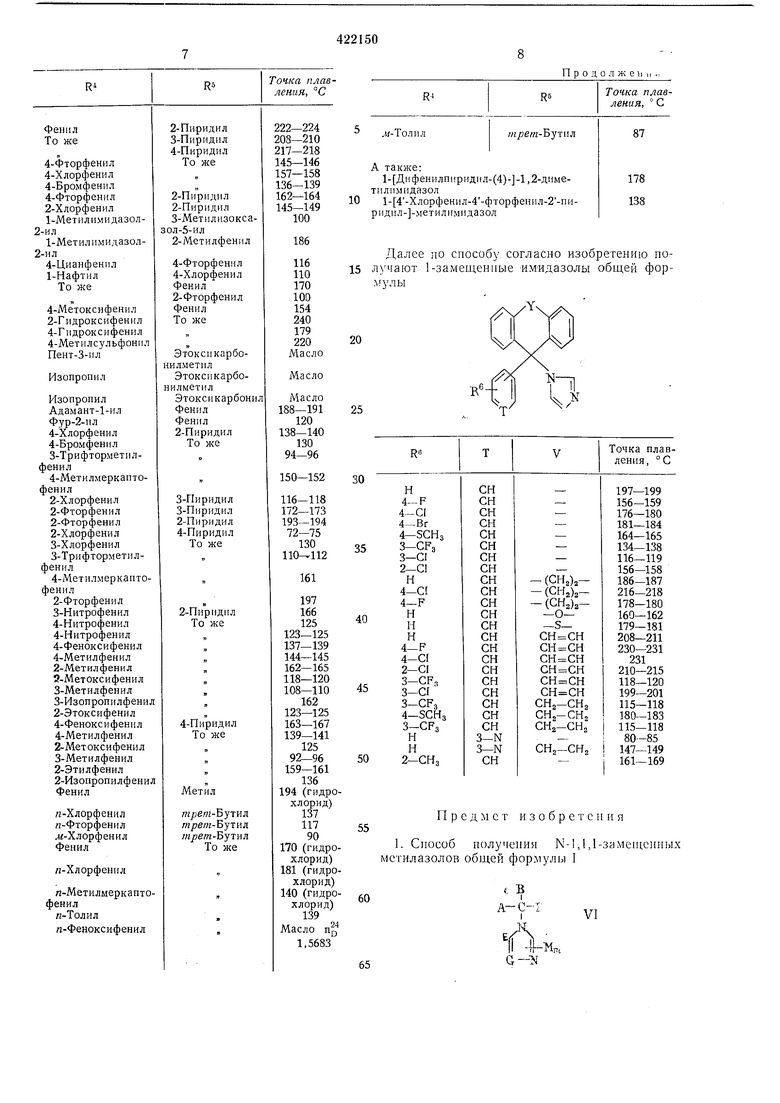
Аналогичным образом иолучают соединения общей формулых
где А- неразветвленный или разветвленный алкил с 1-5 атомами углерода, циклопропил, адамант-1-ил; фенил, нафтил, которые могут быть замещены однократно или многократно атомом галогена, алкилом, содержащим 1 - 4 атома углерода, алкоксилом с 1--2 атомами углерода, трифторметилом, метилтио-, окси-, фенилоксигрунпой, метилсульфонилом, карбоксилом, метоксикарбонилом, циано-, нитро-, амино- и диметиламиногруппой;
В -фенил, который может быть замещен галогеном, метилом, метоксилом, метилтио-, диметилам ино-, нитро-, фенилокситруппой, а также означает 2-фурил, 2-тиенил, 1-метилимидазолил-(2), 3-метил-1,2-оксазолил-(5), 5метил-1,2-оксазолил-(3), или 2-п:иридинИЛ, 3пиридинил, 4-пиридинил;
А и В вместе означают циклическую систему формулы II
II
где Y означает -(СН2)2-, -СН СН-, О, S;
D - фенил, который может быть замещен галогеном, метилом, метилтиогруппой, трифторметилом, алкоксикарбонил, содержащий в алкоксильной группе 1-2 атома углерода, алкоксикарбонилалкил, имеющий в алкоксильной и алкильной группе от 1 до 2 атомов углерода;
Е означает атом азота, -СН-группу;
G означает атом азота, -СН-грул:пу;
I
М Означает атом водорода, метил, фенил,
т-1, 2,
отличающийся тем, что тионилазолид общей формулы III
Чи.
Т-4-l -S-l -Ь-Мл; III
ш
де Е, G, М и т имеют вышеприведенные значения,
подвергают взаимодействию с карбинолом общей формулы IV
В
А-С-Б он Ш
где А, В, D имеют выщеприведенные значения,
с последующим выделением целевого продукта известным способом.
2.Способ по п. 1, отличающийся тем, что реакцию проводят в среде инертного органического растворителя.
3.Способ по пп. 1 и 2, отличающийся тем, что реакцию проводят при температуре
от-20 до -fl50°C.


| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ СУЛЬФОНИЛАМИНОКАРБОНИЛТРИАЗОЛИНОНА И ИХ СОЛИ, ИСХОДНЫЕ СОЕДИНЕНИЯ ДЛЯ ИХ ПОЛУЧЕНИЯ И ГЕРБИЦИДНОЕ СРЕДСТВО НА ИХ ОСНОВЕ | 1993 |
|
RU2125559C1 |
| ПРОИЗВОДНЫЕ ЦИКЛОАЛКАНО-ПИРИДИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ | 1997 |
|
RU2194698C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1,3,3-ТРЕХЗАМЕ1ЦЕННЫХ 3-АЗОЛИЛПРОПИНОВ | 1971 |
|
SU430551A1 |
| ПРОИЗВОДНЫЕ ХИНОЛИН-2-ИЛ-МЕТОКСИБЕНЗИЛГИДРОКСИМОЧЕВИНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И 4-(ХИНОЛИН-2-ИЛ-МЕТОКСИ)ФЕНИЛ-ЦИКЛОАЛКИЛКЕТОН В КАЧЕСТВЕ ИСХОДНОГО СОЕДИНЕНИЯ ДЛЯ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ХИНОЛИН-2-ИЛ-МЕТОКСИБЕНЗИЛГИДРОКСИМОЧЕВИНЫ | 1992 |
|
RU2048466C1 |
| 2,4,5-ТРИЗАМЕЩЕННЫЕ ФЕНИЛКЕТОЕНОЛЫ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ ДЛЯ ИХ ПОЛУЧЕНИЯ, СПОСОБ И СРЕДСТВО ДЛЯ БОРЬБЫ С НАСЕКОМЫМИ И ПАУКООБРАЗНЫМИ НА ИХ ОСНОВЕ | 1996 |
|
RU2195449C2 |
| АМИДЫ АЛКОКСИМИНОУКСУСНОЙ КИСЛОТЫ, ФУНГИЦИДНОЕ СРЕДСТВО НА ИХ ОСНОВЕ И СПОСОБ БОРЬБЫ С ГРИБКОВЫМИ ЗАБОЛЕВАНИЯМИ РАСТЕНИЙ | 1996 |
|
RU2167853C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИКЛИЧЕСКИХ АМИДИНОЕ | 1973 |
|
SU382284A1 |
| ЗАМЕЩЕННЫЕ ИМИНОАЗИНЫ, ХЛОРАЗИНИЕВЫЕ СОЕДИНЕНИЯ, СОЕДИНЕНИЯ ПИРИДИНОНА И ГЕРБИЦИДНОЕ СРЕДСТВО НА ИХ ОСНОВЕ | 2001 |
|
RU2265596C9 |
| ЦИКЛИЧЕСКИЕ АЗОТСОДЕРЖАЩИЕ ПРОИЗВОДНЫЕ, СМЕСЬ ИХ ИЗОМЕРОВ, ОТДЕЛЬНЫЕ ИЗОМЕРЫ ИЛИ ИХ СОЛИ | 1994 |
|
RU2126002C1 |
| АЗОТСОДЕРЖАЩИЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ В ВИДЕ РАЦЕМАТА ИЛИ ОТДЕЛЬНЫХ ЭНАНТИОМЕРОВ, ЯВЛЯЮЩИЕСЯ ИНГИБИТОРАМИ БИОСИНТЕЗА ЛЕЙКОТРИЕНА | 1992 |
|
RU2080321C1 |



Даты
1974-03-30—Публикация
1971-02-16—Подача