(54) СПОСОБ ВЫДЕЛЕНИЯ УГЛЕВОДОРОДОВ,
ИМЕЮЩИХ ПОДВИЖНЫЕ АТОМЫ ВОДОРОДА,
ИЗ УГЛЕВОДОРОДНЫХ СМЕСЕЙ дится в равновесии с жидкой фазой, в соотношении, зависящем от модификации концентраций неметаллнзированных углеводородов в жидкой фазе после указанного контакта. Нужно отметить, что, в частности, более сильная 5 металлизация более кислых углеводородов приводит к увеличению относительной концентрации этих углеводородов в жидкой фазе по отношению к менее кислым углеводородам, следовательно, происходит соответствующее ю обеднение паровой фазы, равновесной с жидкой фазой, этим более кислым углеводородом и, другими словами, обогащение паровой фазы менее кислым углеводородом. Если повторять эти операции контактиро- is вания, а именно, осуществить непрерывный противоток через несколько тарелок колонны для дистилляции, потребуется весьма мало тарелок для получения паровой фазы, свободной от более кислого или более металлизиро- 20 ванного углеводорода, в условиях, полностью аналогичных тем, которые предусматриваются при фракционной дистилляции смеси углеводорода с явно различными летучестями. Рассматриваемые металлоорганические со- 25 единения представляют собой продукты замещения этим-и металлами подвижных атомов водорода в углеводородах. Для этих целей пригодны щелочные металлы литий, натрий и калий. Эти металлоорганические соединения могут быть получены из любых соединений, имеющих подвижные водороды. Хорошие результаты получены, например, с третичныМИ ароматическими аминами, такими как N-диметил- 35 анилин, которые имеют в своих ядрах атомы водорода, способные замещаться атомами металлов, или с такими ароматическими углеводородами, как изопропилбензол, изобутилбензол, 1,2,4-триметилбензол, 1,2,3-триметил- о бензол, 1,3,5-триметилбензОЛ, и другие полиалкилбензолы. Реакция может быть проведена или в жидкой гомогенной фазе, или в массе твердого металлоорганического соединения; следова- д тельно, металлоорганические соединения могут быть или полностью или частично растворимы в жидкой реакционной среде. Таким образом, в колонне для дистилляции реакция трансметаллизации происходит на Q тарелках или в среде жидкой фазы, если реакцию проводят в гомогенных условиях, или частично или полностью в среде твердой фазы, если реакцию проводят в гетерогенных условиях. В последнем случае тонко измельчен- 55 ное твердое производное поддерживают в виде суспензии в жидкости с помощью турбулентности, создаваемой на тарелках для улучшения контакта пар - жидкость. Реакцию трансметаллизации выгодно про- QQ водить в присутствии основных катализаторов. которые благоприятствуют, а точнее ускоряют эту реакцию. Эти катализаторы должны быть стойкими к металлоорганическим соединениям. Первую группу этих катализаторов об- 65 30 разуют третичные амины, у которых группы, фиксированные на атоме азота, являются алкильными или циклоалкильнымя. Нетретичные амины не могут быть использованы потому, что водород, связанный непосредственно с атомом азота, всегда будет более -подвижным, чем водороды разделяемых углеводородов, так что они будут подвергаться металлизации предпочтительнее, чем углеводороды. В качестве третичных аминов, пригодных для этих целей, можно указать, например, триэтиламин, трилролиламин, трибутиламин, I,N-димeтилциклoгeкcилaмин, или такие мостиковые амины, как триэтилендиамин или хинуклидин. Однако, когда хотят работать в гомогенной жидкой фазе, предпочтительными являются основные катализаторы второй группы, которые в это же время способны образовывать хелатные соединения с атомами металлов металлоорганического соединения. Эти основные катализаторы представляют собой третичные ди- или полиамины, у которых группы, фиксированные на атомах азота, являются алкильными или циклоалкильными группами, и у которых по крайней мере два из их атомов азота достаточно близко расположены по отношению друг к другу, чтобы обеспечить образование хелатов. Эти третичные диамины или полиамины позволяют ускорить реакции, намного увеличить растворимость металлоорганических соединений и регулировать протекание этих реакций. Другие основания, хелатирующие или нет с электронным дублетом, который может ассоциироваться с металлоорганическими соединениями, которые содержат кислород (простые эфиры) или фосфор (фосфины), не могут быть использованы, потому что они разрушаются металлоорганическими соединениями, В качестве примеров можно упомянуть хелатирующие диамяны, представляющие собой следующие продукты: Ы,Ы,|Ы,Ы-тетраалкилэтилендиамин; М ,Ы,М ,М-тетраалкилПропилендиамнн; Гч1,Ы,,Ы-тетраалкил-1,2-диаминоциклогексан; алкильными группами могут являться метильная, этильная, пропильная или бутильная. Кроме того, хелатирующие полиам-ины, соответствующие формуле R-(N-R), где X- 1, 2, 3, 4, R и R являются метильньши, этильньгми, профильными, изопропильными, н-бутильнымИ, гбутильными, третбутильными или циклогексильными груп пами. позволяют получать хорошие результаты, Можно, например, использовать следующие полиамины. (СНз) 2N-С2Н4-N (СНз) -С2Н4-N (СНз) 2, (СНз) sN-C2H4 N (СНз)-С2Н4-N (СНз)-С2Н4-М(СНз)2,
которые легко получаются при метилировании диэтилентриамина и триэтилентетрами-па.
Особенно хороплие результаты получены с N,,N - тетраметил-1,2-диамипоц.иклогексаном, который как хелатирующий агент сравним с Ы,Ы,Н,Ы-тетраметилендиамином, но летучесть которого меньше, а химическая стабильность выше. Металлоо-рганические соединения, хелатированные этим диамином, хорошо растворимы в М,Н-диметиламине, и металлизация может быть проведена в гомогенной фазе. К,Н,Ы,М-тетраметил-1,2-диаминоциклогексан может быть получен при метилировании 1,2-диаминоциклогексана в формалине или в муравьиной кислоте в соответствии с методикой Эсшвейлера и Кларка.
Также выгодно использовать растворитель, который позволяет или облегчить растворенпе (полное или частичное) металлоорганического соединения, или облегчить его перемеш,ение в виде тонко измельченной суспензии.
Например, растворитель может представлять собой мало кислые ароматические углеводороды, такие как кумол, третбутилбензол, изобутилбензол, диизопропиленбензол. Одним из предпочтительных растворителей является третбутилбензол, цепь которого не может быть металлизирована. В нефтехимической промышленности можно также использовать фракции газойля.
В тех случаях, когда заинтересованы в большей растворимости металлоорганического соединения, в качестве растворителя также могут быть использованы для полярных сред и/или более растворяюш;ихся сред такие растворители, как М,М-диметилавилин, М,Ы-диметилциклогексиламин или любой другой третичный амин. Фракционную дистилляцию предпочтительно проводить в присутствии органических производных металлов II и III групп. Предпочтительными соединениями, очевидно, являются соединения общей формулы Mg(R2), Zn(R2) или А1(Нз), у которых R представляет собой алкильную или арильную группу. Известно, что эти продукты позволяют увеличить растворимость огранических соединений щелочных металлов, снизить тенденцию третичных аминоБ к разложению с образованием двойных связей, уменьшить скорость реакций обмена водород - щелочной металл тем более, чем выше соотношение Mg, Zn, Al: Na.
Активные центры (карбанионы), следовательно, являются менее реакционноспособными в присутствии симметричных магнийорганических соединений и это объясняет снижение тенденции третичных аминов к разложению с образованием двойных связей.
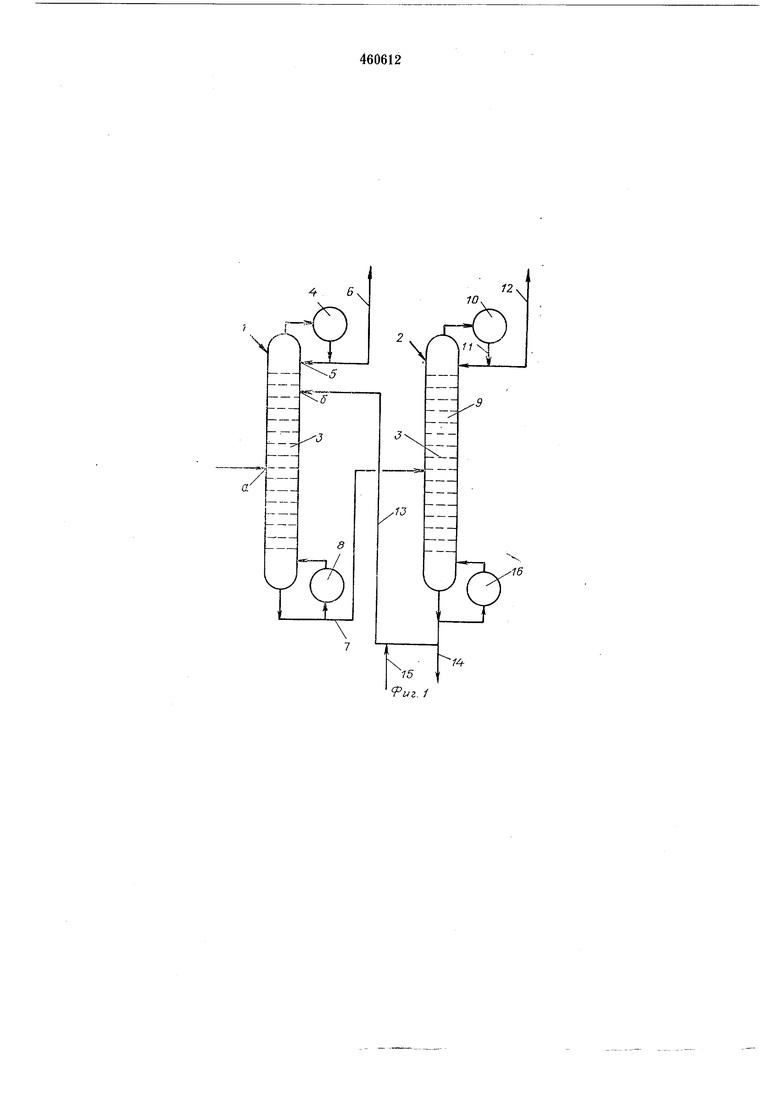
На фиг. 1 приведен вариант схемы осуществления процесса разделения двух углеводородов RiH и RsH, из которых по крайней мере один обладает подвижными водородами, исходя из их смеси, с применением металлоорганического соединения RsNa, производного с подвижными водородами RsH, точка кипения которого выше, чем у этих углеводородов
RiH и R2H, и который менее реакционноспособен по отношению к натрию, чем оба углеводорода RiH и R2H.
Рассмотрим случай, когда, например, RiH являются параксилолом, R2H-метаксилолом, КзН, например, является диметиланилином, RsNa получают при замещении атомов водорода в ядре на натрий. Однако RiH также может означать, например, н-гептан, R2H-тoлyoл, RsH может также быть другим третичным ароматическим амином или таким ароматическим углеводородом, как кумол, изобутилбензол и т. п. Наконец, натдийорганическое соединение
может быть замещено литийорганическим соединением RsLi или калийорганическпм соединением RsK, или их смесью.
Указанное разделение осуществляют на установке, которая состоит из двух дистилляционных колон 1 и 2, тарелкп 3 которых схематически представлены пунктирными горизонтальными линиями (см. фиг. 1).
В колонну 1 соответственно загружают: на уровне точки ввода а разделяемую смесь углеводородов RiH и R2H; на уровне точки ввода б - фазу, содержащую металлоорганическое соединение RsNa, растворитель, состоящий из одного из названных соединений или из избытка соединений RsH, хелатпрующего
агента, и при случае - стабилизирующего металлоорганического соединения указанного типа.
Тогда на тарелках, расположенных между точками ввода а и б соответственно, смесь
разделяемых углеводородов п фаза, содержащая металлоорганическое соединение, находится в равновесии, описываемом тремя химическими уравнениями:
к,
О) 1-х-,
R3Na + RiH:J:R3H + RiNa
(2) (3)
R3Na + R,Hl|:R3H+R,Na
R,Na-f R,H4::R,H + R,Na
45
Таким образом, можно определить относительную кислотность углеводородов по отношению констант равновесия таких реакций, как (1) и (2). Например, R2H является более кислым, чем RiH, тогда Ki больше, чем /Ci, и
г
Кз -- больще единицы. Так, метаксилол
является более кислым, чем параксилол, который имеет ту же кислотность, что и N,Nдиметиланилин. М ,М-диметиланилин отдает почти весь натрий из своего металлоорганического соединения обоим ксилолам, предпочтительнее метаисилолу.
Натриевые ксилолы, хелатированные ди амином, растворимы в Н,Н-димет11ланилине (который в данном случае играет роль и RaH и растворителя); эти хелаты не летучк и концентрация ксилолов в газовой фазе является
только функцией концентраций ненатрпевьи ксилолов в жидкой фазе. Пар аксилол в меньшей степени соединен с металлом, чем метаксилол, его концеитрация в газовой фазе будет более высокой, чем это можно предвидеть из закона Рауля; этот закон применим только к концентрация неметаллизированных ксилолов. Таким образом, модифицируя общую относительную летучесть пары параметаксилол, можно разделить смесь на составляющие. Точка ввода а смеси ксилола, таким образом, иозволяет определить, как при любой обычной дистилляции, зону обогащения и зону истощения колонны 1. Точка ввода б может быть расположена в нескольких тарелках от верха колонны 1, что достаточно для рекуперации малолетучих соединений КзН. Параксилол очень высокой степени чистоты конденсируется в верхней части колонны в конденсаторе 4. Часть конденсата возвращают в виде флегмы по трубопроводу 5, другую часть собирают в трубопровод 6. Смесь, полученная в кубе колонны 1, не содержит параксилола, и натрий распределяется между метаксилолом и М ,Ы-диметиланилином в соответствии с уравнением (2). Эту смесь подают через промежуточный трубопровод 7 во вторую дистилляционную колонну 2 на соответствующую высоту, часть этой смеси отбирают, испаряют в ребойлере 8 и повторно инжектирут в куб колонны 1. В зоне истощения колонны 2 происходит обратимая реакция (2), равновесие смещено влево при испарении метаксилола. Зона обогащения 9 используется только для задерживания паров амина, растворителя и RsH. Таким образом, в верхней части колонны 2 получают метаксилол высокой степени чистоты, часть которого возвращают в виде флегмы после конденсации в конденсаторе 10 по промежуточному трубопроводу 11. Другую часть отбирают по трубопроводу 12. Смесь, получаемая в кубе колонны, содержит составляющие, введенные ранее в колонну 1, т. е. в принципе смесь может быть повторно использована и рециклизована в точку ввода б колонны 1 по трубопроводу 13. Повторное использование смеси металлоорганическое соединение щелочного металла+ растворитель- основной катализатор+стабилизирующее металлоорганическое соединение не может быть полным, так как часть основного катализатора (амина) присоединяется к металлоорганическому соединение и образует побочные без каталитического или растворяющего действия; часть металлоорганического соединения присоединяется к следам воды или сернистых продуктов, имеющихся в смеси ксилолов. Следовательно, для очистки необходимо по трубопроводу 14 непрерывно сцеживать часть смеси из колонны 2 и непрерывно вводить по трубопроводу 15 такое же количество незагрязненной смеси. Сцеженную часть периодически обрабатывают перегонкой в вакууме для рекуперации растворителя без разложения основного катализатора. После обработки водой или спиртом углеводород RsH рекуперируют, а натрий, содержащийся в сливе, может быть рекуперирован в виде соды. Для уменьшения до минимума количества разложенного амина применяют три методи. ки: 1)проводят две дистилляции в колоннах 1 и 2 при пониженном давлении, чтобы иметь возможность работать при температуре, наиболее низкой, но явно ограничить потерю загрузки на тарелках; 2)используют по возможности более стабильный амин (основной катализатор), т. е. более стойкий к действию металлоорганических соединений. Интересные результаты были получены при использовании N,N,N,iN-TeTраметил-1,2-диаминоциклогексана; этот хелатирующий амин обладает большой растворяющей способностью и позволяет получить большую разделительную возможность при хорошей стойкости к действию натрия. Эта стабильность объясняется тем, что ядро циклогексана металлизируется очень мало, и образование двойной связи между двумя соседними атомами углерода очень замедленно; 3)работают в присутствии стабилизирующего металлоорганического соединения. Предшествующее описание применимо также, например, для разделения н-гептана и толуола. В этом случае RsH (который может быть М,М-диметиланилином или кумолом) имеет промежуточную кислотность между RjH (толуол) и R2H (гептан); кислотность к-гептана (как и всех насыщенных углеводородов) очень мала и константа /(з будет очень большой, так же, как общая относительная летучесть пары н-гептан-толуол, так что число тарелок при дистилляции должно быть очень небольщим. Принцип разделения двух углеводородов RiH и RzH, описанный в применении к фиг. 1, может быть применен к разделению большего числа углеводородов. Например, можно осуществить разделение трех таких углеводородов, как этилбензол, параксилол и метаксилол, в установке, содержащей две единицы такого типа, который представлен на фиг. 1. Легко летучий этилбензол менее реакционноспособен по отношению к натрийорганическим соединениям, чем параксилол. Следовательно, вначале можно осуществить в колонне 1 на первой установке разделение параксилола и этилбензола, с одной стороны, и метаксилола, с другой стороны; смесь параксилол-этилбензол получают в верхней части колонны 1 в царовой фазе, а метаксилол отделяют на второй колонне 2 первой установки, как описано выше. Раздеение параксилола и этилбензола в указанной аровой фазе затем может быть осуществлео после их конденсации во второй из упомяутых установок, после введения конденсироанной смеси в колонну 1 этой второй уста9
новки в точке ввода, аналогичной упомянутой точке а, тогда как разделение производится в условиях, аналогичных тем, что описаны выше для разделения иараКСилола и метаксилола.
При двойном разделении возможно применить различные металлоорганические соединения на первой и второй установках соответственно. Это также относится к растворителям и т. п.
Во многих случаях для поддержания возможно более длительной активности органических соединений щелочных металлов предпочтительно работать при относительно низких температурах, обычно ниже 100°С, дистилляцию, следовательно, проводят при частичном вакууме.
Однако нет необходимости в том, чтобы некоторая часть колонны на фиг. 1 работала при низкой температуре, особенно, если в верхних секциях каждой колонны осуществляется разделение неметаллизированных соединений и ребойлеры 8 и 16 связаны с колоннами 1 и 2.
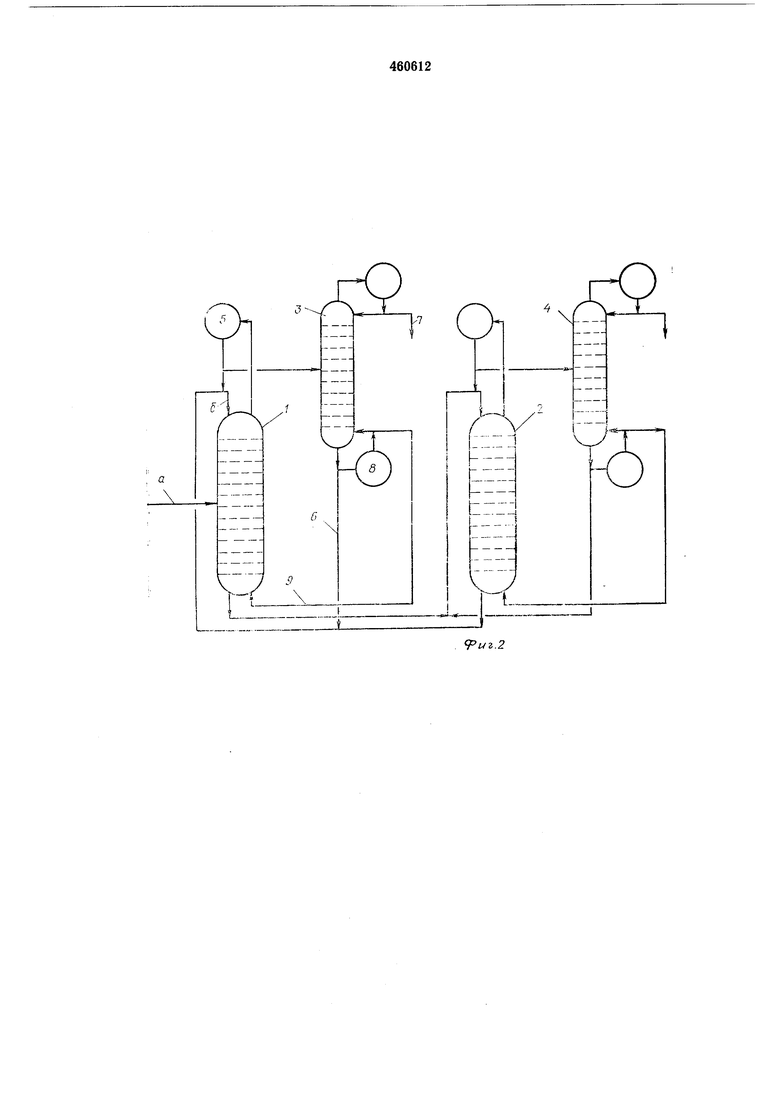
На фиг. 2 представлена схема установки, на которой операцию дистилляции в присутствии металлоорганических соединений осуществляют в колоннах 1 и 2 при частичном вакууме, а операции разделения неметаллизированных соединений-в раздельных колоннах 3 и 4, которые могут работать при атмосферном давлении.
Например, предложено разделять в этих условиях параксилол и метаксилол, смеси, которые содержат их, работая, как описано, или аналогичным образом.
Смесь параксилола и метаксилола подается через точку ввода а колонны 1, фаза, содержащая металлоорганическое соединение, вводится выше уровня тарелок в точку ввода б; жидкую флегму обеспечивают или частью конденсата, выходящего из конденсатора 5 колонны 1, или введением тяжелых продуктов из колонны 3, работающей при атмосферном давлении, через промежуточный трубопровод 6, или из обоих источников сразу.
Конденсат из колонны 1 содержит параксилол, соединенние RaH, высвобожденное из металлоорганического соединения RsNa, и главным образом растворитель. Параксилол более летуч и поэтому легко рекуперируется в 7 при обычной дистилляции в колонне 3, тяжелые продукты вновь натравляют в цикл, как указано выше.
Эта модифицированная установка позволяет, кроме того, при желании, использовать ребойлер 8 колонны 3, для получения пара, необходимого для колонны 1, этот пар подводят к кубу -колонны через промежуточный трубопровод 9. Таким образом, устраняют недостатки, связанные с работой кипятильника, работающего однов1ременно под вакуумом в присутствии соединений, чувствительных к теплу и имеющих тенденцию загрязнять поверхности теплообмена, недостатки, которые увели10
чивают потери металлизированных продуктов. В описанном ранее рассматривается только тот случай, когда соединение НзН, соответствующее металлоорганическому соединению, 5 является менее летучим и менее кислым, чем один из углеводородов разделяемой смеси.
В некоторых случаях, а именно при разделии очень мало летучих ароматических углеводородов, таких как тетраметилбензолы, ди10 этиленбензолы или кумолы, исходят из металлоорганических соединений, соответствующих соединениями КзН, более летучих и более кислых, чем углеводороды RiH и RaH. Кроме того, это остается справедливым также и для 15 углеводородов, более летуч1их, чем ксилолы, которые могут быть разделены с помощью бензилнатрия, производного толуола, которое одновременно является более летучим и более кислым, чем ксилолы.
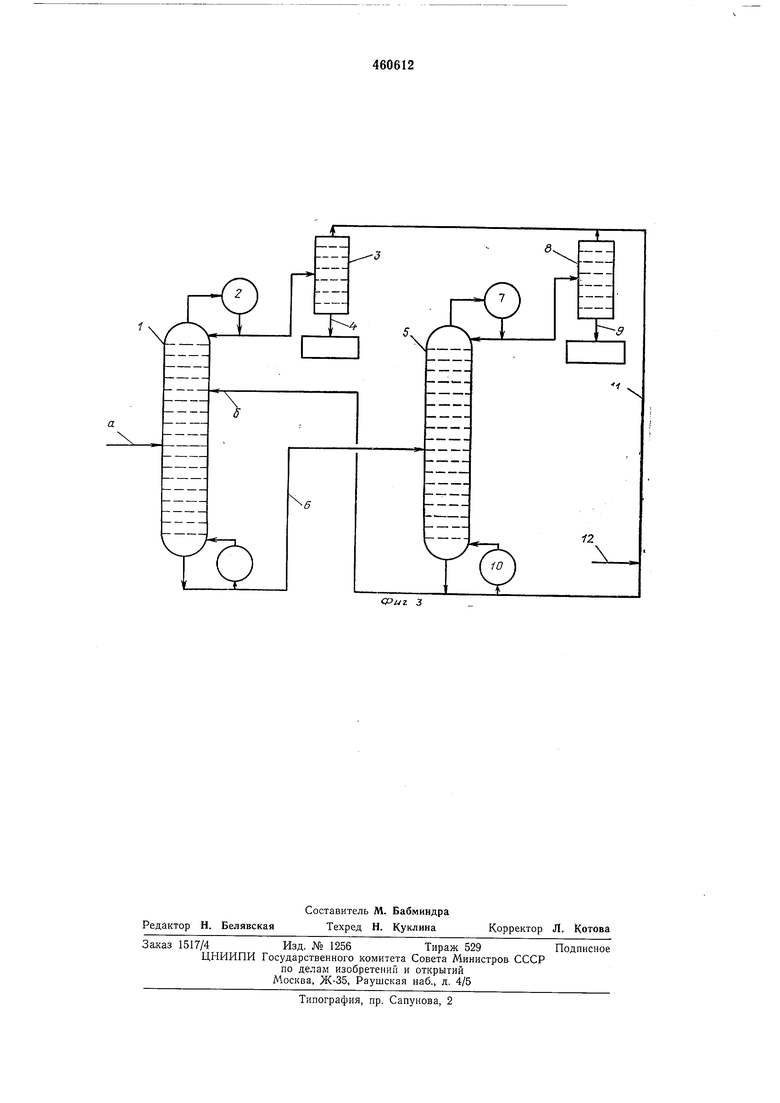
0 На фиг. 3 показана схема установки, в которой может быть осуществлен вариант процесса.
Эта установка состоит из колонны 1, предпочтительно работающей при пониженном 5 давлении, смесь углеводородов и R2H предпочтительно вводят в эту колонну в точка а противотоком фазе, содержащей металлоорганическое соединение, вводимой в точке б в этой же колонне выше точки а. Паро0 вая фаза, получаемая в верхней части колонны 1, содержит соединение RsH и менее кислый углеводород RiH. После конденсации в конденсаторе 2 ее фракционируют, в свою очередь, в отдельной колонне 3, работающей 5 при атмосферном давлении, RiH сцеживают в емкость 4 из куба колонны 3.
Регенерирующая колонна 5 снабжается по промежуточному трубопроводу 6 продуктами, сцеженными из нижней части колонны 1, из 0 ее верхней части выходит паровая фаза, содержащая смесь соединения RsH и другого углеводорода RsH. Эту смесь после конденсации в конденсаторе 7 в свою очередь фракционируют в отдельной колонне 8, работающей при 5 атмосферном давлении; R2H сцеживают в емкость 9 из куба колонны 8.
Регенерации в колонне 5 благоприятствуют введение избытка соединения RsH в куб этой колонны и его относительно высокая кислотность. Можно также упразднить кипятильник 10 в колонне 5 и вводить в виде цара в куб этой колонны такое количество соединения RaH, -которое необходимо для обеспечения функционирования колонны 5, и перевода в 5 паровую фазу всего количества соединения RsH, содержащегося в смеси, вводимой в эту колонну через промежуточный трубопровод 6. Эти количества R2H в виде паров могут подводиться через промежуточный трубопровод 11 В виде головных фракций колонн 3 и 8 и/или определенного источника, условно схематически показанного поз. 12.
В некоторых случаях также подают в обе
основные колонны 1 и 5, в их куб, растворитель в виде фазы для транспортировки метал11
лорганического соединения, тогда как этот растворитель сам по себе обладает -более высокой летучестью, чем разделяемые углеводороды и значительно меньшей кислотностью.
Таким образом, имеется процесс, -который может быть использаван различным образом и который 1позволяет получить важные модификации коэффициентов -распределен1ия, которые обычно устанавливаются между углеводородами в смеси в отсутствии металлоорганических соединений рассматриваемого типа и, следовательно, достигнуть высоких степеней разделения, что крайне важно в случае разделения углеводородов, которые могут иметь летучесть одного и того же порядка.
Коэффициент С распределения смесей двух углеводородов определяется по формуле
-YIY
С х,х
где У - молярная концентрация соединения RiH IB паровой фазе;
УЗ - молярная концентрация соединения R2H в -паровой фазе;
Х - молярная концентрация соединения RiH и в жидкой фазе;
Х - молярная концентрация соединения RsH и RsNa в жидкой фазе.
Две последние концентрации заменены средними Молярными -концентрациями суспензии твердое вещество - жидкость.
В отсутствии органощелоЧНых соединений этот фактор С совпа-дает с относительной летучестью RiH по отношению .
Пример 1. Смешивают 0,05 моля фенилнатрия в смеси 40 см (0,39 моля) Ы,М-диметиланилина и 20 см (0,153 моля) N,;N,N,Nтетраметилэтнлендиамина.
Натрий немедленно распределяется между бензолом И диметила-нилином по равновесию металлизации: диметиланилин несколько более кислый, чем бензол, Находясь гв большей концентрации, отбирает большую часть натрия.
Смесь доводят до 50°С и мгновенно вводят 2 см параксилола и 2 см метаксилола.
Эти два -ксилола, более кислые, чем бензол и диметилакилин, металлизируются предпочтительнее, метаксилол металл изируется в большей степени, чем параксилол.
Поддерживают температуру на уровне 50°С и через 15 Мин после введения ксилола отбирают -при дкстилляциИ в вакуум-е и конденсируют маленькую фракцию, состав которой в значительной мере зависит от состава пара, находящегося в равновесии с жидкостью, находящейся В колбе в момент отбора. ИК-Спектроскопичеоким анализом -этой фракциИ после промывки «подкисленной водой для удаления амина устано-влен следующий относительный состав: параксилола 79%, метаксилола 21%, что соответствует коэффициенту распределения между газовой фазой и жидкой -фазой ,75, или коэффициент распределения очень высок для обычных относительных лету12
честей параксилол/метаксилол при 50°С, который равен (схрт) 50 1,055.
Пример 2. Работают, как в примере 1, изменив только количества добавленных ксилолов, т. е. 4 см метаксилола.
Относительный состав газовой фазы следующий: па-раксилола 62%, метаксилола 38%, что соответствует коэффициенту распределения ,63.
Этот .пример хорошо иллюстрирует, что для определенного количества натрия общий процент замещенного натрием ксилола ниже, когда количество ксилола увеличивается и, следовательно, -коэффициент распределения станавится меньше.
Пример 3. Работают, как в примере 1, но паракоилол заменяют ортоксилолом; следовательно, добавляют в среду для металлизации
2 см метаксилола и 2 см ортоксилола.
Относительные концентрации газовой фазы следующие: метаксилола 61%, ортоксилола 39%, что соответствует коэффициенту распределения ,56.
Эта величина выше равновесной для жидкой -фазы (арт),22 и указывает, таким образом, на то, что в указанных условиях ортоксилол является более кислым, чем метаксилол.
Пример 4. Используют те же условия работы, что и в примере 1, но не добавляют К1,;М,ЫЫ-тетраметилтилендиенина; металлоорганические соединения не растворимы в жидкой фазе и постепенно медленно присоедияяют твердый фенилнатрий. Мгновенно прибавляют 3 см параксилола и 3 см метаксилола.
Данные об изменении коэффициента распределения С в зависимости от увеличения
времени реакции приведены ниже.
Время реакции т, минКоэффициент
распределения С
О1,05
31,12
151.78
602,24
902,44
Возможно намного увеличить скорость данного явления, повышая температуру или используя основные нерастворимые катализаторы.
П-римвр 5. Смешивают 0,05 моля фенилнатрия, 30 см (0,39 моля) Ы,Н-диметиланилина и 80 см (0,58 моля) триэтиламина. Устанавливают температуру 40°С и в один момент вводят: 1 см па-раксилола и 3 см метаксилола.
Как в -примере 4, реакция является гетерогенной li коэффициент распределения между газовой и жидкой фазами очень -близок к единице. Коэффициент распределения между парами И суслензии является функцией времени.
он равен.
13
ремя реакции т, мин
Коэффициент распределения С
О . 1,05 5 15 1,70 1,72 180 1,57
Как можно видеть, скорость реакции больше, чем в предшествующем случае, это свидетельствует о том, что триэтиламин является хорошим основным катализатором реакции.
Пример 6. Этот «ример показывает, что наблюдается уменьшение коэффициента распределения, когда время реакции очень велико. Это уменьшение наблюдалось для гетерогенной реакции, а также для гомогенной реакции.
Смешивают 0,05 моля фенилнатрия, 50 см (0,39 моля) Ы,Ы-диметиланилина и 20 см (0,153 моля) Ы;Н,М ,М -тетраметилендиамина.
Устанавливают температуру на уровне 40°С и мгновенно вводят 2 см параксилола и 2 см метаксилола.
Отгоняют в .вакууме при 40°С ири различных временах реакции. Коэффициент распределения, соответствуюшнй этой гомогенной реакции,составил:
Время реакции тКоэффициент
распределения С
10 мин5,90
30 мин5,92
1час5,65
2час5,86 6 час5,10
24 час4,10
Дезактивация идет тем быстрее, чем выше темлература реакции. Время, необходимое для появления этой дезактивации, однако остается большим, чем время обычного пребыван ия фаз на тарелках колонны дистилляции.
Пример 7. Проводят разделение тройной смеси: параксилол, метаксилол, ортоксилол.
Смешивают 0,05 моля фенилнатрия, 50 см (0,39 моля) М,Ы-диметиланилина и 20 см (0,153 моля) М,М,|М,М-тетраметилэтилендиамина.
Устанавливают температуру 40°С и сразу вводят 2 см параксилола, 2 см метаксилола, 1 см ортоксилол а.
Коэффициент разделения, измеренный для этой реакции в гомогенных условиях, дал следуюш,ие результаты:
Время реакции т, час Коэффициент разделения
С пара/мета мета/орто 12,51,53
181,711,53
Коэффициент разделения мета/орто показывает, что ортоксилол является более кислым, чем метаксилол, как это уже было показано в Примере 3.
Пример 8. Готовят М,Ы;Н,М-тетраметил1,2-диаминоциклогексан и повторяют опыт примера 1 в тех же условиях, но заменяя
14
Ы,Н,М ,-тетраметилэтилендиамина эквивалентным количеством М,Ы,К ,Н-тетраметил ,2-диаминоциклогексана. Полученный коэффициент разделения несколько выше коэффициента разделения примера 1 и равен 3,92.
Затем полученную смесь нагревают 48 час при 80°С; установлено, что коэффициент разделения в пределах ошибки эксперимента равен еще 3,9, что подтверждает очень большую
стабильность Ы,Ы,М ,М-тетраметил-1,2-диаминоциклогексана в присутствии щелочноорганических соединений.
Пример 9. Работают в условиях примера 1, но в присутствии 0,05 моля фенилнатрия
и 0,0125 моля М§(СбН5)5, полученного при действии фенилнатрия на фенилмагнийбромид.
Установлено, что после 10 мин при 80°С коэффициент разделения С равен 3,70 и что коэффициент остается равным этой величине в пределах ощибки опыта, после выдерживания смеси в течение 90 час при 80°С. Этот пример показывает стабилизирующую роль присутствия в реакционной среде соединения
магния.
Существует прямое соотношение между составами паровой фазы, равновесной с жидкой фазой указанной смеси углеводородов при контакте с используемыми металлоорганическими соединениями, с одной стороны, и константами равновесия /Сз таких реакций трансметаллизации, которые были описаны выше, с другой стороны. Эти константы равновесия, как, например, в предшествуюших примерах,
Moryt быть вычислены из исследования (определения) состава паровой фазы. И, наоборот, они (составы) могут быть вычислены из экспериментальных определений констант равновесия /Сз.
Эти константы были определены в следуюшем примере для многих пар углеводород RiH и НгН, прИ исследовании их жидких ф приведенных в контакт с металлоорганическиг соединением R.M (М представляет собой атом
щелочного металла), относительных пропорций их составлякзщих RiH, RaH, RiM и RaM.
И, наконец, обрабатывают образовавшиеся смеси триметилфосфатом или диметилсульфатом для количественного преврашения составляющих RiM и R2M в продукты RiCH3) и R3CH3 соответственно (составляющие R3M также превращаются в продукты КСНз) и определяют (газовой хроматографией) различные компоненты превращенных таким образом фаз. Из найденных при этом величин можно вычислить величины констант равновесия /Сз рассматриваемых пар. Пример 10. Осуществляют вышеуказанные определения, работая в условиях примера 8, используя относительные пропорции соответствующих углеводородов, указанных ниже (трансметаллизация натриевым производным диметиланилина в присутствии N,N,N,Nтетраметил-1,2-диамнноциклогексан). Полу15
ченные для указанных пар углеводородов величины Кз приведены ниже:
метаксилол, параксилол9,4
параксилол, этиленбензол5,4
толуол, параксилол9,0
метаксилол, ортоксилол1,1
псевдокумол, параксилол3,5
мезитилен, параксилол9,2
трет, бутилбензол, параксилол О бензол, параксилолО
параксилол, парацимол1,2
здетацимол, парацимол4,0
параксилол10
этилбензол, изобутилбензол9.
Пример 11. Работают в условиях примера 10, но используют вместо натриевого производного калиевое производное диметиланилина. Измеренные величины Ks приведены ниже:
метаксилол, параксилол27
этилбензол, паракеилол4
ортоксилол, метаксилол2
метацимол, парацимол7
Пример 12. Смешивают 0,05 моля фенилнатрия, 50 см кумола, 0,05 моля N,N,N,Nтетраметил-1,2-диами1Ноциклогексана.
Выдерживают температуру 40°С и сразу вводят 0,05 моля параксилола и 0,05 моля метаксилола. Реакция гомогенная. Перегоняют в вакууме за время мин. Коэффициент разделения С равен 3,1.
Обработка жидкости диметилсульфатом подтверждает, что кумол практически не металлизируется, копстанта равновесия реакции металлизации равна 9,5, соотношение концентраций неметаллизировапных ксилолов в жидкой фазе равно соотношению концентраций ксилолов в паровой фазе.
Пример 13. Смешивают 0,05 моля фенилнатрия, 50 мл трет, бутилбензола и 0,05 моля Ы,М,К ,М-тетраметил -1,2 - диаминоциклогексана.
Устанавливают температуру 40°С и сразу вводят 0,10 моля параксилола и 0,02 моля метаксилола. Перегоняют в вакууме за время т 30 сек и за время т 5 мин. Коэффициент распределения С не зависит от времени и равен 4,5.
Эта величина соответствует также K.,5, константе, определенной при обработке жидкости диметилсульфатом, трет, бутилбензол не металлизируется в этих условиях.
Пример 14. Смешивают 0,05 моля фенилнатрия, 50 мл трет, бутилбензола и 0,05 моля М,М,М ,К-тетраметил - 1,2 - диам иноциклогексана.
Устанавливают температуру 40°С и сразу вводят 0,02 моля параксилола, 0,05 моля метаксилола и 0,05 моля мезитилена. Перегоняют в вакууме за время т 1 мин. Коэффициент распределения, полученный для пара- и метаксилола равен 1,6.
Константа равновесия /Сз равна 9,5, константа равновесия мезитилена по отношению к метаксилолу в присутствии ш;елочнооргани16
ческого соединения равна 0,98. Эти константы были определены при обработке жидкости диметилсульфатом, трет, бутилбензол не металлизируется в этих условиях.
Пример 15. Смешивают 0,05 моля фенилнатрия, 50 мл трет, бутилбензола и 0,05 моля Ы,Ы,Ы,М-тетраметил - 1,2 - диаминоциклогексана.
Устанавливают температуру 40°С и сразу вводят 0,02 моля параксилола, 0,05 моля метаксилола и 0,05 моля псевдокумола. Перегоняют в вакууме за время т 1 мин. Коэффициент распределения С, полученный для пара- и Метаксилола равен 1,72.
Константа равновесия Кз равна 9,5, константа, соответствуюш;ая равновесию псевдокумола и метаксилола в присутствии шелочноорганического соединения, равна 2,6. Эти константы были определены при обработке ж идко сти ДИМ ет ил сул ьф а том.
Очень простой метод определения констант /Сз, который проиллюстрирован примерами 10-15, позволяет быстро определить относительные кислотности для любых пар углеводородов, в которых, по крайней -мере один, обладает подвижными атомами водорода.
Его схематическое применение к изучению многих пар углеводородов позволяет вывести экспериментально следуюш;ие правила и факты.
Катиоп шелочного металла играет преобладаюш,ую роль, измеренные величины /Сз в значительной мере независимы от группы з в соответствуюш,их металлоорганических соединениях, используемых основных катализаторов или хелатирующих диаминов. Однако не имеется единой шкалы кислотности. Она меняется от одного ш;елочного катиона к другому. Таким образом, в случае ароматических углеводородов, имеюших несколько заместителей в ядре, относительная кислотность метасоединений по отношению к парасоединениям больше у калийорганяческих производных, чем у натрийорганических соединений.
Всегда в отношении ароматических углеводородов, имеюших несколько заместителей в самом ядре, наблюдалось, что метасоединение является более кислым, чем гарасоединение, и это еш;е более справедливо по отношению к органокалиевым производным, чем к натрийоргапическим.
Получают для каждой рассматриваемой пары константы кислотности, ::1роъ1ежуточные между величинами, найденными с натрийорганическими и калийорганическими соединениями соответственно, когда используют смесь этих соединений.
Нужно также отметить, что с некоторой степенью точности МОЖНО вычислить изменение кислотности, вносимое дополнительным заместителем при использовании принципов аддитивности свободной энергии, хорошо известных из органической химии. Таким образом, исходя из кислотностей орто-, мета- и пара17
ксилолов, можно вычислить их и для три- и тетрабензолов и т. д.
Итак, способ, -согласно изобретению, -применим к разделению практически всех углеводородных смесей, в которых по крайней мере один из этих углеводородов обладает подвижными водородами. Специалист, располагающий такими возможностями, как выбор реактивов и регулирование параметров, применяемых для калсдой реакции, практически всегда сможет разобраться в условиях работы, позволяющих эффективно разделить такие смеси, независимо от природы их компонентов. Действительно, наблюдается, что константы относительной кислотности никогда не идентичны для различных щелочных ионов, так что можно -утверждать, что два соединения, которые не разделились при использовании одного из этих щелочных металлов, будут обязательно делиться при использовании другого.
Следовательно, -можно утверждать, что вероятность того, что два ароматических -соединения RiH и R2H имеют сразу три следующие характеристики:
0,,l относительная летучесть R.H/RsH,
0,,,l -отно-сительная кислотность RiH/RaH в при-сутствии натрия,
0,,,l относительная кислотность RiH/RjH в присутствии калия,
практически равна нулю, и разделение всегда будет возможно, и ему всегда будет благоприятствовать применение щелочноорганических соединений.
Более конкретно в качестве примера можно подчеркнуть, что изобретение ох1ватывает следующие разделения:
-насыщенные углеводороды (этилбензол/ параксилол)-мета-ксилол/ортоксилол,
-насыщенные углеводороды/бензол,
-Насыщенные углеводороды/толуол,
-насыщенные углеводороды/ароматические углеводороды Сд,
-насыщенные углеводороды/ароматические углероды Сю,
18
-гемиллитен/псевдокумол/ортоэтилтолуол/ мезитилен,
-ортоэтплтолуол/метаэтилтолуол/параэтилтолуол,
-ортоцимол/метацимол/парацимол,
-ортодиэтилбензол/1,2,3,5-тетраметилбензол/1,2,3,5-тет-раметилбензол,
-насыщенные углеводороды /а-метилнафталин/р-метилнафталин.
Разделение диметил-нафталинов и более конкретно 2,6-диметилнафталина,
-н-бутилбензол (втор. бутилбензол)изобутилбензол/трет. -бутилбензол,
-ортодиизопропилбензол(метадиизопропилбензол)парадиизопропилбензол, и т. п.
Таким образом, из приведен-ных примеров видно, что степень разделения углеводородов во всех Приведенных примерах очень высока, что позволяет выделять при фракционной дистилляции целевые продукты высокой чистоты.
Предмет изобретения
1.Способ выделения углеводородов, Имеющих подвижные атомы водорода, из углеводородных смесей, отличающий 1C я тем, что, с целью повыщения чистоты целевых продуктов, указанные смеси подвергают фракционной дистилляции в присутствии органических производных щелочных металлов.
2.Способ по п. 1, отличающийся тем, что органические производные щелочных металлов -подвергают -контакту с разделяемой смесью углеводородов, преимущественно в виде раствора или дисперсной фазы в Среде растворителя, стойкого к действию органических соединений.
3.Способ по ип. 1 и 2, о т л и ч а ю щИ и С я тем, что процесс ведут преимущественно в присутствии основных катализаторов, представляющих собой третичные амины и/или хелатирующие третичные полиамины, а также металлоорганического соединения общей формулы Mg(R2), Zn(R2) или A1(R3).
4 6
/2. W,
f









| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ИЗВЛЕЧЕНИЯ НЕПРОРЕАГИРОВАВШЕГО КСИЛОЛА ИЗ УКСУСНОЙ КИСЛОТЫ В ПРОИЗВОДСТВЕ ТЕРЕФТАЛЕВОЙ ИЛИ ИЗОФТАЛЕВОЙ КИСЛОТЫ (ВАРИАНТЫ) | 2005 |
|
RU2311403C2 |
| Способ выделения параксилола из смеси с8 ароматических углеводородов | 1971 |
|
SU507222A3 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ПАРАКСИЛОЛА ИЗ ПО МЕНЬШЕЙ МЕРЕ ДВУХ СЫРЬЕВЫХ ПОТОКОВ, СОДЕРЖАЩИХ ИЗОМЕРЫ КСИЛОЛА | 2014 |
|
RU2687492C2 |
| ОПТИМИЗИРОВАННОЕ ЖИДКОФАЗНОЕ ОКИСЛЕНИЕ | 2005 |
|
RU2388738C2 |
| СПОСОБ ПЕРЕРАБОТКИ Св-АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ | 1971 |
|
SU429578A3 |
| СПОСОБ ПОЛУЧЕНИЯ ОРТОКСИЛОЛА | 2001 |
|
RU2197462C1 |
| ОПТИМИЗИРОВАННОЕ ЖИДКОФАЗНОЕ ОКИСЛЕНИЕ | 2005 |
|
RU2388743C2 |
| КАТАЛИЗАТОР И СПОСОБ КОНВЕРСИИ УГЛЕВОДОРОДОВ | 2012 |
|
RU2570427C1 |
| ОПТИМИЗИРОВАННОЕ ЖИДКОФАЗНОЕ ОКИСЛЕНИЕ | 2005 |
|
RU2393146C2 |
| СПОСОБ ВЫДЕЛЕНИЯ МЕТАКСИЛОЛА ИЗ СМЕСИ КСИЛОЛОВ | 1970 |
|
SU269805A1 |

01
.17
.ZIL
-4
12
Авторы
Даты
1975-02-15—Публикация
1972-02-25—Подача