Изобретение относится к способу получения новых производных триазинобензимидазола, которые могут найти применение в качестве пестицидов.
Известна реакция образования 1,3-диарилимидазолидинов взаимодействием NiN-диарилэтилендиамина с 30%-пым раствором формальдегида.
Основанный на известной реакции предлагаемый способ получения производных триазпнбензимидазола общей формулы I
tOOUH,
NY
где R-
алкил с 1-18 атомами углерода, алкенил Сз-Ci8, алкинил С2-Се, циклоалкил Сз-Ci2, который может быть замещен одной или несколькими алкильными группами Ci-€4;
циклогексилалкил, -алкенил или -алкинил с I-3 углеродными атомами в цепи;
эндометиленциклогексил метил, эндометиленциклогексенилметил, трициклодецил, трициклодеценил;
феналкил, дифеналкил, или трифеналкил с 1-6 атомами углерода в алкильном остатке, фенильные ядра которых могут быть замещены галоидом, алкилом с 1-4 атомами углерода, алкоксилом с 1-4 атомами углерода, алкилмеркапто- или диалкиламиногруппами с 1-4 атомами углерода;
фенил или нафтил, которые могут быть замещены галоидом, алкилом или галоидалкилом с 1-4 атомами углерода, трифторметилом, окси, алкокси с 1-4 атомами углерода, фенокси, алкилмеркаптогруппой с 1-4 атомами углерода; N,N-диалкил Ci-C аминоалкил с 2-4
атомами углерода;
оксиалкил с 2-12 атомами углерода, алкоксиалкил или диалкоксиалкил с 2-18 атомами углерода, алкилмеркаптоалкил с 2-18 атомами углерода, диалкилфосфинилалкил с
3-9 атомами углерода, фурфурилалкил с 1 - 4 атомами углерода в алкильпой цени, морфолиноалкил с 1-4 атомами углерода в алкильиой цепи, пирролидиноалкил с 1-4 атомами в алкильной цепи, пиперидиноалкил с
1-4 атомами углерода в алкильной цепи или карбалкоксиалкил с 2-12 атомами углерода, заключающийся в том, что 2-метоксикарбониламинобензимидазол формулы II
Соосн,
NH
подвергают взаимодействию с первичным амином формулы H2N-R и формальдегидом, где R имеет указанные значения.
На 1 моль 2-метоксикарбоииламинобензимидазола рекомендуется вводить не менее 2 молей формальдегида.
Предпочтительный вариант предлагаемого способа заключается в том, что 2-метоксикарбониламинобензимидазол формулы II суспендируют или растворяют в соответствующем растворителе, прибавляют 1-2 моля амина и при перемешивании 2-4 моля водного формальдегида. Реакцию проводят при О-80°С, предпочтительно при 20-40°С, однако температура не является решающим фактором. Продукт реакции, как правило, находится в растворе п его можно отделить от присутствующего 2-метоксикарбонилам-инобензимидазола.
Упариванием и обработкой остатка таким инертпым растворителем, как бензин, или переосаждеиием, например из метиленхлорида бензином, триазинобензимидазол выделяют в чистом виде.
Кроме описанных в примерах, можно использовать следующие амины:
изоампламин, изооктиламин, нониламин, и-дециламии, изодециламии, я-ундециламии, пентадециламин, гексадециламии, октадециламин, н-октадецен-(9)-ил-амин, циклобутиламин, 2-метилциклопентиламин, Ы,Ы-диметил-, К,Н-диэтил-, Н,М-дибутил-, 1М,М-метилэтил-, М-метил-Ы-пропил-, М-этил-М-изобутилэтилендпамин, - пропилендиамин, - тетраметилендиамин, - гексаметилендиамин, 3-аминогексагидротолуол, 4-аминогексагидро- и-ксилол, 4-изопропилциклогексиламин, 4-этилциклогексиламин, 2,6-диэтиланилин, 4-грет.бутиланилин, 2-, 3- и 4-хлоранилин, 2-, 3- и 4-аминофенол, а- и р-нафтиламин, 3-фенилпропиламин, 2фенилэтиламин, 4-фенилбутиламин, дифенилметиламин, 2,2-дифенилэтиламин, 2-, 3- и 4хлорбензиламин, 2-{2-хлорфенил)-этиламин, 2-, 3- и 4-метилбензиламин, 2-этилтиоэтиламин, 4-метилтиобутиламин, 1- и 4-аминогексанол, диметил- (2-аминоэтил) -фосфиноксид, диэтил- (4-аминобутил) -фосфиноксид, N-аминометилморфолин, N- (3-аминопропил) -морфолин, N-аминоэтилпирролидин, N-аминометил- и N-амииоэтилпиперидин, фурфуриламин, аминоуксуснометиловый и этиловый эфир, 2-аминопропионовометиловый эфир, 3-аминомасляноэтиловый эфир, 6-аминокапроновометиловый и- этиловый эфир, аланинометиловый эфир, 7 11новалерьяновометиловый эфир, -аминовалерьяновоэтиловый эфир, 4метоксибензиламин, 4-г/зег.-бутилциклогексиламин, 2-амино-1,3,5-триметилбензол, 2-аминобутан, 2-этилгексиламин, н-тридециламин и тетрадециламин, изотетрадециламии.
В качестве растворителя можно применять умеренно или слабополярные растворители, преимущественно низкокипящие, такие как метиленхлорид, хлороформ, четыреххлористый углерод; такие простые эфиры, как диэтиловый эфир, диизопропиловый эфир и тетрагидрофуран; такие сложные эфиры как уксуснометиловый и этиловый эфир или такие кетоиы, как ацетои или метилэтилкетон. Предпочтительно применяют хлороформ или метиленхлорид. 2-метоксикарбоииламинобензимидазол можно получать взаимодействием о-фенилендиамина с диметиловым эфиром S-метилизотиомочевинодикарбоновой кислоты. Получение необходимых для осуществления реакции аминов также известно из литературных источНИКОВ.
Целевые продукты выделяют известными приемами. А) Пример 1. 57,3 г (0,3 моля) 2-метоксикарбониламннобензимидазола суспендируют в 550 мл метиленхлорида, добавляют 55,5 г (0,3 моля) додециламина и нагревают до 35°С. При этой температуре прибавляют по каплям при иеремешиваиии 68 мл (0,8 моля)
35%-ного водного раствора формальдегида. Затем перемегиивают 1 ч при 38°С, и при перемешивании охлаждают.
Пепрореагировавп1ий 2-метоксикарбонилампнобеизимидазол отфильтровывают (иосле
сушки получают 4 г), водный слой отделяют и метиленхлорпдный раствор сушат над сульфатом магния. После упаривания получают 122,7 г кристаллического вещества с т. пл. 75°С. Для удаления непрореагировавшего
амина его перемешивают с 200 мл бензина
(30-85°С) и получают таким образом 95 г
(79% от теоретического) 1-метокснкарбонил3-додецил-сыл ж. гексагидротриазииобензимидазола с т. пл. 86-87°С.
tOOCH, .,
11 Т 1 I
(СНг), СН,
Найдено, %: С 69,3; Н 9,2; N 14,0.
С2зНзбН422. Мол. вес 400.
Вычислено, %: С 69,0; Н 9,0; N 14Д
В ИК-снектре соединения имеется характерная для карбонила полоса поглощения при
1720 , и полосы поглощения при 1620
и 1595 см, характерные для двойной связи.
Пример 2. 57,3 г (0,3 моля) 2-метоксикарбониламинобензимидазола суспендируют в 900 мл метиленхлорида и прибавляют 39 г (0,3 моля) З-диэтиламино-1-пропиламина. Суспензию нагревают до 35°С. При этой температуре добавляют по каплям при перемешиваиии 60 .мл (0,7 моля) 35%-ного водиогораствора формальдегида. Перемешивают в течение 2 ч при 38°С, затем охлаждают, перемв цшвая.
Непрореагировавший 2-метоксикарбониЛ аминобензимидазол отфильтровывают (после сушки получают 41 г), водный слой отделяют и метиленхлоридный раствор сушат над сулЬ фатом натрия.
После упаривания получают масляный остаток, который перемешивают с бензином
Найдено, %: С 63,0; Н 8,5; N 19,8.
СкчНогМзО-з. Мол. вес, 345.
Вычислено, %: С 62,6; Н 7,8; N 20,2.
Пример 3. 38,2 г (0,2 моля) 2-метоксикарбониламинобензимидазола суспендируют в 600 мл хлороформа, прибавляют 14,6 г (0,2 моля) м-бутиламина и нагревают до 35°С. При этой температуре прикапывают при перемешивании 68 мл (0,8 моля) 35%-ного водного раствора формальдегида. Затем перемепшвают в течение 1 ч при 38°С. Бензимидазол при протекании реакции растворяется. После охлаждения отделяют водный слой и органическую фазу сушат над сульфатом натрия. После отфильтровывания и упаривания получают масло, застываюшее при затирании с н-гексаном.
Выход 1 -метоксцкарбонил-3-«-бутил-с«ж.и.гексагидротриазинобензимидазола 41 г (71% от теоретического), т. пл. 109°С. , СООСИ,
ГГТ
N,N.
J U П Q П
Найдено, %: С 62,8; Н 7,2; N 19,5.
Ci5H2oN402. Мол. вес. 288.
Вычислено, %: С 62,5; Н 6,94; N 19,45.
В ИК-спектре этого соединения имеются характерная для карбонила полоса поглош еиия при 1745 и полосы поглощения двойной связи при 1620 см и 1595
при 30-85°С. После декантации раствор уиаривают, полученный маслообразный остаток снова растворяют в метиленхлориде и промывают дважды водой. Метиленхлоридный раствор сушат над сульфатом магния, упаривают и обезгаживают в высоком вакууме при комнатной температуре.
Выход неперегоняемого масла 37 г (36% от теоретического).
Czlij
.N-CHr iHr iKrNC
Пример 4. 57,3 г (0,3 моля) 2-метоксикарбониламинобензимидазола суспендируют в 900 мл метиленхлорида, прибавляют по каплям 26,7 г (0,3 моля) 3-метоксипропиламина и нагревают до 35°С. При этой температуре при перемешивании прикапывают 68 мл (0,8 моля) 35%-иого водного раствора формальдегида п продолжают перемешивание в течение 1 ч при 38°С. По охлажденпп отфильтровывают от небольшого количества непрореагировавшего исходного бензимидазола. Водную фазу отделяют и метиленхлоридный раствор сушат над сульфатом магния. После отфильтровывания и упаривания получают масло, кристаллизующееся при затирании с н-гексаном.
Выход 1 -метоксикарбонил-3- (З-метоксипроиил) - сы..мл1.гексагидротриазииобензимидазола 63 г (69% от теоретического), т. пл. 73- 74°С.
СО О to
113
NY
N-(CHsVQ- 7
N
35
Найдено, %: С 59,3; Н 6,9; N 18,7.
Ci5H2oN4O3. Мол. вес 304.
Вычислено, %: С 59,2; Н 6,6; N 18,7.
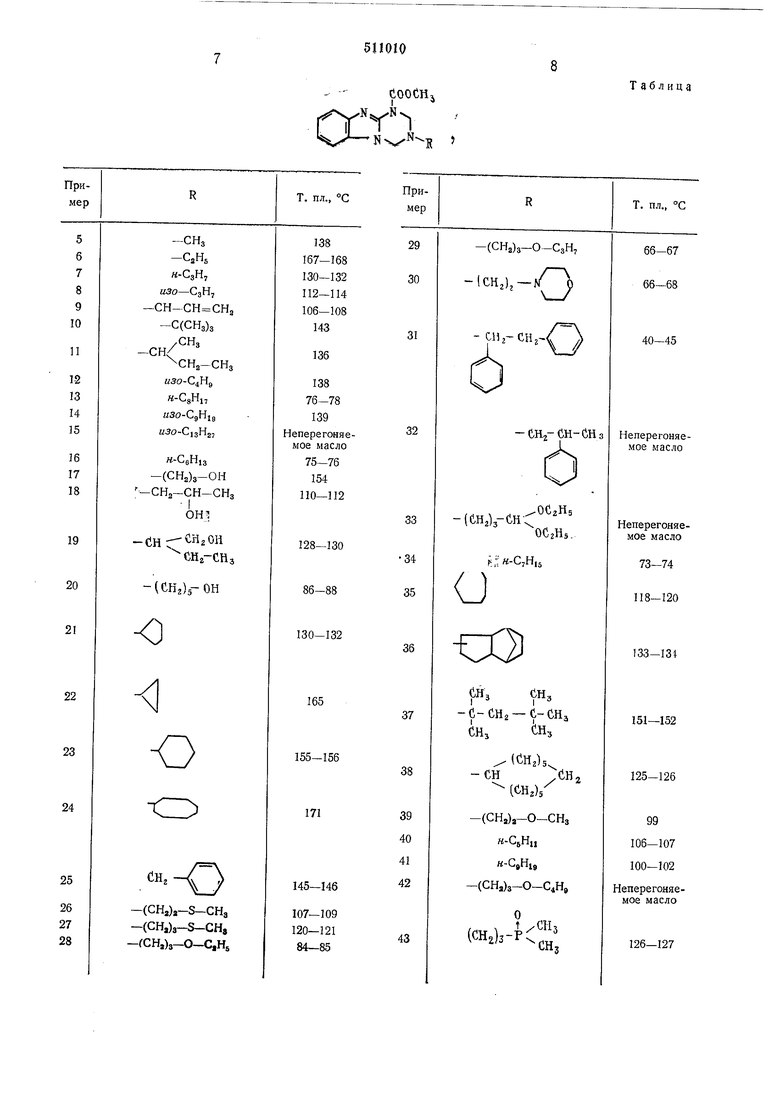
В НК-спектре полученного соединения имеется полоса поглощения, характерная для карбонила при 1750 см-, и полосы поглощения двойной связи при 1625 и 1600 смПриведенные в таблице вещества получены аналогично примерам 1-4,
Таблица
СООСН,
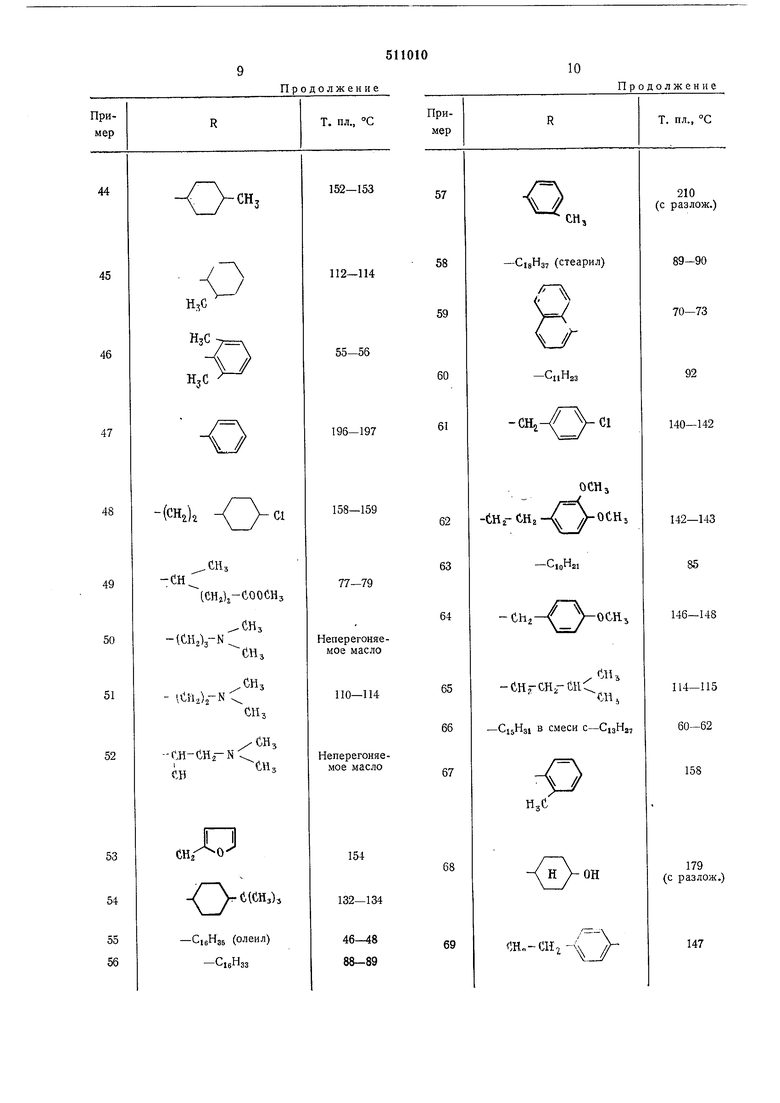
Продолжение
Продолжен ие
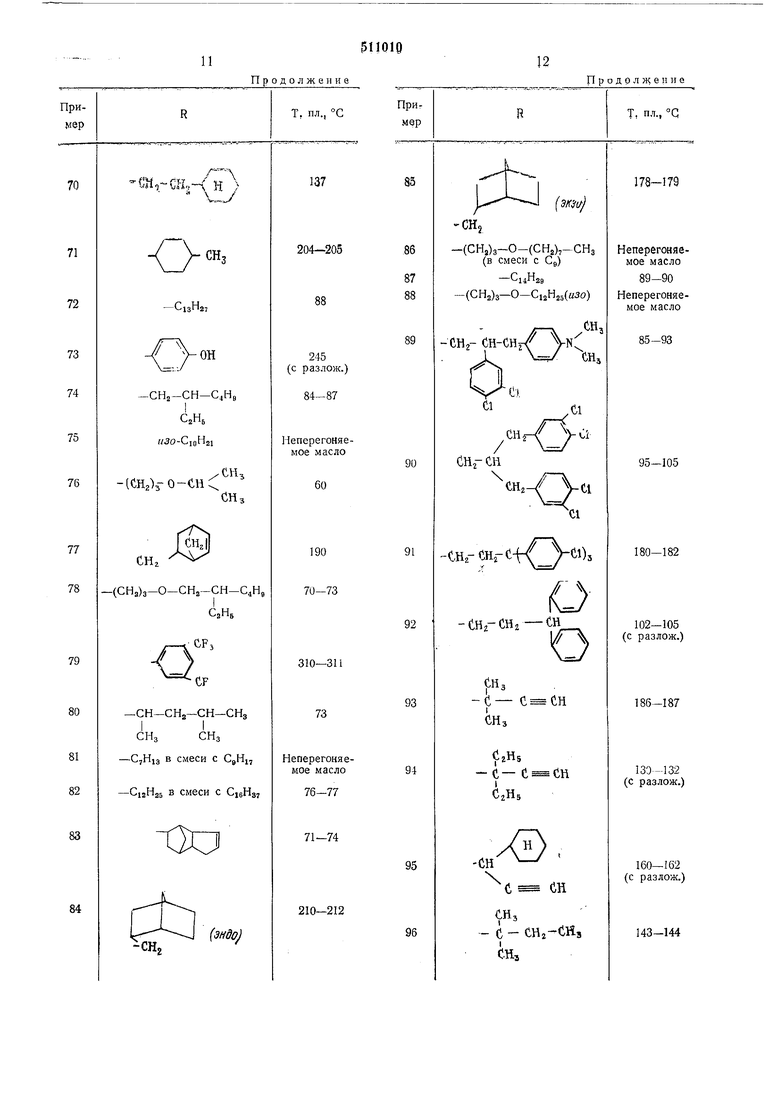
Продолжение
Продолжение 13 Формула изобретения 1. Способ юлучения производных триазинобензимндазола общей формулы I СООСНз R -алкил с 1 -18 атомами углерода, алкеппл Сз-С|8, алкинпл €2-Cs, циклоалкил Сз- С|2, который может быть замещен одной или песколькими алкпльными группами пиклогексилалкил, -алкенил или -алкинил с 1-3 углеродными атомами в цепи, эндометиленциклогексил метил, эндометилеициклогексенилметил, трициклодецил, трициклодеценил;феналкил, дифеналкил или трифеналкил с 1-6 атомами углерода в алкиленовом остатке, фенильиые ядра которых могут быть замещены галоидом, алкилом с 1-4 атомами углерода, алкоксилом с 1-4 атомами углерода, алкилмерканто- или диалкиламииогрупнами с 1-4 атомами углерода; фенил или нафтил, которые могут быть замещены галоидом, алкилом, или галоидалкилом с 1-4 атомами углерода, трифторметилом, окси, алкокси с 1-4 атомами углерода, фенокси, алкилмеркаптогруппой с 1-4 атомами углерода; Ы,Ы-диалкил Ci-С4 аминоалкил с 2-4 атомами углерода; оксиалкил с 2-12 атомами углерода, алкоксиалкил или диалкоксиалкил с 2-18 атомами углерода, алкилмеркаптоалкил с 2-18 атомами углерода, диалкилфосфииилалкил с 3-9 атомами углерода, фурфурилалкил с 1-4 атомами углерода в алкильной цепи, морфолииоалкил с 1-4 атомами углерода в алкильной цепи, пирролидиноалкил с 1-4 атомами в алкильной цепи, пиперидииоалкил с 1-4 атомами углерода в алкильной цепи или карбалкоксиалкил с 2-12 атомами углерода, отличающийся тем, что 2-метоксикарбоииламинобеизимидазол формулы II 511010 СООСНз одвергают взаимодействию с первичным мином формулы H2N-R и формальдегидом, где R-имеет указанные значения, с последуюи;нм выделением целевого продукта известными приемами. 2. Способ по п. 1, отличающийся тем, что на 1 моль 2-метоксикарбониламинобензимидазола в реакцию вводят не менее 2 молей формальдегида. Приоритет по признакам: 18.05.72 при R-алкил с 1-18 атомами углерода, алкенил Сз-Cis, циклоалкил Сз-Ci2, который может быть замещен одной или несколькими алкильными группами Ci-С4, трициклодецил;феналкил, дифеналкил с 1-6 углеродными атомами в алкиленовом остатке, фенпльные ядра которых могут быть замещены галоидом, алкилом с 1-4 атомами углерода, алкоксилом с I-4 атомами углерода, алкилмеркаптогруппой с 1-4 атомами углерода; фенил или нафтил, которые могут быть замещены галоидом, алкилом или галоидалкилом , оксигруппой, алкоксигруппой с 1-4 атомами углерода, феноксигруппой или алкилмеркаптогруппой с 1-4 атомами углерода;оксиалкил с 2-12 атомами углерода, алкоксиалкил или диалкоксиалкил с 2-18 атомами углерода, алкилмеркантоалкил с 2-18 атомами углерода; диалкилфосфинилалкил с 3-9 ато.мами углерода; фурфурил-, морфолииоалкил с 1-4 атомами углерода в алкильной цени; нирролидино-, пиперидиноалкил с 1-4 атомами углерода в алкильной цепи или карбалкоксиалкил с 2-12 атомами углерода. 19.02.73 приК-N,N- диалкил аминоалкил с 2-4 атомами углерода.



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения бис-триазинобензи-мидазолов | 1974 |
|
SU509238A3 |
| ПРОИЗВОДНЫЕ ГАЛОГЕНЗАМЕЩЕННОГО БЕНЗИМИДАЗОЛА И ИХ КИСЛОТНО-АДДИТИВНЫЕ СОЛИ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ И ФУНГИЦИДНОЕ СРЕДСТВО | 1996 |
|
RU2170735C2 |
| МЕТАЛЛОЦЕНОВЫЕ СОЕДИНЕНИЯ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 1997 |
|
RU2201935C2 |
| 2-АМИНО-4-БИЦИКЛОАМИНО-1,3,5-ТРИАЗИНЫ, ГЕРБИЦИДНОЕ СРЕДСТВО НА ИХ ОСНОВЕ И СПОСОБ БОРЬБЫ С СОРНЯКАМИ | 1997 |
|
RU2314297C2 |
| Способ получения производных оксазола | 1976 |
|
SU627753A3 |
| ПРОИЗВОДНЫЕ БЕНЗИМИДАЗОЛА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1987 |
|
RU2062778C1 |
| ПРОИЗВОДНЫЕ 1Н-3-АРИЛ-ПИРРОЛИДИН-2,4-ДИОНА, ИСХОДНЫЕ И ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ ДЛЯ ИХ ПОЛУЧЕНИЯ И СРЕДСТВО ДЛЯ БОРЬБЫ С ПОВРЕЖДАЮЩИМИ РАСТЕНИЯ НАСЕКОМЫМИ И КЛЕЩАМИ | 1994 |
|
RU2144034C1 |
| НОВЫЕ ЗАМЕЩЕННЫЕ СУЛЬФАМАТНЫЕ ПРОТИВОСУДОРОЖНЫЕ ПРОИЗВОДНЫЕ | 2003 |
|
RU2328502C2 |
| Способ получения производных 1,2,4-триазола или их солей | 1975 |
|
SU615857A3 |
| Способ получения солей пири-диНилАМиНОАлКилОВыХ эфиРОВ | 1978 |
|
SU799658A3 |


Авторы
Даты
1976-04-15—Публикация
1973-05-16—Подача