1
Изобретение относится к гомогенному асимметрическому гидрированию ненасыщенных соединений, в частности к катализаторам для этого процесса.
Известен катализатор для асимметричео кого гидрирования замещенных акриловых кислот, состоящий из раствора комплексного соединения металла V111 группы Периодической системы элементов,, например родия, и оптически активного метилпропилфенилфосфина, взятого в количестве 1-3 моля на 1 моль металла.
Однако на таком катализаторе степень асимметрического гидрирования не превыщает, 15%.
Для повыщения асимметрической активности катализатора предложен катализатор, в котором в качестве оптически активного лиганда взят оптически активный фосфин или арсин, имеющий по крайней мере однуфенильную группу, которая имеет в качестве заместителя в о-положении окси-, алкоксигруппу, содержащую 1-12 атомов углерода, или арилоксигруппу, предпочтительно метилфенил-о-анизилфосфин или метилниклогексил-о-анизилфосфин.
При асимметрическом гидрировании -замещенных
ациламидоакриловых кислот и/или их солей на предложенном катализаторе можно с хорощим выходом получать оптически активные оС -аминокислоты.
Примерами -аминокислот, антиподы которых могут быть быстро получены с использованием катализатора по данному изобретению, являются аланин, п -хлорфенилаланин, триптофан, фенилаланин, 3-(3,4-диоксифенил)-аланин, 5-окситриптофан, лизин, гистидин, тирозин, лейцин, глютаминовая кислота и валин.
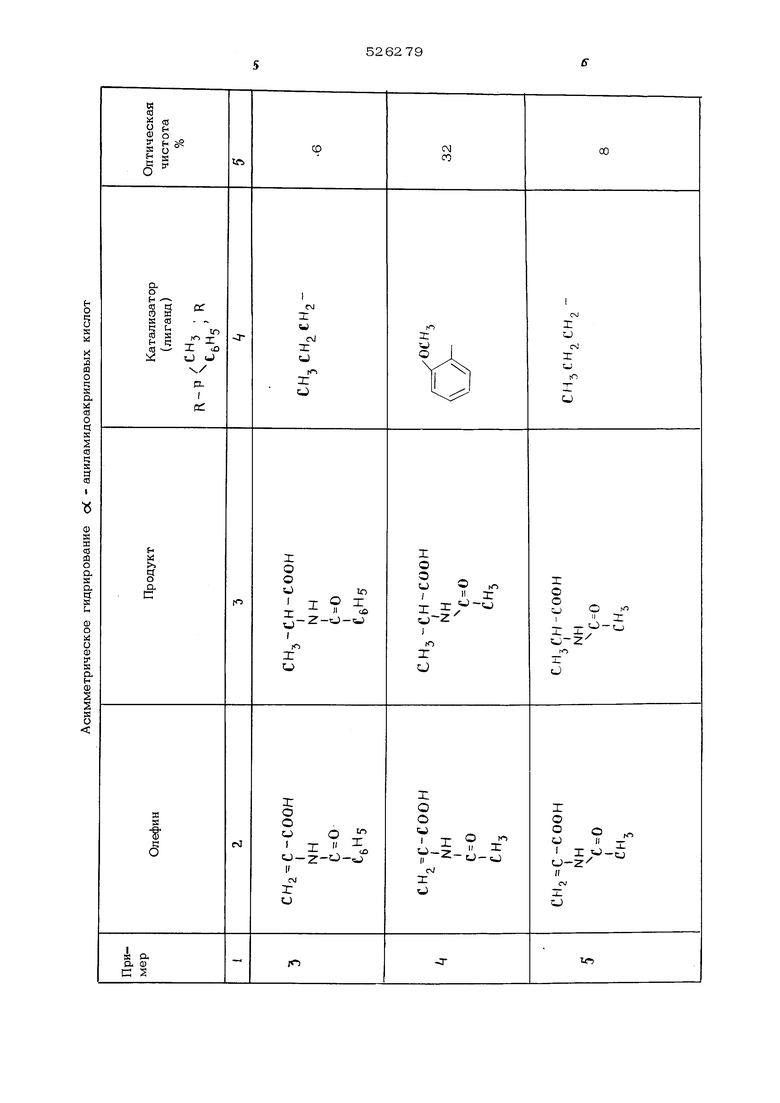
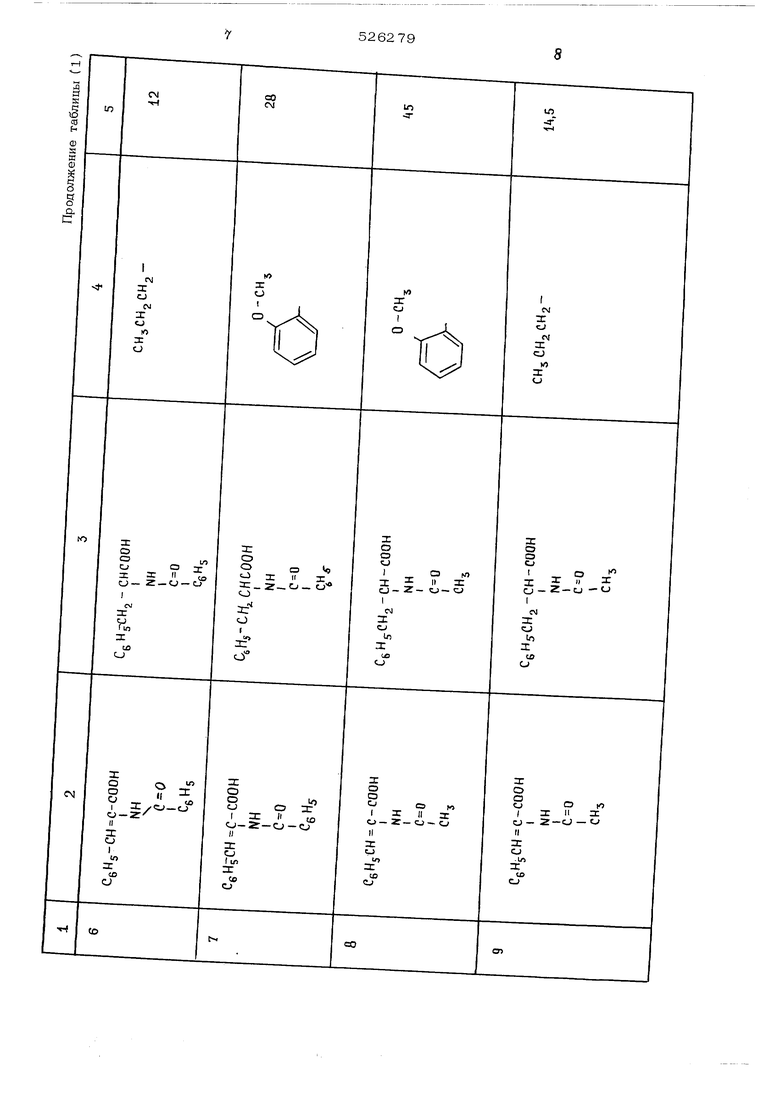
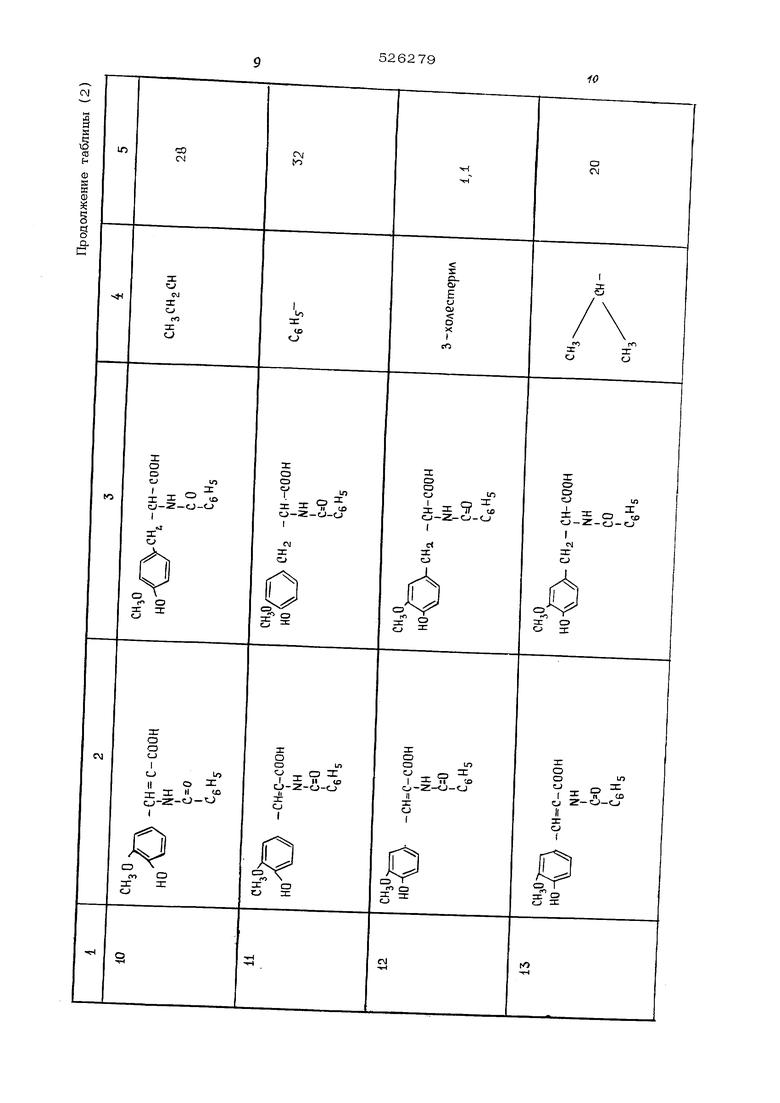
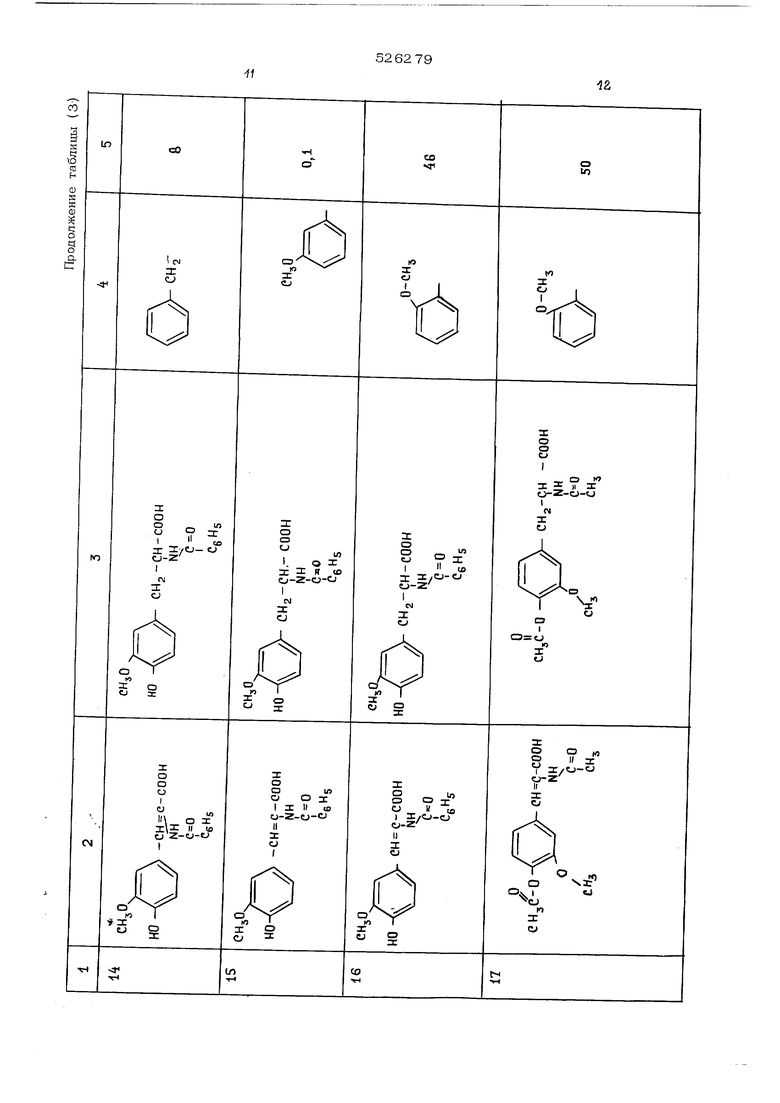
Оптически активные катализаторы гидрирования представляют собой растворы комплексного соединения металла, выбранного из группы, состоящей из родия, иридия, рутения, осмия, палладия и платины, в сочетании по крайней мере с одним эквивалентом оптически активного фосфинового и/или арсинового лиганда. Предпочтительным металлом является родий. ФосфиноБый ИЛИ арсиновый лиганд может быть, например, формулы , где А представляет собой фосфор или мышьяк, и Pg. 1 и R--, каждый независимо выбирается из группы, состоящей из водорода; алкила или алкоски, имеющих по крайней мере один атом углерода и максимум 12 атомов углерода; замещенного алкила с заместителями, выбранными из группы, включающей амино, карбонил, арил, нитро и алкокси имеющих максимум 4 углеродных атома; ари ла; арилокси; фенила; замещенного фенила с заместителями, выбранными из группы, вклю чающей а-лкокси и алкия, окси, арилокси, ам но и нитро, причем количество заместителей составляет менее 3; циклоалкила, имеющего по крайней мере 3 углеродных атома; замещенного циклоалкила; пиррила, тиенила; фури ла; пиридила; пиперидила и 3-холестерила. В качестве оптически активных фосфинов и арсинов могут использоваться, например, метилэтилфосфин, метилизопропилфосфин, этил бутилфосфин, изопропилизобутилфосфин, метил фенилфосфин, этилфенилфосфин, пропилфенилфосфин, бутилфенилфосфин, фенилбензилфосфин фенилпирролфосфин, этилизопропилизобутилофосфин, метилфенил-4-метилфенилфосфин, этил фенил-4-метилфенилфосфин, метилизопропилфенилфосфин, этилфенил-2,4,5-триметилфенил фосфин, фенилбензил-4-диметиламинофенилфосфин, фенилпиридилметилфосфин, фенилцикло пентилэтилфосфин, циклегексилметилизопропил фосфин, о-метоксифенилметилфенилфосфин, о-метоксифенилциклогексилметилфосфин и соответствующие мыщьяковые аналоги. Оптически активные фосфины и арсины, со держащие по крайней мере одну фенильную группу, которая имеет заместитель в о-поло жении, такой как окси, алкокси, имеющий по крайней мере один атом углерода и максимум 12 углеродных атомов, и арилокси, являются предпочтительными соединениями. Хорощие результаты получают с метилфенил-о-анизилфосфином и метилциклогексил-о-анизилфосфином. Соотнощение лиганда и металла должно составлять по крайней мере 1 эквивалент лиганда на 1 моль металла, предпочтительно 2 эквивалента лиганда на 1 мол металла. Пример 1.В реактор для гидрирования, снабженный прибором, измеряющим давление и температуру, и нагревающими устройствами, загружают 25 вес.ч. -бензамндо-4-ок:си-3-метоксикоричной кислоты, 186 вес.ч. метанола и 64 вес.ч. 5%-ного раствора гидроокиси натрия. Реактор тщательно очищают от каких-либо следов воздуа и окончательно устанавливают давление одорода 3,5 атм и температуру 25 С. Раствор катализатора готовят раствореним 0,0059 г 1,5-гексадиенродийхлорида Rh (1,5-гексадиен) СРз в 2 мл бензоа в атмосфере азота, добавляют 0,О139 г (+}-метилфенил-о-анизилфосфина в 1,3 мл ензола и затем пропускают через смесь воорода в течение 5 мин. Полученный раствор катализатора нагнетают в автоклав под давлением водорода. Гидрирование начинается немедленно и завершается по истечении 3-4 час при 2 5 С. Анализ полученного раствора показал оптическую чистоту (56,4%) натриевой соли N -бензоил- 3- (4 -окси- 3 метоксифенил)- -аланина, соответствующую содержанию 78% L - и 22% D - изомеров. Пример 2.В автоклав емкостью 1 л загружают 25 г оС -бензамидо-4-окси-3-метоксикоричной кислоты, ЗОО мл метанола и 0,6 мл 5%-ного водного раствора NctOH. Смесь перемешивают при 25 С под давлением 2,8 атм чистого водорода до тех пор, пока не убедятся в отсутствии утечки. Затем добавляют приблизительно 1 мл{О,О1%) (О,О5% Rh. -фосфина) раствора катализатора через отверстие без снижения давления. Раствор катализатора готовят растворением в атмосфере азота 0,О050 г Rh (1,5-гексадиена) Ctj в 0,33 мл раствора метилфенил-о-анизилфосфина {удельное вращение о 1 J) +42 , метанол) в бензоле (содержание - О,О41 г/мл ) и разбавлением до объема 1 мл метанолом. Реакционную массу перемещивают со скоростью 1400 об/мин. Водород начинает абсорбироваться после 2-5 минутного индукционного периода, и гидрирование заканчивается через 2 часа. Метанол упаривают и кислоту растворяют в одномолярном водном растворе Na ОН. Катализатор экстрагируют бензолом и возвращают на регенерацию. Свободную аминокислоту затем осаждают добавлением концентрированной НС8 . Получают 24 г N - бензоил - 3 -(4-окси-З-метоксифенил)-аланина, содержащего 73% L -антипода и 27% D -антипода. Примеры 3-17. Аналогично получают другие оптически активные о(. -аминокислоты с использованием катализаторовданного изобретения. При этом используют родиевый катализатор с фосфиновым лигандом, указанным в таблице. Полученная оптическая чистота аминокислоты также приводится в таблице.
s w
x
2
Ю
о
a. я о ct s
CO
I
6
Ф
a «a
Q
о
CL
s
CL
и
s u
Ш
о о
Q) tr
Q.
tu
2
s о
11
П 13 Пример 18. В автоклав загружа ют 25 г (0,085 моля) ацетата оС -ацета мидо-( 4-окси-З-метокси)коричной кислоты, ЗОО мл метанола и 0,36 мл 50%-ного ЫаО Давление смеси азота и водорода (50/50) автоклаве поддерживают равным 2,46 атм. Раствор катализатора готовят растворен ем О,О050 г {0,023 ммоля) (1.5-ге садиен) CCQ. в 0,5 мл бензола и добавлением под N2 О,051 ммоля (+) - метилЦИ1. -огексил-о-аназилфосфина (оптическая чистота около 90%) в 2,4 мл бензола. Водород пропускают через этот раствор в течение 10 мин. Раствор катализатора затем добавляют в автоклав. Гидрирование проводят при 60°С в течение 4 час. Продукт, полученный упариванием растворителя, представляет собой ацетат N -ацетил-3-(4-окси-3-метоксифенил)-аланина, удельное вращение которого + 38,2° ( Na -соль в воде Чистый ацетат /V -ацетил-3-(4-окси-3-метоксифенил)- L -аланина, также, как и натриевая соль в воде, имеет удельное вращение L р + 54,0°. Таким образом, оптическая чистота полу ченного в результате гидрирования продукта равна 7О,7%, т.е. он содержит 85% L -антипода и 15% D -антипода. Аналогично при использовании ( - ) метилциклогексил-о-анизилфосфина (оптическая чистота около 8О%) получают продукт гидрирования, содержащий преобладающее количество D -антипода (оптическая чистота смеси реакционного продукта 65%). Таким образом при соответствующем подборе (+)или (-)-фосфина можно получать любой анти под в преобладающем количестве. Пример 19. Применяют методику, сходную с методикой примера 18 с использованием ( -) - метилциклогексил-о-анизилфосфина в качестве оптически активного лиганда и о( -бензамидо-4-окси-З-метоксикоричной кислоты в качестве -замещенной- ot -ациламидоакриловой кислоты. 5 Полученный в пезультатй гидокрованпя N -бензоил- 3- (4-окси 3 метокснфенил) -аланин содержит большое колгпество D -антипода (опт1г-1еская чистота реакционного продукта около 6 5%). о б D е т мула к 1.Катализатор для асимметрг-хческого П дрирования замещенных акриловых кислот, состоящий EI3 раствора комплексного соед.ине)Г1тя металла VJU группы Период1Г1еской с);стемы элементов и оптически активного лнганда, взятого в количестве 1-3 моля ка 1 моль металла, о т л и ч а ю щ к и с я тем. что с целыо повышения acим eтpнчecкoй активности катализатора, он содержит Е качестБ-а лиганда оптически активный фосфин ил арсин, меющий по крайней мере одну ную группу, которая имеет в качестве зсгместителя в о-положенпи окси-, алкоксп.гпулпу, содержащую 1-12 атомов углеоода, luri арилоксигруппу. 2.Катализатор по п. 1, с щ и и с я тем, что в качес: V11I группы Перлодической ментов он содержит родий. 3.Катализатор по п. 1, е т л и ч а ; щ и и с я тем. что в качестве ог.т1гческ активного фосфина он содео:кит -о-анизилфосфнп или метилциклог - анизилфосфин. Приоритет по признакам: 11.05.70 - по признаку п. 1, закл;оча.щемуся в использоЕан1{и в качестве катализатора раствора комплексного со./дннения ,;е- талла Vltl группы Периодической сисге.;ы элементов и оптически активного л;;га:;да, и по признаку п. 2; 08.03.71 - по признаку п. 1, у1саз;-1нно 1 в отличительной части формулы, и по ггоизга- ку п. 3.




Авторы
Даты
1976-08-25—Публикация
1974-02-14—Подача