(54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ПИПЕРАЗИНА
ИЛИ ИХ СОЛЕЙ где 17 представляет собой 1 или 2; Х- атом кислорода или серы; R- представляет собой атом водорода или алкильный радикал, содер жащий 1-3 агома углерода; Het означает гшридил, метилпиридил, метоксипиридил, пириыидинил, оксипиримидинил, ме ток сипи римидинил, аминопиримидинил, диме- тиламинопиримидинил, пиридазинил, пиразинил, хинолил, хиназолинил, гиазолил-1,3, метилтиазо лил-1,3, бензогиазолилгруппа СН - N/ -N-Het всегда связана с бензольным адром, или заключающийся в том, что конденсируют галогенсодержащее производное общей формулы 5 1СН2Ы В-4; где П , X и R ттмеют указанные значения;2 представляет собой атом хлора или группа -СН - Z всегда связана с бензольным ядрок, с N -монозамещенным пиперазином общей формулы 6 где Het имеет указанные значения. Конденсацию проводят в псушрном растворителе, выбираемом из спиртов с высоко температурой сипения, например в бутаноле или пептачоле, или иногда - в алифатичеоком амиде, ){апример в диметилформамиде или диметпламиде уксусной кислоты, или в неполярном растворителе, выбираемом из числа ароматических углеводородов, например в толуоле или ксилоле. Ведут процесс при 1ОО-140 С в присутствии акцептора кислоты, образующейся в ходе реакции. Акцептор кислоты может быть выбран из числа солей щелочных или щелочноземельных металлов карбоновой кислоты, например бикарбоната натрия или калия, карбоната каль ция, или из числа третичных органических оснований, например диметиламина, пиридина или триэтшшмина. При желании можно также заменять эти соли или основания избыточным количеством выбранного N -мо нозамещенного пиперазина. Кроме того, для получения производных общей формулы 4, в которой Het замещен оконрадикалом, желательно проводить конденсацию с производным 6, в котором Hei замещен легко гидрогенизируемым радикалоЦ например бензолоксирадикалом. Затем продукт конденсации подвергают гидрогенолизу в присутствии катализатора, например nai ладия на угле, по известному методу для освобождения функциональной оксигруппы от ее защитной группы. Производные общей формулы 4 являются слабыми основаниями, которые могут быть с помощью кислот переведены в кислые аддитивные соди. В качестве кислот, которые могут быть использованы для образования этих солей, можно назвать, например, из числа неорганических кислот хлористоводородную, бромкстоводородную, серную, фосфорную кяслоты, а из органических - уксусную, пропи- оновую, малеиновую, фумаровую, винную, лимонную, щавелевую, бензойную кислоты. Производные общей формулы 4 могут быть подвергнуты очистке различными физическими способами, нагфимер путем дистипляции, кристаллизации или хроматографии, или же - химическими способами, например путем образования добавочных солей, кристаллизации последних и разложения с помощью щелочных агентов. В приведенных примерах температуры плавления определяли в блоке Кофлера (К) или в капиллярной трубке (кап). Пример 1 . (Кумарашш-5-метил)-1-{пкримидинил-2 )-4-пиперазин j /-Л СН, J S. л -t -iV-/i- В т-ечение 9 час нагревают до кипения смесь, состоящую из 16,9 г (0,1 моль) хлорметил-5-кумарана т. пл, (К) 41-42°С И 32 г (0,2 моль) (пиримидиннл-2)-1-пнперазина в 1оО мл безводного толуола, Отделяющийся хлоргидрат (пиримидинил-2 )- -1-пиперазина фильтруют, а фильтрат несколько раз экстрагируют раствором метансу л ьфокис-по ты. Кислотный экстракт промывают простым эфиром, а затем подщелачивают избыточным количеством карбоната калия.. Полученное таким образом основание экстрагируют с помощью хлороформа, а хлормуравьиный раствор несколько раз промывают водой, вы- сущивают на карбонате калия и выпаривают при умерершом давлении. Получают 25 г осадка, коачэрый рекристаллизуют в 7О мл этанола. В конечном итоге получают 19 г {кумаранил-5-метил)--1-(ш1римидинил-2 )-4-пиперазина в виде белых кристаллов, плавящихся при 102 С (К). Пример 2 . (Кумарапил-5-метил) {тиазолш1 2 )-4-11Иперазп11
сн, -тГЪДр
чО.
1)и 1О() С в течение б час нагревают смесь, состоящую из 16,9 г (0,1 моль) хло)мотнл-5-кумарана, 33,8 г (0,2 моль) ( ТИПЗОЛ1Ш-2 )-1-пиперазина, 500 мл безводного толуола и 1О мл диметидформами- да. Отдоляющийся хлоргидрат (тиазолил-2 )- -1-пиперазпиа фильтруют, а фильтрат несколько раз экстрагируют 1 н. раствором метансульфокислоты.
Кислотный раствор промывают простым
помощью хлороформа, а хлормуравьиаый раствор несколысо раз промывают водой, высушивают иа карбонате калия и выпаривают при умеренном давлении.
Получают осадок, который рекристаллизуют в этаноле. В конечном итоге получают 11 г (кумара1Щл-5-метил)-1-(тиазолил-2)-4-пиперазина в виде кристаллов, плавящихся при 95 С (К).
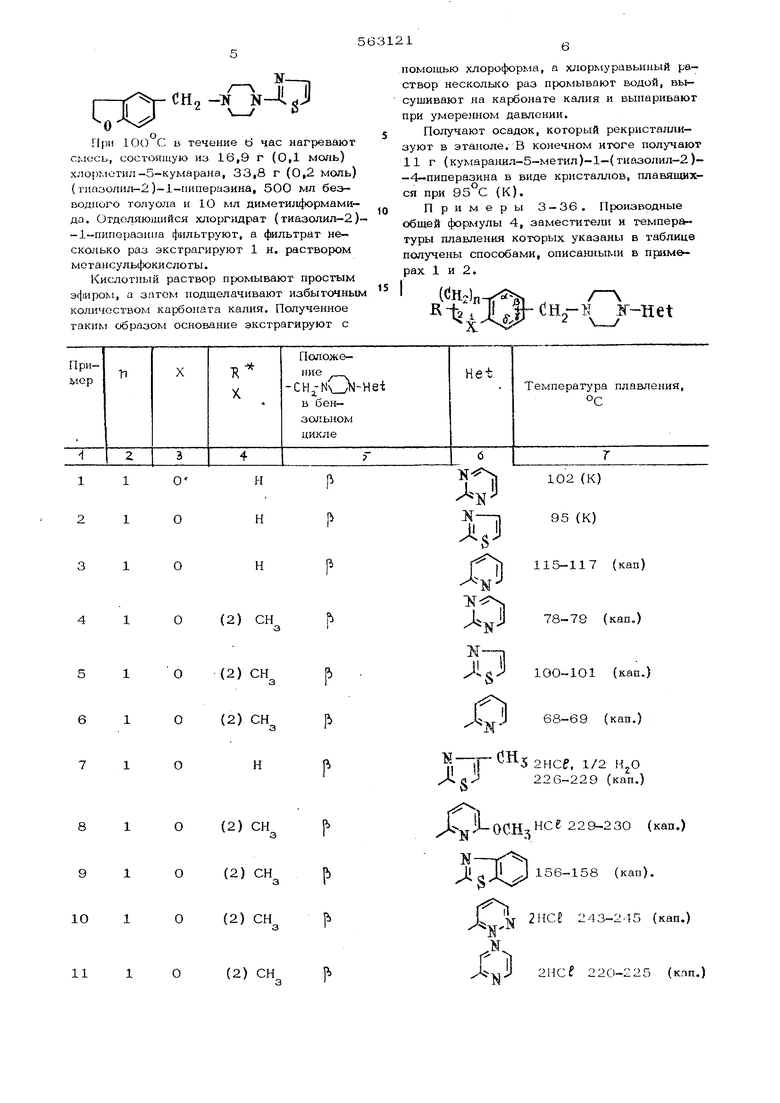
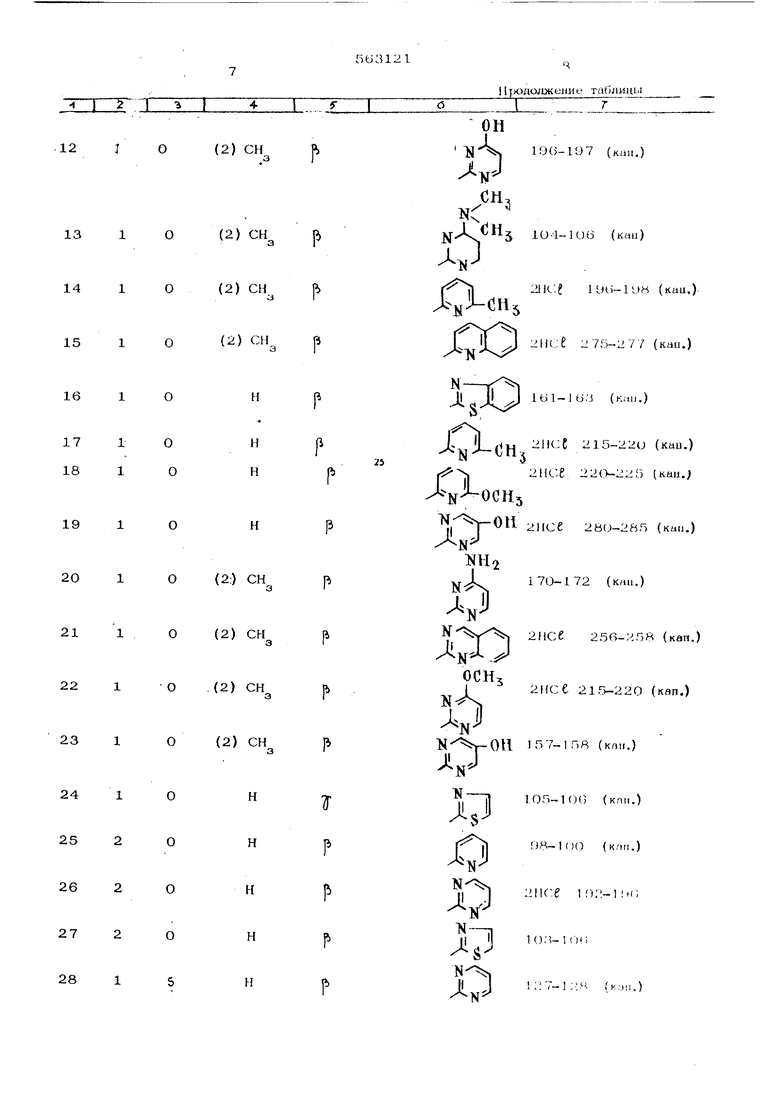
Примеры 3-36. Производные общей формулы 4, заместители и температуры плавления которых указаны в таблице получены способами, описанными в примерах 1 и 2.
563121
9
10 Продолжение таблицы



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных бензодиоксола | 1973 |
|
SU507232A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ДИ- или ТРИФЕНИЛПРОПИЛПИПЕРАЗИНА | 1971 |
|
SU294334A1 |
| ПРОИЗВОДНЫЕ 8-ТРИФТОРМЕТИЛХИНОЛИНКАРБОНОВОЙ КИСЛОТЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ИНГИБИРОВАНИЯ ВИРУСА ИММУНОДЕФИЦИТА | 1995 |
|
RU2140919C1 |
| ПРОИЗВОДНЫЕ ПИПЕРАЗИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1997 |
|
RU2180660C2 |
| ПИРИДИЛТИОСОЕДИНЕНИЯ ДЛЯ БОРЬБЫ С БАКТЕРИЯМИ HELICOBACTER | 1995 |
|
RU2149872C1 |
| ПРОИЗВОДНЫЕ ПИРИДАЗИНАМИНОВ, А ТАКЖЕ ИХ СОЛИ ИЛИ СТЕРЕОХИМИЧЕСКИЕ ИЗОМЕРНЫЕ ФОРМЫ, АНТИВИРУСНАЯ КОМПОЗИЦИЯ И ГЕТЕРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ | 1990 |
|
RU2051149C1 |
| 2,5,7-ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ОКСАЗОЛПИРИМИДИНА | 2011 |
|
RU2557246C2 |
| НОВЫЕ ДИАМИДЫ ПИРИМИДИН-4,6-ДИКАРБОНОВОЙ КИСЛОТЫ ДЛЯ СЕЛЕКТИВНОГО ИНГИБИРОВАНИЯ КОЛЛАГЕНАЗ | 2003 |
|
RU2344129C2 |
| Способ получения -пиримидинилпиперазинов | 1972 |
|
SU437287A1 |
| ВИЧ-ИНГИБИРУЮЩИЕ 5-КАРБО- ИЛИ ГЕТЕРОЦИКЛИЧЕСКИЕ ЗАМЕЩЕННЫЕ ПИРИМИДИНЫ | 2005 |
|
RU2403244C2 |

(2) СН указывает на то, что метильная группа в Сырьем, применяемым для получения производных из примеров 3-36, являются следующие соединения: галогенированные производные формулы5 хлорметил-5-кумаран (для примеров 3 7 и 16-19); метил-2-хлормегил-5-кумаран (для примеров 4-6, 8-15 и 20-23); хлорметил-6-хроман (для примеров 25- 28); хлормегил-5-тиркумаран (для примеров 28-ЗО); хлорметил-6-тиохроман (для примеров |31-33) и хл:орметил-8-тиохроман (для примеров 34-3), пиперазины формулы 6 (пиридил-2)-1-пиперазии (для примеров 3, 6, 25, 29, 32 и 35); (пиримидинил-2)-1-пиперазин (для примеров 4, 26, 28, 31 и 34); (тиазолил-2)-1-пиперазин (для примеров 5, 24, 27, ЗО, 33 и 36); (метил-4-тиазолил-2)-1-пиперазин (для примера 7); (метокси-6-пнридилг-2)-1-Ш1перазин (дл примеров 8 и 19); (бензотиазолил-2)-1-пиперазин (для примеров 9 и 16); 0 гетероцикле закреплена в положении 2. (пиридазинил-6)-1-пш1еразин (для примера 1О); (пиразинил-2)-1-пиперазин (для примв. ра 11); (окси-4-пиримидинил-2)-1-пиперазин (для примера 12); (окси-5-пиримидинил-2 )-1-пиперазин (для примеров 19 и 23); (диметиламино-4-пиримидинилА2 )-1-Ш1еразин (для примера 13); (амино-4-пиримидинил-2 )-1-пиперазин для примера 2О); (метокси-4-пиримидинил-2 )-1-пиперазин для примера 22). Формула изобретения Способ получения производных пиперазиа общей формулы где Г7 1 и 2; X - атом кислорода, серы; R - атом водорода, алкил с 1-3 атомами углерода; Het пиридил, метилпиридил, метоксипиридил, пиримидинил, оксипиримидинил. 11 могоксипиримидкнил, аминопнримидинил, димогиламииоинрлмидинил, пиридазинил, пиразниил, хинолил, хипазолинил, тиазолил-1,3, метилтиазол1 л-1,3, боизотиазолил; А,, х т-1-Т чгруппа 2 всегда связана с бензольным ядром, или их солей, отличающийся тем, что галогенпроизводное общей формулы (СН 1 -s.3 Г -Н-(Нг2 где п , Л, R - имеют указанные значения;I - атом хлора, брома;is гпуппа CHrZ всегда связана с бензольным ядром, 5631 1 подвергают взаимодействию с прюизводным пиперазииа обшей форму;ш1 / У|.-,т . имеет указанные значения, растворителе, выбранноь из спиртов с высокой температурой кипения, из алифахкческих амидов, ароматических углеводородов, при 1ОО-140°С в присутствии акцептора кислоты, с последую1Щ-1М выделени s целевого продукта в свободном виде ил в виде соли, Источники Ю1формации, принятые вовшмание при экспертизе: i 1. Описание к патенту Франции № 2952J - С 07 d 51/70. 11.О5.71.
Авторы
Даты
1977-06-25—Публикация
1974-04-01—Подача