Настоящее изобретение относится к новому производному 8-трифторметилхинолинкарбоновой кислоты, которое ингибирует рост вируса иммунодефицита человека (далее называется ВИЧ), или к его фармацевтически приемлемым соли или эфиру.
Уровень техники
ВИЧ главным образом инфицирует CD4-положительные лимфоциты (помощник/индуктор), постепенно уменьшая количество клеток и вызывая в конечном итоге синдром приобретенного иммунодефицита (далее обозначается СПИД). В связи с этим было предпринято множество попыток лечения СПИДа, но разработка вакцины чрезвычайно трудна, поэтому желательна разработка антивирусных агентов. Хотя получившие в настоящее время одобрение противовирусные агенты, обладающие ингибирующей активностью относительно обращенной транскриптазы, присущей вирусу, продлевают жизнь больным СПИДом, эти агенты не могут полностью вылечить это заболевание. Кроме того, эти ингибирующие агенты имеют большою число проблем, связанных с побочными эффектами, такими как миелопатия и заболевания пищеварительной системы и т.д., которые проявляются в значительной степени, и высокой частотой появления у пациента, которому вводится такой агент в течение длительного периода времени, устойчивых к лекарству вирусов, а также ряд других проблем. Таким образом, существует крайняя необходимость в разработке новых лекарственных препаратов и схем лечения с использованием комбинации большого числа агентов.
Недавно сообщалось об анти-ВИЧ активности DR-3355, который является оптическим изомером синтетического антибактериального агента Офлоксацина, который имеет скелет хинолинкарбоновой кислоты (J.Nozaki, Renard el: al., AIDS 4, 1283(1990)). Однако, когда авторы настоящего изобретения изучили подавляющую заболевание активность DR-3355 в отношении ВИЧ-инфицированных клеток в соответствии с методом R.Pauwe/et Al., описанным ниже, они не обнаружили никакой анти-ВИЧ активности. Также описана анти-ВИЧ активность Норфлоксацина, Эноксацина, Ципрофлоксацина, Ломефлоксацина, Дифлоксацина, Тосуфлоксацина и дp.(WO/13541), но для этих соединений также не выявлено никакой анти-ВИЧ активности.
Для осуществления настоящего изобретения заявители изучили анти-ВИЧ активность различных видов производных хинолинкарбоновых кислот и установили, что производное хинолинкарбоновой кислоты, гидрофобность которого повышена и противобактериальная активность которого ослаблена за счет введения трифторметильной группы в 8-ое положение и циклическая диаминовая группа (например, пиперазинильная группа или гомопи-перазинильная группа, которая может быть замещена) замещена фенильной группой или ароматической гетероциклической группой в 7-ом положении, может специфически подавлять рост ВИЧ в ВИЧ-инфицированных клетках и, кроме того, обладает способностью подавлять цитопатогенное действие БИЧ.
Описание изобретения
Настоящее изобретение включает производное 8-трифторметилхинолинкарбоновой кислоты, представленной формулой (I) или его фармацевтически приемлемые соль или эфир: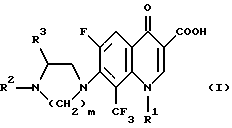
где R1 представляет собой низшую алкильную группу, низшую галагеналкильную группу или циклоалкильную группу, R2 представляет собой фенильную группу, которая может быть замещена R0, 5-ти или 6-ти членную гетеромоноциклическую группу, содержащую 1 или 2 гетероатома, выбираемых из N, О и S, которая может быть замещена R0, или ароматическую гетероциклическую конденсированную группу, в которой указанная ароматическая гетеромоноциклическая группа и бензольное кольцо сконденсированы, R0 выбирается из группы, включающей галоген, низший алкил, фторзамещенный низший алкил, низшую алкокси-группу или низшую алкилгруппу, R3 представляет собой водород или низшую алкильную группу и m принимает целые значения 2 или 3.
Преимущественный вариант осуществления изобретения
Низшая алкильная группа R1 в приведенной выше формуле (I) включает, например, C1-C4-алкильные группы, такие как метил, этил, пропил, изопропил, бутил, изобутил, втор.-бутил и трет.бутил и др., предпочтительными являются метильная, этильная пропильная и изопропильная группы, особенно предпочтительны метильная и этильная группа.
Низшая галогеналкильная группа R1 включает, например, галоген-C1-C4-алкильные группы, такие как трифторметильная, хлорметильная, дифторметильная, трифторметильная, фторэтильная, 2-хлорэтильная, 2-бром-этильная, 2-иодэтилбная, 2,2,2-трифторэтильная, 3-фторпропильная, 3-хлорпропильная, 3-бромпропильная и 4-фторбутильная и др. группы, предпочтительными являются 2-фторэтильная, 2-хлорэтильная и 2,2,2-трифторэтильная группы, особенно предпочтительной является 2-фторэтильная группа.
Циклоалкильная группа R1 включает, например, C3-C6-циклоалкильные группы, такие как циклопропильная, циклобутильная, циклопентильная, циклогексильная и др., предпочтительными являются циклопропильная, циклобутильная и циклопентильная, особенно предпочтительна циклопропильная группа.
Ароматическая гетероциклическая группа или ароматическая конденсированная группа (в дальнейшем гетероциклическая группа) R2 включает, например, 2-тиенил, 2-фурил, 2-оксазолил, 2-тиазолил, 2-имидазолил, 2-,3- или 4-пиридил, 2-, 4- или 5-пиримидинил, 2-пиразинил, 3-пиридазинил, 2-бензоксазолил, 2-бензотиазолил и 2-бензимидазолил, предпочтительно группы 2-тиенил, 2-фурил, 2-оксазолил, 2-тиазолил, 2-имидазолил, 2-,3- или 4-пиридил, 2-,4- или 5-пиримидинил, 2-пиразинил и 3-пиридазинил, особенно предпочтительны группы 2-пиридил и 2-пиримидинил.
Заместитель R0 фенильного или ароматического гетероциклического кольца R2 включает, например, атом галогена, такой как фтор, хлор, бром, иод и т.д. ; C1-C4-алкильную группу, такую как метил, этил, пропил, изопропил, бутил, втор. -бутил, изобутил, трет.бутил и т.д.; замещенную фтором C1-C4-алкильную группу, такую как моно-, ди- и трифторметил, 2-фторэтил,2- или 3-фторпропил, 2-3- или 4-фторбутил и т.д.; C1-C4-алкоксильную группу, такую как метокси, этокси, пропокси, изопропокси, изобутокси, втор.-бутокси, тре.-бутокси и т. д.; C1-C4-алкилтио группу, такую как метилтио, этилтио, пропилтио, изопропилтио, бутилтио, изобутилтио, вторбутилтио, третбутилтио и т.д.; предпочтительны атомы фтора, хлора и группы метил, этил, трифторметил, метокси, этокси, метилтио и этилтио, особенно предпочтительны атомы фтора, хлора и группы метил, трифторметил, метокси и метилтио.
Низшая алкильная группа R3 включает, например, C1-C4-алкильную группу, такую как метил, этил, пропил, изопропил, бутил, изобутил, втор.-бутил, трет.-бутил и т. д.; предпочтительны группы метил, этил, пропил и изопропил, особенно предпочтительны группы метил и этил.
Карбоксильная группа соединения, представленного выше формулой (I), может быть защищена защитной группой с образованием сложного эфира. В качестве такой защитной группы может быть использована, например, C1-C4-алкильная группа, такая как метил, этил, пропил, изопропил, бутил, изобутил, и т.д., или аралкильная группа, такая, как бензил, фенилэтил и т. д. , или C2-C5-алканоилоксиалкильная группа, которая, in vivo легко гидролизуется с образованием карбоксильной группы, такая как ацетоксиметил, пивалоилоксиметил и т.д.: C1-C4-алкоксикарбонилоксиалкильная группа, такая как группы 1-(этоксикарболнилокси)этил, 1-(изопропоксикарбонилокси)этил и т.д., N,N-диалкилзамещенная аминокарбонилалкильная группа, такая как N,N-диметиламинокарбонилметильная группа и т.д.; N,N-диалкилзамещенная аминоалкильная группа, такая как 2-(N,N-диметиламино)этильная группа и т.д.; алкильная замещенная 5- или 6-членным насыщенным гетеромоноциклическим кольцом, содержащим 1 или 2 гетероатома, который выбирают из группы, включающей N, О или S, такая как 2-морфолиноэтил, 2-пиперидиноэтил, 2-(4-метилпиперидино)этил и т.д.; или группа (5-метил-2-оксо-1,3-диоксолен 4-ил)метил.
В конце описания приведены таблицы 1-10 с соединениями общей формулы I.
Более предпочтительными соединениями формулы (1) являются такие соединения, как:
1-циклопропил-6-фтор-8-трифторметил-1,4-дигидро-4-оксо-7-[4-(2-пиримидинил)пиперазин-1-ил]хинолин-карбоновая кислота;
1-циклопропил-6-фтор-8-трифторметил-1,4-дигидро-4-оксо-7-[4-(2-пиридил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-8-трифторметил-1,4-дигидро-4-оксо-7-[4-(2-метоксифенил)пиперазин-1-ил]хинолин-3-карбоновая-кислота;
1-циклопропил-6-фтор-8-трифторметил-1,4-дигидро-4-оксо-7-(4-фенилпипераэин-1-ил)хинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-8-трифторметил-1,4-дигидро-4-оксо-7-[4-(3-хлорфенил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-8-трифторметил-1,4-дигидро-4-оксо-7-[4-(4-фторфенил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-8-трифторметил-1,4-дигидро-4-оксо-7-[4-(3-трифторметилфенил)пиперазин-1-ил]хинолин-3-карбоновая кислота
6-фтор-8-трифторметил-1,4-дигилро-4-оксо-1-метил-7-[4-(2-пиримидинил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
6-фтор-8-трифторметил-1,4-дигидро-4-оксо-1-метил-7-[4-(2-пиридил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
1-этил-6-фтор-8-трифторметил-1,4-дигидро-4-оксо-7-[4-(2-пиримидинил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
1-этил-6-фтор-8-трифторметил-1,4-дигидро-4-оксо-7-[4-(2-пиридил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
1-этил-6-фтор-8-трифторметил-1,4-дигидро-4-оксо-7-[4-(2-метоксифенил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
6-фтор-8-трифторметил-1,4-дигидро-4-оксо-1-изопропил-7-[4-(2-пиримидинил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
6-фтор-трифторметил-1,4-дигидро-4-оксо-1-изопропил-7-[4-(2-пиридил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
6-фтор-8-трифторметил-1,4-дигидро-4-оксо-1-изопропил-7-[4-(2-метоксифенил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
6-фтор-1-(2-фторэтил)-8-трифторметил-1,4-дигидро-4-оксо-7-[4-(2-пиримидинил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
6-фтор-1-(2-фторэтил)-8-трифторметил-1,4-дигидро-4-оксо-7-[4-(2-пиридил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
6-фтор-1-(2-фторэтил)-8-трифторметил-1,4-дигидpo-4-oкco-7-[4-(2-метoкcифeнил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
6-фтор-8-трифторметил-1,4-дигидро-4-оксо-1-метил-7-[4-(2-метоксифенил)пиперазин-1-ил)хинолин-3-карбоновая кислота;
6-фтор-8-трифторметил-1,4-дигидро-4-оксо-1-метил-7-[4-(2-хлорфенил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
6-фтор-8-трифторметил-1,4-дигидро-4-оксо-1-метил-7-(4-фенилпиперазин-1-ил)хинолин-3-карбоновая кислота;
6-фтор-8-трифторметил-1,4-дигидро-4-оксо-1-метил-7-[4-(4-фторфенил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
6-фтор-8-трифторметил-1,4-дигидро-4-оксо-1-метил-7-[4-(2-тиазолил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
6-фтор-8-трифторметил-1,4-дигидро-4-оксо-1-метил-7-[4-(2-метилтиофенил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
1-этил-6-фтор-8-трифторметил-1,4-дигидро-4-оксо-7-[4-(4-метоксифенил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
1-этил-6-фтор-8-трифторметил-1,4-дигидро-4-оксо-7-[4-(4-хлорфенил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
1-этил-6-фтор-8-трифторметил-1,4-дигидро-4-оксо-7-[4-(4-хлор-2-пиридил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
1-этил-6-фтор-8-трифторметил-1,4-дигидро-4-оксо-7-[4-(2-фторфенил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
1-этил-6-фтор-8-трифторметил-1,4-дигидро-4-оксо-7-[4-(3-метоксиифенил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
1-циклопропил-6-фтор-8-трифторметил-1,4-дигидро-4-оксо-7-[4-(2-пиридил)пиперазин-1-ил]хинолин-3-карбоновая кислота, 2-морфолиноэтиловый эфир;
6-фтор-8-трифторметил-1,4-дигидро-4-оксо-1-метил-7-[3-метил-4-(2-пиримидинил)пиперазин-1-ил]хинолин-3-карбоновая кислота и
6-фтор-8-трифторметил-1,4-дигидро-4-оксо-1-метил-7-[4-(2-пиримидинил)гомопиперазин-1-ил]хинолин-3-карбоновая кислота.
Еще более предпочтительными соединениями являются такие соединения как:
1-циклопропил-6-фтор-8-трифторметил-1,4-дигидро-4-оксо-7-[4-(2-пиридил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
6-фтор-8-трифторметил-1,4-дигидро-4-оксо-1-метил-7-[4-(2-пиримидинил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
6-фтор-8-трифторметил-1,4-дигидро-4-оксо-1-метил-7-[4- (2-пиридил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
1-этил-6-фтор-8-трифторметил-1,4-дигидро-4-оксо-7-[4-(2-пиридил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
6-фтор-8-трифторметил-1,4-дигидро-4-оксо-1-метил-7-[4-(4-фторфенил)пиперазин-1-ил]хинолин-3-карбоновая кислота и
6-фтор-8-трифторметил-1,4-дигидро-4-оксо-1-метил-7-[4-(4-(2-тиазолил)пиперазин-1-ил]хинолин-3-карбоновая кислота.
И наиболее предпочтительными соединениями являются:
1-циклопропил-6-фтор-8-трифторметил-1,4-дигидро-4-оксо-7-[4-(2-пиридил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
6-фтор-8-трифторметил-1,4-дигидро-4-оксо-1-метил-7-[4-(2-пиримидинил)пиперазин-1-ил]хинолин-3-карбоновая кислота;
6-фтор-8-трифторметил-1,4-дигидро-4-оксо-1-метил-7-[4-(2-пиридил)пиперазин-1-ил] инолин-3-карбоновая кислота;
Соединения, представленные формулой (I), получают Способом A или Способом B, которые приведены ниже.
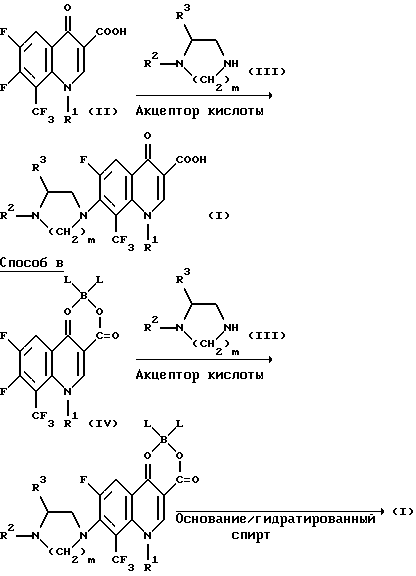
где заместители R1, R2, R3 и m принимают указанные выше значения, а L представляет собой фтор или ацетокси-группу.
В соответствии со Способом A требуемое соединение (I) получают взаимодействием хинолинкарбоновой кислоты (II) с циклическим диамином (III) в присутствии или отсутствии акцептора кислоты и в присутствии растворителя или без растворителя.
В данной реакции в качестве растворителя предпочтительно использовать апротонные полярные растворители, такие как диметилсульфоксид, N,N-диметилформамид, триамид гексаметилфосфорной кислоты, N,N-диметилацетамид и т.д. ; также могут использоваться кетоны, такие как ацетон, метилэтилкетон и т.д. ; простые эфиры, такие как диэтиловый эфир, тетрагидрофуран, диоксан и т.д.; сложные эфиры, такие как этилацетат и т.д.; спирты, такие как метанол, этанол, пропанол, изопропанол, бутанол и т.д.; и нитрилы, такие как ацетонитрил и т.д. В качестве акцептора кислоты могут быть использованы третичные амины, такие как 1,8-диазобицикло[5.4.0]-7- ундецен, 1,5-диазобицикло[4.3.0]-5-нонен, триэтиламин, трибутиламин, пиридин, пиколин, лутидин, коллидин и т.д.; алкоголяты металлов, такие как метилат натрия, этилат натрия, трет.-бутилат калия и т.д.; или неорганические основания, такие как карбонат натрия, карбонат калия и т.д.
Предпочтительно используют акцептор кислоты в количестве от эквимолярного до 5 молей на моль соединения (II), но в случае использования указанных выше третичных аминов, они могут добавляться в большом избытке в качестве растворителя. Избыток циклического диамина (III) также действует как акцептор кислоты так, что реакция протекает гладко даже в отсутствии других акцепторов кислоты. Реакцию проводят в интервале температур от 0 до 200oC, обычно в течение 0.5-24 часов.
В соответствии со Способом B желаемое соединение (I) получают взаимодействием хелатного соединения бора (IV) с циклическим диамином (III) в присутствии или в отсутствие акцептора кислоты, в присутствии растворителя или без растворителя аналогично тому, как это описано в способе A, с получением соединения (V). Затем это соединение обрабатывают гидратированным спиртом в присутствии основания для разложения хелата. Реакцию конденсации по способу B проводят в тех же условиях, которые описаны выше для способа A.
В качестве основания для разложения хелата по указанному выше Cпособу B могут быть использованы гидроксиды щелочных металлов, такие как гидроксид натрия, гидроксид калия и т. д. ; карбонаты щелочных металлов, такие как карбонат натрия, карбонат калия и т.д.; третичные амины, такие как 1,8-диазобицикло[5.4.0] -7-ундецен, 1,5-диазобицикло[4.3.0]-5-нонен, триэтиламин, 4-диметиламинопиридин и т.д.; алкоголяты металлов, такие как метилат натрия, этилат натрия, трет.-бутилат калия и т.д.
Предпочтительно используют акцептор кислоты в количестве от эквимолярного до 5-кратного избытка на моль соединения (V), однако акцептор кислоты может быть использован в большом избытке.
В качестве гидратированного спирта, который может быть использован как растворитель, используют, например, метанол, этанол, пропанол, изопропанол и/или бутанол и т.д., содержащие от 5 до 90 вес.% воды.
Реакцию проводят при температуре в интервале температур от 0 до 150oC в течении 0.5-24 часов.
В описанных выше реакциях по окончании реакции желаемые соединения могут быть выделены обработкой реакционных смесей обычными методами и, при необходимости, могут быть очищены обычными методами, такими как перекристаллизация, колоночная хроматография и т.д.
Полученные таким образом соединения (I) при необходимости могут быть переведены в соли обычными методами.
Соединение (I'), в котором заместитель R2 в вышеуказанной формуле (I), представляет собой ароматическую гетероциклическую кольцевую группу, также получают в соответствии с приведенным ниже Способом C.
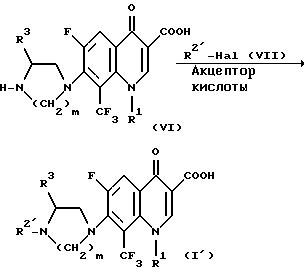
где заместители R1 и R3 принимают указанные выше значения, a R2 представляет собой ароматическую гетероциклическую группу.
Реакцию в соответствии со Способом C проводят таким же образом, как это описано для Способа A.
То есть соединение (I') получают взаимодействием хинолинкарбоновой кислоты (VI) с соединением (VII), которое берут в количестве от эквимолярного до 5-ти кратного мольного избытка, в присутствии акцептора кислоты и в присутствии растворителя или без растворителя.
По Способу C в качестве растворителя предпочтительно использовать апротонные полярные растворители, такие как диметилсульфоксид, N,N-диметилформамил, триамид гексаметилфосфорной кислоты, N,N-диметилацетамид и т.д.; также могут использоваться кетоны, такие как ацетон, метилэтилкетон и т.д.; простые эфиры, такие как диэтиловый эфир, тетрагидрофуран, диоксан и т.д.; сложные эфиры, такие как: этилацетат и т.д.; спирты, такие как метанол, этанол, пропанол, изопропанол, бутанол и т.д.; нитрилы, такие как ацетонитрил и т.д.
В качестве акцептора кислоты могут быть использованы третичные амины, такие как 1,8-диазабицикло[5.4.0]-7-ундецен, 1,5-диазабицикло [4.3.0]-5-нонен, триэтиламин, трибутиламин, пиридин, пиколин, лутидин, коллидин и т.д.; или неорганические основания, такие как карбонат натрия, карбонат калия и т. д.
Предпочтительно используют акцептор кислоты в количестве от эквимолярного до 10-кратного избытка на моль соединения (VII), но в случае использования указанных выше третичных аминов они могут вводиться в очень большом избытке в качестве растворителя.
Реакцию проводят в интервале температур от 0 до 200oC, обычно в течение от 1 до 24 часов. Используемое в синтезе по Способу C в качестве исходного реагента соединение (VI) получают реакцией соединения (II) или (IV) в качестве исходного реагента с диамином (III), в котором заместитель R2 представляет собой водород, аналогично тому, как это описано для Способов A или B.
Соединение (II), используемое в качестве исходного реагента в приведенном выше Способе A, получают, например, по способу D из соединения (VII), полученного по методу, описанному в японской патентной заявке N 66180/1989 (см., например Японскую патентную заявку N 255183/1993).
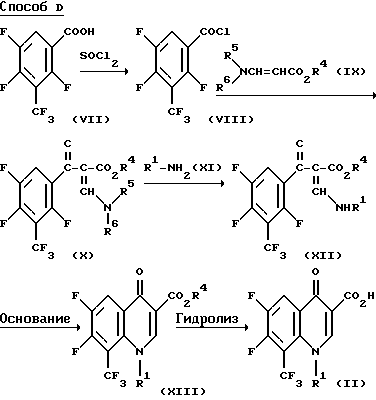
где R1 принимает заданные выше значения, R4 представляет собой низшую алкильную группу, а R5 и R6 представляют собой алкильные группы, которые могут быть одинаковыми или разными.
Используемое в качестве исходного реагента в Способе B хелатное соединение бора (VI) легко получают из соединения (II), полученного по Способу D, или его низшего алкилового эфира (XII) в соответствии со Способом E (см., например. Японскую патентную заявку N 124873/1990 (Справочный номер 7) и Японскую патентную заявку N 287577/1991 (Справочный номер 4)).
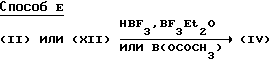
В некоторых случаях соединения формулы (I) могут иметь оптические изомеры. Оптические изомеры соответствующих целевых соединений (I) могут быть получены проведением вышеуказанных реакций с использованием оптически разделенных исходных соединений на соответствующей стадии. Кроме того, оптические изомеры могут быть выделены при обработке смеси оптических изомеров, используя обычные методы разделения оптических изомеров.
Карбоксильная группа соединения формулы (I) может быть защищена с образованием сложного эфира, как это описано выше. Реакцию этерификации, исходя из соответствующего карбоксильного соединения и спирта, проводят обычными методами (см. , например, метолом кислотно-катализируемой конденсации-дегидратации, через хлорангидрид, методом конденсации-дегидратации карбодиимидом и т.д.).
Соединения формулы (I) могут быть использованы для лечения СПИДа, вызванного ВИЧ. С этой целью соединения могут быть введены, например, перорально в виде таблеток, капсул, гранул, порошка, сиропа и т.д., парентерально с помощью внутривенных инъекций, внутримышечных инъекций, свечей и т.д. Эти препараты могут быть приготовлены известными методами с использованием, если это необходимо, добавок, таких как связующий агент, разрыхляющий агент, смазывающее вещество, стабилизатор и т.д. Доза варьируется в зависимости от возраста, веса, серьезности заболевания, формы и времени введения препарата и т.д., обычно соединение формулы (I) вводят взрослым в дозе приблизительно от 10 до 500 мг в день однократно или за несколько раз. При пероральном введении соединения формулы (I) крысам в дозе, в несколько раз превышающей приведенный выше уровень (вычислено по весу), токсическое действие не выявлено.
Настоящее изобретение поясняется более подробно с помощью Примеров и Справочных примеров, приведенных ниже.
Пример 1
Синтез 1-циклопропил-6-фтор-8-трифторметил-1,4-дигидро-4-оксо-[4-(2-пиримидинил)пиперазин-1-ил]хинолин-3-карбоновой кислоты
В 20 мл пиридина растворяют 1.0 г (0.003 моля) 1-циклопропил-6,7- дифтор-8-трифторметил-1,4-дигидро-4-оксохинолин-3-карбоновой кислоты и 1.23 г (0.0075 моля) 1-(2-пиримидинил)пиперазина и эту смесь перемешивают при 105oC в течение 3 часов. Затем растворитель удаляют при пониженном давлении и остаток хроматографируют на колонке с силикагелем (элюент - смесь хлороформ: метанол= 9.5: 0.5), получают 0.68 г 1-циклопропил-6-фтор-8-трифторметил-1,4-дигидро-4-оксо-[4-(2-пиримидинил)пиперазин-1-ил] хинолин-3-карбоновой кислоты в виде желтого порошка.
Температура плавления от 285 до 287oC.
ЯМР (ДМСО d6), δ м.д.: 0.91 (2Н, м), 1.17-1.18 (2H, м), 3.49 (4Н, ушир. с), 3.94 (4Н, ушир.с), 4.07 (1Н, м), 6.69-6.71 (1Н, т, J=9.3 Гц), 8.06-8.09 (1Н, д, J=11.7 Гц), 8.42-8.43 (2Н. д, J= 4.4 Гц), 8.85 (1Н, с), 14.58 (1Н, с).
Масс-спектр (химическая ионизация): м/е=478(М++1).
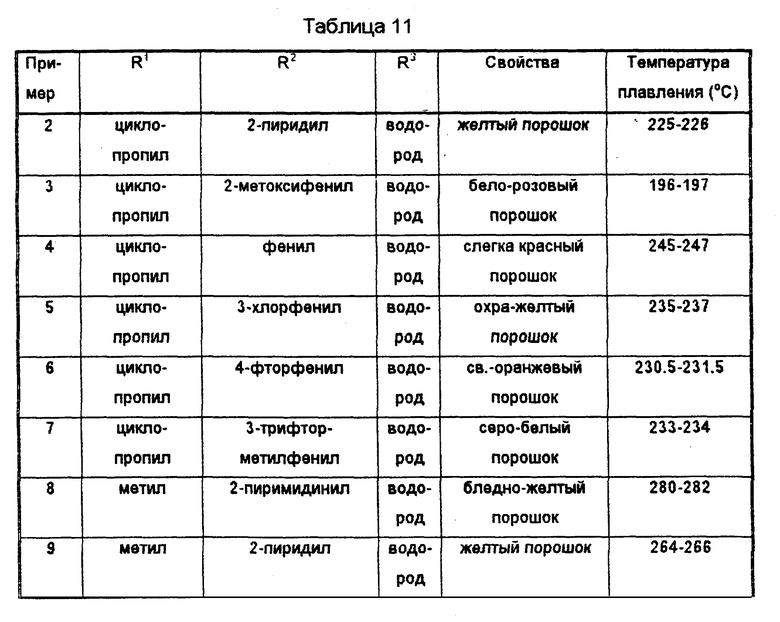
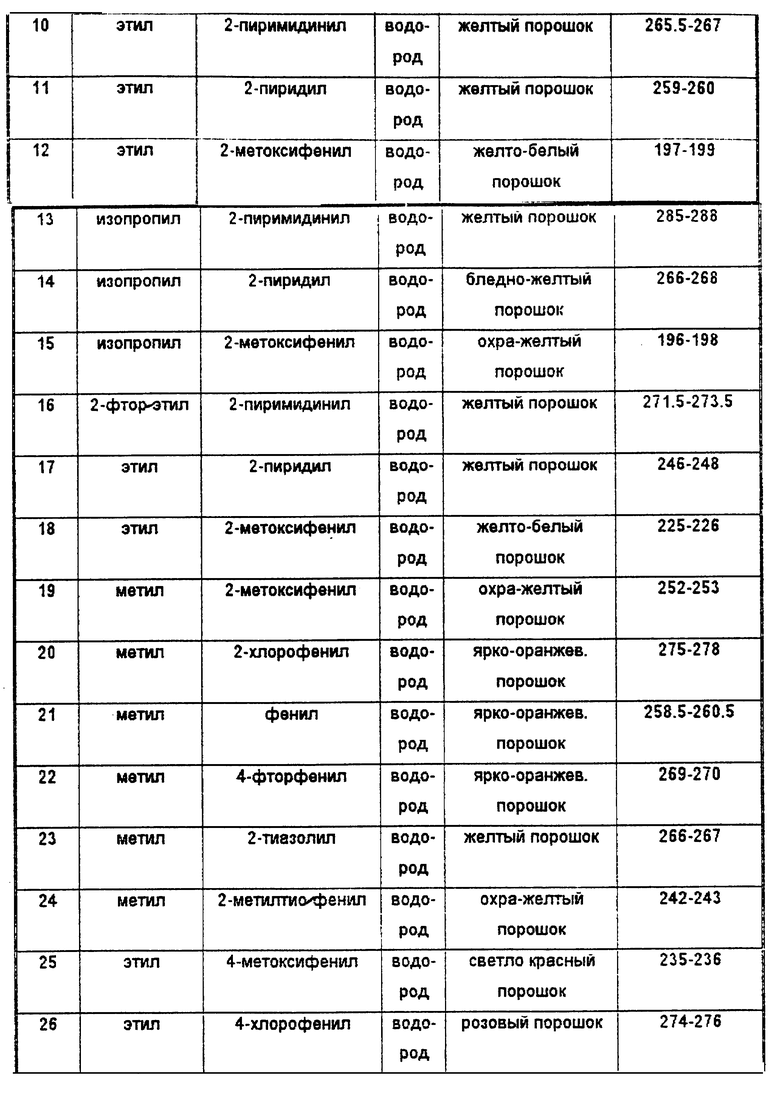
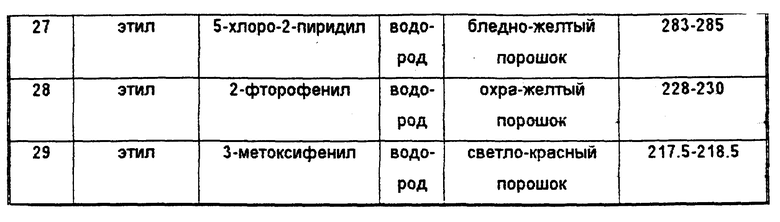
Примеры 2-29
Способом, аналогичным способу Примера 1, синтезируют соединения, приведенные в Таблице 11.
Пример 30
Синтез 2-морфолиноэтилового эфира 1-циклопропил-6-фторо-8-трифторметил-1,4-дигидро-4-оксо-7-[4-(2-пиридил)пипераpин-1-ил] -хинолин-3-карбоновой кислоты
К 5 мл метиленхлорида добавляют 100 мг (0.21 ммоля) 1-циклопропил-6-фторо-8-трифторметил-1,4-дигидро-4-оксо-7-[4-(2-пиридил)пиперазин-1-ил] -хинолин-3-карбоновой кислоты, 0.055 г (0.42 ммоля) 4-(2-гидроксиэтил)морфолина, 0.045 г (0.37 ммоля) 4-диметиламинопиридина и 0.091 г (0.48 ммоля) гидрохлорида 1-этил-3-(3-димитил-аминопропил)карбодиимида, смесь оставляют при комнатной температуре на 7 дней, затем растворитель упаривают при пониженном давлении. Остаток хроматографируют на колонке (элюент - смесь хлороформ : метанол : 28%-ный водный аммиак = 40:9:1), получают 60 мг 2-морфолиноэтилового эфира 1-циклопропил-6-фтор-8-трифторметил-1,4-дигидро-4-оксо-7-[4-(2-пиридил)пиперазин-1-ил] - хинолин-3-карбоновой кислоты в виде светло-желтого порошка.
Температура плавления от 203 до 205oC.
Масс-спектр (химическая ионизация): м/е=590 (М++1).
Пример 31
Синтез 6-фтор-8-трифторметил-1,4-дигидро-4-оксо-1-метил-7-[3-метил-4-(2-пиримидинил)пиперазин-1-ил]-хинолин-3-карбоновой кислоты.
В 30 мл пиридина растворяют 1.5 г (0.0049 моля) 6,7-дифтор-8-трифторметил-1,4-дигидро-1-метил-4-оксо-хинолин-3-карбоновой кислоты и 1.5 г (0.015 моля) 2-метилпиперазина, смесь перемешивают при 105oC в течение 3 часов и затем растворитель упаривают при пониженном давлении. К остатку добавляют этанол, выпавшие кристаллы отфильтровывают, промывают этанолом, сушат и получают 1.49 г 6-фтор-8-трифторметил-1,4-дигидро-4-оксо-1-метил-7-(3-метилпиперазин-1-ил)-хинолин-3-карбоновой кислоты.
К 20 мл N,N-диметилформамида добавляют 1.49 г (0.0039 моля) полученной 6-фтор-8-трифторметил-1,4-дигидро-4-оксо-1-метил-7-(3-метилпиперазин-1-ил)-хинолин-3-карбоновой кислоты, 0.88 г (0.0077 моля) 2-хлоропиримидина и 0.78 г (0.0077 моля) триэтиламина, смесь перемешивают при 130oC в течение 10 часов и затем растворитель упаривают при пониженном давлении.
Остаток хроматографируют на колонке с силикагелем (элюент - смесь хлороформ: метанол = 9:1), получают 0.35 г 6-фтор-8-трифторметил-1,4-дигидро-4-оксо-1-метил-7-[3-метил-4-(2-пиримидинил)пиперазин-1-ил] -хинолин-3-карбоновой кислоты в виде охра-желтого порошка.
Температура плавления от 283 до 284.5oC.
Масс-спектр (химическая ионизация): м/е=466 (М++1).
Элементный анализ: Вычислено, %: C 53.17, H 4.25, N 14.76, C21H19F4N5O3•1/2H2O. Найдено, %: C 53.47, H 4.07, N 14.95.
Пример 32
Синтез 6-фтор-8-трифторметил-1,4-дигидро-4-оксо-1-метил-7-[4-(2-пиримидинил)гомопиперазин-1-ил]-хинолин-3-карбоновой кислоты
В 12 мл пиридина растворяют 0.8 г (0.0026 моля) 6,7-дифтор-8-трифторметил-1,4-дигидро-1-метил-4-оксо-хинолин-3-карбоновой кислоты и 2.1 г (0.0118 моля) 1-пиримидинил)гомопиперазина, полученную смесь перемешивают при 10oC в течение 3 часов и затем растворитель упаривают при пониженном давлении. Остаток подвергают хроматографированию на колонке с силикагелем (элюент - смесь хлороформ: метанол = 9.5:0.5), получают 0.45 г 6-фтор-8-трифторметил-1,4-дигидро-4-оксо-1-метил-7-[4-(2-пиримидинил)гомопиперазин-1-ил]-хинолин-3-карбоновой кислоты в виде желтого порошка. Температура плавления от 243 до 245oC.
Масс-спектр (химическая ионизация): м/е=466 (М++1).
Элементный анализ: Вычислено, %: C 54.20, H 4.11, N 15.05, C21H19F4N5O3. Найдено, %: C 54.06, H 4.03, N 14.96.
Пример 33
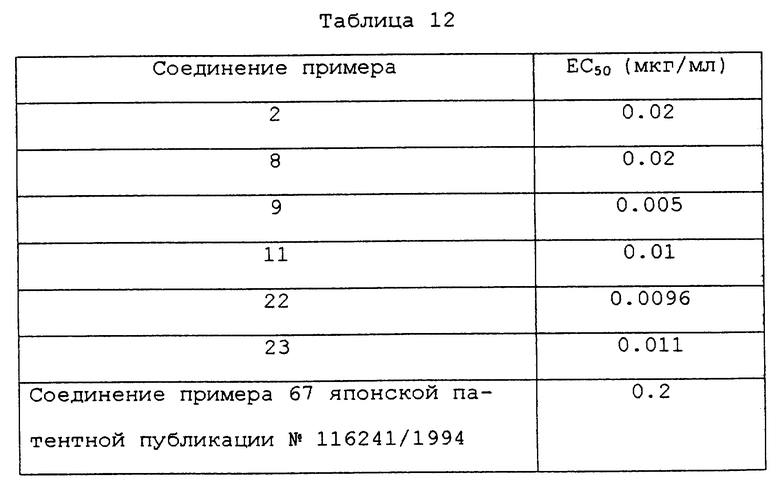
Измерение анти-ВИЧ активности соединений настоящего изобретения проводят в соответствии со способом, описанным R.Pauwel et al.(J. Virological Method 20, p. 309-321 (1988)). To есть МТ-4 клетки центрифугируют (1000xg, 5 минут) и раствор с плавающими клетками, в котором суспендированы полученные клеточные осадки в не содержащей сыворотку среде RPMI-1460, засевают ВИЧ. Смесь выдерживают при 37oC в течение 1 часа и затем добавляют в среду RPMI-1460, в которую добавлено 10% сыворотки плода крупного скота (далее называемой сывороточной средой) смесь промывают и центрифугируют (1000xg, 5 минут). Полученные таким образом ВИЧ-инфицированные клетки и ВИЧ-неинфицированные клетки суспендируют в сывороточной среде из расчета 4•105мл и каждые 100 мкл суспензий распределяют в соответствующие лунки 96-луночного планшета для культуры тканей. Каждые 100 мкл соединений, которые предварительно разбавлены сывороточной средой, распределяют по соответствующим лункам и затем смесь выдерживают при температуре 37oC в течение 5 дней в присутствии 5% диоксида углерода. Аналогично выдерживают ВИЧ-инфицированные клетки и ВИЧ-неинфицированные, к которым не было добавлено соединение настоящего изобретения. По окончании выдерживания оценивают живые клетки с использованием МТТ (3-(4,5-диметил-тиазол-2-ил)-2,5-дифенилтетразолийбромид) для определения подавляющей заболевание клеток активности (анти-ВИЧ) активности, достигаемой при добавлении соединения. Подтверждено, что как в клеточном растворе, так и в растворе, инокулированном вирусом, отсутствует микоплазма.
Активность подавления клеточного заболевания в отношении ВИЧ-неинфицированных клеток, к которым не было добавлено соединение настоящего изобретения, принимается за 100%, а активность клеточного заболевания в отношении ВИЧ-инфицированных клеток, к которым не было добавлено соединение, принимают за 0%. Определяют концентрацию соединения (EC50), при которой наблюдается 50%-ная активность подавления клеточного заболевания в отношении ВИЧ-инфицированных клеток. Полученные результаты представлены в Таблице 12.
Справочный пример 1
Синтез 1-циклопропил-6,7-дифтор-8-трифторметил-1,4-дигидро-4-оксохинолин-3-карбоновой кислоты (II; R1=циклопропил)
К 8.5 г (0.0348 моля) 2,4,5-трифтор-3-трифторметил-бензойной кислоты (VII) добавляют 30 мл бензола, 17 мл тионилхлорида и несколько капель N,N-диметилформамида и полученную смесь нагревают с обратным холодильником в течение 3 часов. По окончании реакции бензол и избыточный тионилхлорид упаривают при пониженном давлении, получают хлорангидрид 2,4,5-трифтор-3-трифторметилбензойной кислоты (VIII).
Затем в 30 мл безводного тетрагидрофурана растворяют 5.47 г (0.0383 моля) этилового эфира 3-диметиламиноакриловой кислоты (IX; R4=R5=метил) и к полученному раствору добавляют 4.2 г (0.0415 моля) триэтиламина и при комнатной температуре постепенно, по каплям к смеси добавляют раствор вышеуказанного хлорангидрида в 7 мл безводного тетрагидрофурана. По окончании добавления полученную смесь выдерживают при 50oC в течение 3 часов, охлаждают до комнатной температуры и затем фильтруют. К фильтрату добавляют 3.9 г (0.0417 моля) гидрохлорида циклопропиламина (XI; R1=циклопропил) и смесь перемешивают при 40oC в течение 30 минут. Смесь охлаждают до комнатной температуры и фильтруют, фильтрат концентрируют при пониженном давлении и остаток хроматографируют на колонке с силикагелем (элюент - смесь этилацетат: толуол= 1:4), получают 10.63 г этилового эфира 2-(2,4,5-трифтор-3-трифторметилбензоил)-3-циклoпpoпилaминoaкpилoвoй кислоты (XII; R1=циклопропил, R3= этил) в виде светло-желтого твердого вещества. Это соединение растворяют в 100 мл безводного диэтилового эфира и к раствору, при охлаждении льдом, постепенно добавляют 1.6 г (0.0416 моля) 62.4 %-ного гидрида натрия в минеральном масле, смесь перемешивают при комнатной температуре в течение 1 часа. К реакционной смеси добавляют 41.7 мл 1 н. соляной кислоты, смесь быстро перемешивают, чтобы вся реакционная смесь стала кислой. Выпавшие кристаллы отфильтровывают, промывают водой и затем промывают диэтиловым эфиром, получают 7.32 г этилового эфира 1-циклопропил-6,7-дифтор-2,8-трифторметил-1,4-дигидро-4-оксохинолин-3-карбоновой кислоты (XIII; R1=циклопропил, R3=этил) в виде белого порошка.
Температура плавления от 184 до 185oC.
Масс-спектр (химическая ионизация): м/е=362 (М++1).
Затем 0.8 г (0.0022 моля) этого сложноэфирного соединения суспендируют в смеси 5 мл уксусной кислоты, 3 мл волы и 0.3 мл концентрированной серной кислоты и при помешивании смесь нагревают с обратным холодильником в течение 2 часов. После охлаждения смеси до комнатной температуры к ней добавляют воду, нерастворимые вещества отфильтровывают и собранный фильтрованием остаток промывают водой и затем сушат, получают 0.7 г 1-циклопропил-6,7-дифтор-8-трифторметил-1,4-дигидро-4- оксохинолин-3-карбоновой кислоты (II; R1циклопропил) в виде белых кристаллов.
Температура плавления от 210 до 212oC.
Масс-спектр (химическая ионизация): м/е=334 (М++1).
Справочный пример 2
Синтез 1-этил-6,7-дифтор-8-трифторметил-1,4-дигидро-4-оксохинолин-3-карбоновой кислоты (II; R1=этил)
Проводят аналогичную Справочному примеру 1 реакцию с использованием этиламина (XI; R1= этил) вместо гидрохлорида циклопропиламина, получают 1-этил-6,7-дифтор-8-трифторметил-1,4-дигидро-4-оксохинолин-3-карбоновую кислоту (II; R1=этил) в виде белого порошка.
Температура плавления от 159 до 162oC.
Масс-спектр (химическая ионизация): м/е=322(М++1).
Справочный пример 3
Синтез 6,7-дифтор-8-трифторметил-1,4-дигидро-1-метил-4-оксохинолин-3-карбоновой кислоты (II; R1=метил)
Проводят аналогичную Справочному примеру 1 реакцию с использованием гидрохлорида метиламина (XI; R1=метил) вместо гидрохлорида циклопропиламина, получают 6,7-дифтор-8-трифторметил-1,4-дигидро-1-метил-4-оксохинолин- 3-карбоновую кислоту (II; R1=метил) в виде белого порошка.
Температура плавления от 197.5 до 199oC.
Масс-спектр (химическая ионизация): м/е=308 (М++1).
Справочный пример 4
Синтез 6,7-дифтор-8-трифторметил-1,4-дигидро-1-изопропил-4-оксохинолин-3-карбоновой кислоты (II; R1=изопропил)
Проводят аналогичную Справочному примеру 1 реакцию с использованием гидрохлорида изопропиламина (XI; R1=изопропил) вместо гидрохлорида циклопропиламина, получают 6,7-дифтор-8-трифторметил-1,4-дигидро-1-изопропил-4-оксохинолин-3-карбоновую кислоту (II; R1=изопропил) в виде белого порошка.
Температура плавления от 197.5 до 200oC.
Масс-спектр (химическая ионизация): м/е=336 (М++1).
Справочный пример 5
Синтез 6,7-дифтор-1-(2-фторэтил)-8-трифторметил-1,4-дигидро-4-оксохинолин-3-карбоновой кислоты (II; R1=фторэтил)
Проводят аналогичную Справочному примеру 1 реакцию с использованием гидрохлорида 2-фторэтиламина (XI; R1=фторэтил) вместо гидрохлорида циклопропиламина, получают 6,7-дифтор-1-(2-фторэтил)-8-трифторметил-1,4-дигидро-4-оксохинолин-3-карбоновую кислоту (II; R1=фторэтил) в виде белого порошка.
Температура плавления от 183 до 185oC.
Масс-спектр (химическая ионизация): м/е=340 (М++1).
Справочный пример 6
Синтез 1-(2-пиримидил)гомопиперазина
К смеси 10.0 г (0.1 моля) гомопиперазина, 2.9 г (0.025 моля) 2-хлорпиримидина, 6.9 г (0.025 моля) карбоната калия и каталитического количества йодида калия добавляют 50 мл ацетонитрила и смесь нагревают с обратным холодильником в течение 11 часов. Смесь охлаждают до комнатной температуры и затем фильтруют, полученный фильтрат концентрируют при пониженном давлении и остаток хроматографируют на колонке с силикагелем (элюент - смесь хлороформ: метанол= 8:2), получают 2.14 г 1-(2-пиримидил)гомопиперазина в виде светло-желтой жидкости.
Масс-спектр (химическая ионизация): м/е=179 (М++1).
Справочный пример 7
Синтез 1-(2-метилтиофенил)пиперазина
К 2.8 г (0.02 моля) 2-метилтиоанилина и 13.7 г (0.044 моля) гидробромида N-бис(2-бромэтил)амина добавляют 40 мл этанола и смесь нагревают с обратным холодильником в течение 10 часов. После охлаждения смеси до комнатной температуры к ней добавляют 10.2 г карбоната натрия и полученную смесь нагревают с обратным холодильником в течение 10 часов. После охлаждения реакционной смеси до комнатной температуры и последующего фильтрования полученный фильтрат концентрируют при пониженном давлении и остаток хроматографируют на колонке с силикагелем (элюент - смесь хлороформ : метанол : 28%-ный водный аммиак = 40:9:1) получают 1.31 г 1-(2-метилтиофенил)пиперазина в виде светло-желтой жидкости.
Масс-спектр (химическая ионизация): м/е=209 (М++1).
Справочный пример 8
Синтез 1-(2-тиазолил)пиперазина
В 50 мл ацетонитрила растворяют 5.0 г (0.0305 моля) 2-бромтиазола, затем к раствору добавляют 13.1 г (0153 моля) пиперазина, 8.4 г (0.061 моля) карбоната калия и каталитическое количество йодида калия и полученную смесь нагревают с обратными холодильником в течение 5 часов. Смесь охлаждают до комнатной температуры и затем фильтруют, полученный фильтрат концентрируют при пониженном давлении и остаток хроматографируют на колонке с силикагелем (элюент - смесь хлороформ : метанол : 28%-ный водный раствор аммиака=40:9: 1), получают 3.62 г 1-(2-тиаэолил)пиперазина в виде бесцветной жидкости.
Масс-спектр (химическая ионизация): м/е=170 (М++1).
Промышленная применимость
В соответствии с настоящим изобретением предлагается новое производное 8-трифторметиленхинолин-карбоновой кислоты, которое специфически подавляет рост ВИЧ в ВИЧ-инфицированных клетках и также обладает активностью, подавляющей цитопатогенный эффект ВИЧ, или его фармацевтически приемлемые соль или сложный эфир.



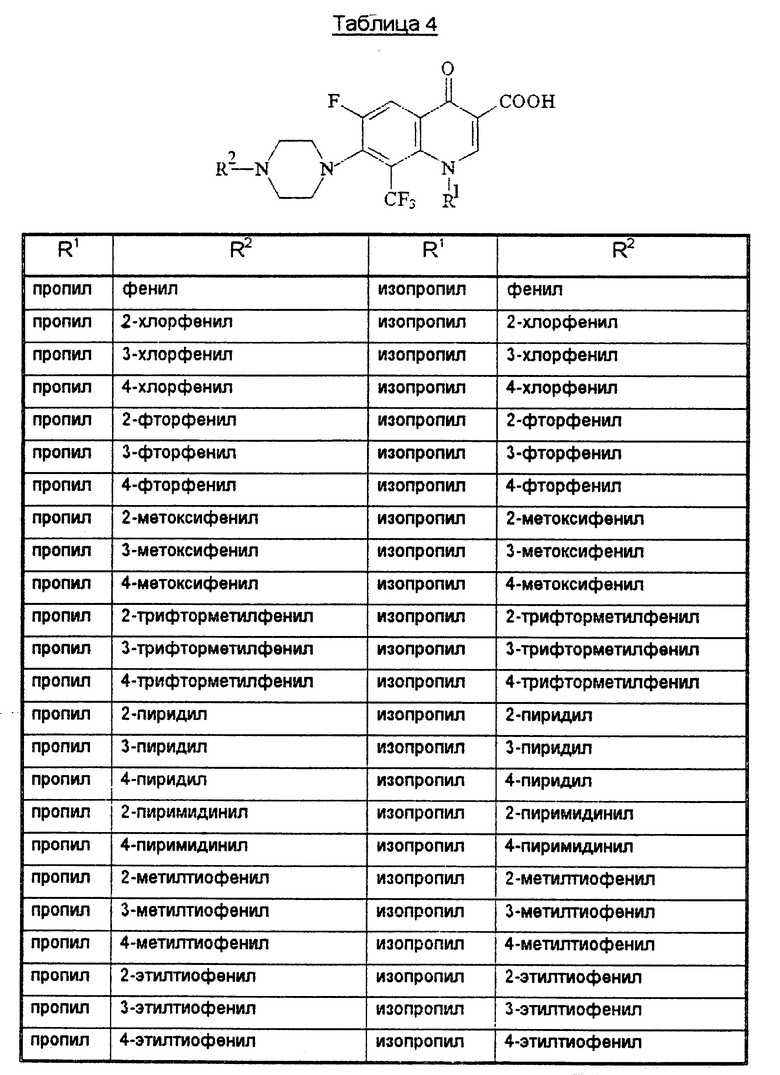
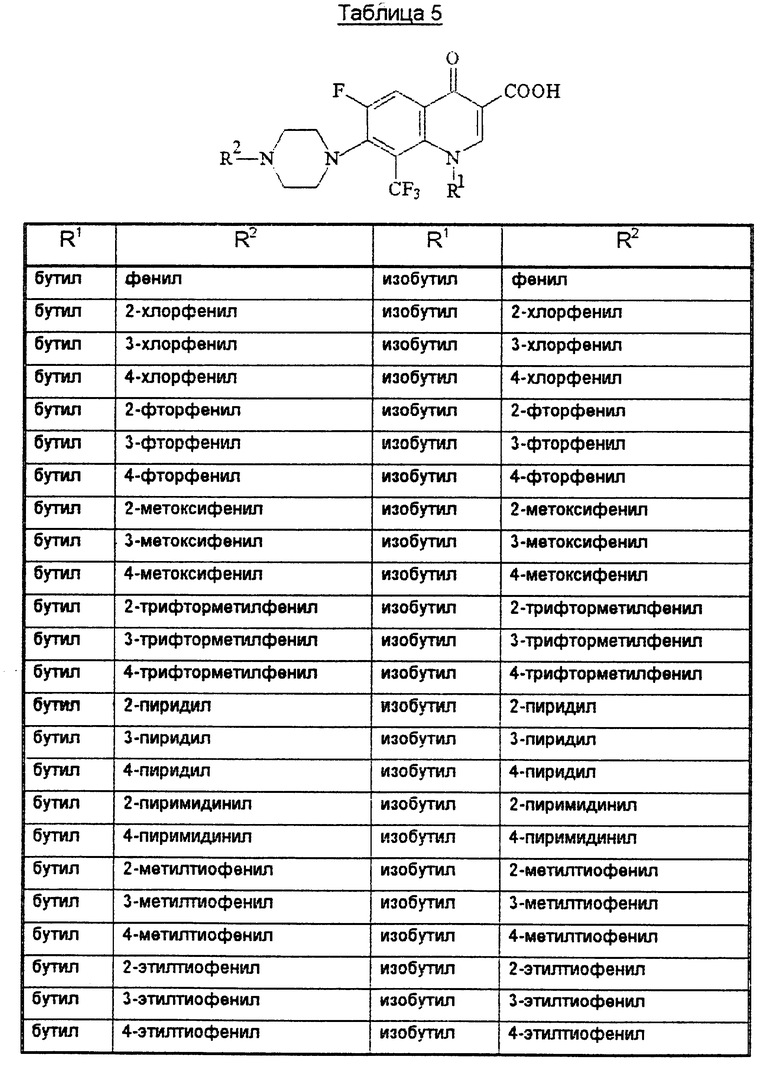
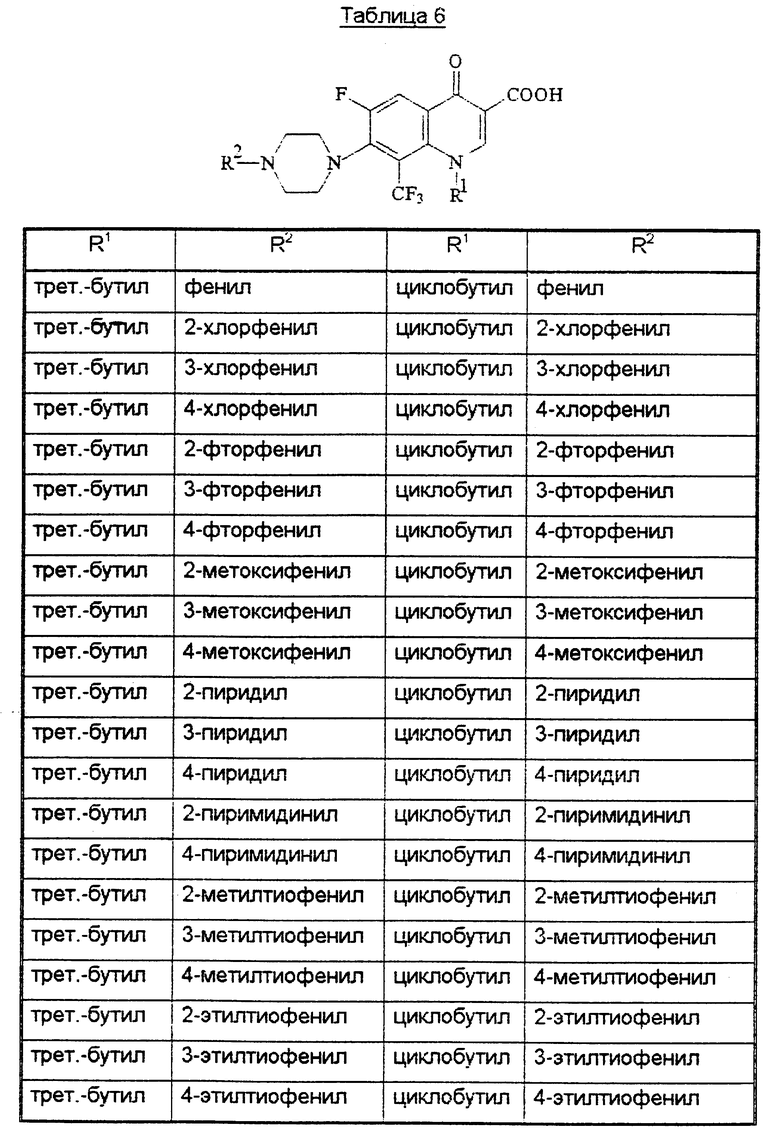
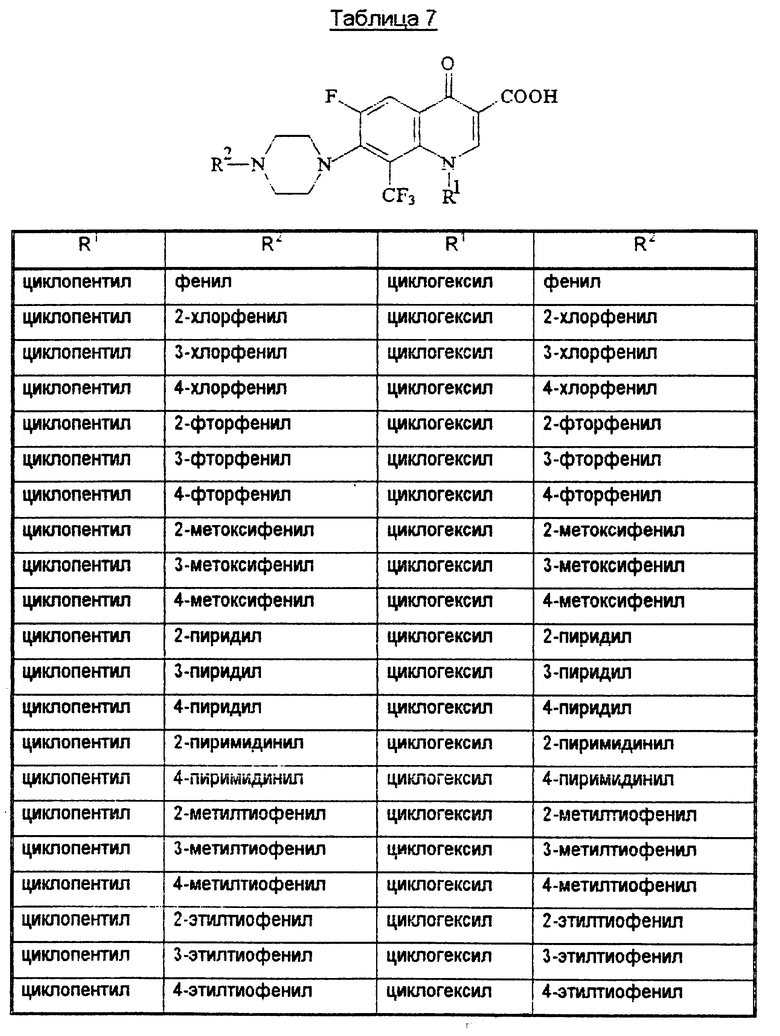
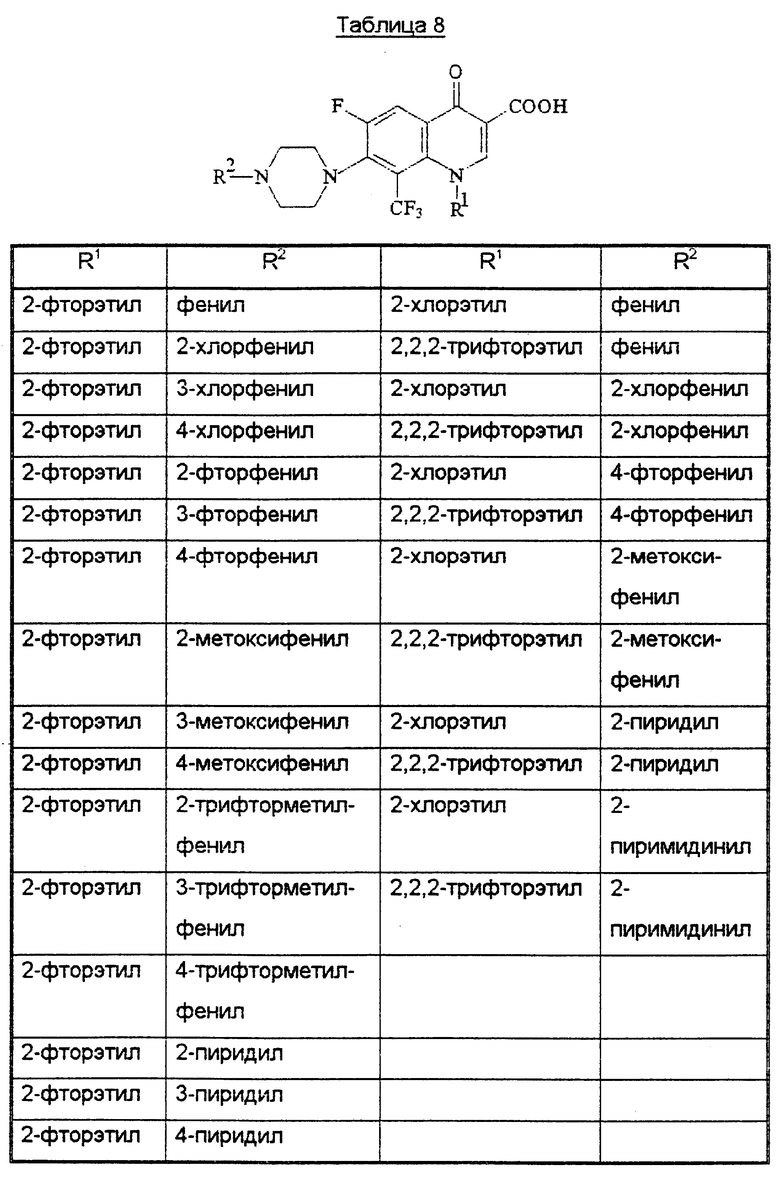

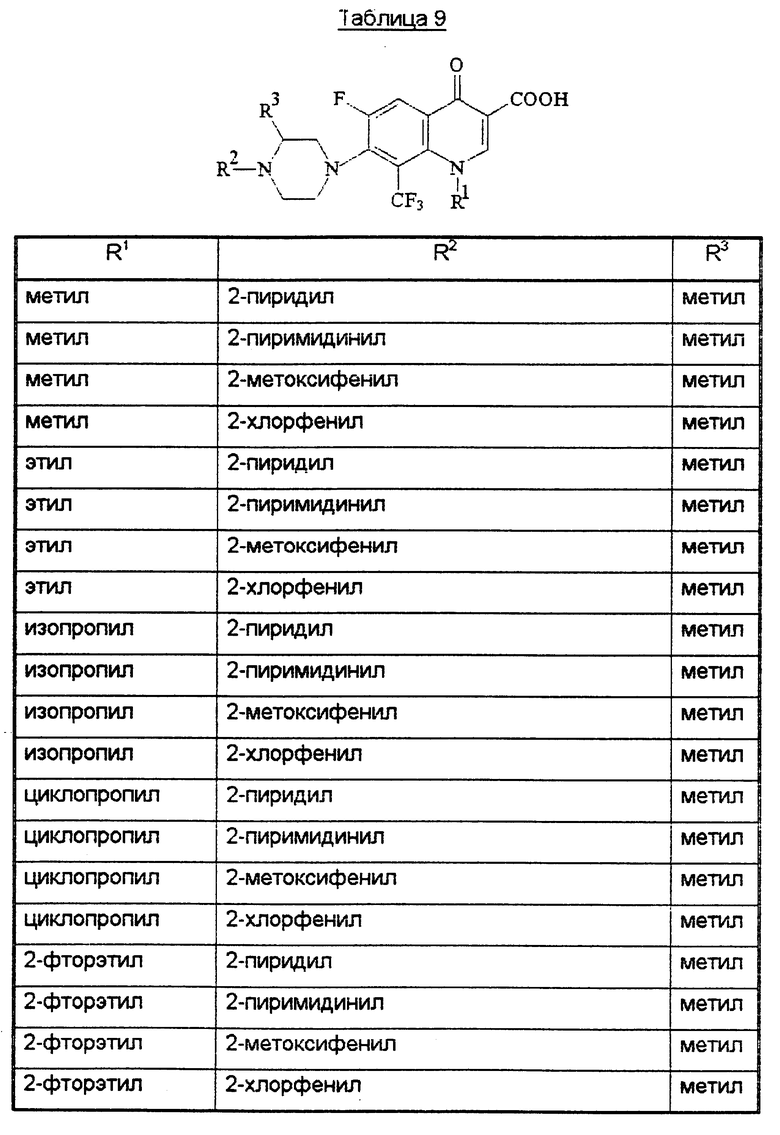
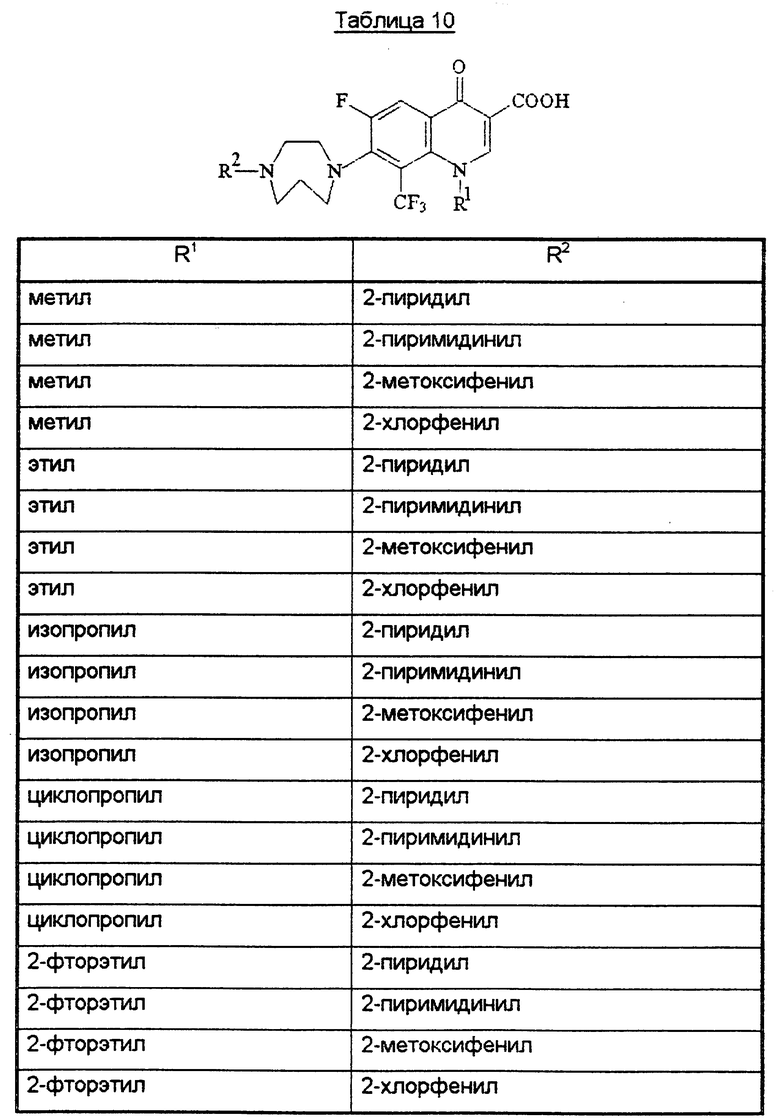
Производное 8-трифторметилхинолинкарбоновой кислоты формулы Т, где R1 - низший алкил, низший галогеналкил или циклоалкил; R2 - фенил, возможно замещенный R0, 5-ти или 6-тичленный гетеромоноцикл, содержащий 1 или 2 гетероатома (N или S), возможно замещенный R0, или конденсированная с бензольным кольцом 5-членная полигетеромоноциклическая группа, содержащая 2 гетероатома (N, О или S), R0 - галоген, алкил, фторзамещенный низший алкил, низший алкоксил, низший тиоалкил; R3 - Н или низший алкил, m = 2 или 3, или его его фармацевтически приемлемая соль, или сложный эфир, ингибирует рост вируса иммунодефицита человека. 3 с. и 21 з.п. ф-лы, 12 табл.
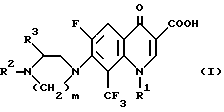
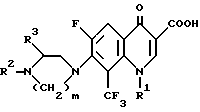
где R1 представляет собой низшую алкильную группу, низшую галогеналкильную группу или циклоалкильную группу;
R2 представляет собой фенильную группу, которая может быть замещена R0, 5- или 6-членную ароматическую гетеромоноциклическую группу, содержащую 1 или 2 гетероатома, выбираемых из N, S, которая может быть замещена R0, или конденсированная с бензольным кольцом 5-членная полигетеромоноциклическая группа, содержащая 2 гетероатома, выбираемых из N, O и S, R0 выбирается из группы, включающей атом галогена, низший алкил, фторзамещенный низший алкил, низшую алкоксигруппу или низшую алкилтиогруппу;
R3 представляет собой водород или низшую алкильную группу;
m принимает целые значения 2 или 3,
или его фармацевтически приемлемые соль или сложный эфир.
5. Производное 8-трифторметилхинолинкарбоновой кислоты по п.1 или его фармацевтически приемлемые соль или сложный эфир, в котором R1 выбирают из группы, включающей метил, этил, 2-фторэтил и циклопропил.
| Способ получения 1-этилимидазолов | 1973 |
|
SU501671A3 |
| ДИНАМИЧЕСКИЙ ТОРМОЗ | 2017 |
|
RU2652330C1 |
Авторы
Даты
1999-11-10—Публикация
1995-06-07—Подача