Изобретение относится к области эф ров тиофосфорных кислот, а именно к н вым эфирным производным днтиофосф ной кислоты общей формулы КО(СДО)„ SCH,CHCH,OR где Т - моно- и/или полиалкил (С, -C , фенил, R - водород или ацил , Т - алкил или ацил С.-С.„К или П 0-1, ЭтиСоединения являются эффективными присадками к смазочным маслам на минеральной основе. Известны металлосодержащие эфирн производные дитиофосфорной кислоты, которые применяются в промышленнос ти как присадки к смазочным маслам, например ЛАНИ-317, ВНИИНП-354, ДФ-11, МИИИП-22 к l. По термоокислительной и противонзносной активности эти соединения уступают, либо в отдельных случаях идентичны карбалкоксиметиловым эфирам дитиофосфорной кислоты 2. Однако и эти последние обладают недостаточно высокой активностью. Целыо изобретения являются новые эфирные производные дитиофосфорной кислоты указанной общей формулы, обладающие улучшенными термоокислительными и противоизносными свойствами в отношении смазочных масел. Указанные соединения вводят в масло в количестве 2-7 вес«% При этом, например, термоокислительная стабилкгность масла МТ-16 повышается до 130-200 мин, коэффициент лакообраЗования снижается до О,3-0,1 и критическая нагрузка увеличивается до 136-17О кгс, это значительно превосходит результаты, достигаемые с помощью известных присадок. Синтез предлагаемых соединений может быть выполнен согласно cлeдyк шим стадиям. Первоначально моио- и/нли нолиШ1кил () (} -ЧО1Ь1 или их мопоглнколевые э ||иры конденсируют с понтасул фндом фос()ора, взя1Ъ1м в С1 ехнометричес ком отношении при 1()0-130 XЗ в прису1 ствии или в отсутствие растворителя. Полученные с выходом до 100% диэфиродитиофосфориые кисло1Ъ1 нейтрализуют содой или поташом и обрабатывают при 60-120 С в среде полярного растворителя (диоксана, спирта и т.д.) простыми или сложными монохлоргидриновыми э4)ирами глицерина. Последние должны быть предварительно получены взаимодействием эпихлоргидрина со спиртами или карбоновыми кислотами C,-C|g или алкил (C|-C,g) фенолами или их моногликолевыми эфирами в присутствии кислотных или основных катапизаторов. Взаимодействие калиевых или натриевых солей диэфиродитиофосфор- ных кислот с указанными монохлоргидри новыми эфирами глицерина приводит к по лучению целевого продукта с выходом 90-98% от теоретического. На заключительной стадии синтеза вторичные спиртовые группы в предлагаемых эфирных производных дитиофосфорной кислоты могут быть этерифицированы карбоновыми кислотами или их ангидридам в присутствии катализатора. Пример. 34,4г втор-октаде- цилфенола загружают в реактор, нагреваю при перемешивании до 100°С и порционно добавляют 12 г пенсасульфида фосфора, отводя и поглощая выделяющийся Б ходе реакции сероводород. Через 3 реакцию завершают, реакционную массу охлаждают, разбавляют гептаном и обрабатывают поташом до нейтральной реакции. Избыток поташа отделяют фильтрова- нием фильтрат вьшаривают, получая 45,6 калиевой соли ди-(втор-октадецилфенил)-дитиофосфорной кислоты, которую раство ряют в диоксане и конденсируют с 16,7 г н-бутилового эфира монохлоргидрина глицерина при перемешивании и нагревании до 80 С в течение 18 ч. По окончании реакции отгоняют в вакууме диоксан и остаток обрабатывают н-валериановой кислотой при 108- 110°С в присутствии следов серной кислоты в среде толуола. Через 12 ч реакционную смесь обрабатывают водным раствором соды, верхними толуопьный слой промывают водой, высушивают и выпаривают в вакууме, Оста тсж (46,8 г) - прозрачная вязкая ж/шкость темно-желтого цвета, представляю ан собой )iipn(.x3 соодииоиие .7С5М),Р ЗСН,СНСН ОС.Н ОС( что подтверждают результапл определения молекулярной массы и элемепшого состава. В ПК-спектре соединения отчет ливо проявляются полосы поглощения при 5G3 см (валешиые колебания связи Г-б), 098 см (вапент1П)1е колебания связи Р 5 ), 748, 812 и 870 см (деформационные колебс лия связей С-Н в ароматическом ядре), 1238 см (деформационные колебания связи Р-О-С), 1252 см, (деформационные колебания связи С-О-С), дублет около 161О см (валентные колебания связи в ароматическом ядре) и при 1747 см (валентные колебания связи ), а также при 640 (валентыр колебания связи С алифат.- S ) . Таким образом, получен 0,О-ди-(2-и 4-втор -октадецилфенил)-5 - (2-валориат-З-бутокси-н-пропил) дитиофосфат. Выход 93,9% от теоретического. Пример 2. В условиях, описанных в примере 1, конденсируют 21,6 г смеси 0-, м- и п-крезолов и 22,2 г , Полученную реакционную массу нейтрализуют бикарбонатом натрия до нейтральной реакции, выделяют натровую соль диэфиродитиофосфорной кислоты и конденсируют ее с ,8 г н-октадецилового эфира монохлоргидрина глицерина при перемешивании и нагревании до 110°С в среде абсолютного изопропилового спирта в течение 24 ч. В заключение, как и в примере 1, вторичт.ш спн(товые гидроксилы блокируют анетилированием уксусным ангидридом в среде пиридина. После выпаривания легкокипящих непревращеннь1х реагентов в вакууме в атмосфере азота получают 66,3 г соединения-дитиофосфат 0,0-ди( 2-,3-и 4-метилфенил)-6 -( 2-ацетат-З-октадецокси-н-пропил) (-,л-п-СН-С,Н,0),Р , ОС{0)СНз со свойствами, указанными в таблице, и рисунком ПК-спектра, близким к придыдушему. Р:5ыход от теоретическото. Пример 3. 41,2 г т хничоского п-изооктилфенола и 22,2 г конденсируют, как описано в примере 1 , inniтрализуют потпшом и обрабатывают полученную калиевую соль диэфиродитиофосфорной кислоты 35,2 г сложного эфира мочохпоргидрина глицерина и карбоно(л-шрел -сд сдо р о 0,0-аи- 4-трет-октил4Онил)- 3 -(2-окси-3-карбоксилат-С| -С10 -и- пропил) дитиофосфат. В ИК-спектре, как и следовало ожидать, проявляются пики поглощения, характерные для эфирных производных дитиофосфорной кислоты (пример 1). В то же время в ИК-спектре наблюдается новый пик при 1225 см , отвечающий деформациош0 1м колебаниям связи С-О во вторичных спиртовых гидроксилах. Выход эфира 96,0% от теоретического. Пример 4. 43 г мшогликолевого эфира п-трет-бутилфенола конденсируют с 13.7 г пентасульфида фосфора при 12О- 125°С в течение 1,5 ч. Диэфир днтиофосфорную кислоту нейтрализуют потащом в растворе гептаиа. Образующаяся калиевая соль указанной кислоты нерастворима в гептане и выпадает в осадок. После отделения осадка от гептанового раствора его экстрагируют ацетоном. Аце тон растворяет калиевую соль кислоты и (Л-трет - C HjCgH OCjH со свойствами, указанными в табл. 1, и рисунком ИК-спектра, близким к предыдущему, при отсутствии пиков около 750 см и 1747 см. Выход эфира 91,8% от теоретического. П Р и м е Р 5. Проводят синтез соглас но примеру 1, применяя в качестве исходл7; ш-СдН„сдос,н,о),р
Выход 95,7% от теоретического. В ИК-спектре вновь появляется полоса при 1477 см , характеризующая валентные колебания связи С-О в карбонильной группе.
В остальном рисунсж ИК-спектра типичен для предлагаемой группы эфиров (пример 1).
вых кислот (фракции ClI/lvK )итоге из реакционной смиси выделяют 78,5 г соединения следующего строения
8СН,СНСН,ОС(С,,,,)
он
9
SCH,CHCHjOC(C,)
он
50
П Р и м е Р 6. Моногликолевые эфиры смеси моно- и полиалки;1фе11олов, полученных алкнлированием легкокипяшей фракции (18О-250 С) фенолов сланцевой смолы олефинами , обрабатывают при 11О°С в течение 2 ч, переводят в К-соли диэфиродитиофосфорной кислоты, как описано в примере 1, и кшшенсируют позволяет отделить избыток поташа. Ацетоновый раствор выпаривают и получают 51,7 г калиевой соли ди-(п-трет-бутилфеноксиэтил)-дитиофосфорной кислоты в виде белого кристаллического порошка с т. пл. 205,5-206,0°С. Найдено,%: С 55,15; Н 6,50; О 12,48; & 12,40; Р 6,О. Мол. вес. 516. Вычислено,%: С 55,41; Н 6,54; О 12,ЗО; S 12,ЗО; Р 5,95. Мол.вес. 520. 14,3 г этой соли раствор51ют в диоксаие, нагревают раствор и при 80 С jcio6eaляют 6,8 г н-дешшового эфира монохлоргидрина глицерина. Реакцию ведут в течение 16 ч, после чего реакционную массу выпаривают в вакууме в атмосфере азота и получают 19,8 г соедннення О,О-ди-(4-трет-бутнлфеноксиэтил)-S (2гс«кси-3-дец1жси-н-протил)-дитнофосфат следующей формулы : ОН иых реагентов моноглнколевый эфир п-изосжтилфенола, лентасулы|жд фосфора, .бикарбонат натрия и сложный эфир монохлоргидрина глицерина с фракцией СЖК Су-С. Получают соединение О,О-ди-(4-третоктнлфеноксиэтил)- 5 -(2-окси-З-карбоксилат С -С -н-пропил) -дитиофос-фат следующего строения
с п-трет бушлфеноксиэпиювым эфиром монохлоргидрина ivmuepHHa, взятым в стехиометрическом отношении. Полученный продукт этерифииируют уксусной кислотой в условиях примера 1 и в ко(%)о.г
,,)
(СзН7)о-1
(C,H,V,
Выход эфира 88,7% от- теоретического, В ИК-спектре наблюдается увеличение интенсивности поглощения в ароматичес- 15 кой области (700-9ОО см ) ив об.ласти около 1250 см (деформационных колебаний связей С-0 в эфирных группах).
П р и м е р 7. Берут исходные мо- 20 ногликолевые эфиры тех же алкилфенолов, что и в примере 6, конденсируют с ,
%)о.:
)
.О
tS«7)o-l
(HaV: Выход 86,3% от теоретического. Рисунок ИК-спектра синтезированного соединения близок к предыдущему, за исключением нового пика при 1125см (колебания вторичной спиртовой группы) и, наоборот, отсутствия пика при 1747см (колебания карбонильной группы). П р и м е р 8. 24 г моногликолевого эфира технического п-изооктилфенола конденсируют с 5,5 г пентасульфида фосфора при 110°С в течение 2,5 ч и получают 27,1 г соответствующей дизфиГл-трет-С Н СДОСДо),Р: Выход 9.4,6% от теоретического. Рисунок ИК-спектра данного соединения очень близок к спектру вещества, полученного в примере 4. Термоокислительную стабильность и коэффициент лакообразования определяли по отношению к маслу МТ-16 при 2.5О° по ГОСТ 9352-6О. Противоизносные
ночном итоге имделмют гющ-стио О,О-яи-(моио- и 1а1И(1.1Ки;1}О}1Окси:-)Т11л)- - 2-«цетат-3-( 4-т(1ет-Г)утилфен:; ксиэтил)-41-пр 11Ил -анти;-) слепуюшего строения
SCHjCHgCHjOCjH OCjH -п-mpem-C Hj
образующуюся кислоту переводят в натровую соль и обрабатьюают ее алкилфениловым эфиром монохлоргидрина глицерина, при синтезе которого используют указанную выше смесь моно- и полиалкилфенолов из сланцевого сырья. В результате получают соединение О,О-ди(моно-и полиалкилфеноксиэтил)- S - 2-окси-3-( монои полиалкилфенил)-н-пропид1-дитиофосфат общей формулы
()о.
(CeHir s a)
SCHjCHCHjO
он
( 7)0-1
(«0-1
SCH CHCHjOC Hg
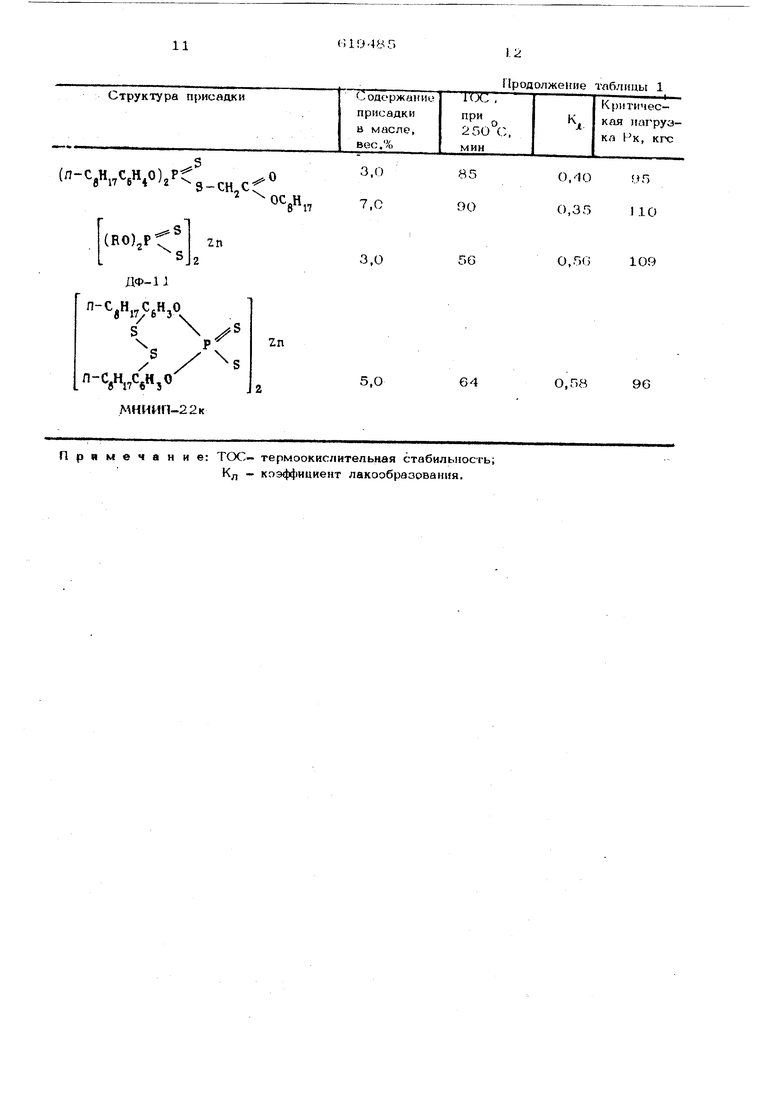
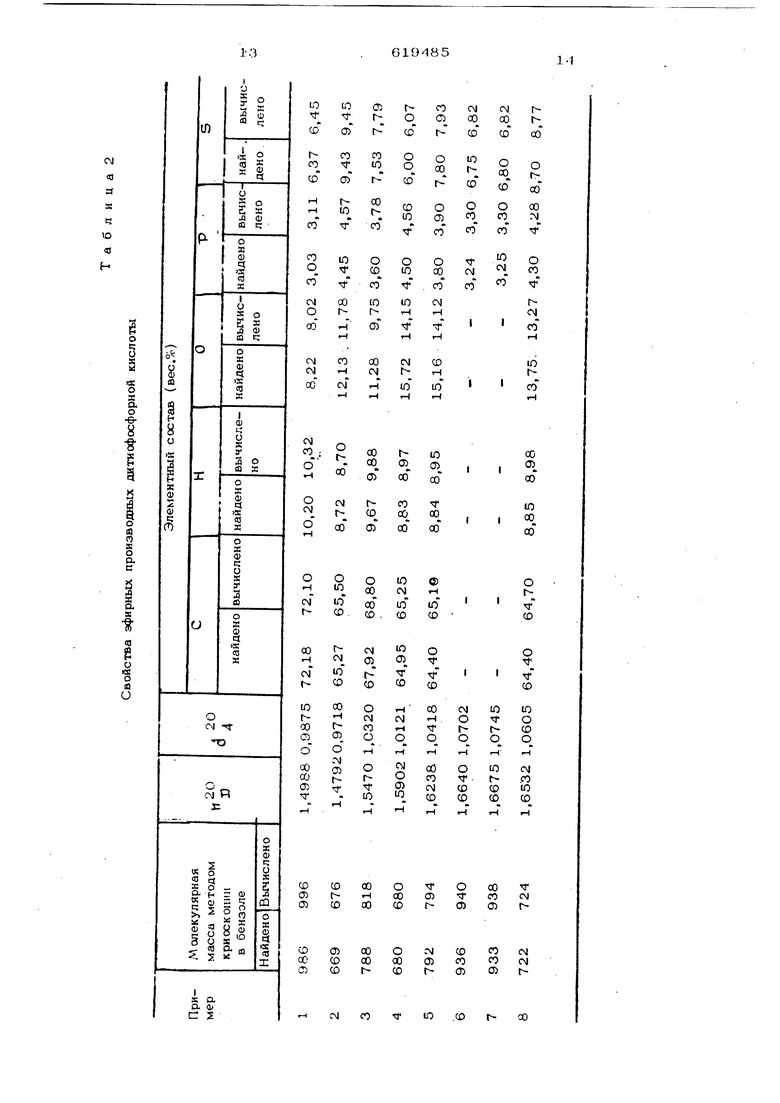
он родитиофосфорной кислоты, )салиевая соль которой имеет т. пл. 180,3-180,5°С и по молекулярной массе и элементному составу полностью соответствует расчетным данным. 21,9 г этой соли раствор$иот в этиловом спирте и конденсируют с 5,7 г н-бутилсжого эфира могохлоргидрина глицерина в течение 18 ч. После вакуум-выпаривания реакционной смеси получают 25,9 г 0,0-ди-(4-треГ-октилфенокснэтил)- S -(2-окси-З-бутокси-н-пропил) дити оф осфата свойства масла с присадками оценивали на четырехшариковой машине трения по. циклу 6О с при скорости вращения верхнего шара 1450 об/мин и диаметру нижних шариков 12,7 мм (по ГОСТ 3722-6О), Результаты испытаний сведены в табл. 1. Свойства всех синтезированных соединений суммированы в табл. 2. Термоокислительные и прэтивоизнэсные свойства с присадками. Т a б л и ц о 1. масла МТ-16





| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения дитиофосфатной присадки к смазочным маслам | 1977 |
|
SU657032A1 |
| Соли азотсодержащего боролидина и дитиофосфорной кислоты в качестве присадки к смазочному маслу | 1981 |
|
SU1002299A1 |
| Смазочная композиция | 1983 |
|
SU1162860A1 |
| Смазочное масло | 1980 |
|
SU863622A1 |
| Смазочное масло | 1980 |
|
SU876701A1 |
| Алкилен-бис(оксиметил-0,0-диизопропилдитиофосфаты) в качестве противозадирных присадок к смазочным маслам | 1980 |
|
SU941378A1 |
| Способ получения зольных дитиофосфатных присадок к моторным маслам | 1977 |
|
SU682526A1 |
| 2,2-Тиобис-(0,0-ди-4- @ -метилциклогексилфенил)дитиофосфат никеля в качестве стабилизатора полипропилена | 1982 |
|
SU1067002A1 |
| 0,0-Ди @ 2,2,2-трис-(бутилкарбонилоксиметилен)этил @ дитиофосфат цинка в качестве противоизносной присадки к смазочным маслам | 1987 |
|
SU1467061A1 |
| Смазочная композиция | 1976 |
|
SU657055A1 |

Масло без присадки (V,
CHCHjOC Hg ОС(0), (сндн.о) SCHjCHCHjOCj Hjs ОС(0)СН5 (, SCH,CHCHaO t -С(0)С,Н„-С„Н,, (,Н,0)2Р SCH,CHCH,OC (.н.): -СН,СНСН,ОС(0),,-СД, (Смесь потапкилфеноМ- S- CHj - ОС{0)СНз (Снесь no flwa 7/fu/r pew// J-OCjH O)2-P - CHj- CHCHgO ( спесь полиа/1кил ено ОНg (л-сд,с,н,ос,н,о),РС -CHj-CH-CHjOC Hg
1,9
50
19
195 0,10 155 175 0,12 138 137 0,20 158 О,17 172 0,13 169 87 0,32 123 98 0.27 136 167 О.15 17О 127 0.21 148 О,19 152 169 0,14 117 0,21 135 112 0.23 131 128 0.19
Примечание: термоокислительная стабилыюсгь;
Кл - кпэф4)ициент лакообразовання.
Продолжение таблицы 1
см «о я
S
с: ю о (со
со t
О) О)
(О
со О) 00 ОС со 00
О) со гСМ со
о -
00
со eg
О)
О) 05 ГгСО
со
СМ
со eg
со 05
О) О) Г
гю .со
СО о 51 м у л а изобретен Эфирные производные дитиофосфори кислоты общей формулы ГЕО(С,Н,0)„1 PC.( L г Л nJa бСН СНСнХ где Тг - моно и/или полиалкил (Cjфенил, Т - водород или аиил , К - алкил или аиил C,-C,g ,Т или ,Н4- . П - 0-1., как присадки к смазочным Маслам на MR неральной основе. Источники информации, принят1 1е во внимание при экспертизе: 1. Кулиев Л. М. Химия и технология присадок к маслам и топливам. М,, Хи- мия, 1972. с. 39-47, 116-12О. 2, Авто(.х:кое свидетельство СССР №543665, кл. С Oi М 1/48, 20.08.74,
Авторы
Даты
1978-08-15—Публикация
1975-08-08—Подача