Изобретение отнсх:ится к синтезу новых производных индола, которые могут найти применение в качестве добавок к полимерам. Известен способ получения 2--фени|| нндол нагреванием ацетофенона с анили ном ij. Целью изобретения являете синтез новых производных 2-фе НИЛ индола. (Предлагаемый способ получения произ водных 2-фенилиндола обшей формулы где R 1 - представляет собой атом водорода, аминогруппу, которая может быть замещена ацетильным или бензоильным радикалом, меркаптогруппу, за мещенную или незамещенную алкильной группой с прямой или разветвленной цепью, содержащей 1-12 атомов углероаа, или циклогексильным радикалом, кар бжсильный радикал, группу , в которой 1 представляет собой изолропиа, сарбсжсиметил, карбэтсжсиметил, карбэгоксийзопропил, ацетил, докозаноил, бензоил, или аллильный радикал, или aJtкильный радикш с прямой или разветвленной цепью, содержащий 6-12 атомов углерода; - атом водорода или аминогруппа, заключается в том, что замещенный ацетофенон общей формутпл О -снгх где Т имеют указанные значения X - галогеи, подвергают взанмэдействию с анилином при температуре кипения )eaкциoкнoй ьмеси. HafiA6HO| что полученные производные 2-4)8ниликдола являются хорошими ста/бнлизаторами полимеров и сополимеров ввнилхлорида, таких как поливинилхлорир,. поливинилхлоридполивинилацетат и поливинилхлоридполивииилсщенхлорид. Пример -(4 Допецвпокснфенвп) индол.. К 32,5 г (0,35 моль) кипящего анилина добавляют в течение 15 мии 33,85 г (0,1 мояь) расплавленного р- хлор- -додецилциклоксиацетофенона . и после этой операции температуру.реакционной среды в теадние 2О мин поддержнвают равной 180 С.
Соединение 1
2-(4-Меркаптофенил) индол
2-(4 - Карбоксифенил)индол 2-(4- Метилтиофенил) индол 2-(4 -Ацетсжсифенил) индол 2-(4 -Карбэтокси-изо-пропилоксифенил 2-(4 - БензолфеНИЛ)индол 2-(2 -Этил-4-« гексилоксифенил) индол 2-(4- Дикоза.ноилоксифё11ил)и1щрл 2-(4 - Изопропилоксифенкл)и1шоп 2-(4 - Карбсксиметоксифенил)индол 2-(4 - Карбэтоксиметсжсифенил)индол 2-(4 -Аллилоаа;ифенвл1вядол
2-(4 - Ме(жаптофенил)индол 2-(4 -И -Адетаминофенил)индол 2-(4 - Бутилтиофеннл)индол 2-(4 - Изопропилтиофенил)индол 2(4 - Циклогексилтиофенил)индол
Таблица
Температура плавления, С
238 (метанол J
204,6 (ацетон/ вода)
225 (толуол)
203,2 (этанол)
106,9 (циклогексан)
2 2 0-2 34 (ацетон)
191
140 (диметилфор1Мамид
196
243
216
214
210 (толуол) 292 (ацетон/вода)
189-191 (этанол)
179 (метанол / ацетон
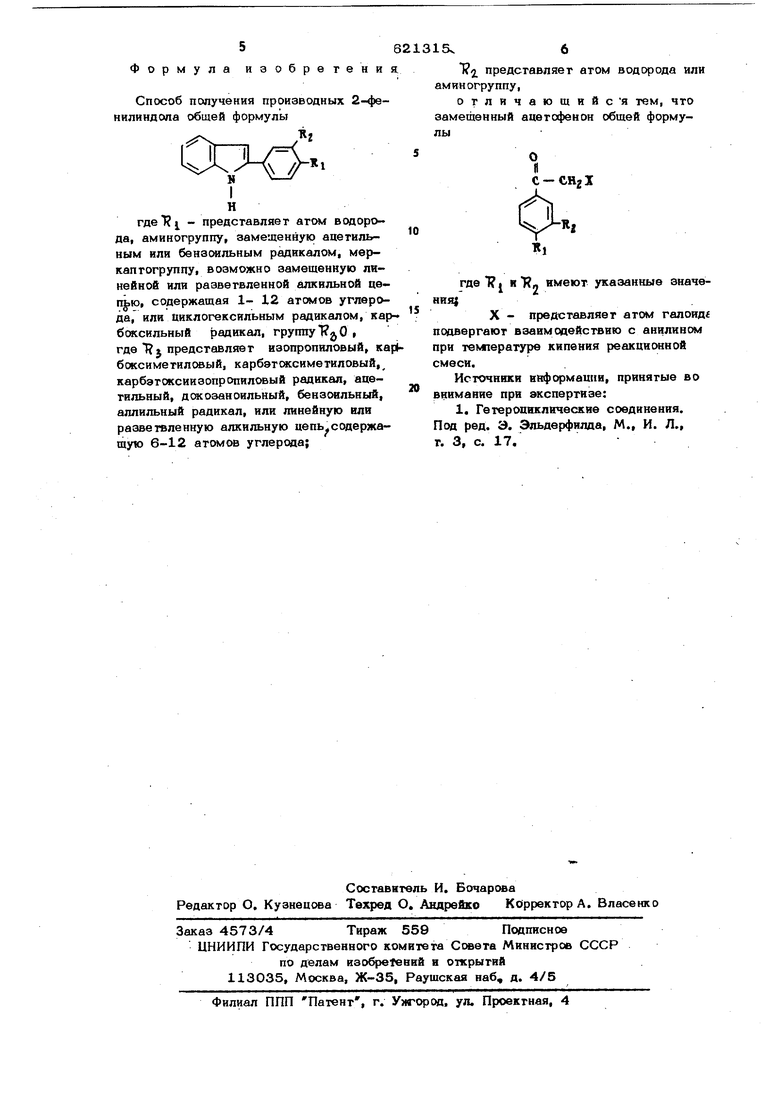
179-181 (этанол) Смесь переливают в разбавленный раствор хлористоводороднсЛ кислоты и подвергают экстракции бензолом. Органическую фазу промывают водой, просушивают и подвергают концентрированию при пониженном давлении. Сырое вещество смачивают смесью тояуолгептан, затем отфильтровывают и просушивают, в результате чего получают 22,6 г 2- 4-додеципфенил) индола. у.пл. 204С, выход 60%. По данному методу, используя соответствующие исхсчаные продукты, полу«ают соединения, пpивeдeнtfыe в таблице. рмула изобретени Способ получения производных 2-фенилиндола общей формулы гдеТ - представляет атом водорода, аминогруппу, замещеннук) ацетильным или бензоильным радикалом, меркаптогруппу, возможно замещенную линейной или разветвленной алкильной цепью, содержащая 1- 12 атомов углерода, или циклогексильным радикалом, кар бсжсильный радикал, группу Т О где представляет изопропиловый, Ka боксиметиловый, карбэтсжсиметиловый, карбэтсжсиизопропиловый радикал, ацетильный, дсжозаноильный, бензоильный, аллильный радикал, или линейную или разветвленную алкильную цепь содержащую 6-12 атомов углерода; 15v6 представляет атом водорода или аминогруппу, огличающийся тем, что замешенный ацетофенон общей формулыгде 1 J н имеют указанные значения}X - представляет атом галоидг подвергают взаимодействию с анилином при температуре кипения реакционной смеси. Источники ннформашш, принятые во внимание при экспертизе: 1. Гетероциклические соединения. Под ред. Э. Эльдерфилда, М., И. Л., т. 3, с. 17,



Авторы
Даты
1978-08-25—Публикация
1976-04-15—Подача