Изобретение относится к органической химии, а именно к получению асимметрическим синтезом оптически активной (-)- Д-фе- нил- у-аминомасляной кислоты и ее аналогов, замещенных в ароматическом кольце, которые могут быть использованы в синтезе лекарственных препаратов.
Известно, что сама незамещенная фенил-у-аминомасляная кислота (ее гидрохлорид) является ценным лекарственным препаратом (фенибут). Все производные у- аминомасляной кислоты являются потенциально физиологически активными соединениями. В ряду производных у-ами- номасляной кислоты (ГАМК) выделяется р- фенил-ГАМК и ее циклический амид: 4-фенил-2-пиролидон. Они обладают рядом
важных особенностей, противосудорожной активностью, транквилизирующими, седативными, адренолитическими свойствами и рассматриваются как медиаторы торможения. В молекуле /J-фенил-ГАМК есть асимметрический центрь обусловливающий потенциальную оптическую активность этой кислоты. Энантиомеры / -фенил-ГАМК (БФТАМК)оказывают различное физиологическое воздействие.
Однако расщепление ВФГАМК на оптические антиподы остается довольно сложной и трудоемкой задачей.
Известен способ получения энантиоме- ров БФГАМК взаимодействием (+) или (-)- ог-фенилэтиламина с N-карбобензокси- fi- Ph- у-аминомасляной кислотой в этаноле с
VI
ГО
g
ч
последующим выделением диастереомер- ных солей (+) или (-)- а -фенилэтиламина и N-КБЗ-БФГАМК дробной кристаллизацией, а также систем и последующим снятием КВЗ-группы гидролизом соляной кислотой; либо такой же кристаллизацией, но солей N-бензоил-ВФГАМК с (+)- или (-)- а-фенилэ- тиламином. При этом химический выход антиподов БФГАМК (ее гидрохлоридов) составляет: в случае N-KB3 замещенной БФГАМК - 30%, для (-) гидрохлорида БФГАМК, в случае N-бензоил-БФГАМК - 45% для того же антипода.
Таким образом, недостатками метода являются невысокие выходы оптически активных БФГАМК, а также сложность проведения процесса.
Цель изобретения - повышение выхода целевого продукта.
Поставленная цель достигается согласно способу, заключающемуся в том, что оптически активный ментиловый эфир коричной кислоты обрабатывают нитромета ном в условиях межфазного катализа с последующим восстановлением полученного продукта присоединения и гидролизом соляной кислотой.
Взаимодействие нитрометана с эфира- ми коричной кислоты протекает в условиях межфазного катализа (МФК) с достаточно высокими выходами. Для синтеза с менти- ловым эфиром отработаны условия проведения реакции. Варьируются температура, время реакции, катализатор, растворитель. Наиболее подходящим являются проведение реакции в среде ДМФА, в качестве катализатора используют тетраэтиламмоний бромид.
Предлагаемый способ отличается от известного тем, что /3-арил - аминомасляные кислоты получаются асимметрическим синтезом, - в качестве исходного продукта берется ментиловый эфир коричной кислоты, обрабатывается нитрометаном в условиях МФВ с последующим восстановлением и гидролизом соляной кислотой.
Использование ментилового эфира в качестве исходного соединения для получения оптически активных аминокислот сходной структуры неизвесно и позволяет получить указанные соединения с высокими выходами более простым способом.
Пример 1,а)К раствору 11т (0,041 моль) ментилового эфира коричной кислоты (la), 10 г (0,164 моль) нитрометана, 0,9 г (0,0041 моль) бромида тетраэтиламмония в 50 мл ДМФА прибавляют 8,2 г (0,059 моль) карбоната калия. Смесь перемешивают при 60-80°С в течение 40 мин. Затем реакционную смесь .фильтруют, добавляют 50 мл воды, экстрагируют бензолом, сушат МдЗСм. Бензол частично упаривают, добавляют гек- сан(20мл). Выпадают белые кристаллы мен- типового эфира / -фенил-у -нитромасляной кислоты (II а).
.Выход: 11,9 г (84%); т. пл. 83°С. ар°д -55,9 (0,99, хлороформ).
Найдено, %: С 69,9; Н 8,9; N 4,0
C20H29CMN
Вычислено. %: С 69.2; Н 8,4; N 4,0.
б)Взвесь 3 г скелетного никелевого катализатора в 50 мл метанола насыщают водородом при комнатной температуре и
энергичном встряхивании, затем прибавляют раствор 3 г (0,009 моль) (II а) в 1.0 мл метанола. Гидрирование проводят при 40°С и сильном встряхивании до полного насыщения смеси водородом. Катализатор уда- ляют фильтрованием, метанол отгоняют в вакууме. Остаток промывают ацетоном и кристаллизуют из водного этанола.
Получают белый порошок ментилового эфира /Ј-фенил-у -аминомасляной кислоты (III а).
Выход 2,8 г (95%), т. пл. 215°С. Найдено, %: С 75,0; Н 9,5, N 4,2 C2oH3iN02CI
Вычислено, %: С 75,7; Н 9,78; N4,42 Для -57,37(0,38; вода. метанол 1:1).
в)Кипячением Ilia с 20%-ным раствором соляной кислоты в течение 5 ч и последующей экстракцией бензолом, отгонкой воды в вакууме выделяют гидрохлорид (-)-/ -фенил-у-эминомасляной кислоты (IVa). IVa неоднократно промывают на фильтре ацетоном (до отрицательной реакции на ментол по ТСХ).
Выход 77%, -3,2 (6,0; ментол). Найдено, %: С 55,8; Н 6,6; N 4,5 CioHi4N02CI
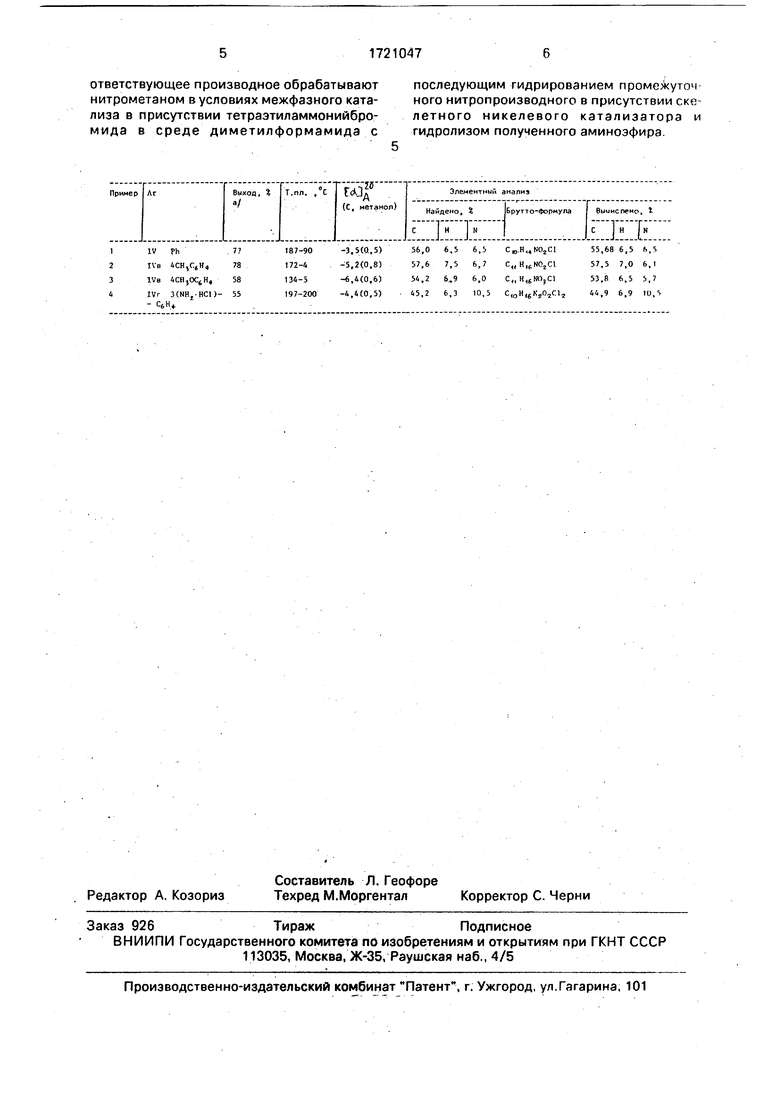
Вычислено, %: С 55,68; Н 6,5; N 4,5 Примеры 2-4. Соединения IV6-r получены аналогично IVa по описанной ме- тодике.
В таблице приведены данные элементного анализа и удельного вращения гидро-хлори- дов/3 - А -у - аминомасляныхкислот(гУа-г).
Формула изобретения Способ получения гидрохлоридов (-) арил- у-аминомасляных кислот общей формулы HCL-H2N-CH2 - СН (Аг) - СН2-СООН, где Ar-CeHs, 4-СНзСбН4,4-СНзОСбН4 или 3-{NH2 xHCl), асимметрическим синтезом, вклю- чающий стадию гидролиза соляной кислотой при температуре кипения реакционной смеси, отличающийся тем, что, с целью увеличения выхода целевого продукта, ментиловый эфир коричной кислоты или ее соответствующее производное обрабатывают нитрометаном в условиях межфазного катализа в присутствии тетраэтиламмонийбро- мида в среде диметилформамида с
последующим гидрированием промежуточ- ного нитропроизводного в присутствии скелетного никелевого катализатора и гидролизом полученного аминоэфира.

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОХЛОРИДА-4-АМИНО-3-ФЕНИЛБУТАНОВОЙ КИСЛОТЫ | 1993 |
|
RU2072984C1 |
| СПОСОБ ПОЛУЧЕНИЯ (S) ( + ) N,N'-ЭTИЛЕН- ?ЯС- | 1971 |
|
SU305647A1 |
| СПОСОБ ЭНАНТИОСЕЛЕКТИВНОГО СИНТЕЗА (S)-ПРЕГАБАЛИНА | 2012 |
|
RU2529996C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГАММА-БУТИРОБЕТАИНА И ЕГО ГИДРОХЛОРИДА | 2019 |
|
RU2720985C1 |
| Способ получения 3,4-диарил-гамма-аминомасляных кислот или их циклических амидов | 1985 |
|
SU1298204A1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-КАРБАМОИЛМЕТИЛ-4-ФЕНИЛ-2-ПИРРОЛИДОНА | 2017 |
|
RU2663899C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-(АЗОЛ-1-ИЛ)ЭТАНАМИНОВ | 2006 |
|
RU2317984C2 |
| Способ получения 4,4-дифенилбутина-1 | 1990 |
|
SU1745714A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 3-ФЕНИЛ-4-АМИНОБУТАНОВОЙ КИСЛОТЫ | 2000 |
|
RU2190595C2 |
| Способ получения сульфонамидов алкилфенилкарбоновых кислот | 1981 |
|
SU1088664A3 |
Изобретение относится к аминокислотам, в частности к получению гидрохлоридов (-)- /3-арил-у -аминомасляных кислот общей формулы: HCI-HaN-CHa-CHfAr)СН2-С(0)-ОН, где Аг СбН5, 4 - СНзСеН4, 4 - СНзОСбН4 или 3-(NH2 НС)-СбН4- обладающих противосудорожной активностью, транквилизирующими и седативными свойствами, что может быть использовано в медицине. Цель - увеличение выхода целевых продуктов. Синтез ведут реакцией ментило- вого эфира коричной кислоты или ее замешенного производного с нитрометаном в условиях межфазного катализа в присутствии (С2Нб)4М® BI°B среде ( (0)H с последующим гидрированием промежуточного нитропроизводного в присутствии скелетного никелевого катализатора и гидролизом полученного аминоэфира HCI при кипении. Выход 55-77%. Эти условия увеличивают выход целевых продуктов до 55-77% (против 30-45%) и исключают стадию дробной кристаллизации с (-)- Јфенил- этиламином. 1 табл.

| Сытинский И.А | |||
| ГАМК в деятельности нервной системы, Л.: Наука, 1972, с | |||
| Способ применения резонанс конденсатора, подключенного известным уже образом параллельно к обмотке трансформатора, дающего напряжение на анод генераторных ламп | 1922 |
|
SU129A1 |
| Способ получения гидрохлоридов (+)-или (-)- @ -фенил- @ -аминомасляной кислоты | 1986 |
|
SU1432051A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Авторское свидетельство СССР № 1413899,кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1992-03-23—Публикация
1990-02-15—Подача