(5.4) СПОСОБ БОРЬБЫ С ГРИБКОВЫМИ МИКРООРГАНИЗМАМИ Изобретение относится к химическим средствам борьбы с вредителями сельского хозяйства,конкретно к спос бу борьбы -с грибковыми листовыми фотопатогенными микроорганизмами на основе производства динитроанилинов. Известно, что 2,6-дихлор-4-нитроанилин эффективен против некоторых видов грибковых заболеваний l . Одним из наиболее распространенны фунгицидов является марганцевая соль этилеийнс-(дитиокарбаминовой) кислоты 2J. Однако указанные фунгициды недостаточно активны для борьбы с ложномучнистой росой и фитофторозом. Цель изобретения - изыскание новы способов борьбы с фитопатогенннми микроорганизмами на основе производных динитроанилинов. Указанная цель достигается исполь зованием способа борьбы с грибковыми микроорганизмами путем обработки их или их биотопов производными динитро анилинов формулы I: I X где X - N(R)z, N(R)CH2-тeтepoцикл, (R5)OR6 или R - Н или С -Сз алкил, причем, когда R - Н, R - Су вторичной алкил, когда R t Н, R представляет собой С -С4 алкил, Ср- циклоалкил, С - алкенил, хлорированный алкил или хлорированный С т, - алкенил, один из радикалов Rпредставляет собой Н, тогда как другой представляет собой Н, фенилтиогруппу или алкоксигруппу, гетероцикл представляет собой остаток 2,5-диметилпирролидина, пиперидина, алкилпиперидина, гексагидроазепина, 2,2-диметилазиридина или С - С , алкилпиперазина, R-Н; метил,этил или фенил, К.° - представляет собой метил, этил или бутил; R- - этил, причем указанное соединение используют в виде жидкого состава, содержащего от 2000 до 10 ч. соединения на 1 млн., или в виде дуста в композиции, содержащей от 0,05 до 5,0 вес.% соединения. Соединения формулы Г получают известными способами. Формы применения препаратов на основе соединений формулы I обычные: дусты, смачивающиеся порошки, эмульсии и т,д.
Хорошие результаты получают при использовании жидких композиций, содержащих 2000 до 10 ч. на 1 млн. активного соединения, при использовании дустов - с композициями, содержащими примерно от 0,05 до 5,0% или более (по весу) активного соединения Активные соединения желательно наносить на пораженные фитопатогенными грибками участки полей в дозах примено от 10 г до 2 кг/г.
Серии испытаний, описанные ниже, служат примером использования соединений этого типа для уменьшения как сферы действия, так и степени заболевания виноградной лозы ложномучнистой росой. В испытаниях соединения наносили в виде раствора или эмульсии, полученной смешением 70 мг испытуемого соединения с 1,925 мл смеси, приготовленной из 500 мл ацетона, 500 мл этанола и 100 мл полиоксиэтиленсорбитанмонолаурата. Композицию, содержащую испытуемое соединение, разбавляли затем деионизованной водой для получения желаемой концентрации, которую измеряли в частях на миллион. В этих испытаниях в качестве растения-хозяина использовали Vitis vlnlfera, а в качестве болезнетворного микроорганизма - Plasmopara V i t i со 1 а .
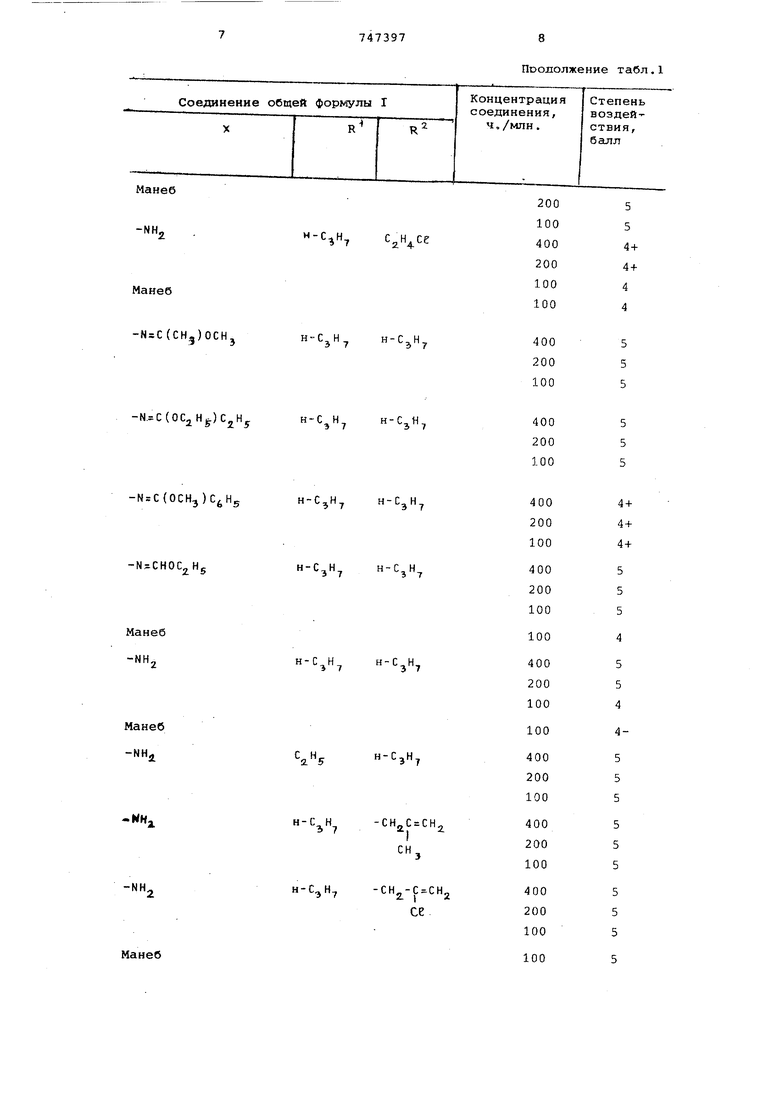
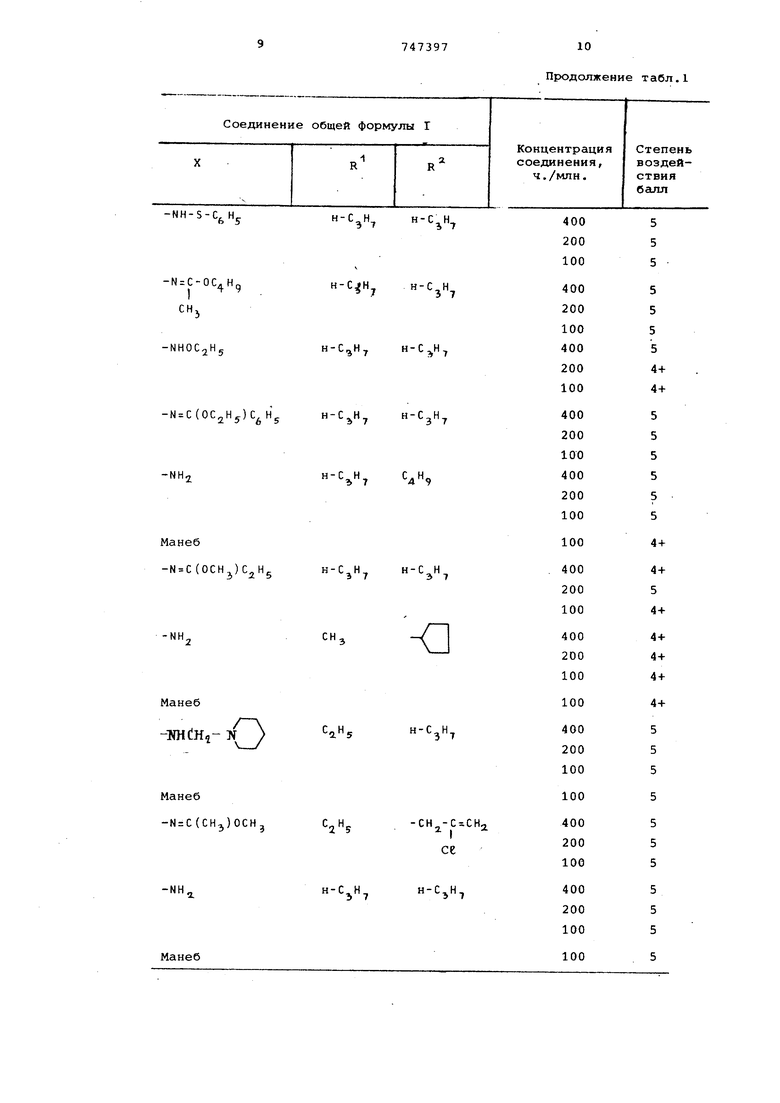
Оценку степени воздействия испытуемых соединений на возбудителей грибковых заболеваний у растений производили по пятибалльной шкале, причем 1 балл означает отсутствие фунгицидного эффекта, 5 баллов - полное подавление грибковых микроорганизмов.
Все испытания проводили в теплице. 5 Поскольку условия испытаний в каждый конкретный день могли различаться, в каждом опыте по испытанию соединений по изобретению проводили парал лельное испытание эталона Манеб для сравнения результатов (этот принцип нашел отражение в том, как сгуппированы полученные результаты в табл. 1).
Таблица 1




| название | год | авторы | номер документа |
|---|---|---|---|
| БЕНЗАМИДЫ И КОМПОЗИЦИИ НА ИХ ОСНОВЕ ДЛЯ ИСПОЛЬЗОВАНИЯ В КАЧЕСТВЕ ФУНГИЦИДОВ | 2003 |
|
RU2483540C2 |
| БЕНЗАМИДЫ И КОМПОЗИЦИИ НА ИХ ОСНОВЕ ДЛЯ ИСПОЛЬЗОВАНИЯ В КАЧЕСТВЕ ФУНГИЦИДОВ | 2003 |
|
RU2314690C2 |
| Способ борьбы с грибными заболеваниями растений | 1973 |
|
SU736856A3 |
| ПРОИЗВОДНЫЕ ГАЛОИДПИРИМИДИНА, ФУНГИЦИД, СПОСОБ БОРЬБЫ С ГРИБКОВЫМИ ЗАБОЛЕВАНИЯМИ СЕЛЬСКОХОЗЯЙСТВЕННЫХ КУЛЬТУР И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ | 1997 |
|
RU2191186C2 |
| Средство абсциссии, дефолиации и десикации неодревесненных частей растений | 1974 |
|
SU572170A3 |
| ГЕРБИЦИД | 1973 |
|
SU404191A1 |
| ФТОРОАЛКОКСИАМИНОТРИАЗИНЫ | 1992 |
|
RU2047607C1 |
| СССРОпубликовано 23.1.197,3. Бюллетень N° 8 Дата опубликования описания 26.VI. 1973УДК 632.951(088.8) | 1973 |
|
SU367575A1 |
| ДИОКСИД ЗАМЕЩЕННОГО ТИАДИАЗИНОНА, СПОСОБ ЕГО ПОЛУЧЕНИЯ, ЕГО ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2812578C1 |
| МИКРОБИЦИДi | 1973 |
|
SU373917A1 |

/-
iNHCH -N )
н-С Н н-С НМанеб
Манеб
-NHo
-NH,
.
-NHOCHa
н-С
Э
-СН2С СН
-NH,
4100 50 25
4
1
3 3 + 1
5 5 5
4 +
5
4
э
5
4 +
5
4 + 4 + Манеб -о -WiCHi
-UHtfHi-N;
Сн.
Сн,
Q
-ЗЯНОНг
г
СН7
/-
(Mъ н-с,н н-СлН
NHCHj-if CHj H-c, S
-ШСНа-тГ
lH5
Манеб
4
-NH,,
Продолжение табл.1
00 50
4+ 5
25 12,5
4
4 +
00 50 25
4- 4+ 4+ 3+ 12,5
00 50 25
4 + 4 + 4
00 50 25
4+
5
4 +
12,5
4
4+ 4+ 4+ 4 100
50
25
12,5
3+ 3
100 50 25 12,5
2- 1
5 5 44400200 100 -СН,
Соединение общей формулы I
-NH,
с,,
Манеб
-N C(CH.5)OCHj
-N. C(.)C,jHy ., H-CjM
-КгС(ОСНз).
Н-С,Н
-NsCHOC,jH5
н-С,Н
Манеб -NH
Манеб
-NH,
zV
-NH,
N Н,.
н-ЦН,
Манеб
Поололжение табл,1
Концентрация соединения, ч,/млн.
5 5
4 + 4 + 4 4
400 200 100
400 200 100
400
4 + 4 + 4 + 200 100
400 200 100
100
400
5 5 4 200 100
100
4-СзН
400
5 200
5 5
100
СИ ,
400
5 5 5
I 200
сн. 100
400 200
се 100
100
-NH-S-C Н
-N
-S СН,
н-С,Н
-NHOC Hj
-N CCOC Hj-lC Hj
СдН,
-NH, Манеб -N C(OCH)C.2H5
Манеб
-WitlH,- N )
N/
Манеб -NrCCCH jOCHJ
,
-NH.
Манеб
Продолжение табл.1
5
5 5
5 5 5
5
4+
4+
5 5 5 5 5 5
100
4+
400
5 5 5
т 200 100
100
400
СН,
I се 200 100
5 5 5
400
С,Н, 200 100
100 4J
Другая серия испытаний иллюстрирует эффект использования соединений формулы 1 для-защиты растений от фитофтороэа (ржавчины). В этой серии испытаний в качестве растений-хозяев использовали томаты, выращенные на полевых участках, которые заражали фитофторозом, естественным путем (болезнетворный микроорганизм Phytophtora Infestans).
(1Нг :«
М;С (СН,,)ОСН н-С,Н,
н-С,Н
NH.
Н-С.,Н,
NH.
NH,
, г
С1
в начале испытаний возраст растений около б недель. Испытуемые соединения наносили на растения 7 раз с интервалами примерно 7 дней. Эффективность борьбы с заболеванием оценивали 4 раза с интервалами 4-5 дней начиная с конца последней серии опрыскивания растений испытуемых соединениями.
Степень распространения фитофтороза на необработанных контрольных участках составляла при первом наблюдении 27%, возрастая примерно до 80% и ньше при последнем наблюдении.
Эффективность борьбы с заболеванием, достигнутая с помощью испытуемых соединений, оценивается в табл. степенью излечения, выраженной в процентах (по сравнению с необработанными контрольными растениями).
Таким образом, указанные соединения обладают высокой фунгицидной ак ИВНОСТЬЮ.
Формула изобретения Способ борьбы с грибковыми микроорганизмами путем обработки их или
Соединения, использованные в этой серии испытаний, переводили в подходящую лекарственную форму - 25%-ные смачивающиеся порошки (пасты), из которых готовили водные дисперсии, содержащие определенную концентрацию активного соединения, указанную в табл. 2. Дисперсии наносили на растения путем опрыскивания из расчета 1400 л/га.
Таблица 2
их биотопа активнодействующим веществом, отличающееся тем, что, с целью усиления эффективности способа обработку ведут динитроанилиновЕлм производными формулы
.К
R
--N
02N-v,A..7vfO
$07
X
N(R
,2 , N ( R) СНд -гетероцикл,
5 где X N-C(R5)R или N-CHOR ;
R - Н или
Cj- С -алкил, причем, когда R -Н ;
R С f вторичный алкил;
0 когда R ФН, R - ,-алкил, С5- циклоалкил, С алкенил, хлорированный Cj, - алкил или хлорированный С т, - алкенил; один из радикалов , тогда как другой представляет собой 5 ;Н, фенилтиогруппу или алкоксигруппу, гетероцикл представляет собой остаток 2,5-диметилпирролидина, пиперидина, алкилпиперидина, гексагидроазепина, 2,2-диметилазиридина или С -С2алкилпипераэииа, R - Н; R - метил, этил или фенил; R - метил, этил или бутил; R - этил, причем указанное соеди нение используют в виде жидкого состава, содержащего от 2000 до 10 ч соединения на 1 млн или в виде дуста в композиции, содержащей от 0,05 до 5,0 вес.% соединения. Приоритет по признакам 23.06.75 1 2. R - водород или С -C-j-алкил, R - вторичный алкил; С - С --алкил, нил; хлорированный С -алкил или хло рированный С -алкенил; RS- водород; гетероцикл - остаток 2,5-диметилпирролидина, пиперидина; Я - водород; R - метил/ R - метил, этил; R - этил. 19.03.76 при R - фенилтиогруппа алкоксигруппа; гетероцикл - остаток .-алкилпиперидина, гексагидроазепина, 2,2 диметилазиридина, или С -Cj, алкилпиперазина;R - этил, фенил; R - бутил. Источники информации, принятые во внимание при экспертизе 1.Мельников Н.Н. Химия пестицидов. М., 1968, с. 104. 2.Мельников Н.Н. Химия пестицидов. М., 1968, с. 241 (прототип).
Авторы
Даты
1980-07-23—Публикация
1976-06-22—Подача