ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Изобретение относится к технологии пестицидов, и в частности, к диоксиду замещенного тиадиазинона, способу его получения, его гербицидной композиции и его применению.
УРОВЕНЬ ТЕХНИКИ
Борьба с сорняками является одним из самых важных этапов на пути достижения высокоэффективного сельскохозяйственного производства. Промышленность производит и поставляет на рынок различные гербициды, в том числе гербициды на основе ингибитора фотосистемы II (PS II), и другие подобные гербициды, например, в патентных документах US3920641, US3989507 и в других патентных документах раскрываются соединения общей формулы 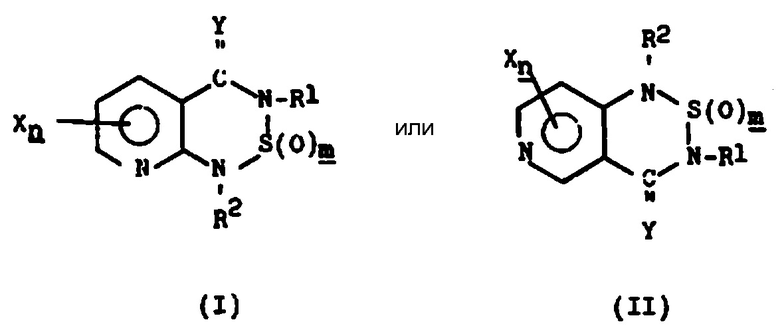 ; в патентном документе DE2656289A1 и в других патентных документах раскрываются соединения общей формулы
; в патентном документе DE2656289A1 и в других патентных документах раскрываются соединения общей формулы 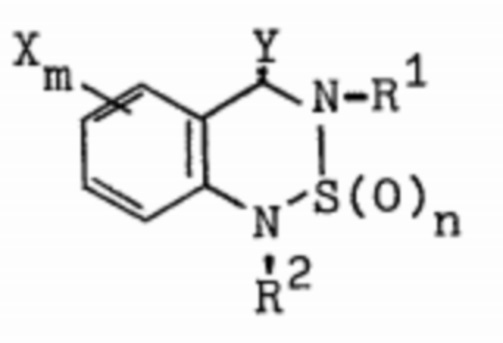 , среди которых разработанный фирмой BASF гербицид бентазон на основе бензотиадиазинона применяют в основном на сельскохозяйственных культурах, таких как рис, соя, арахис, пшеница и другие культуры, для предотвращения и борьбы с широколистными сорняками и осокоцветными сорняками, но он неэффективен в случае злаковых сорняков. Однако, ученые по-прежнему непрерывно проводят исследования и разрабатывают новые гербициды, обладающие высокой эффективностью, безопасностью, высокими экономическими характеристики и различными механизмами действия, для решения проблем, таких как растущий рынок, резистентность сорняков, продолжительность действия и экономическая эффективность пестицидов, а также растущая озабоченность людей по поводу загрязнения окружающей среды.
, среди которых разработанный фирмой BASF гербицид бентазон на основе бензотиадиазинона применяют в основном на сельскохозяйственных культурах, таких как рис, соя, арахис, пшеница и другие культуры, для предотвращения и борьбы с широколистными сорняками и осокоцветными сорняками, но он неэффективен в случае злаковых сорняков. Однако, ученые по-прежнему непрерывно проводят исследования и разрабатывают новые гербициды, обладающие высокой эффективностью, безопасностью, высокими экономическими характеристики и различными механизмами действия, для решения проблем, таких как растущий рынок, резистентность сорняков, продолжительность действия и экономическая эффективность пестицидов, а также растущая озабоченность людей по поводу загрязнения окружающей среды.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В настоящем изобретении предлагается диоксид замещенного тиадиазинона, способ его получения, его гербицидная композиция и его применение. Это соединение обладает высокой гербицидной активностью в отношении злаковых сорняков, широколистных сорняков или ширицевых сорняков, и обладает высокой селективностью в отношении сельскохозяйственных культур, таких как соя, кукуруза, рис или пшеница.
Техническое решение задачи, предлагаемое изобретением, приведено далее.
Диоксид замещенного тиадиазинона, изображаемый общей формулой I
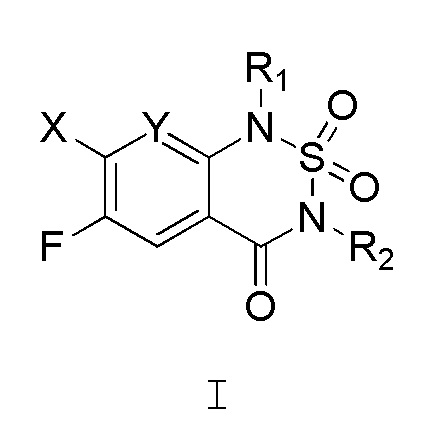
где
R1 и R2 каждый независимо представляет водород, циано, алкил, алкенил, алкинил, циклоалкил, циклоалкил-алкил, формил-алкил, циано-алкил или гидроксил-алкил с галогеном или без галогена, арил, арил-алкил, гетероциклил, гетероциклил-алкил, R3-O-(алкил)n-, R3-S-(алкил)n-, R3-(CO)-(алкил)n-, R3-(CO)-O-(алкил)n-, R3-O-(алкил)n-(CO)-, R3-S-(CO)-(алкил)n-, R3-O-(CO)-(алкил)-, R3-O-(CO)-O-(алкил)-, R3-SO2-(алкил)n-, R4R5N-(CO)-, R4R5N-(алкил)n-, R3-(CO)-NR6-, R4R5N-(CO)-NR6-, 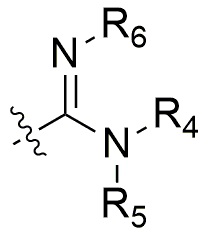 или R4R5R6Si-O-(алкил)n-;
или R4R5R6Si-O-(алкил)n-;
каждый R3 независимо представляет алкил, алкенил, алкинил, циклоалкил или циклоалкил-алкил с галогеном или без галогена, арил, арил-алкил, гетероциклил или гетероциклил-алкил;
R4, R5 и R6 каждый независимо представляет водород, алкил, алкенил, алкинил, циклоалкил или циклоалкил-алкил с галогеном или без галогена, арил, арил-алкил, гетероциклил или гетероциклил-алкил;
n представляет 0 или 1;
X представляет водород или галоген; Y представляет C-Z или N; Z представляет водород или галоген; и когда X представляет галоген, Z представляет водород,
"арил" или "гетероциклил" является незамещенным или замещенным с помощью, по меньшей мере, одной (1, 2, 3, 4, 5) из следующих групп: галоген, нитро, циано, тиоцианато, циано-алкил, меркапто, гидроксил, гидроксил-алкил, карбоксил, формил, азидо, триалкил-силил, диалкил-фосфоно, незамещенный или замещенный гетероциклил, гетероциклил-алкил, арил или арил-алкил, алкил, алкенил, алкинил, циклоалкил, циклоалкенил, циклоалкил-алкил, циклоалкенил-алкил, циклоалкил, замещенный с помощью алкила, OR", SR", -алкил-OR", -O-алкил-OR", -алкил-SR", COR", -алкил-COR", -O-алкил-COR", COOR", -алкил-COOR", -O-алкил-COOR", COSR", SOR", SO2R”, -O-SO2R", -алкил-SO2R", OCOR", -алкил-OCOR" или SCOR" с галогеном или без галогена; амино, амино-карбонил, амино-карбонил-алкил или амино-сульфонил, который является незамещенным или замещен с помощью одной или двух групп, выбранных из группы, состоящей из R", COR", COOR", SO2R", -алкил-SO2R" или OR" с галогеном или без галогена; или любые два смежных углеродных атомов в кольце соединены с -CH2CH2CH2-, -OCH2CH2-, -OCH2O-, -OCH2CH2O- или -CH=CH-CH =CH- группами с образованием конденсированного кольца;
каждый R" независимо представляет алкил, алкенил, алкинил, циклоалкил, циклоалкил-алкил, циклоалкенил, циклоалкенил-алкил и незамещенный или замещенный гетероциклил, гетероциклил-алкил, арил или арил-алкил.
Предпочтительно, когда R1 и R2 каждый независимо представляет водород, циано, C1-C8 алкил, C2-C8 алкенил, C2-C8 алкинил, C3-C8 циклоалкил, C3-C8 циклоалкил-C1-C8 алкил, формил-C1-C8 алкил, циано-C1-C8 алкил или гидроксил-C1-C8 алкил с галогеном или без галогена, арил, арил-C1-C8 алкил, гетероциклил, гетероциклил-C1-C8 алкил, R3-O-(C1-C8 алкил)n-, R3-S-(C1-C8 алкил)n-, R3-(CO)-(C1-C8 алкил)n-, R3-(CO)-O-(C1-C8 алкил)n-, R3-O-(C1-C8 алкил)n-(CO)-, R3-S-(CO)-(C1-C8 алкил)n-, R3-O-(CO)-(C1-C8 алкил)-, R3-O-(CO)-O-(C1-C8 алкил)-, R3-SO2-(C1-C8 алкил)n-, R4R5N-(CO)-, R4R5N-(C1-C8 алкил)n-, R3-(CO)-NR6-, R4R5N-(CO)-NR6-,  или R4R5R6Si-O-(C1-C8 алкил)n-;
или R4R5R6Si-O-(C1-C8 алкил)n-;
каждый R3 независимо представляет C1-C8 алкил, C2-C8 алкенил, C2-C8 алкинил, C3-C8 циклоалкил или C3-C8 циклоалкил-C1-C8 алкил с галогеном или без галогена, арил, арил-C1-C8 алкил, гетероциклил или гетероциклил-C1-C8 алкил;
R4, R5 и R6 каждый независимо представляет водород, C1-C8 алкил, C2-C8 алкенил, C2-C8 алкинил, C3-C8 циклоалкил или C3-C8 циклоалкил-C1-C8 алкил с галогеном или без галогена, арил, арил-C1-C8 алкил, гетероциклил или гетероциклил-C1-C8 алкил;
n представляет 0 или 1;
X представляет водород или галоген, Y представляет C-Z или N, Z представляет водород или галоген, и когда X представляет галоген, Z представляет водород;
"арил" или "гетероциклил" является незамещенным или замещенным с помощью, по меньшей мере, одной (1, 2, 3, 4, 5) из следующих групп: галоген, нитро, циано, тиоцианато, циано-C1-C8 алкил, меркапто, гидроксил, гидроксил-C1-C8 алкил, карбоксил, формил, азидо, три-C1-C8 алкил-силил, ди-C1-C8 алкил-фосфоно; гетероциклил, гетероциклил-C1-C8 алкил, арил или арил-C1-C8 алкил, который является незамещенным или замещен с помощью 1-3 групп, выбранных из группы, состоящей из галогена, C1-C8 алкила, галоген-C1-C8 алкила, C1-C8 алкокси или амино; C1-C8 алкил, C2-C8 алкенил, C2-C8 алкинил, C3-C8 циклоалкил, C3-C8 циклоалкенил, C3-C8 циклоалкил-C1-C8 алкил, C3-C8 циклоалкенил-C1-C8 алкил, C3-C8 циклоалкил, замещенный с помощью C1-C8 алкила, OR", SR", -(C1-C8)алкил-OR", -O-(C1-C8)алкил-OR", -(C1-C8)алкил-SR", COR", -(C1-C8)алкил-COR", -O-(C1-C8)алкил-COR", COOR", -(C1-C8)алкил-COOR", -O-(C1-C8)алкил-COOR", COSR", SOR", SO2R", -O-SO2R", -(C1-C8)алкил-SO2R", OCOR", -(C1-C8)алкил-OCOR" или SCOR" с галогеном или без галогена; амино, амино-карбонил, амино-карбонил-C1-C8 алкила или амино-сульфонила, который является незамещенным или замещен с помощью одной или двух групп, выбранных из группы, состоящей из R", COR", COOR", SO2R”, -(C1-C8)алкил-SO2R" или OR" с галогеном или без галогена; или любые два смежных углеродных атомов в кольце соединены с -CH2CH2CH2-, -OCH2CH2-, -OCH2O-, -OCH2CH2O- или -CH=CH-CH=CH- группами с образованием конденсированного кольца;
каждый R" независимо представляет C1-C8 алкил, C2-C8 алкенил, C2-C8 алкинил, C3-C8 циклоалкил, C3-C8 циклоалкил-C1-C8 алкил, C3-C8циклоалкенил, C3-C8 циклоалкенил-C1-C8 алкил и гетероциклил, гетероциклил-C1-C8 алкил, арил или арил-C1-C8 алкил, который является незамещенным или замещен с помощью 1-3 групп, выбранных из группы, состоящей из галогена, C1-C8 алкила, галогенированного C1-C8 алкила, C1-C8 алкокси или амино.
Более предпочтительно, когда R1 и R2 каждый независимо представляет водород, циано, C1-C6 алкил, C2-C6 алкенил, C2-C6 алкинил, C3-C6 циклоалкил, C3-C6 циклоалкил-C1-C6 алкил, формил-C1-C6 алкил, циано-C1-C6 алкил или гидроксил-C1-C6 алкил с галогеном или без галогена, арил, арил-C1-C6 алкил, гетероциклил, гетероциклил-C1-C6 алкил, R3-O-(C1-C6 алкил)n-, R3-S-(C1-C6 алкил)n-, R3-(CO)-(C1-C6 алкил)n-, R3-(CO)-O-(C1-C6 алкил)n-, R3-O-(C1-C6 алкил)n-(CO)-, R3-S-(CO)-(C1-C6 алкил)n-, R3-O-(CO)-(C1-C6 алкил)-, R3-O-(CO)-O-(C1-C6 алкил)-, R3-SO2-(C1-C6 алкил)n-, R4R5N-(CO)-, R4R5N-(C1-C6 алкил)n-, R3-(CO)-NR6-, R4R5N-(CO)-NR6-,  или R4R5R6Si-O-(C1-C6 алкил)n-;
или R4R5R6Si-O-(C1-C6 алкил)n-;
каждый R3 независимо представляет C1-C6 алкил, C2-C6 алкенил, C2-C6 алкинил, C3-C6 циклоалкил или C3-C6 циклоалкил-C1-C6 алкил с галогеном или без галогена, арил, арил-C1-C6 алкил, гетероциклил или гетероциклил-C1-C6 алкил;
R4, R5 и R6 каждый независимо представляет водород, C1-C6 алкил, C2-C6 алкенил, C2-C6 алкинил, C3-C6 циклоалкил или C3-C6 циклоалкил-C1-C6 алкил с галогеном или без галогена, арил, арил-C1-C6 алкил, гетероциклил или гетероциклил-C1-C6 алкил;
n представляет 0 или 1;
X представляет водород или галоген, Y представляет C-Z или N, Z представляет водород или галоген, и когда X представляет галоген, Z представляет водород;
"арил" или "гетероциклил" является незамещенным или замещенным с помощью, по меньшей мере, одной (1, 2, 3, 4, 5) из следующих групп: галоген, нитро, циано, тиоцианато, циано-C1-C6 алкил, меркапто, гидроксил, гидроксил-C1-C6 алкил, карбоксил, формил, азидо, три-C1-C6 алкил-силил, ди-C1-C6 алкил-фосфоно, гетероциклил, гетероциклил-C1-C6 алкил, арил или арил-C1-C6 алкил, который является незамещенным или замещен с помощью 1-3 групп, выбранных из группы, состоящей из галогена, C1-C6 алкила, галоген-C1-C6 алкила, C1-C6 алкокси или амино; C1-C6 алкил, C2-C6 алкенил, C2-C6 алкинил, C3-C6 циклоалкил, C3-C6 циклоалкенил, C3-C6 циклоалкил-C1-C6 алкил, C3-C6 циклоалкенил-C1-C6 алкил, C3-C6 циклоалкил, замещенный с помощью C1-C6 алкила, OR", SR", -(C1-C6)алкил-OR", -O-(C1-C6)алкил-OR", -(C1-C6)алкил-SR", COR", -(C1-C6)алкил-COR", -O-(C1-C6)алкил-COR", COOR", -(C1-C6)алкил-COOR", -O-(C1-C6)алкил-COOR", COSR", SOR", SO2R", -O-SO2R", -(C1-C6)алкил-SO2R", OCOR", -(C1-C6)алкил-OCOR" или SCOR" с галогеном или без галогена; амино, амино карбонил, амино-карбонил-C1-C6 алкил или амино-сульфонил, который является незамещенным или замещен с помощью одной или двух групп, выбранных из группы, состоящей из R", COR", COOR", SO2R”, -(C1-C6)алкил-SO2R" или OR" с галогеном или без галогена; или любые два смежных углеродных атомов в кольце соединены с -CH2CH2CH2-, -OCH2CH2-, -OCH2O-, -OCH2CH2O- или -CH=CH-CH=CH- группами с образованием конденсированного кольца;
каждый R" независимо представляет C1-C6 алкил, C2-C6 алкенил, C2-C6 алкинил, C3-C6 циклоалкил, C3-C6 циклоалкил-C1-C6 алкил, C3-C6циклоалкенил, C3-C6 циклоалкенил-C1-C6 алкил, и гетероциклил, гетероциклил-C1-C6 алкил, арил или арил-C1-C6 алкил, который является незамещенным или замещен с помощью 1-3 групп, выбранных из группы, состоящей из галогена, C1-C6 алкила, галоген-C1-C6 алкила, C1-C6 алкокси или амино.
Кроме того, предпочтительно, когда R1 и R2 каждый независимо представляет водород, циано; C1-C6 алкил, C2-C6 алкенил, C2-C6 алкинил, C3-C6 циклоалкил, C3-C6 циклоалкил-C1-C3 алкил, формил-C1-C3 алкил, циано-C1-C3 алкил или гидроксил-C1-C3 алкил с галогеном или без галогена, арил, арил-C1-C3 алкил, гетероциклил, гетероциклил-C1-C3 алкил, R3-O-(C1-C3 алкил)n-, R3-S-(C1-C3 алкил)n-, R3-(CO)-(C1-C3 алкил)n-, R3-(CO)-O-(C1-C3 алкил)n-, R3-O-(C1-C3 алкил)n-(CO)-, R3-S-(CO)-(C1-C3 алкил)n-, R3-O-(CO)-(C1-C3 алкил)-, R3-O-(CO)-O-(C1-C3 алкил)-, R3-SO2-(C1-C3 алкил)n-, R4R5N-(CO)-, R4R5N-(C1-C3 алкил)n-, R3-(CO)-NR6-, R4R5N-(CO)-NR6-,  или R4R5R6Si-O-(C1-C3 алкил)n-;
или R4R5R6Si-O-(C1-C3 алкил)n-;
X представляет водород или фтор, Y представляет C-Z или N, Z представляет водород, фтор, хлор, бром или йод, и когда X представляет фтор, Y представляет C-Z, и Z представляет водород.
В еще одном предпочтительном варианте осуществления, R1 и R2 каждый независимо представляет водород, C1-C6 алкил, C2-C6 алкенил, C2-C6 алкинил, R3-(CO)-, R3-O-(CO)- или R3-O-(CO)-O-(C1-C6 алкил)-;
каждый R3 независимо представляет C1-C6 алкил;
X представляет водород или фтор, Y представляет C-Z или N, Z представляет водород, фтор, хлор, бром или йод, и когда X представляет фтор, Y представляет C-Z, и Z представляет водород.
При определении соединения, представленного приведенной выше формулой и всеми приведенными далее структурными формулами, применяемые технические термины, независимо от того, используются ли они отдельно или используются в сложном слове, представляют собой следующие заместители. Алкил, имеющий более чем два углеродных атома, может быть линейным или разветвленным. Например, алкил в сложном слое "-алкил-OR" может представлять -CH2-, -CH2CH2-, -CH(CH3)-, -C(CH3)2-, и другие подобные фрагменты. Алкил представляет собой, например, C1 алкил: метил; C2 алкил: этил; C3 алкил: пропил, такой как н-пропил или изопропил; C4 алкил: бутил, такой как н-бутил, изобутил, третбутил или 2-бутил; C5 алкил: пентил, такой как н-пентил; C6 алкил: гексил, такой как н-гексил, изогексил и 1,3-диметилбутил. Аналогично, алкенил представляет собой, например, аллил, 1-метилпроп-2-ен-1-ил, 2-метилпроп-2-ен-1-ил, бут-2-ен-1-ил, бутил-3-ен-1-ил, 1-метилбут-3-ен-1-ил and 1-метилбут-2-ен-1-ил. Алкинил представляет собой, например, пропаргил, бут-2-ин-1-ил, бут-3-ин-1-ил, 1-метилбут-3-ин-1-ил. По меньшей мере, одна (например, 1, 2 или 3) кратная связь может располагаться в любом положении каждой ненасыщенной группы. Циклоалкил представляет собой карбоциклическую насыщенную кольцевую систему, имеющую, например, от трех до шести углеродных атомов, такую как циклопропил, циклобутил, циклопентил или циклогексил. Аналогично, циклоалкенил представляет собой моноциклоалкенил, имеющий, например, от трех до шести кольцевых углеродных атомов, такой как циклопропенил, циклобутенил, циклопентенил и циклогексенил, в котором двойная связь может находиться в любом положении. Галоген представляет собой фтор, хлор, бром или йод.
Если не указано иное, то применяемые технические термины, независимо от того, используются ли они отдельно или используются в сложном слове, имеют следующие значения. "Арил" по настоящему изобретению включает, но этим не ограничивая, фенил, нафтил, 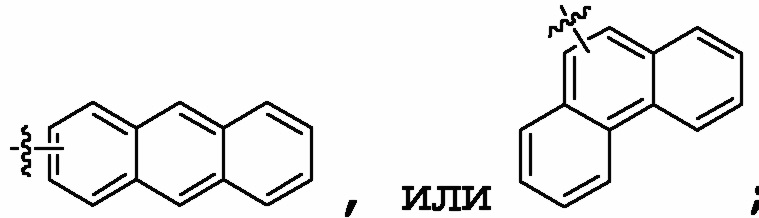 "гетероциклил" включает, но не только, и этим не ограничивая,
"гетероциклил" включает, но не только, и этим не ограничивая, 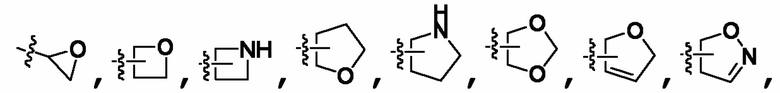
 , который имеет 0, 1 или 2 оксогруппы; но также включает "гетероарил", который представляет собой ароматическую циклическую группу, имеющую, например, от 3 до 6 (например, 3, 4 , 5 или 6) кольцевых атомов, и который может быть также конденсированным с бензольным кольцом, и от 1 до 4 (например, 1, 2 , 3 или 4) гетероатомов в кольце, которые выбирают из группы, состоящей из кислорода, азота и серы.
, который имеет 0, 1 или 2 оксогруппы; но также включает "гетероарил", который представляет собой ароматическую циклическую группу, имеющую, например, от 3 до 6 (например, 3, 4 , 5 или 6) кольцевых атомов, и который может быть также конденсированным с бензольным кольцом, и от 1 до 4 (например, 1, 2 , 3 или 4) гетероатомов в кольце, которые выбирают из группы, состоящей из кислорода, азота и серы. 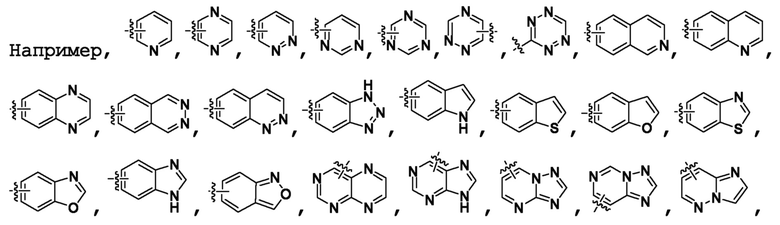
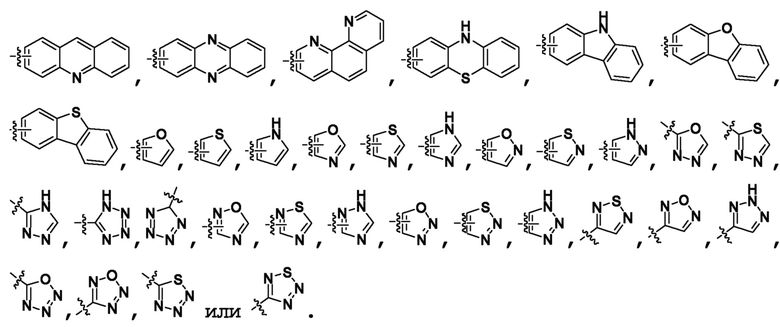
Если группа замещена с помощью группы, то следует иметь в виду, что это означает, что эта группа замещена с помощью одной или более групп, которые являются одинаковыми или различными группами, выбранными из упомянутых выше групп. Кроме того, независимо выбирают одинаковые или различные характеристики замещения, содержащиеся в одинаковых или различных заместителях, и они могут быть одинаковыми или различными. Это также применимо к кольцевым системам, образованным различными атомами и фрагментами. Следует иметь в виду, что для специалистов в данной области является очевидным, что из объема формулы изобретения будут исключены те соединения, которые химически нестабильны при стандартных условиях.
Кроме того, если специально не будет указано иное, то термин, применяемый в настоящем изобретении перед или после нескольких указанных последовательно заместителей (разделенных с помощью "," или с помощью "или"), накладывает ограничение на каждый из заместителей, например, термин "с галогеном или без галогена" в тексте "алкил, алкенил, алкинил, циклоалкил или циклоалкил-алкил с галогеном или без галогена" накладывает ограничение на каждую из следующих групп "алкил", "алкенил", "алкинил", "циклоалкил" и "циклоалкил-алкил"; группа (в том числе гетероциклил, арил, и другие подобные группы) без указания положения ее присоединения может быть присоединена в любом положении, в том числе в C-положении или N-положении; если в этих положения возможно замещение, заместитель может быть замещен в любом положении, при условии, что это не противоречит теории образования валентных связей. Например, если гетероарил 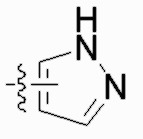 замещен с помощью одного метила, то он может представлять собой
замещен с помощью одного метила, то он может представлять собой 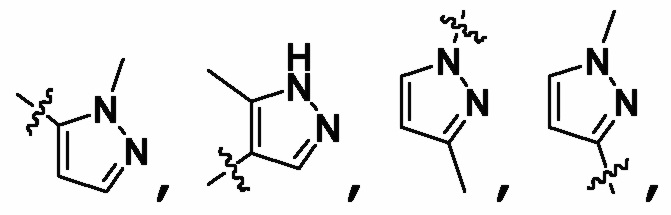 и так далее.
и так далее.
В зависимости от свойств заместителей и способа их присоединения, соединение формулы I и его производные могут существовать в виде стереоизомера. Например, если соединение имеет один или несколько асимметричных атомов углерода, оно может иметь энантиомеры и диастереомеры. Стереоизомер может быть получен из смесей, образующихся в результате проведения синтеза, с помощью обычных методов разделения, например, путем хроматографического разделения. Стереоизомер также может быть получен селективно путем проведения стереоселективных реакций и использования оптически активных исходных материалов и/или вспомогательных веществ. Настоящее изобретение также относится ко всем стереоизомерам и их смесям, которые подпадают под общую формулу I, но конкретно не определены.
Способ получения диоксида замещенного тиадиазинона представляет собой следующее:
в случае, когда R2 в приведенной выше общей формуле I представляет собой водород, способ получения включает следующие стадии:
(1) проведение реакции замещения соединения общей формулы III с электрофильным реагентом 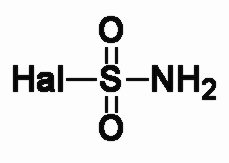 с получением соединения общей формулы II-1;
с получением соединения общей формулы II-1;
(2) проведение реакции внутримолекулярной циклизации соединения общей формулы II-1 с получением соединения общей формулы I-1;
(3) проведение реакции алкилирования соединения общей формулы I-1 и R1'-L с получением соединения общей формулы I-2;
в случае, когда R2 в приведенной выше общей формуле I представляет собой R2', способ получения включает следующие стадии:
(1') получение соединения общей формулы II-2 из соединения общей формулы III в присутствии 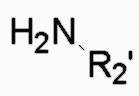 , электрофильного реагента
, электрофильного реагента 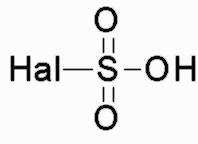 и дегидратирующего реагента;
и дегидратирующего реагента;
(2') проведение реакции внутримолекулярной циклизации соединения общей формулы II-2 с получением соединения общей формулы I-3;
(3') проведение реакции алкилирования соединения общей формулы I-3 и R1'-L с получением соединения общей формулы I-4;
где, Hal и L каждый независимо представляет галоген; R1' и R2' соответственно представляют значения для R1 и R2, определенные выше, исключая водород; X и Y определены выше;
схема химической реакции может быть представлена в следующем виде:
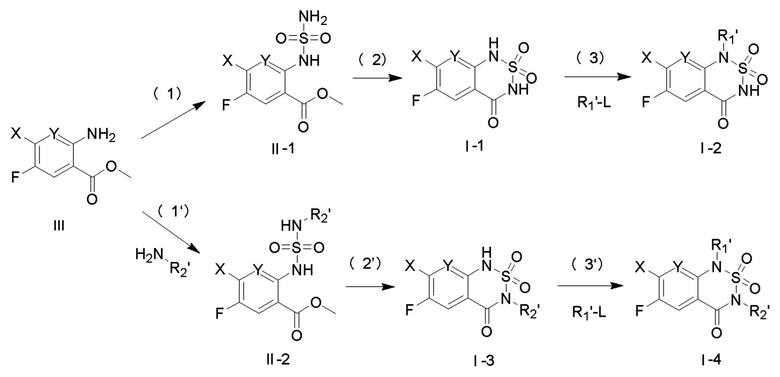
на стадии (1'), дегидратирующий реагент представляет собой, предпочтительно, оксихлорид фосфора, концентрированную серную кислоту, пентаоксид фосфора или пентахлорид фосфора;
стадии (1), (1'), (2), (2'), (3) и (3') все проводят в присутствии оснований и органических растворителей; каждое из оснований независимо выбирают из неорганических оснований (таких как K2CO3, Na2CO3, Cs2CO3, NaHCO3, KF, CsF, KOAc, NaOAc, K3PO4, t-BuONa, EtONa, NaOH, KOH, NaOMe, и других подобных оснований) или органических оснований (таких как пиразол, триэтиламин, DIEA, и других подобных оснований); каждый из органических растворителей независимо выбирают из метанола, этанола, ацетонитрила, дихлорэтана, DMF, DMSO, диоксана, дихлорметана или этилацетата.
Гербицидная композиция, включающая эффективную с точки зрения гербицидного действия дозу, по меньшей мере, одного диоксида замещенного тиадиазинона; предпочтительно, когда гербицидная композиция также включает вспомогательные вещества для приготовления гербицидной композиции.
Способ борьбы с сорняками, который включает нанесение гербицидно эффективной дозы, по меньшей мере, одного из диоксидов замещенного тиадиазинона или гербицидной композиции на растение или пораженный сорняками участок.
Применение, по меньшей мере, одного из диоксидов замещенного тиадиазинона или описанной выше гербицидной композиции для борьбы с сорняками является предпочтительным, когда диоксид замещенного тиадиазинона применяют для предотвращения и/или борьбы с сорняками полезной сельскохозяйственной культуры, где полезная сельскохозяйственная культура представляет собой трансгенную сельскохозяйственную культуру или сельскохозяйственную культуру, подвергнутую обработке методом редактирования гена.
Соединения формулы I по изобретению обладают исключительной гербицидной активностью в отношении широкого спектра важных с экономической точки зрения однодольных и двудольных вредных растений. Активные соединения также эффективно воздействуют на многолетние сорняки, которые образуют побеги из корневищ, корневых побегов или других многолетних органов и с которыми трудно бороться. В этом контексте, как правило, не имеет значения, применяются ли соединения по изобретению до посева, до появления всходов или после появления всходов. В частности, можно привести примеры некоторых представителей флоры однодольных и двудольных сорняков, с которыми можно бороться с помощью соединений по изобретению, не ограничивая их определенными видами. Примерами видов сорняков, на которые эффективно действуют активные соединения, являются, среди однодольных, овес (Avena), плевел (Lolium), лисохвост (Alopecurus), канареечник клубневой (Phalaris), ежовник (Echinochloa), росичка (Digitaria), щетинник (Setaria), а также виды сыти (Cyperus) из однолетних сорняков, и из многолетних видов пырей (Agropyron), бермудская трава (Cynodon), императа (Imperata) и сорго (Sorghum), а также многолетние виды сыти (Cyperus).
В случае двудольных сорняков, спектр действия соединений распространяется на такие виды, как, например, подмаренник (Galium), растение семейства фиалковых (Viola), вероника (Veronica), яснотка (Lamium), звездчатка (Stellaria), щирица (Amaranthus), горчица (Sinapis), ипомея (Ipomoea), сида (Sida), ромашка (Matricaria) и канатник (Abutilon) из числа однолетних сорняков, а также вьюнок (Convolvulus), бодяк (Cirsium), щавель (Rumex) и полынь (Artemisia) из числа многолетних сорняков. Активные соединения по изобретению также позволяют эффективно бороться с вредными растениями, которые встречаются в специфических условиях выращивания риса, такими как, например, ежовник (Echinochloa), стрелолист (Sagittaria), частуха (Alisma), болотница (Eleocharis), камыш (Scirpus) и сыть (Cyperus). Если соединения согласно изобретению наносят на поверхность почвы до прорастания сельскохозяйственной культуры, то всходы сорняков либо полностью предотвращают появление всходов, либо сорняки растут до тех пор, пока не достигнут стадии семядолей, и затем их рост прекращается, и, в конце концов, через три-четыре недели они полностью погибают. В частности, соединения по изобретению проявляют очень высокую активность в отношении метлицы обыкновенной (Aperaspica venti), мари белой (Chenopodium album), яснотки пурпурной (Lamium purpureum), гореца вьюнкового (Polygonum convolvulus), звездчатки средней (Stellaria media), вероники плющелистной (Veronica hederifolia), вероники персидской (Veronica persica), фиалки трехцветной (Viola tricolor) и против видов щирицы (Amaranthus), подмаренника (Galium) и кохии (Kochia).
Несмотря на то, что соединения по изобретению обладают высокой гербицидной активностью в отношении однодольных и двудольных сорняков, тем не менее, не происходит никаких повреждений или происходят повреждения только в незначительной степени сельскохозяйственных растений из экономически важных сельскохозяйственных культур, таких как, например, пшеница, ячмень, рожь, рис, кукуруза, сахарная свекла, хлопок и соя. В частности, соединения по изобретению имеют высокую совместимость со злаками, такими как пшеница, ячмень и кукуруза, в частности, с пшеницей. По этим причинам, соединения по настоящему изобретению подходят в высокой степени для селективной борьбы с ростом нежелательных растений на участках выращивания сельскохозяйственных культур или декоративных растений.
Благодаря своим гербицидным свойствам, эти активные соединения могут быть применены для борьбы с вредными растениями в посевах известных растений или еще не созданных методами генетической инженерии растений. Трансгенные растения, как правило, имеют особенно предпочтительные свойства, например, резистентность к воздействию некоторых пестицидов, в частности, конкретных гербицидов, устойчивость к болезням растений или к воздействию организмов-возбудителей болезней растений, таким как конкретные насекомые или микроорганизмы, такие как грибки, бактерии или вирусы. Другие конкретные свойства относятся, например, к количеству, качеству, стабильности при хранении, составу и конкретным ингредиентам собранного урожая продукта. Так, известны трансгенные растения, имеющие повышенное содержание крахмала или модифицированное качество крахмала или имеющие другой состав жирных кислот в собранном урожае продукта.
Предпочтительным является применение соединений формулы I по изобретению или их солей в случае экономически важных трансгенных культур полезных и декоративных растений, например, злаков, таких как пшеница, ячмень, рожь, овес, просо, рис, маниок и кукуруза, а также в посевах сахарной свеклы, хлопчатника, сои, рапса, картофеля, томатов, гороха и других видов овощей Соединения формулы I могут быть применены в качестве гербицидов в посевах полезных растений, резистентных или ставших резистентными в результате использования методов генной инженерии к фитотоксическому воздействию гербицидов.
Традиционные способы получения новых растений с модифицированными по сравнению с известными растениями свойствами включают, например, традиционные методы селекции и генерации мутантов. В качестве варианта, новые растения с модифицированными свойствами могут быть созданы методами генной инженерии (смотрите, например, патентные документы ЕР-А 0 221 044, ЕР-А 0 131 624). Например, было описано несколько случаев:
- вызванные методами генетической инженерии изменения в сельскохозяйственных культурах с целью модификации крахмала, синтезируемого в растениях (например, патентные документы WO 92/11376, WO 92/14827, WO 91/19806),
- трансгенные сельскохозяйственные культуры, которые являются резистентными к воздействию конкретных гербицидов типа глюфосината (смотрите, например, патентные документы EP-A 0 242 236, EP-A 0 242 246) или типа глифосата (патентный документ WO 92/00377), или типа сульфонилмочевины (патентные документы EP-A 0 257 993, U.S. Pat. No. 5013659A),
- трансгенные сельскохозяйственные культуры, например, хлопок, обладающие способностью продуцировать токсины Bacillus thuringiensis (Bt токсины), которые придают растениям резистентность к конкретным сельскохозяйственным вредителям (патентные документы EP-A 0 142 924, EP-A 0 193 259),
- трансгенные сельскохозяйственные культуры, имеющие модифицированную композицию жирных кислот (патентный документ WO 91/13972).
В принципе, известны многочисленные методы молекулярной биологии, позволяющие получать новые трансгенные растения с модифицированными свойствами; смотрите, например, публикации Sambrook et al., 1989, Molecular Cloning, A Laboratory Manual, 2nd ed. Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y.; или Winnacker "Gene und Klone" [Genes and Clones], VCH Weinheim, 2nd edition 1996, или Christou, "Trends in Plant Science" 1 (1996) 423-431). Для проведения таких генно-инженерных манипуляций можно вводить молекулы нуклеиновой кислоты в плазмиды, которые позволяют осуществить мутагенез или изменение последовательности путем рекомбинации последовательностей ДНК. Используя упомянутые выше стандартные методы, можно, например, заменять основания, удалять частичные последовательности или добавлять природные или синтетические последовательности. Для того чтобы связать фрагменты ДНК друг с другом, к фрагментам могут быть присоединены адаптеры или линкеры.
Растительные клетки, имеющие пониженную активность генного продукта, могут быть получены, например, путем экспрессирования, по меньшей мере, одной подходящей антисмысловой РНК, смысловой РНК для достижения эффекта косупрессии, или путем экспрессирования, по меньшей мере, одного соответствующим образом сконструированного рибозима, который специфически расщепляет транскрипты упомянутого выше генного продукта.
Для этой цели могут быть использованы как молекулы ДНК, которые включают всю кодирующую последовательность генного продукта, включая любые фланкирующие последовательности, которые могут присутствовать, так и молекулы ДНК, которые содержат только части кодирующей последовательности, при этом необходимо, чтобы эти части были достаточно длинными, чтобы вызывать антисмысловой эффект в клетках. Также можно использовать последовательности ДНК, которые имеют высокую степень гомологии с кодирующими последовательностями продукта гена, но не являются полностью идентичными.
При экспрессировании молекул нуклеиновых кислот в растениях, синтезированный белок может быть локализован в любом желаемом компартменте растительных клеток. Однако для достижения локализации в определенном компартменте, можно, например, связать кодирующую область с последовательностями ДНК, обеспечивающими локализацию в определенном компартменте. Такие последовательности известны специалистам в данной области. (смотрите, например, публикации Braun et al., EMBO J. 11 (1992), 3219-3227; Wolter et al., Proc. Natl. Acad. Sci. USA 85 (1988), 846-850; Sonnewald et al., Plant J. 1 (1991), 95-106).
Клетки трансгенных растений могут быть регенерированы в целых растениях с использованием известных методов. Трансгенные растения, в принципе, могут быть растениями любого требуемого вида растений, то есть как однодольными, так и двудольными растениями. Таким образом, могут быть получены трансгенные растения с измененными свойствами путем сверхэкспрессии, подавления или ингибирования гомологичных (= природных) генов или генных последовательностей или путем экспрессии гетерологичных (= чуждых) генов или генных последовательностей.
При применении активных соединений по изобретению в случае трансгенных сельскохозяйственных культур, помимо эффектов против вредных растений, которые можно наблюдать в случае других сельскохозяйственных культур, часто возникают эффекты, специфичные для применения в случае соответствующей трансгенной сельскохозяйственной культуры, например, модифицированные или специально расширенный спектр сорняков, с которыми можно проводить борьбу, измененные нормы внесения, которые могут быть использованы для внесения, предпочтительно хорошая совместимость с гербицидами, к воздействию которых трансгенные культуры являются резистентными, и влияние на рост и урожайность трансгенных сельскохозяйственных культур. Таким образом, в изобретении также предлагается применение соединений по изобретению в качестве гербицидов для борьбы с вредными растениями в случае трансгенных сельскохозяйственных культур.
Кроме того, соединения по изобретению обладают исключительными свойствами регулирования роста сельскохозяйственных культур. Они принимают участие в регуляции метаболизма у растений и могут быть использованы для целенаправленного контроля составляющих растение компонентов и облегчения процесса уборки урожая, например, путем инициирования потери влаги и сдерживания роста. Кроме того, в большинстве случаев, они также могут применяться для регулирования и подавления нежелательного вегетативного роста, не нанося при этом серьезных повреждений растениям. Подавление вегетативного роста играет важную роль для многих однодольных и двудольных сельскохозяйственных культур, поскольку таким образом можно уменьшить или полностью предотвратить серьезные повреждения растений.
Соединения по изобретению могут применяться в составе обычных препаратов в форме смачивающихся порошков, концентратов эмульсий, распыляемых растворов, дустов или гранул. Поэтому, в изобретении также предлагаются гербицидные композиции, содержащие соединения формулы I. Соединения формулы I могут быть приготовлены в форме препаратов различными методами в зависимости от преобладания тех или иных биологических и/или физико-химических параметров. Примерами подходящих вариантов препаратов являются смачивающиеся порошки (WP), водорастворимые порошки (SP), водорастворимые концентраты, концентраты эмульсий (EC), эмульсии (EW), такие как эмульсии масло-в-воде и вода-в-масле, распыляемые растворы, концентраты суспензий (SC), масляные дисперсии (OD), масляные или водные дисперсии, смешивающиеся с маслом растворы, дусты (DP), суспензии капсул (CS), композиции для протравливания семян, гранулы для разбрасывания и внесение в почву, гранулы (GR) в форме микрогранул, гранулы для распыления, гранулы с нанесенным слоем покрытия и гранулы для всасывания, диспергируемые в воде гранулы (WG), водорастворимые гранулы (SG), препараты, используемые в методе нанесения минимального объема (ULV), микрокапсулы и воски. Эти отдельные типы препаратов в принципе известны и описаны, например, в публикациях Winnacker-Küchler, "ChemischeTechnologie" [Chemical Technology], Volume 7, C. Hauser Verlag Munich, 4th. Edition 1986; Wade van Valkenburg, "Pesticide Formulations", Marcel Dekker, N.Y., 1973; K. Martens, "Spray Drying" Handbook, 3rd Ed. 1979, G. Goodwin Ltd. London.
Необходимые для приготовления препаратов вспомогательные вещества, такие как инертные материалы, поверхностно-активные вещества, растворители и другие добавки также известны и описаны, например, в публикациях Watkins, "Handbook of Insecticide Dust Diluents and Carriers", 2nd Ed., Darland Books, Caldwell N.J., H. v. Olphen, "Introduction to Clay Colloid Chemistry"; 2nd Ed., J. Wiley & Sons, N.Y.; C. Marsden, "Solvents Guide"; 2nd Ed., Interscience, N.Y. 1963; McCutcheon's "Detergents and Emulsifiers Annual", MC Publ. Corp., Ridgewood N.J.; Sisley and Wood, "Encyclopedia of Surface Active Agents", Chem. Publ. Co. Inc., N.Y. 1964; Schönfeldt, "GrenzflüchenaktiveÄthylenoxidaddkte" [Surface-active ethylene oxide adducts], Wiss. Verlagagesell. Stuttgart1976; Winnacker-Küchler, "ChemischeTechnologie" [Chemical Technology], Volume 7, C. Hauser Verlag Munich, 4th Edition 1986.
Смачивающиеся порошки представляют собой препараты, которые равномерно диспергируются в воде и которые, помимо активного соединения, а также разбавителя или инертного вещества, содержат поверхностно-активные вещества ионогенного и/или неионогенного типа (смачивающие вещества, диспергаторы), например, полиэтоксилированные алкилфенолы, полиэтоксилированные жирные спирты, полиэтоксилированные жирные амины, сульфаты полигликолевых эфиров жирных спиртов, алкансульфонаты, алкилбензолсульфонаты, лигнинсульфонат натрия, 2,2'-динафтилметан-6,6'-дисульфонат натрия, дибутилнафталинсульфонат натрия или еще олеоилметилтауринат натрия. Для приготовления смачивающихся порошков, гербицидно активные соединения тонко измельчают, например, в обычных устройствах, таких как молотковые мельницы, вентиляторные мельницы и воздушно-струйные мельницы, и смешивают одновременно или последовательно со вспомогательными веществами препарата.
Концентраты эмульсий приготавливают путем растворения активного соединения в органическом растворителе, например, бутаноле, циклогексаноне, диметилформамиде, ксилоле или же в относительно высококипящих ароматических соединениях или углеводородах или смесях растворителей, с добавлением одного или более поверхностно-активных веществ ионогенного и/или неионогенного типа (эмульгаторов). Примерами эмульгаторов, которые могут быть использованы, являются алкиларилсульфонаты кальция, такие как додецилбензолсульфонат кальция, или неионогенные эмульгаторы, такие как полигликолевые эфиры жирных кислот, алкиларилполигликолевые эфиры, полигликолевые эфиры жирных спиртов, продукты конденсации оксида пропилена с оксидом этилена, алкиловые полиэфиры, эфиры сорбитана, например, эфиры сорбитана и жирных кислот или эфиры полиоксиэтиленсорбитана, например, эфиры полиоксиэтиленсорбитана и жирных кислот.
Дусты приготавливают путем измельчения активного соединения с тонкоизмельченными твердыми веществами, например, тальком, природными глинами, такими как каолин, бентонит и пирофиллит, или диатомитом. Концентраты суспензий могут быть на водной основе или на масляной основе. Они могут быть приготовлены, например, путем мокрого помола с использованием обычных промышленных бисерных мельниц при добавлении или без добавления упомянутых выше поверхностно-активных веществ, например, в случае приготовления препаратов других типов.
Эмульсии, например, эмульсии масло-в-воде (EW), могут быть приготовлены, например, с помощью мешалок, коллоидных мельниц и/или статических смесителей, используя водно-органические растворители и, при необходимости, упомянутые выше поверхностно-активные вещества, например, в случае приготовления препаратов других типов.
Гранулы могут быть приготовлены либо путем распыления активного соединения на адсорбирующий гранулированный инертный материал, либо путем нанесения концентратов активного соединения на поверхность носителей, таких как песок, каолиниты или гранулированный инертный материал, с помощью адгезивных связующих, например, поливинилового спирта, полиакрилата натрия или же минеральные масла. Соответствующие активные вещества могут быть также гранулированы методом, с помощью которого обычно гранулируют удобрения, при необходимости, в виде смеси с удобрениями. Диспергируемые в воде гранулы обычно приготавливают обычными методами, такими как распылительная сушка, грануляция в псевдоожиженном слое, тарельчатая грануляция, смешивание с использованием высокоскоростных смесителей и экструзия без использования твердого инертного материала.
По поводу приготовления гранул методами тарельчатой грануляции, грануляции в псевдоожиженном слое, экструзии и распылительной сушки, смотрите, например, процессы, описанные в публикациях "Spray-Drying Handbook" 3rd ed. 1979, G. Goodwin Ltd., London; J. E. Browning, "Agglomeration", Chemical and Engineering 1967, pages 147 ff.; "Perry's Chemical Engineer's Handbook", 5th Ed., McGraw-Hill, New York 1973, pp. 8-57. Более подробную информацию по поводу приготовления продуктов для защиты сельскохозяйственных культур можно найти, например, в публикациях G. C. Klingman, "Weed Control as a Science", John Wiley and Sons Inc., New York, 1961, pages 81-96 и J. D. Freyer, S. A. Evans, "Weed Control Handbook", 5th Ed., Blackwell Scientific Publications, Oxford, 1968, pages 101-103.
Агрохимические препараты обычно содержат от 0,1 до 99% по массе, в частности, от 0,1 до 95% по массе, активного соединения формулы I. В смачивающихся порошках, концентрация активного соединения составляет, например, от приблизительно 10 до 99% по массе, недостающее до 100% по массе количество состоит из обычных компонентов препарата. В концентратах эмульсии, концентрация активного соединения может составлять приблизительно от 1 до 90%, предпочтительно, приблизительно от 5 до 80% по массе. Препараты в виде дустов содержат от 1 до 30% по массе активного соединения, предпочтительно, от 5 до 20% по массе активного соединения, в то время как растворы для распыления содержат приблизительно от 0,05 до 80%, предпочтительно, от 2 до 50%, по массе активного соединения. В случае диспергируемых в воде гранул, содержание активного соединения частично зависит от того, находится ли активное соединение в жидкой или твердой форме, а также от используемых при гранулировании вспомогательных веществ, наполнителей и других подобных вспомогательных веществ. В диспергируемых в воде гранулах, содержание активного соединения составляет, например, от 1 до 95% по массе, предпочтительно, от 10 до 80% по массе.
Кроме того, препараты активного соединения могут включать вещества для повышения клейкости, смачивающие вещества, диспергирующие вещества, эмульгаторы, пенетранты, консерванты, антифризы, растворители, наполнители, носители, окрашивающие вещества, противовспенивающие вещества, замедлители испарения и регуляторы pH и вязкости, которые в каждом случае являются общепринятыми.
На основе этих препаратов могут быть также приготовлены комбинации с другими пестицидно активными веществами, например инсектицидами, акарицидами, гербицидами и фунгицидами, а также с антидотами, удобрениями и/или регуляторами роста, например, в форме готовой смеси или баковой смеси.
Подходящие активные соединения, которые могут быть объединены с активными соединениями по изобретению в смешанных препаратах или, например, в баковой смеси, представляют собой активные соединения, описанные, например, в руководстве World Herbicide New Product Technology Handbook, China Agricultural Science and Farming Techniques Press, 2010.9 и в цитируемых в изобретении публикациях. Например, следующие активные соединения могут быть упомянуты в качестве гербицидов, которые могут быть объединены с соединениями формулы I (примечание: соединения либо названы с использованием их "тривиального названия" в соответствии с рекомендациями Международной организация по стандартизации (ISO), или с использованием их химических названий, в соответствующем случаев, вместе с их стандартным кодовым номером): ацетохлор, бутахлор, алахлор, пропизохлор, метолахлор, s-метолахлор, претилахлор, пропахлор, этахлор, напропамид, R-левовращающий изомер напропамида, пропанил, мефенацет, дифенамид, дифлуфеникан, этапрохлор, бефлубутамид, бромбутид, диметенамид, диметенамид-Р, этобензанид, флуфенацет, тенилхлорид, метазахлор, изоксабен, флампроп-М-метил, флампроп-М-пропил, аллидохлор, петоксамид, хлоранокрил, ципразин, мефлуидид, моналид, делахлор, принахлор, тербухлор, ксилахлор, диметахлор, цисанилид, тримексахлор, кломепроп, пропизамид, пентанохлор, карбетамид, бензоилпроп-этил, ципразол, бутенахлор, тебутам, бензипрам, 1379, дихлофлуанид, напроанилид, диэтатил-этил, напталам, флуфенацет, бензадокс, хлортиамид, хлорфталимид, изокарбамид, пиколинафен, атразин, симазин, прометрин, цианатрин, аметрин, пропазин, дипропетрин, SSH-108, тербутрин, тербутилазин, триазифлам, ципразин, проглиназин, триэтазин, прометон, симетон, азитротрин, деметрин, диметаметрин, проциазин, мезопразин, себутилазин, секбуметон, тербуметон, метопротрин, цианатрин, ипазин, хлоразин, атратон, пендиметалин, эглиназин, циануровая кислота, индазифлам, хлорсульфурон, метсульфурон-метил, бенсульфурон метил, хлоримурон-этил, трибенурон-метил, тифенсульфурон-метил, пиразосульфурон-этил, мезосульфурон, иодсульфурон-метил натрий, форамсульфурон, циносульфурон, триасульфурон, сульфометурон метил, никосульфурон, этаметилсульфон-метил, амидосульфурон, этоксисульфурон, циклосульфамурон, римсфурон, азимсульфурон, флазасульфурон, моносульфурон, моносульфурон-эфир, флукарбазон-натрий, флупирсульфурон-метил, галосульфурон-метил, оксасульфурон, имазосульфурон, примисульфурон, пропоксикарбазон, просульфурон, сульфосульфурон, трифлоксисульфурон, трифлусульфурон-метил, тритосульфурон, натрия метсульфурон метил, флуцетосульфурон, HNPC-C, ортосульфамурон, пропирисульфурон, метазосульфурон, ацифлуорфен, фомезафен, лактофен, фторгликофен, оксифлуорфен, хлорнитрофен, аклонифен, этоксифен-этил, бифенокс, нитрофлуорфен, хлометоксифен, фтордифен, фторнитрофен, фурилоксифен, нитрофен, TOPE, DMNP, PPG1013, AKH-7088, галосафен, хлортолурон, изопротурон, линурон, диурон, димрон, флуометурон, бензтиазурон, метабензтиазурон, кумилурон, этидимурон, изоурон, тебутиурон, бутурон, хлорбромурон, метилдимрон, фенобензурон, SK-85, метобромурон, метоксурон, афесин, монурон, сидурон, фенурон, флуотиурон, неберон, хлороксурон, норурон, изонорурон, 3-циклооктил-1, тиазфлурон, тебутиурон, дифеноксурон, парафлурон, метиламин трибунил, карбутилат, триметурон, димефурон, моносоурон, анизурон, метиурон, хлоретурон, тетрафлурон, фенмедифем, фенмедифам-этил, десмедифам, асулам, тербукарб, барбан, профам, хлорпрофам, роумат, свеп, хлорбуфам, карбоксазол, хлорпрокарб, фенасулам, BCPC, CPPC, карбасулам, бутилат, бентиокарб, вернолат, молинат, триаллат, димепиперат, эспрокарб, пирибутикарб, циклоат, авадекс, ЕРТС, этиолат, орбенкарб, пебулат, просульфокарб, тиокарбазил, CDEC, димексано, изополинат, метиобенбенкаром, 2,4-D бутиловый эфир, MCPA-Na, 2,4-D изооктиловый эфир, MCPA изооктиловый эфир, 2,4-D натриевая соль, 2,4-диметиламиновая соль, MCPA-тиоэтил, MCPA, 2,4-D-пропионовая кислота, соль 2,4-D пропионовой кислоты, 2,4-D масляная кислота, MCPA пропионовая кислота, соль MCPA пропионовой кислоты, MCPA масляная кислота, 2,4,5-D, 2,4,5-D пропионовая кислота, 2,4,5-D масляная кислота, соль MCPA амина, дикамба, эрбон, хлорфенак, сайсон, TBA, хлорамбен, метокси-TBA, диклофоп-метил, флуазифоп-бутил, флуазифоп-п-бутил, галооксифоп-метил, галоксифоп-Р, хизалофоп-этил, хизалофоп-п-этил, феноксапроп-этил, феноксапроп-п-этил, пропакизафоп, цигалофоп-бутил, метамифоп, клодинафоп-пропаргил, фентиапроп-этил, хлоразифоп-пропинил, поппенат-метил, трифопсим, изоксапирифоп, паракват, дикват, оризалин, эталфлуралин, изопропалин, нитралин, профлуралин, продинамин, бенфлуралин, флухлоралин, динитрамин, дипропалин, хлорнидин, металпропалин, динопроп, глифосат, анилофос, глуфозинат аммоний, амифофос-метил, сульфосат, пиперофос, биалафос-натрий, бенсулид, бутамифос, прокарб, 2,4-DEP, H-9201, зитрон, имизапир, имазетапир, имазхаин, имазамокс, имазамокс аммониевая соль, имазапик, имазаметабенз-метил, флуроксипир, флуроксипир изооктиловый эфир, клопиралид, пиклорам, трихлопир, дитиопир, галоксидин, 3,5,6-трихлор-2-пиридинол, тиазопир, флуридон, аминопиралид, дифлуфензопир, триклопир-бутотил, клиодинат, сетоксидим, клетодим, циклоксидим, аллоксидим, клефоксидим, бутроксидим, тралкоксидим, тепралоксидим, бутидазол, метрибузин, гексазинон, метамитрон, этиозин, аметридион, амибузин, бромоксинил, бромоксинил октаноат, иоксинил оксоаноат, иоксинил, дихлобенил, дифенатрил, пираклонил, хлороксинил, иодобонил, флуметсулам, флорасулам, пеноксулам, метосулам, клорансулам-метил, диклозулам, пироксулам, бенфурезат, биспирибак-натрий, пирибензоксим, пирифталид, пириминобак-метил, пиритиобак-натрий, бензобицилон, мезотрион, сулькотрион, темботрион, тефурилтрион, бициклопирон, кетодпирадокс, изоксафлутол, кломазон, феноксасульфон, метиозолин, флуазолат, пирафлуфен-этил, пиразолинат, дифензокват, пиразоксифен, бензофенап, нипираклофен, пирасульфотол, топрамезон, пироксасульфон, кафенстрол, флупоксам, аминотриазол, амикарбазон, азафенидин, карфентразон- этил, сульфентразон, бенкарбазон, бензфендизон, бутафенацил, бромацил, изоцил, ленацил, тербацил, флупропацил, цинидон-этил, флумиклорак-пентил, флумиоксазин, пропизамид, МК-129, флумезин, пентахлорфенол, диносеб, динотерб, динотерб ацетат, диносам, DNOC, хлорнитрофен, мединотерб ацетат, динофенат, оксадиаргил, оксадиазон, пентоксазон, флуфенацет, флутиацет-метил, фентразамид, флуфенпир-этил, пиразон, бромпиразон, метфлуразон, кусакира, димидазон, оксапиразон, норфлуразон, пиридафол, хинхлорак, хинмерак, бентазон, пиридат, оксазикломефон, беназолин, кломазон, цинметилин, ZJ0702, пирибамбенз-пропил, инданофан, хлорат натрия, далапон, трихлоруксусная кислота, монохлоруксусная кислота, гексахлорацетон, флупропанат, циперкват, бромфеноксим, эпроназ, метазол, флуртамон, бенфурасат, этофумесат, тиоклорим, хлортал, фторхлоридон, таврон, акролеин, бентранил, тридифан, хлорфенпропметил, тидиаризонамин, фенисофам, бусоксинон, метоксифенон, сафлуфенацил, клацифос, хлоропон, алорак, диэтамкват, этнипромид, ипримидам, ипфенкарбазон, тиенкарбазон-метил, пиримисульфан, хлорфлуразол, трипропиндан, сулгликапин, просульфалин, камбендихлор, аминоциклопирахлор, родетанил, беноксакор, фенклолим, флуразол, фенхлоразол-этил, клохинтоцет-мексил, оксабретринил, MG/91, циометринил, DKA-24, мефенпир-диэтил, фурилазол, флюксофеним, изоксадифен-этил, дихлормид, галоксифен-метил, DOW848, UBH-509, D489, LS 82-556, KPP-300, NC-324, NC-330, KH-218, DPX-N8189, SC-0744, DOWCO535, DK-8910, V-53482, PP-600, MBH-001, KIH-9201, ET-751, KIH-6127 и KIH-2023.
Для применения, препараты, которые находятся в производимой промышленностью и доступной на рынке форме, в соответствующих случаях разбавляют обычным методом, например, с использованием воды в случае смачивающихся порошков, концентратов эмульсий, дисперсий и диспергируемых в воде гранул. Продукты в форме дустов, гранул для внесения в почву или разбрасывания на почву и распыляемых растворов обычно не разбавляют другими инертными веществами перед применением. Норма внесения соединений формулы I зависит от внешних условий, таких как температура, влажность, природа используемого гербицида и других подобных факторов. Она может изменяться в широких пределах, например, от 0,001 до 1,0 кг/га или более активного вещества, но предпочтительно составляет от 0,005 до 750 г/га, в частности, от 0,005 до 250 г/га.
Конкретный вариант осуществления изобретения
Далее представлены варианты осуществления с целью подробной иллюстрации настоящего изобретения, но их никоим образом не следует воспринимать в качестве какого-либо ограничения для настоящего изобретения. Объем изобретения будет определен в пунктах формулы изобретения.
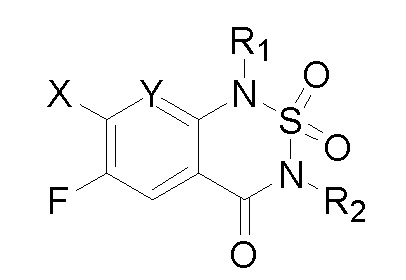
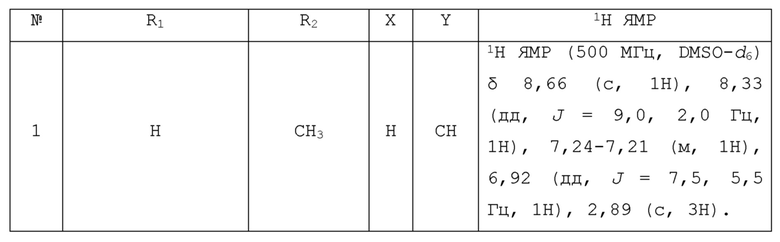
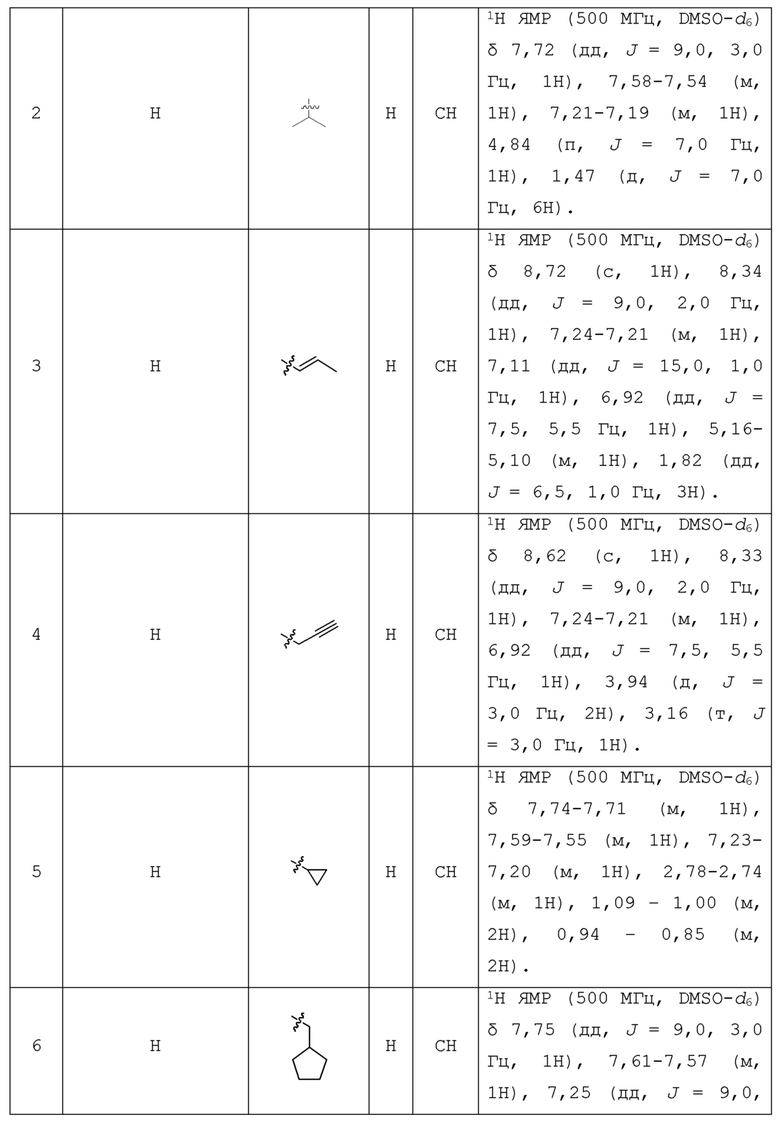
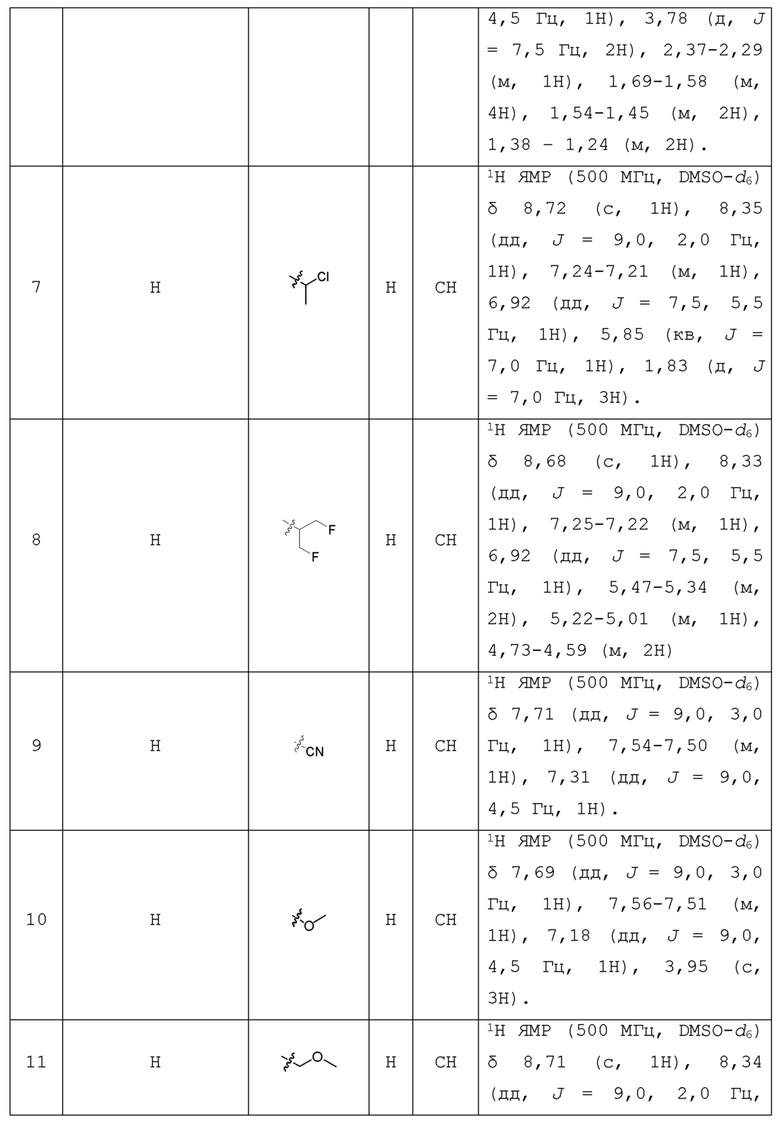
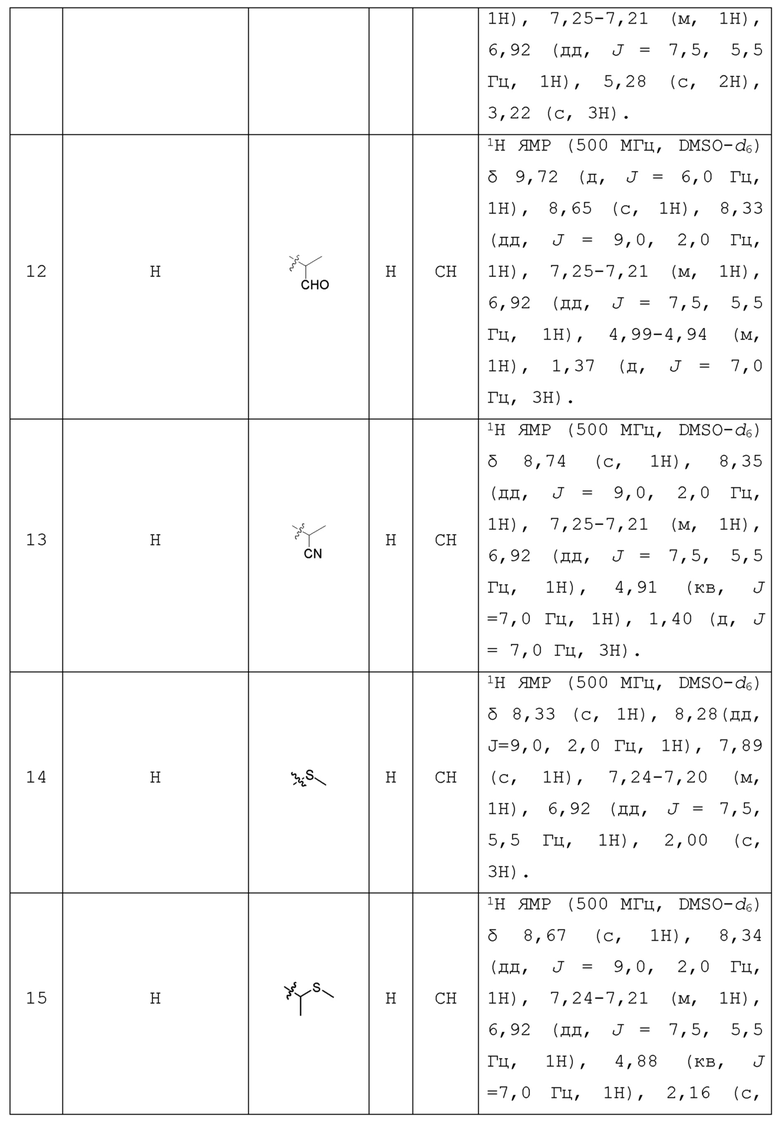
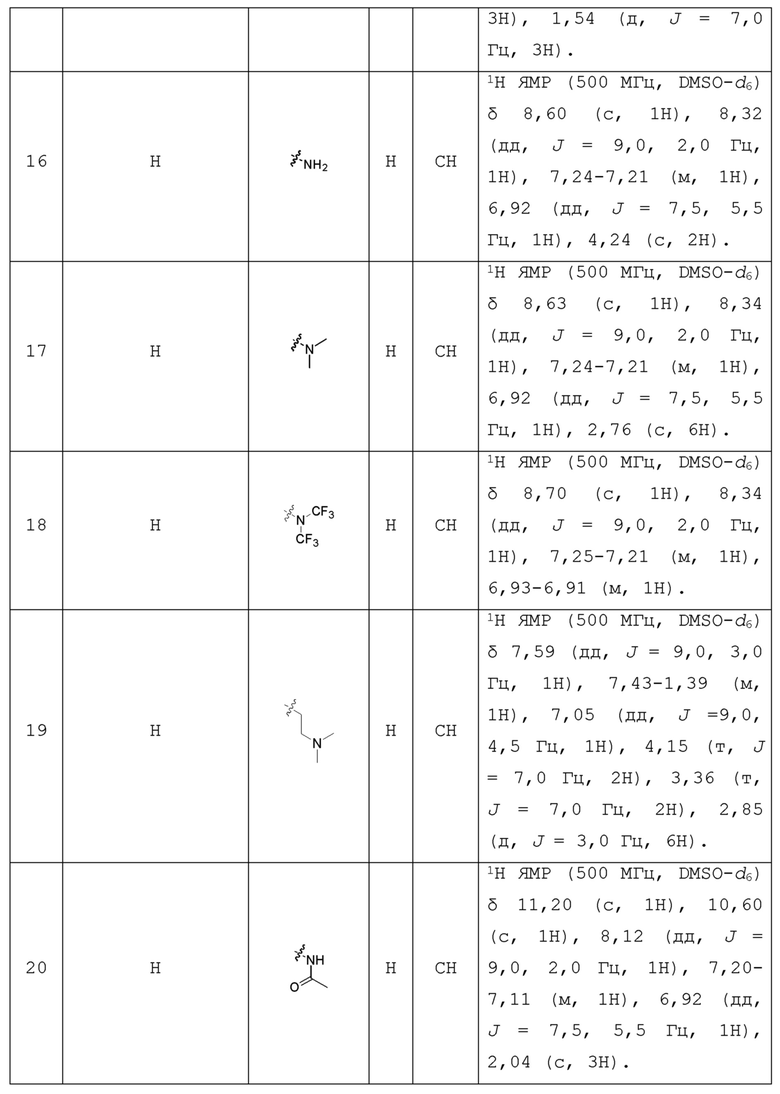
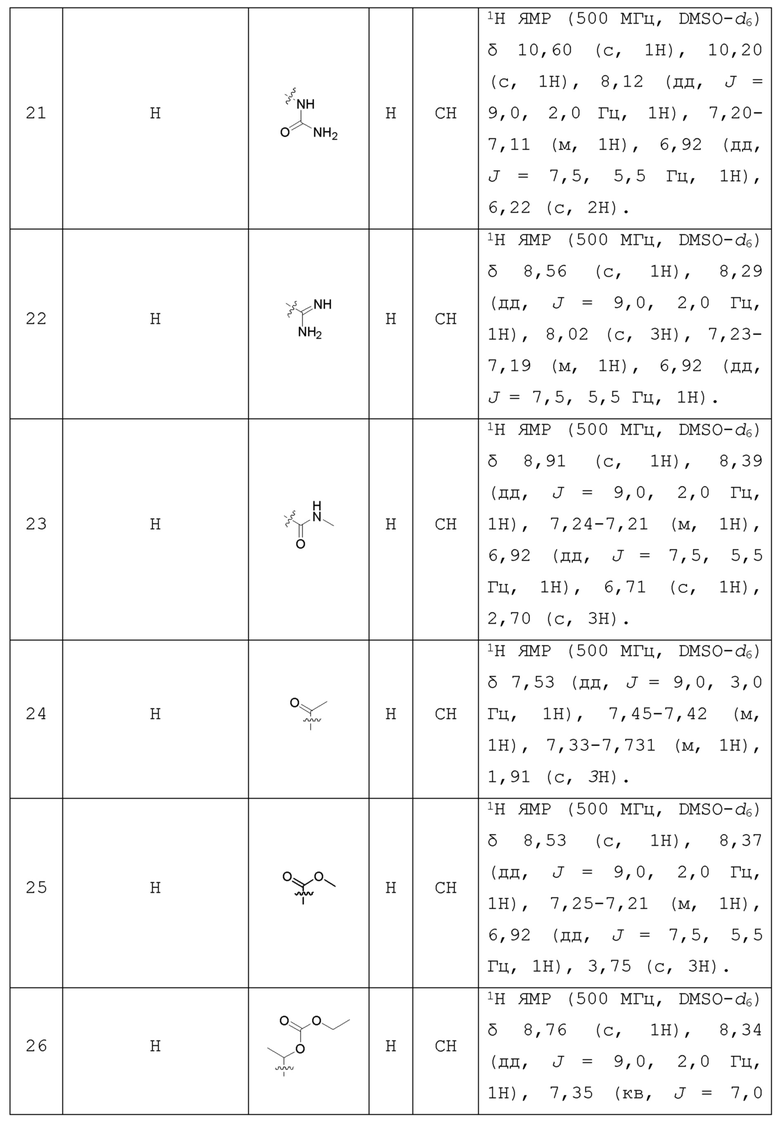
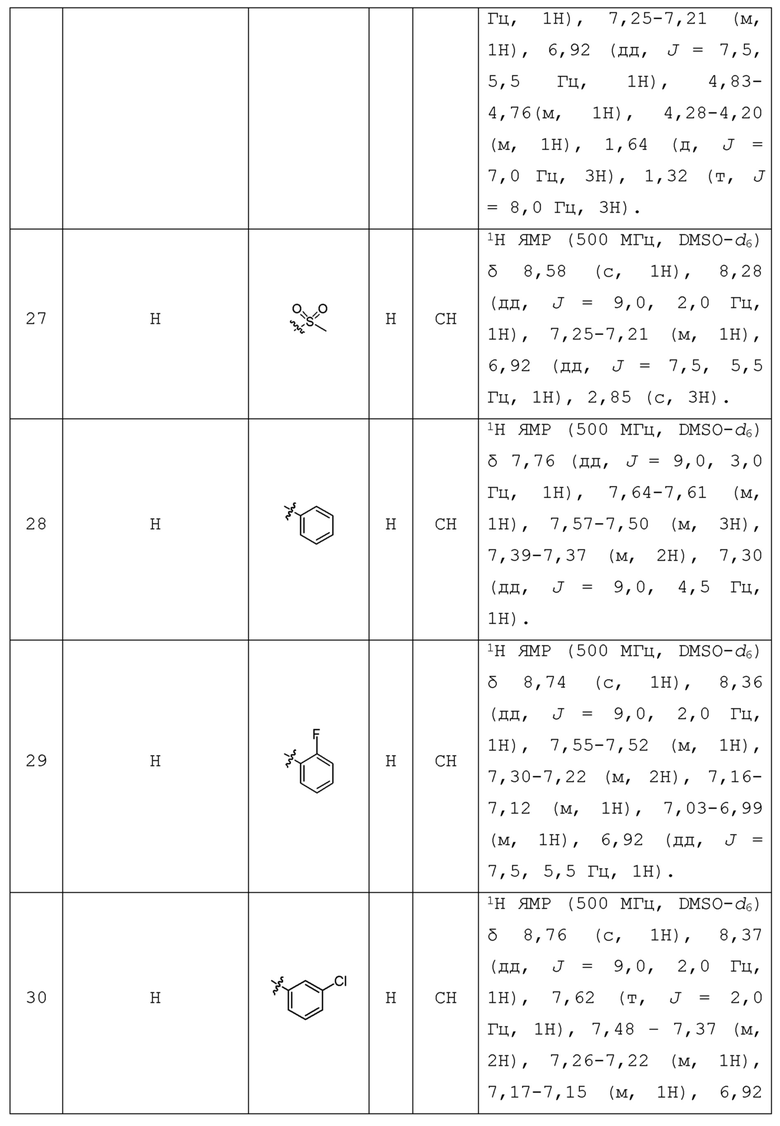
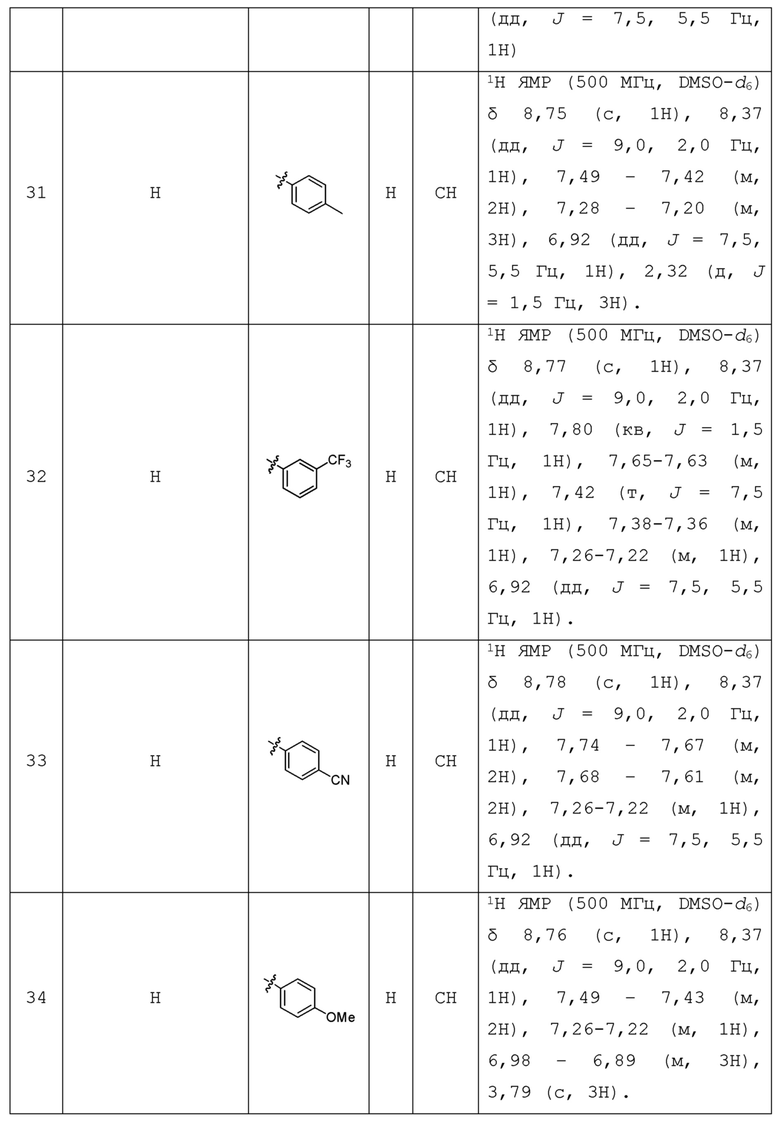
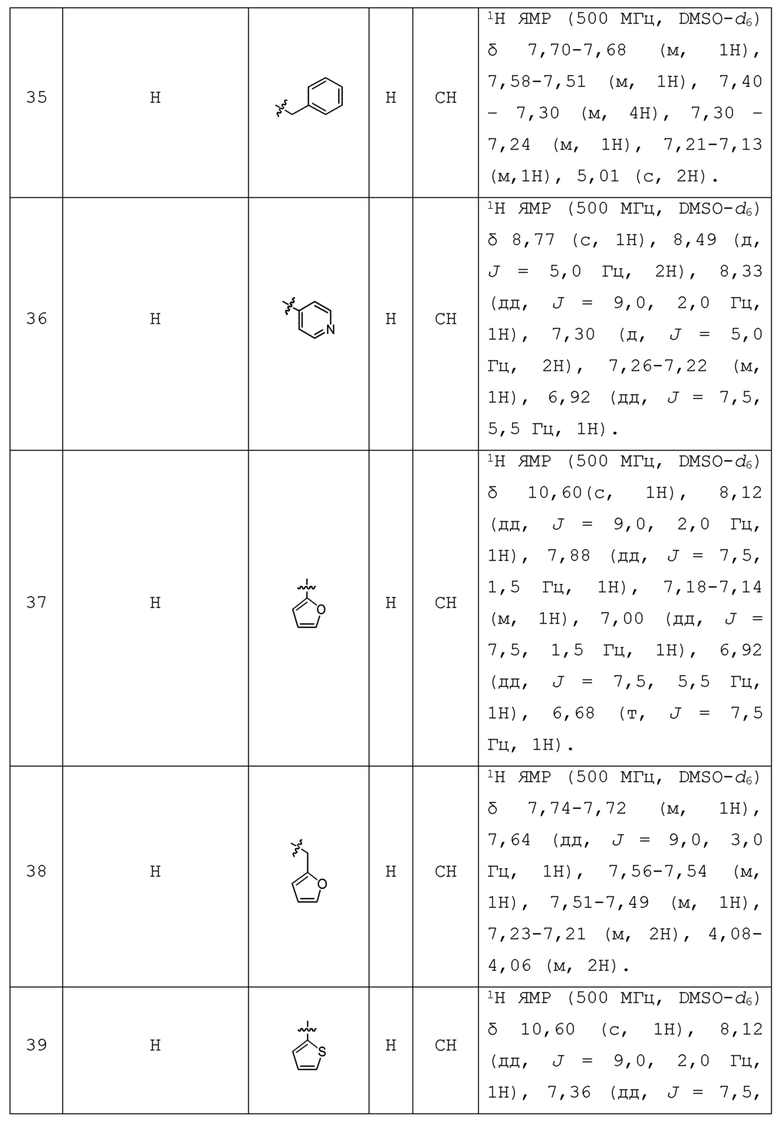
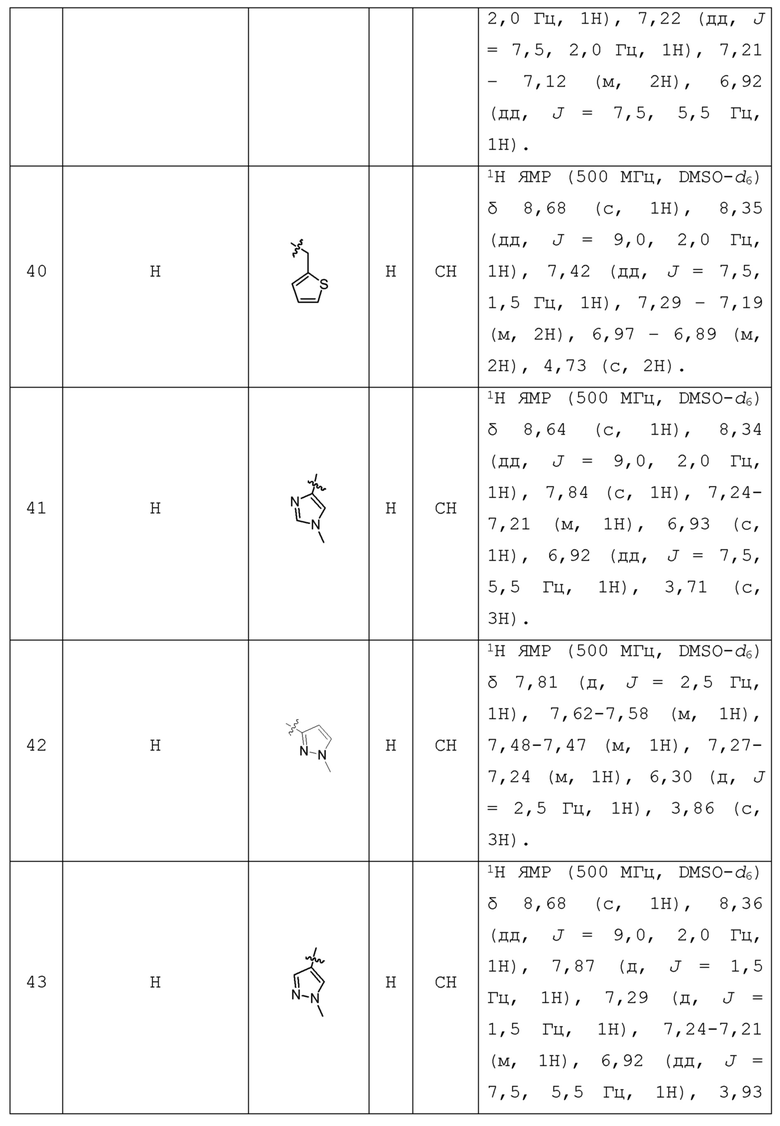
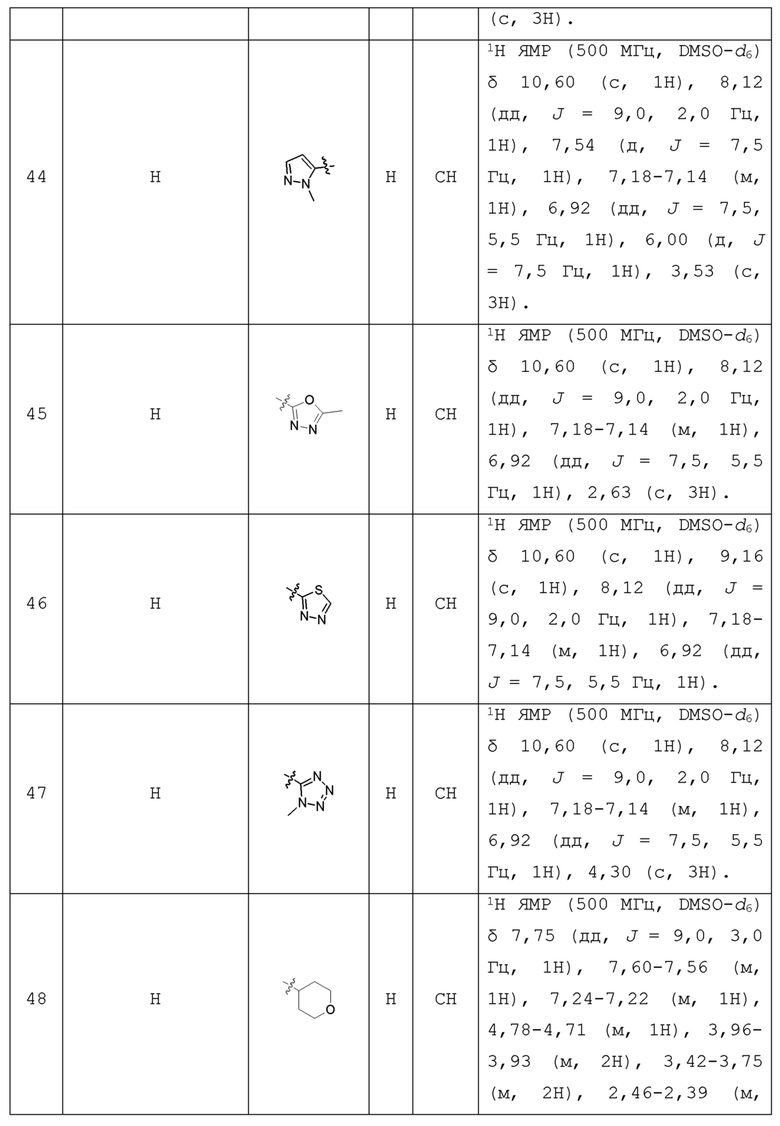
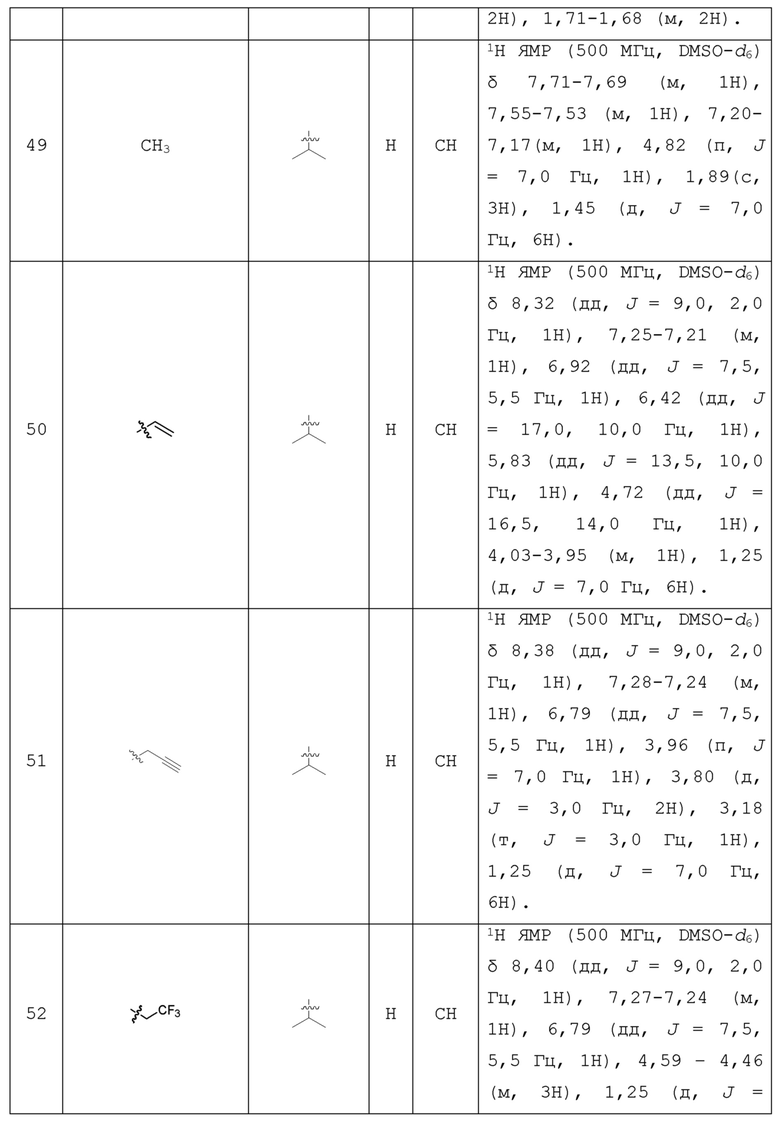
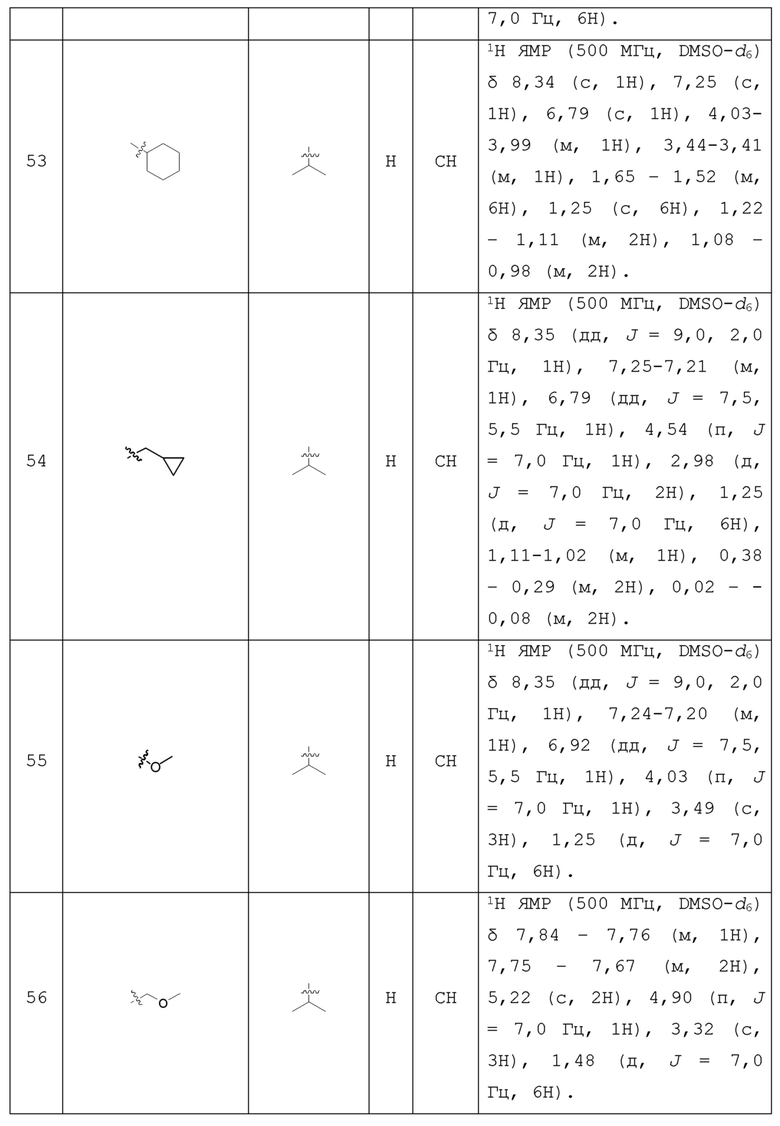
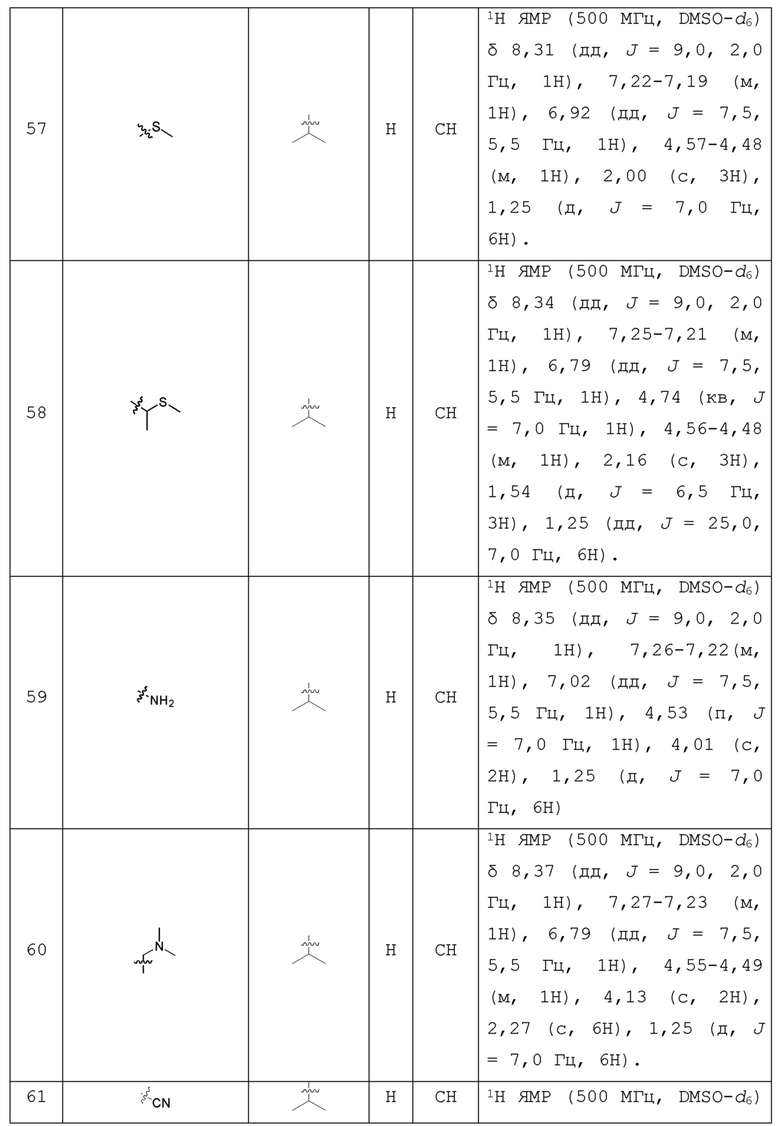
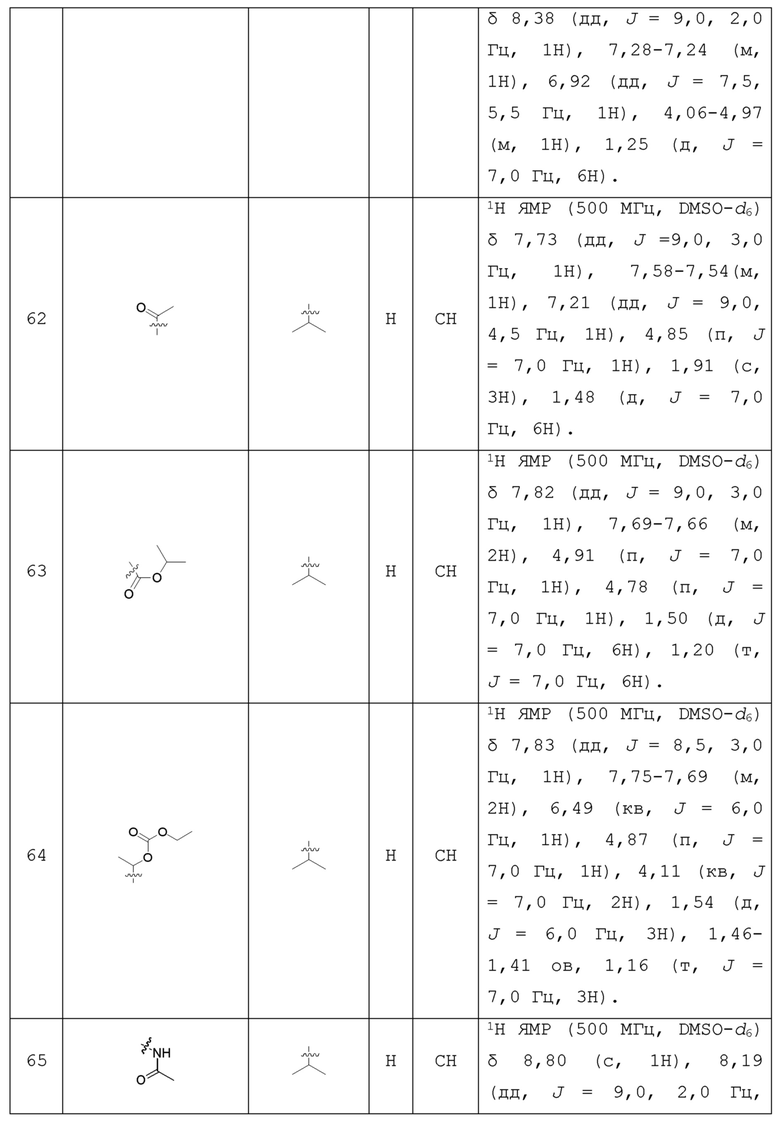
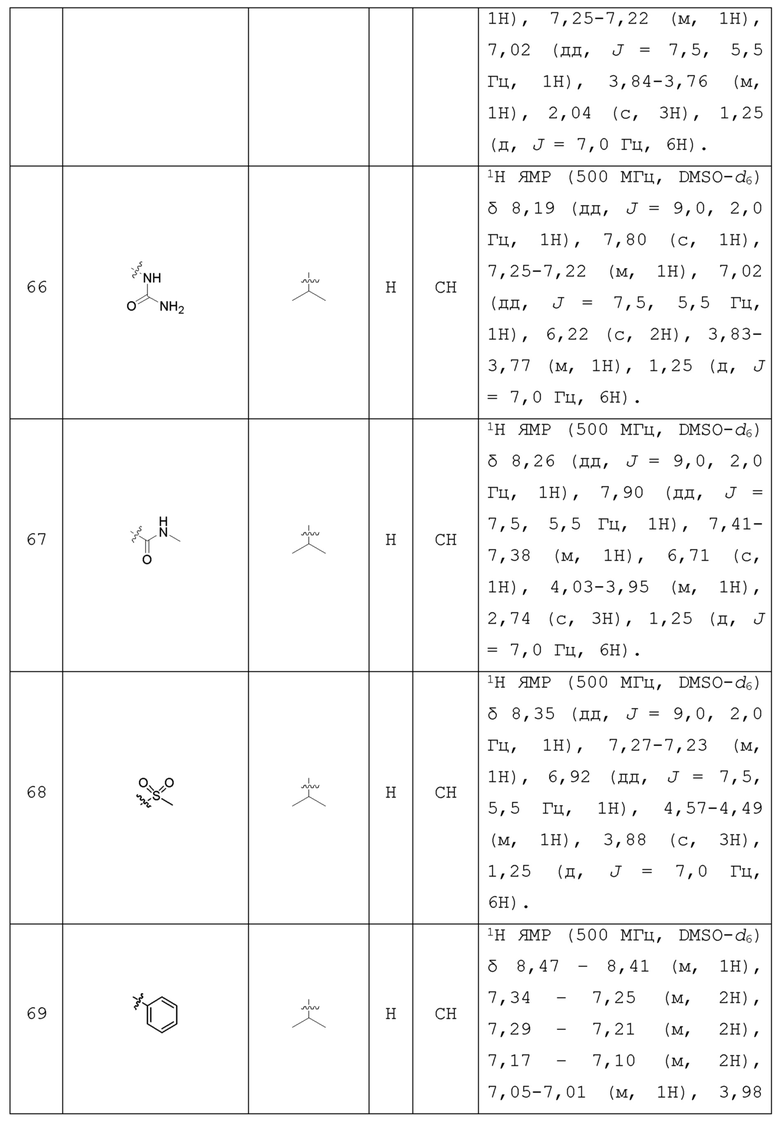
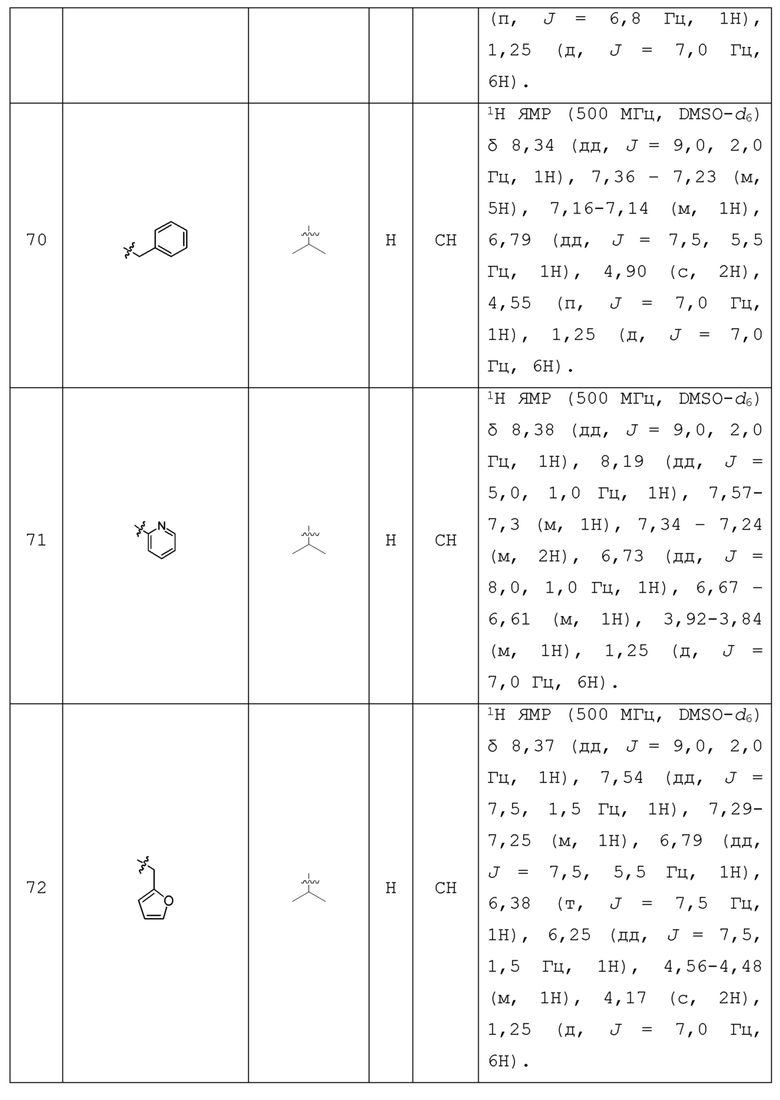
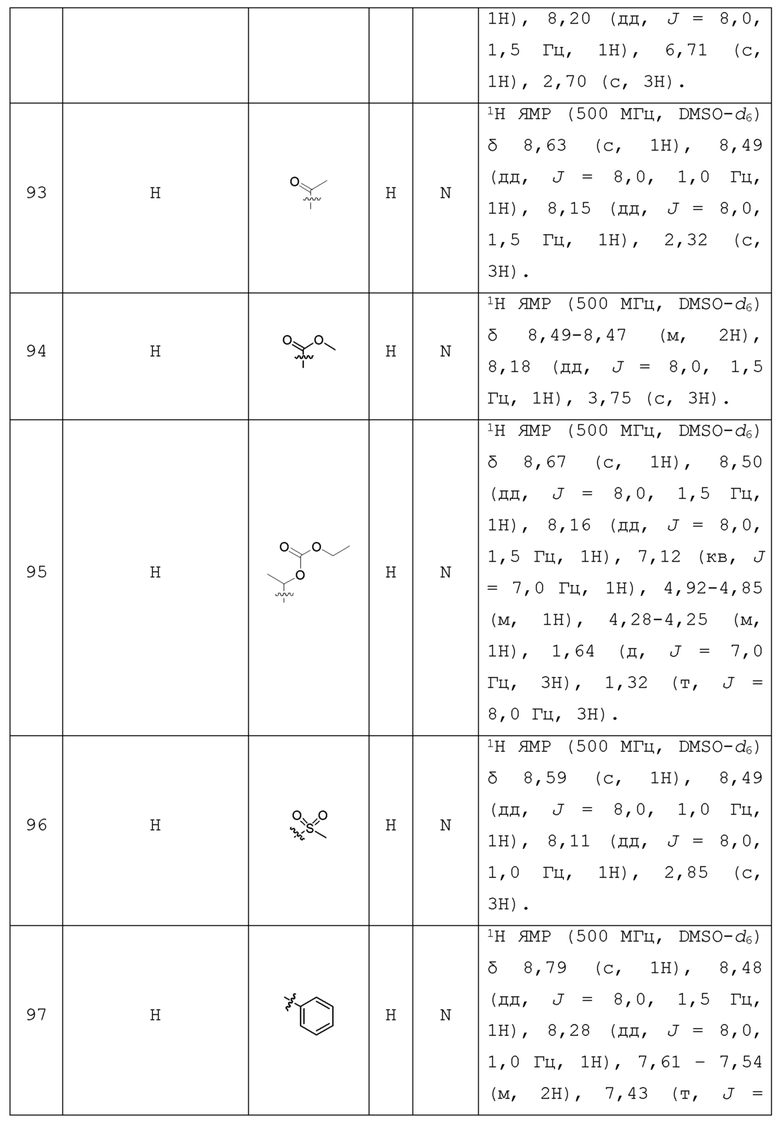
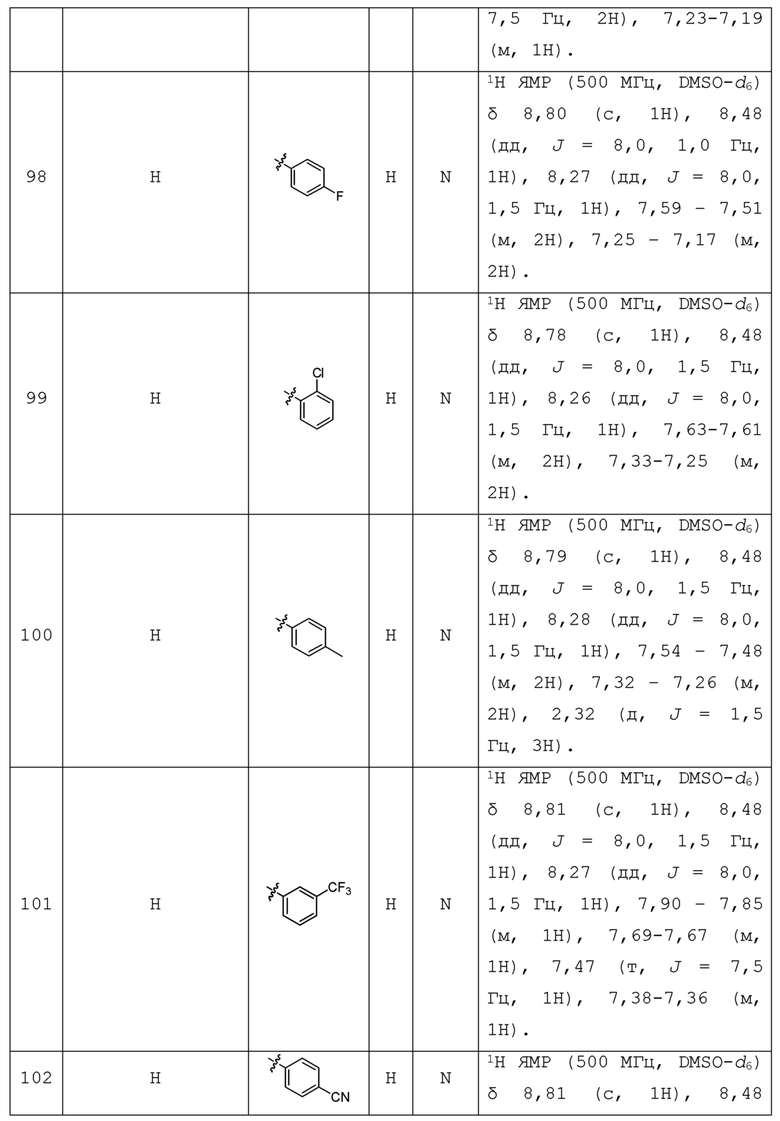
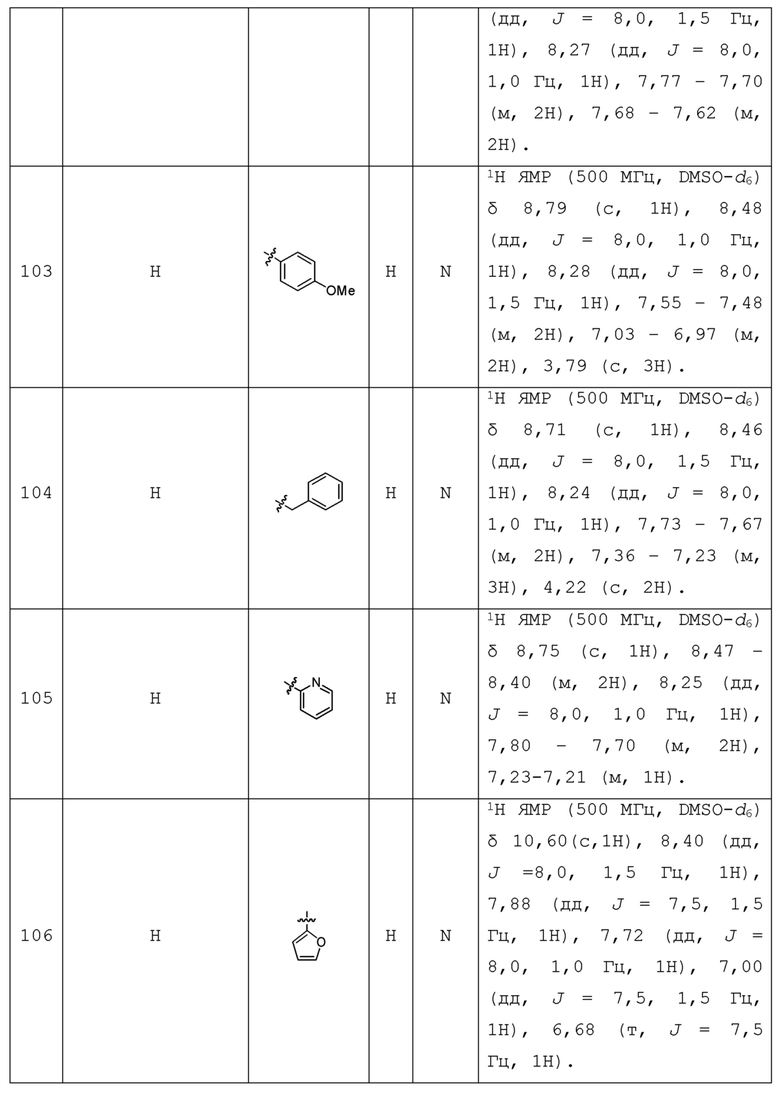
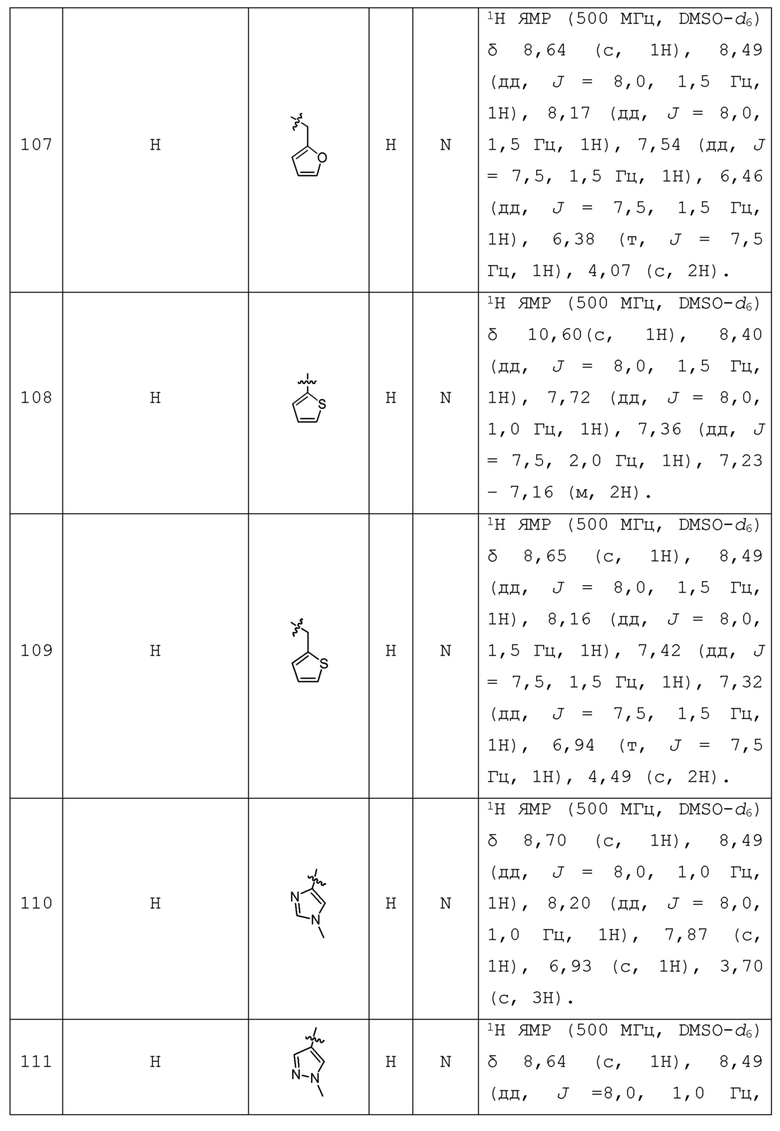
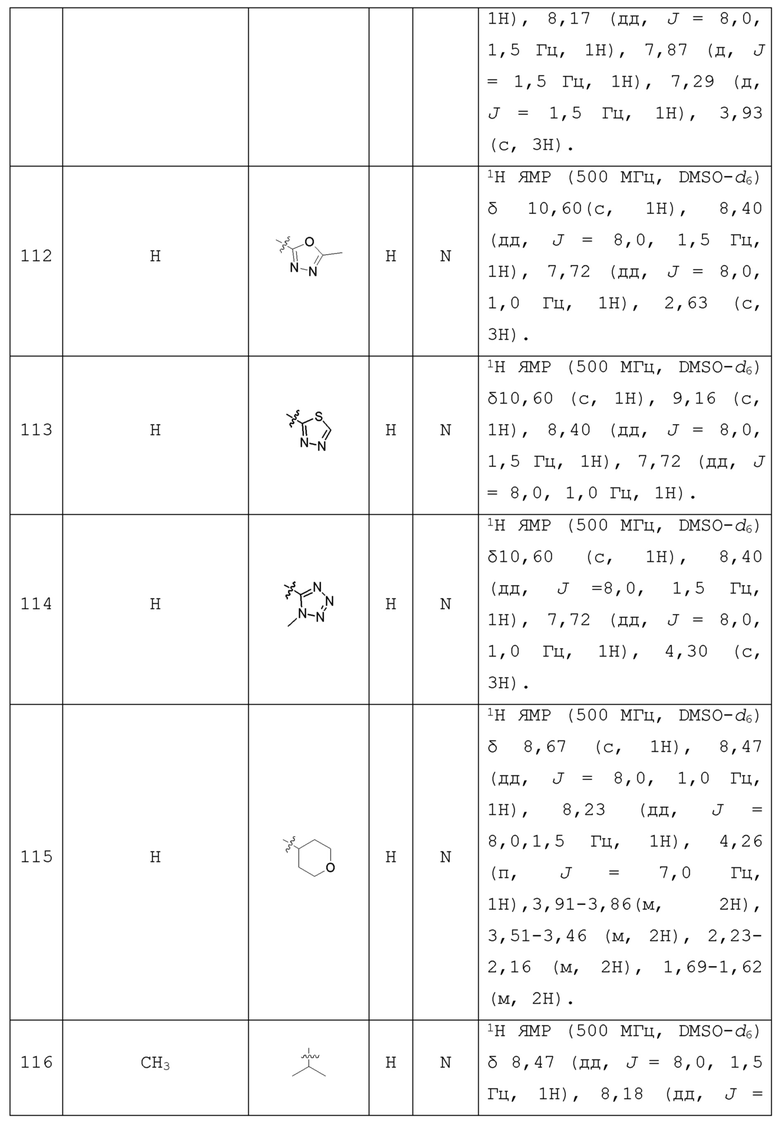
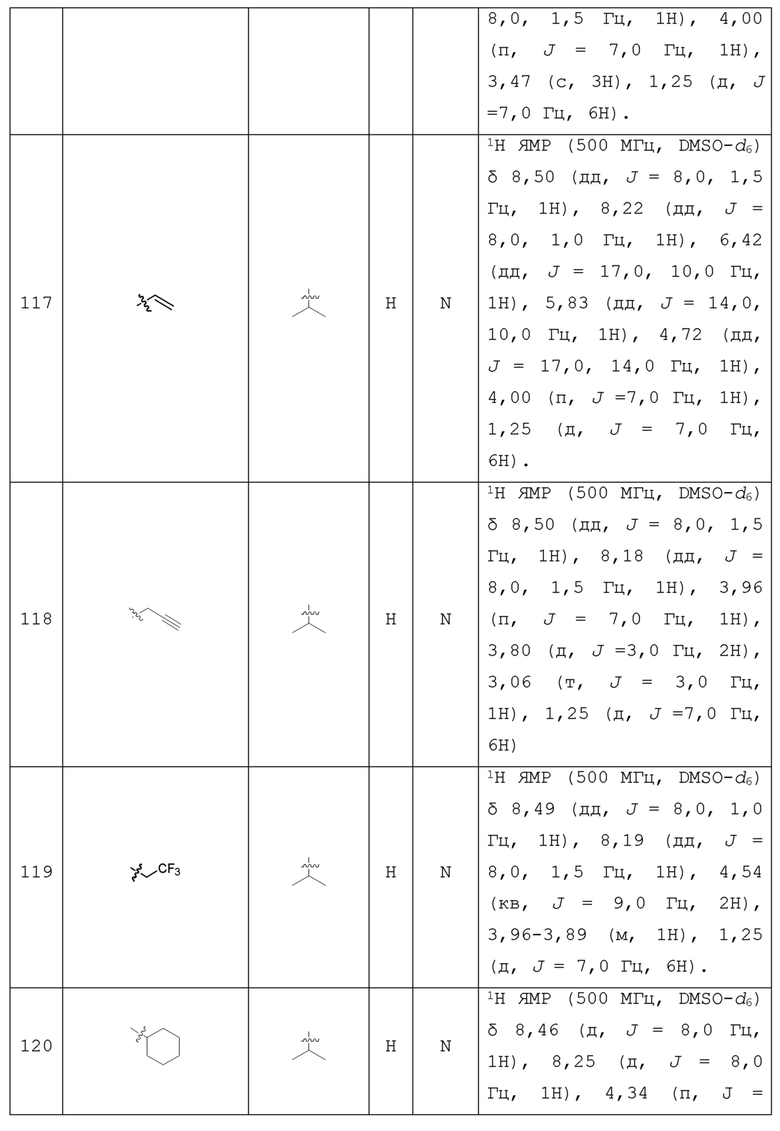
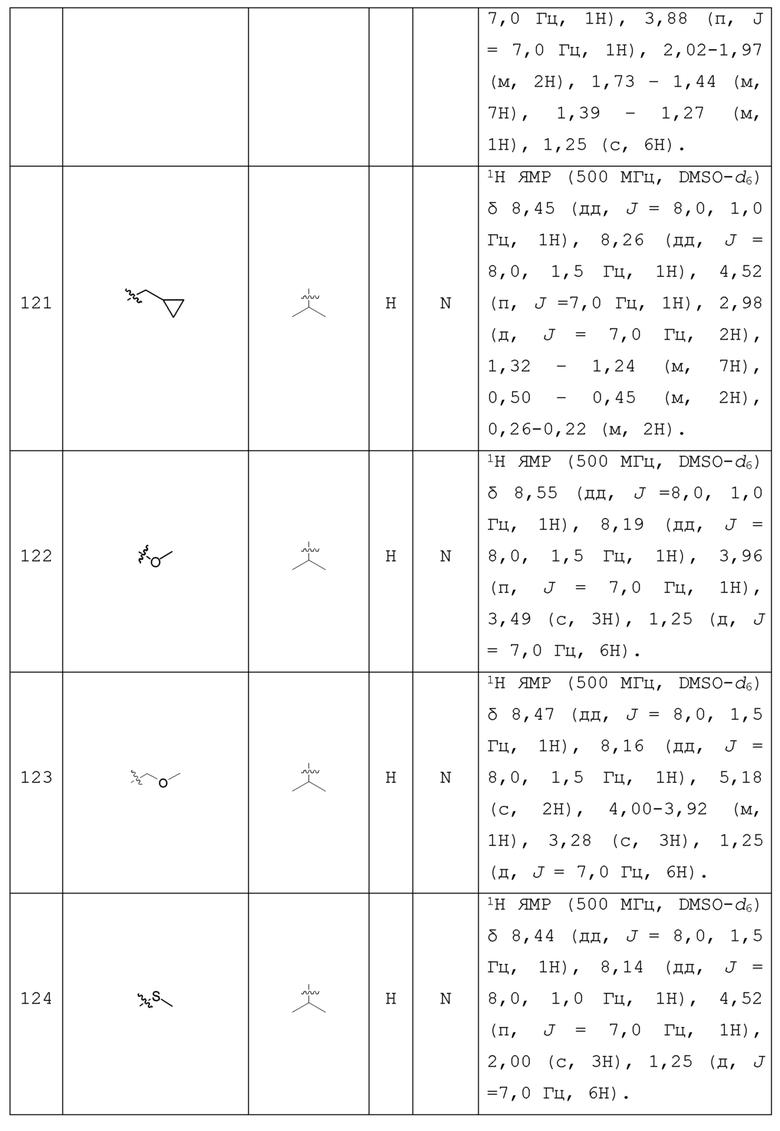
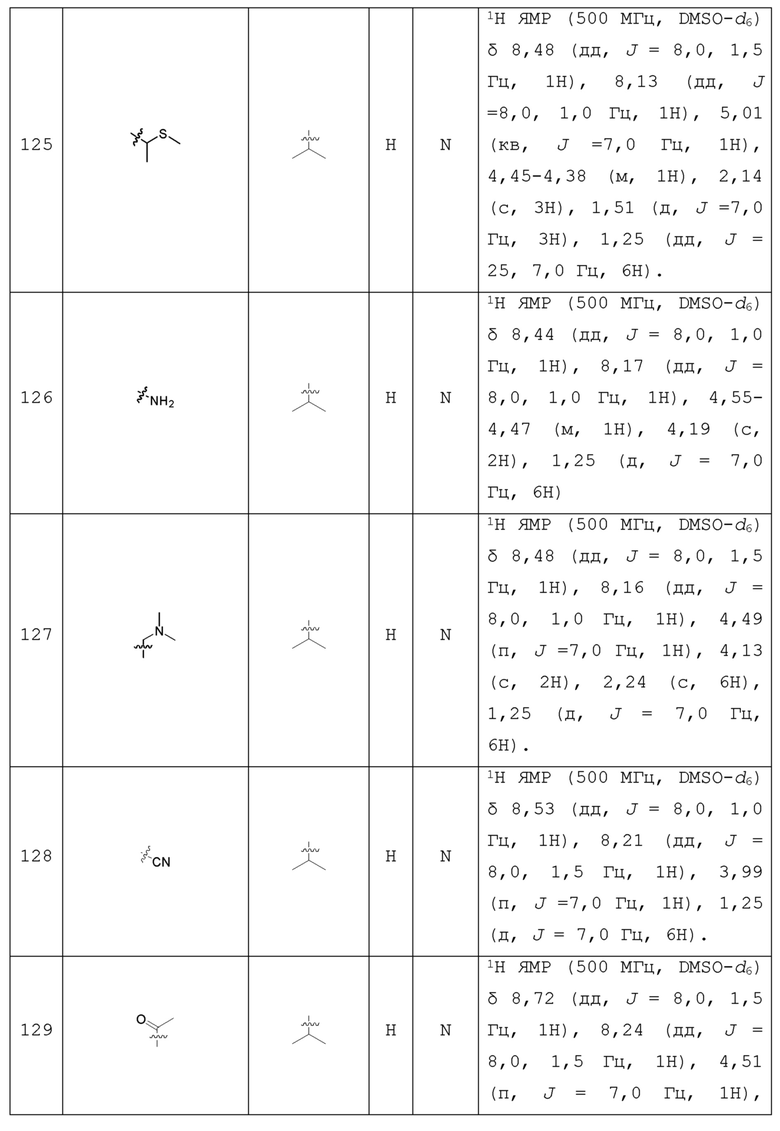
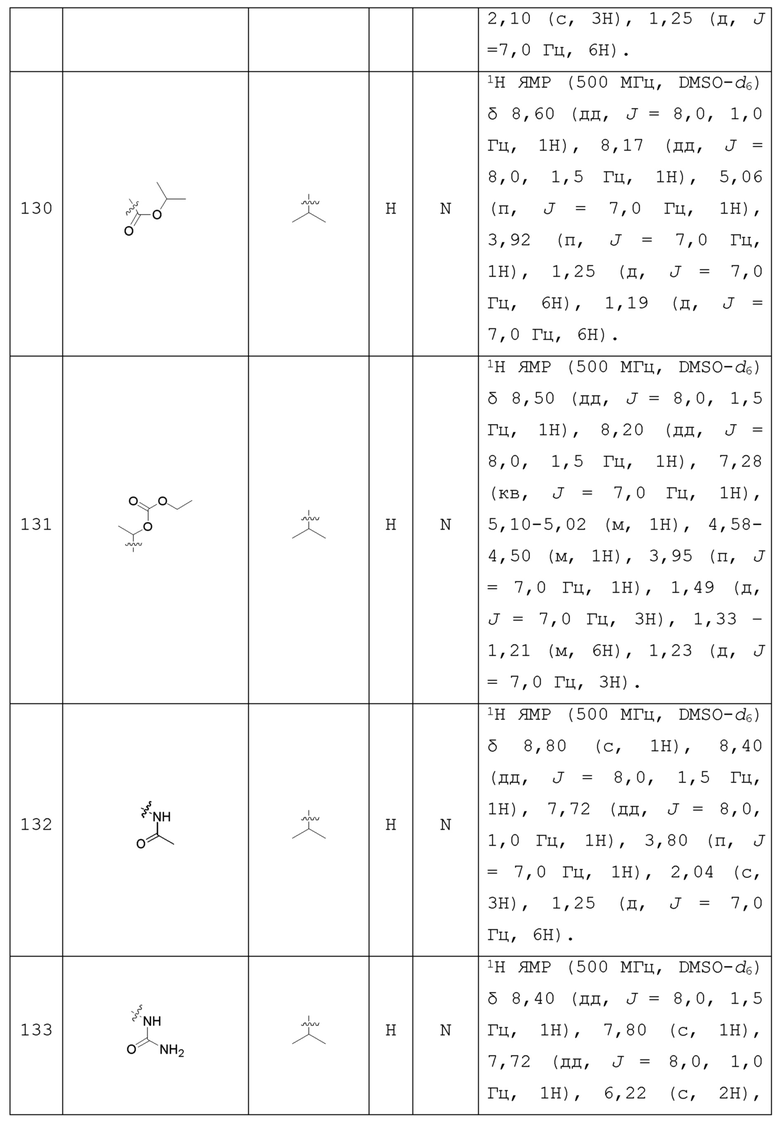
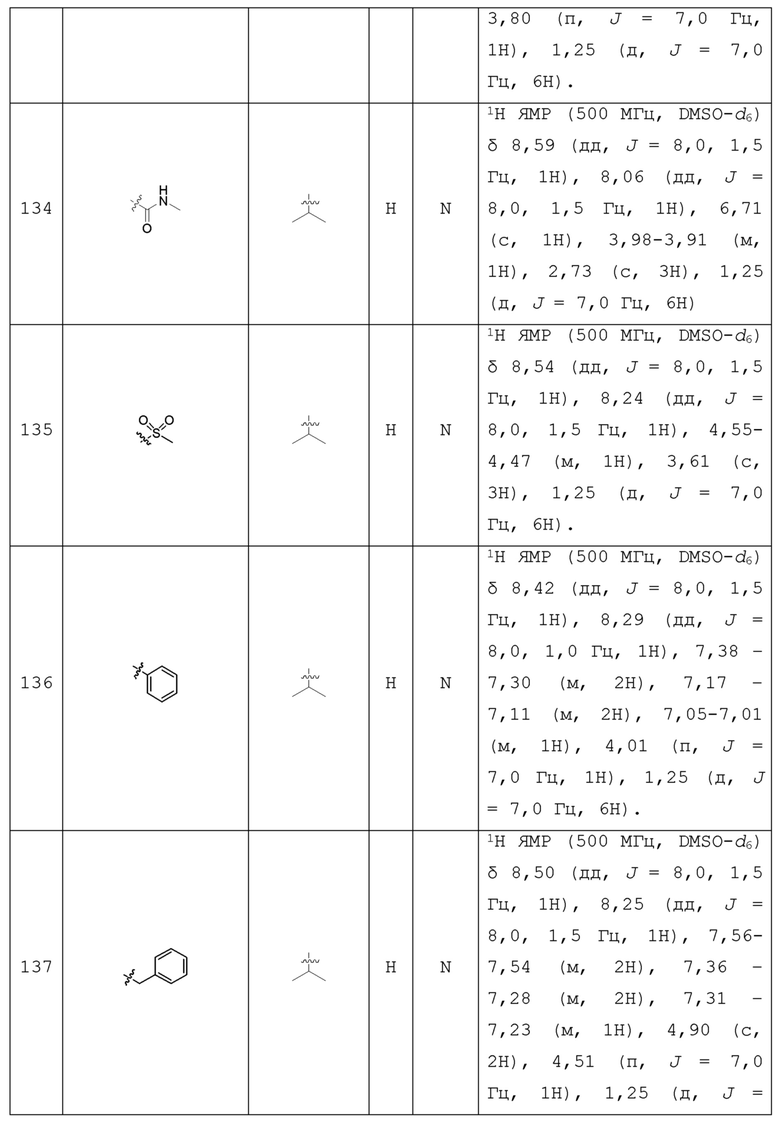
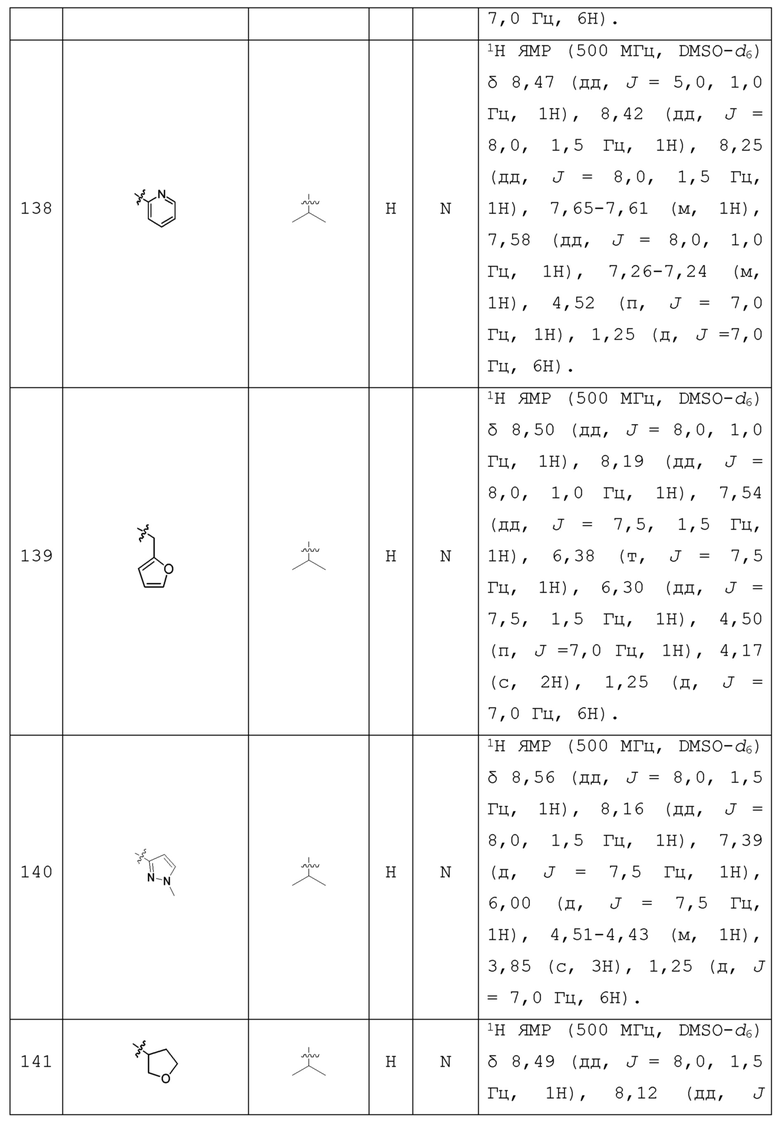
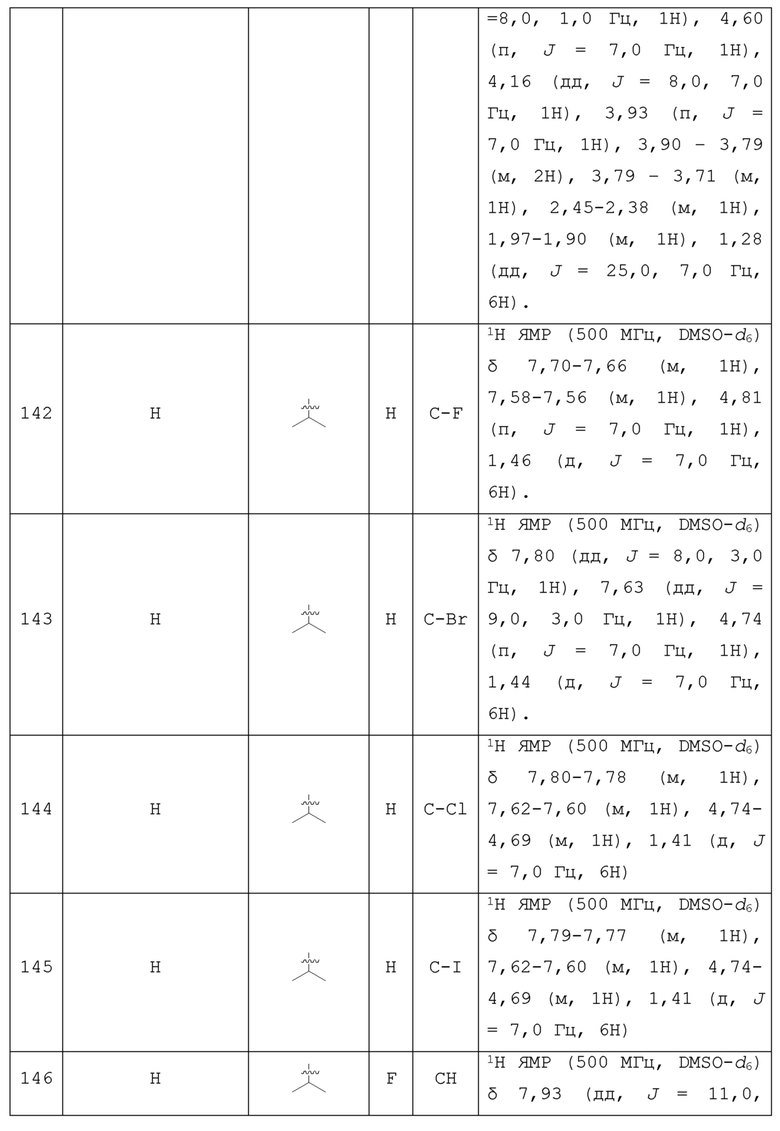
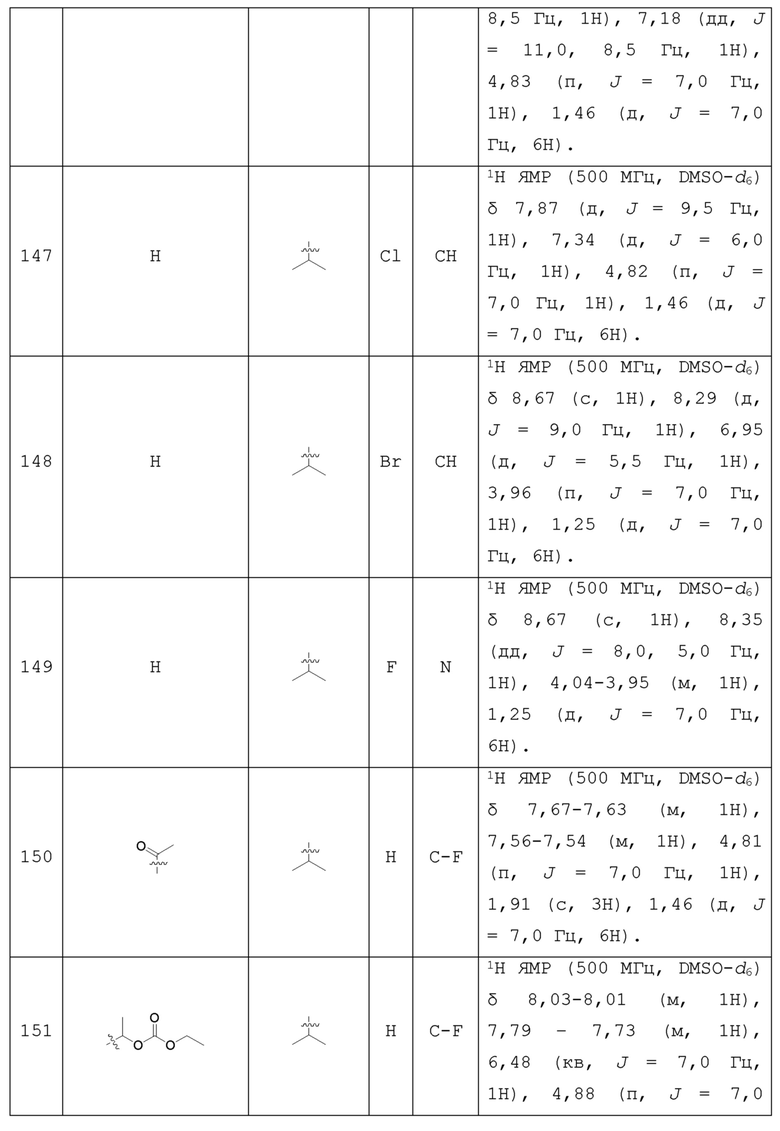
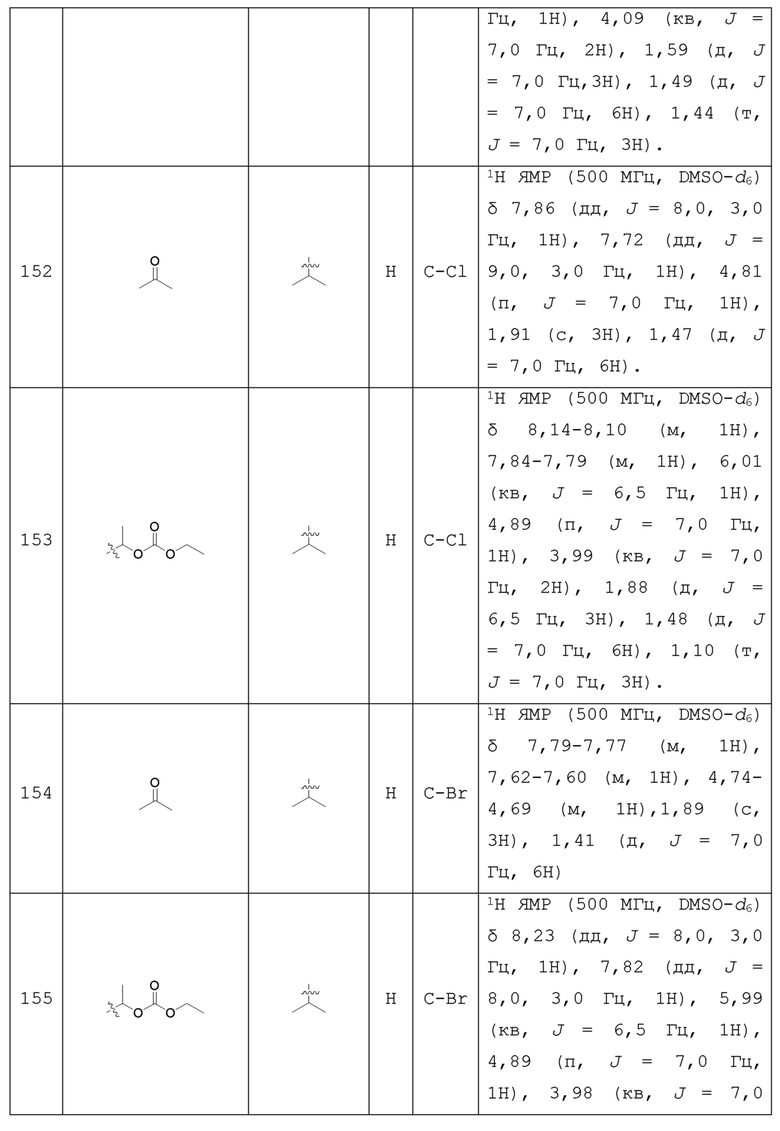
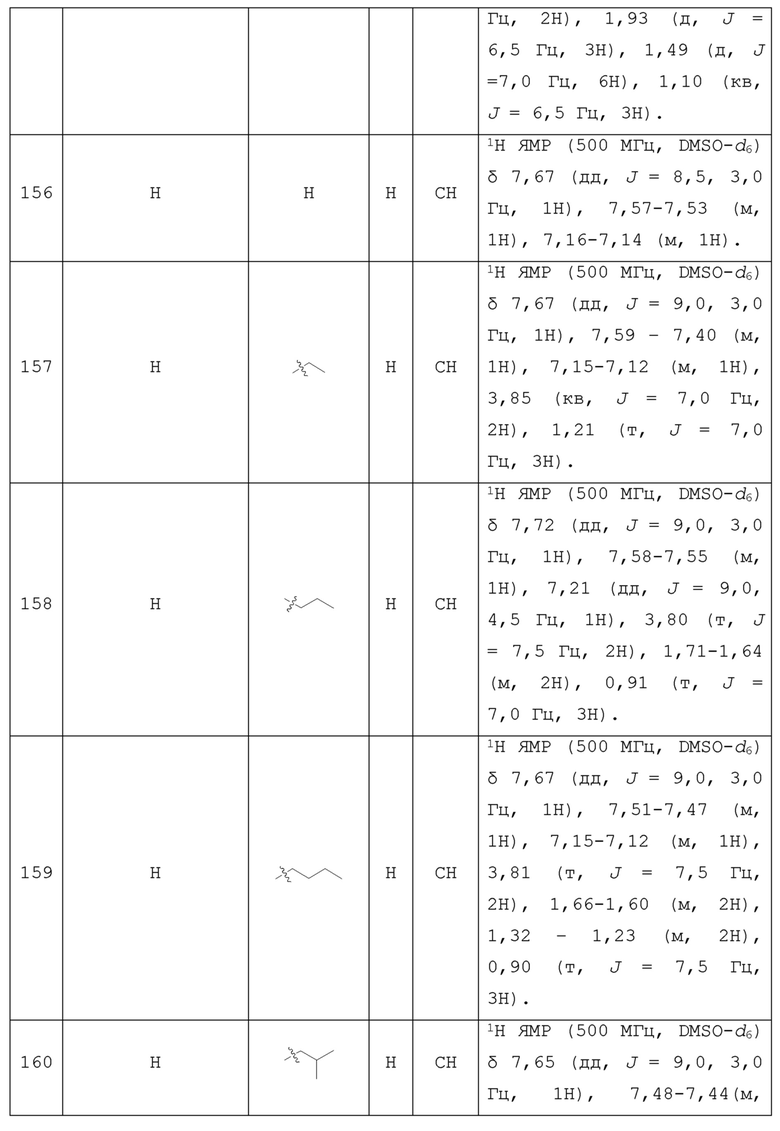
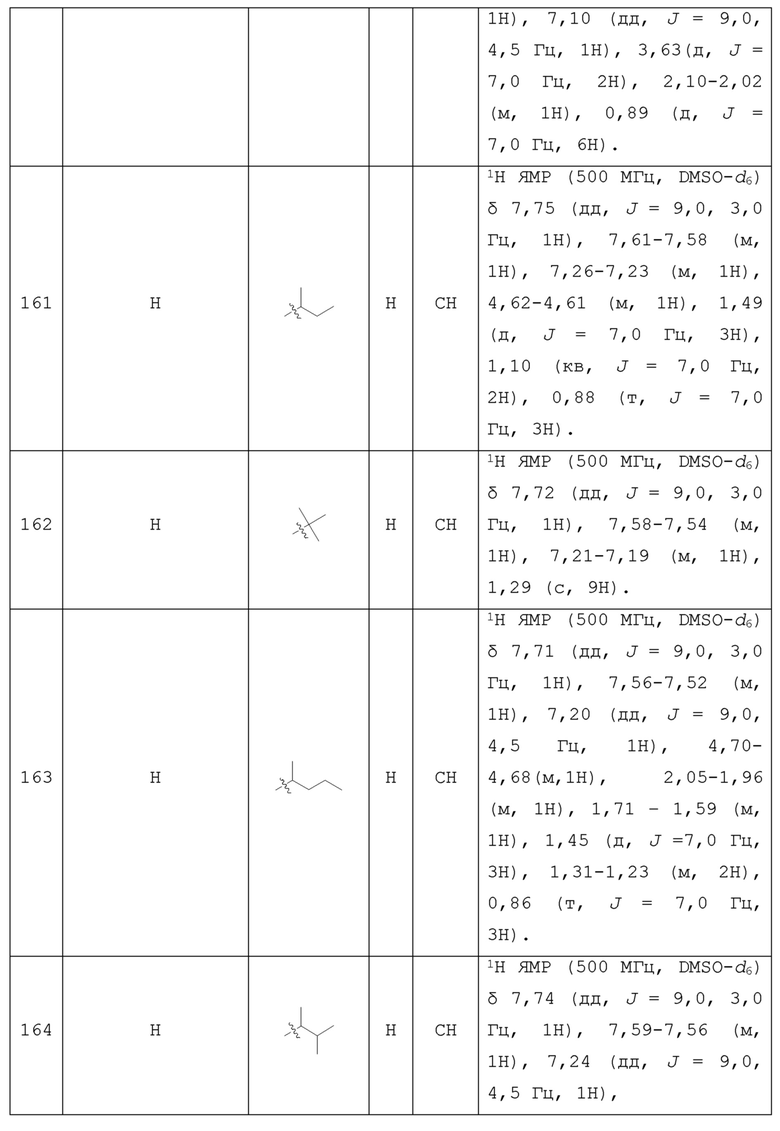
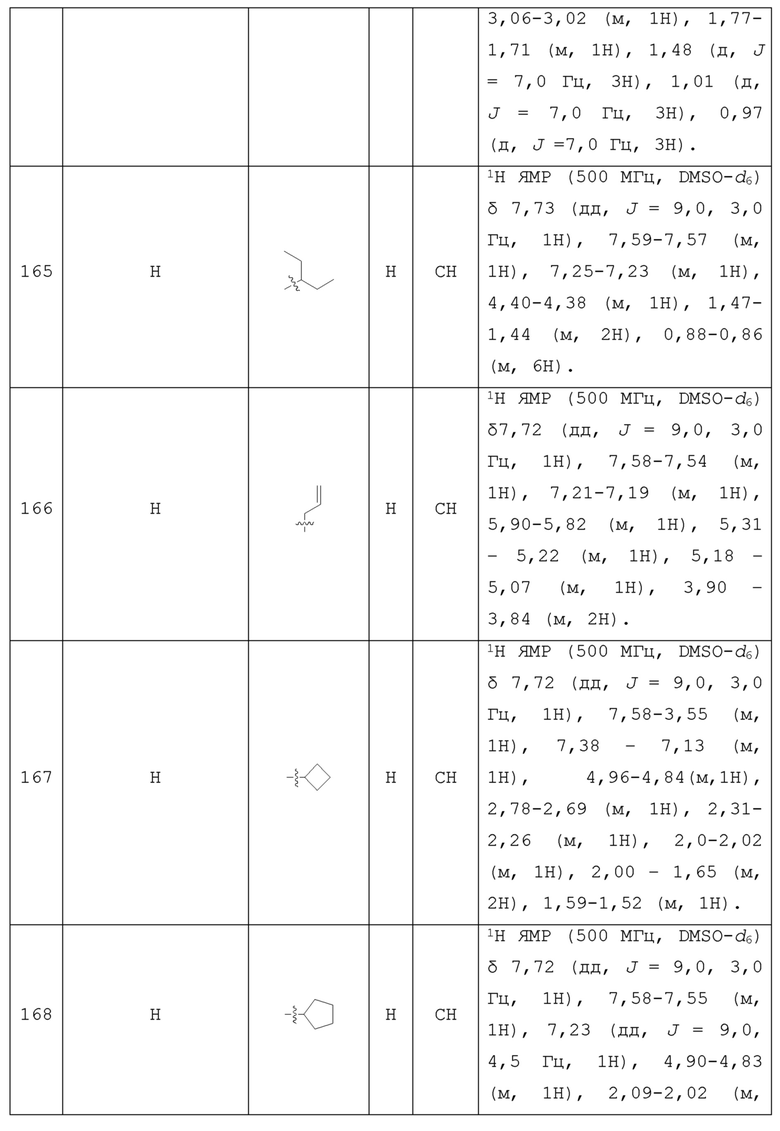
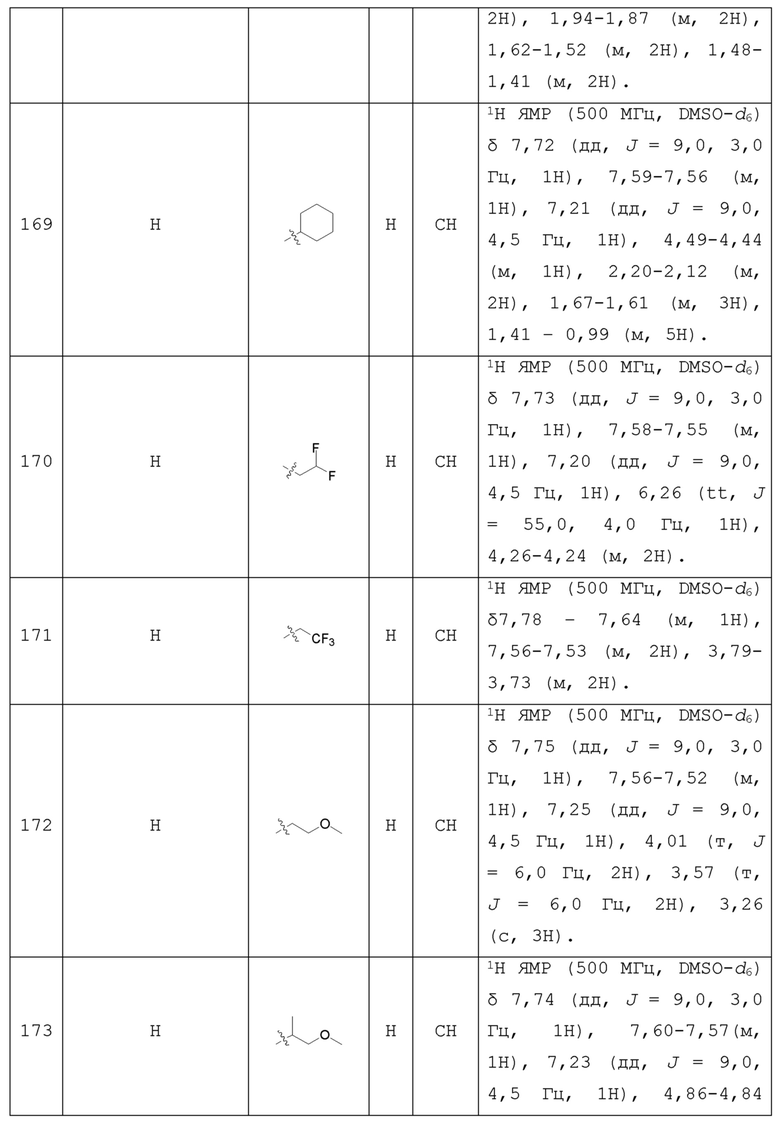
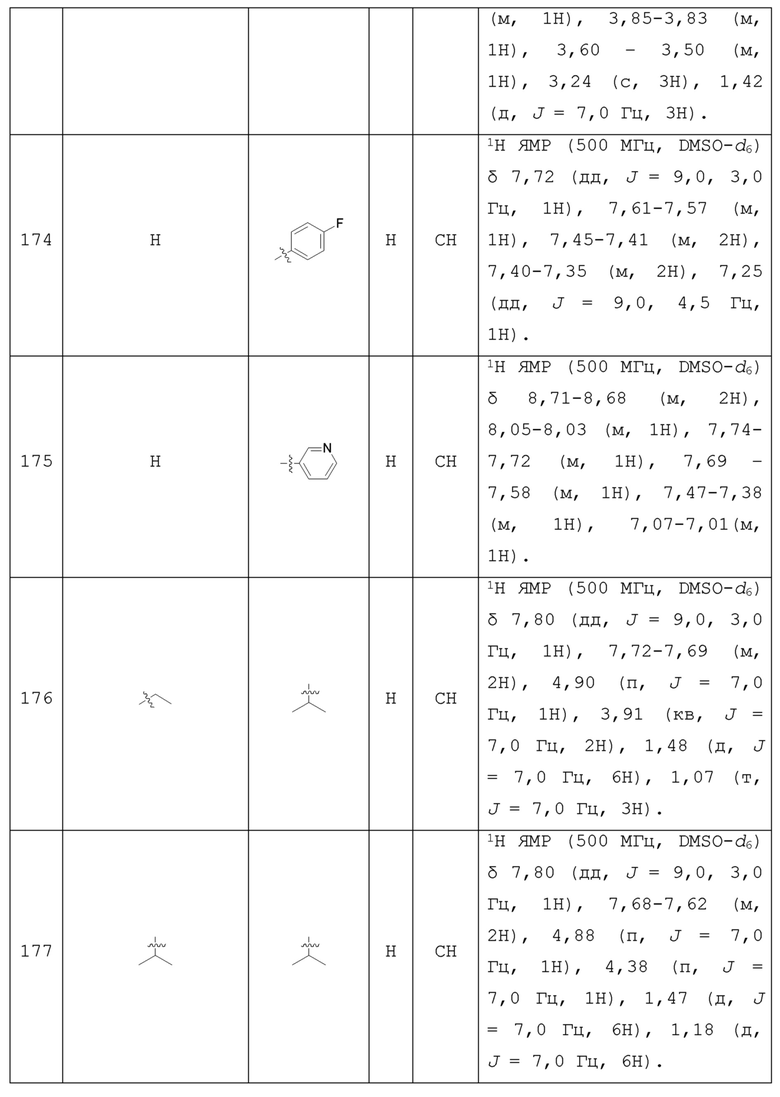
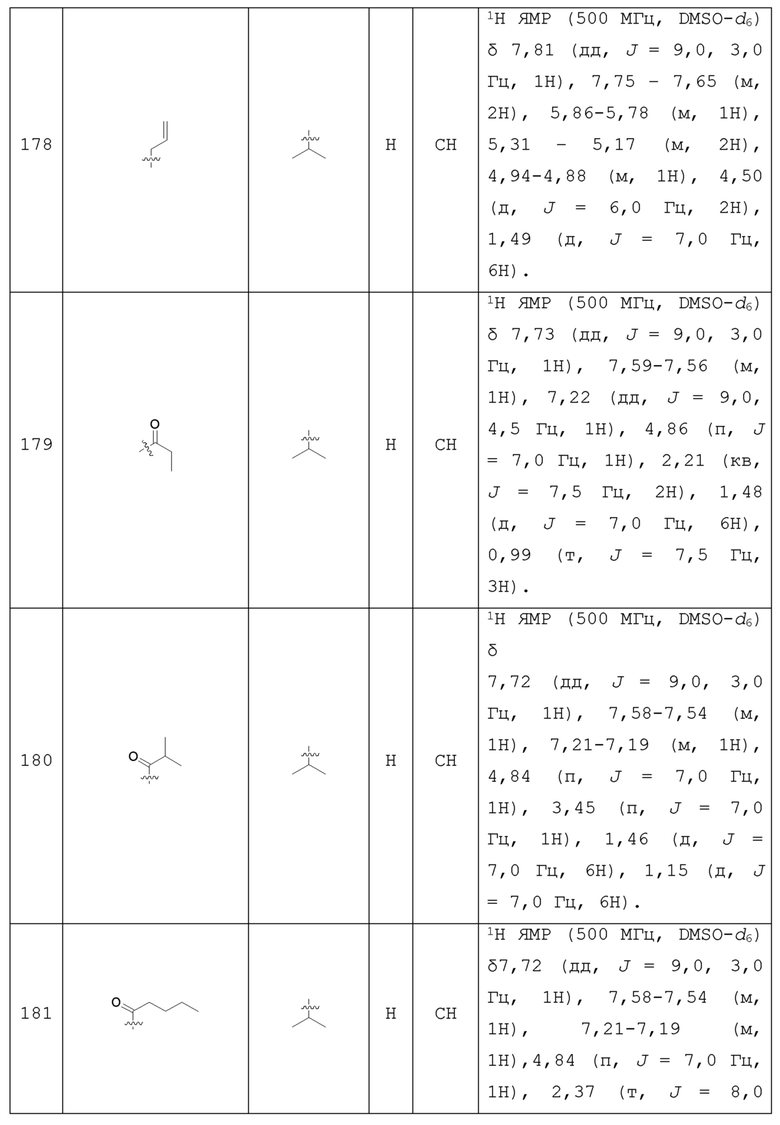
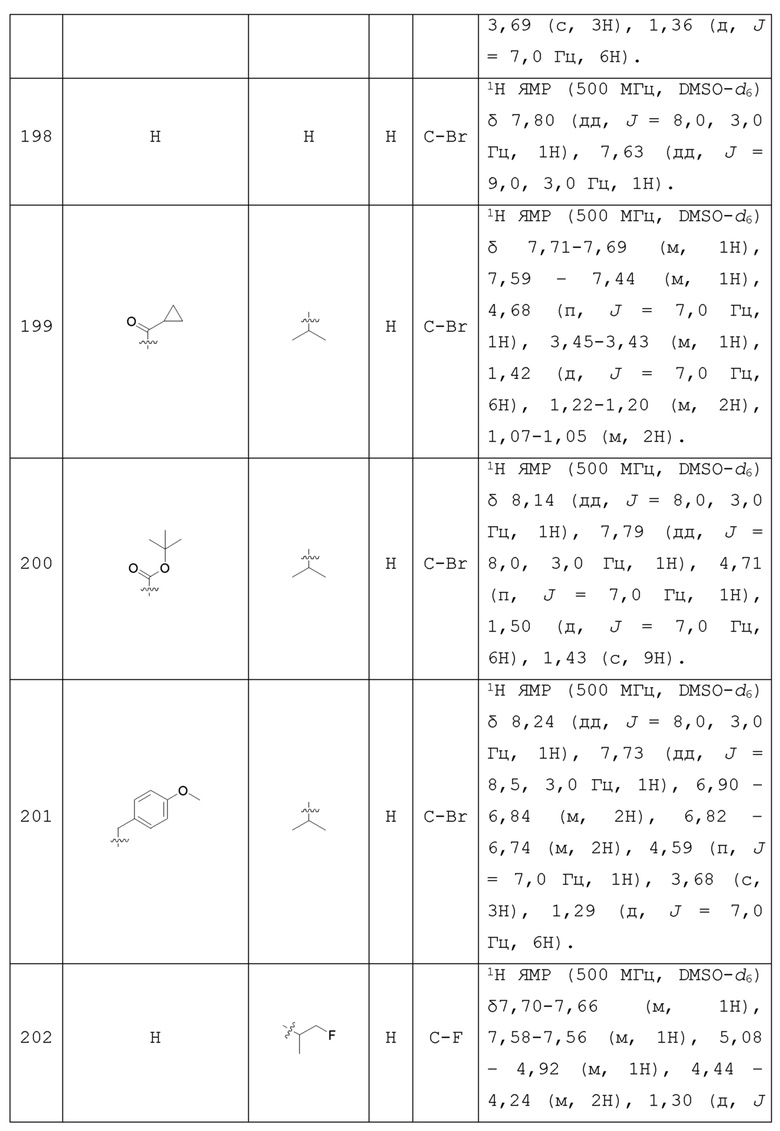
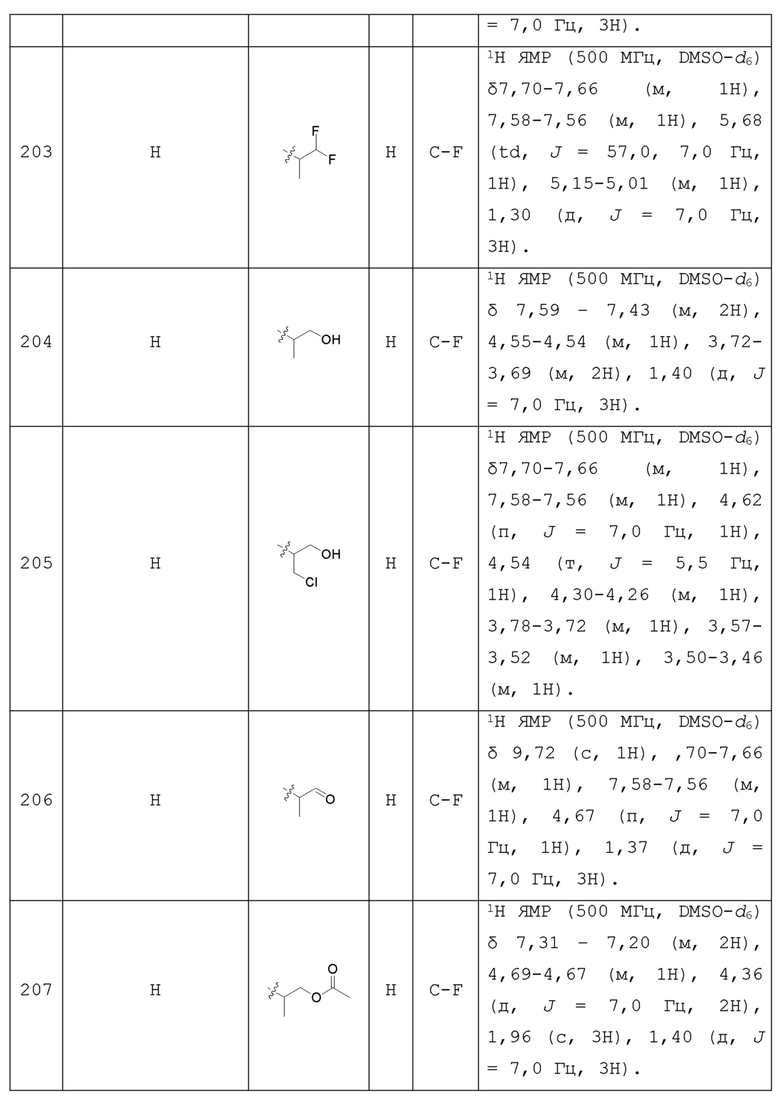
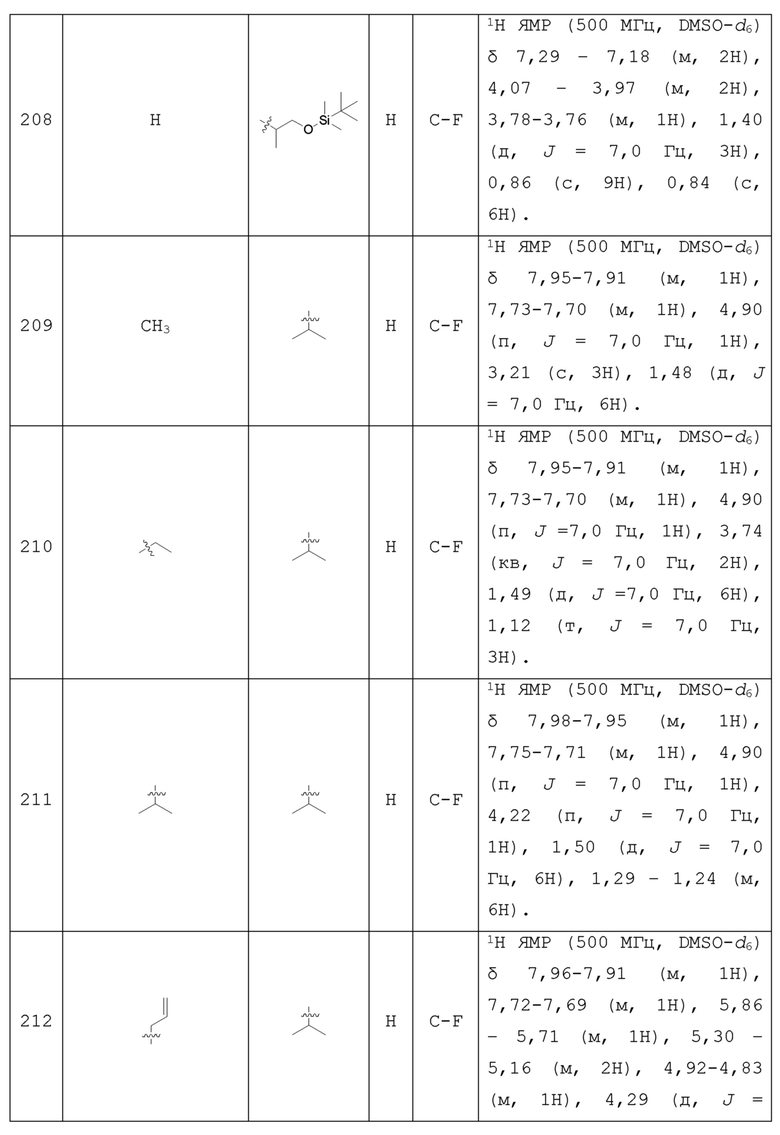
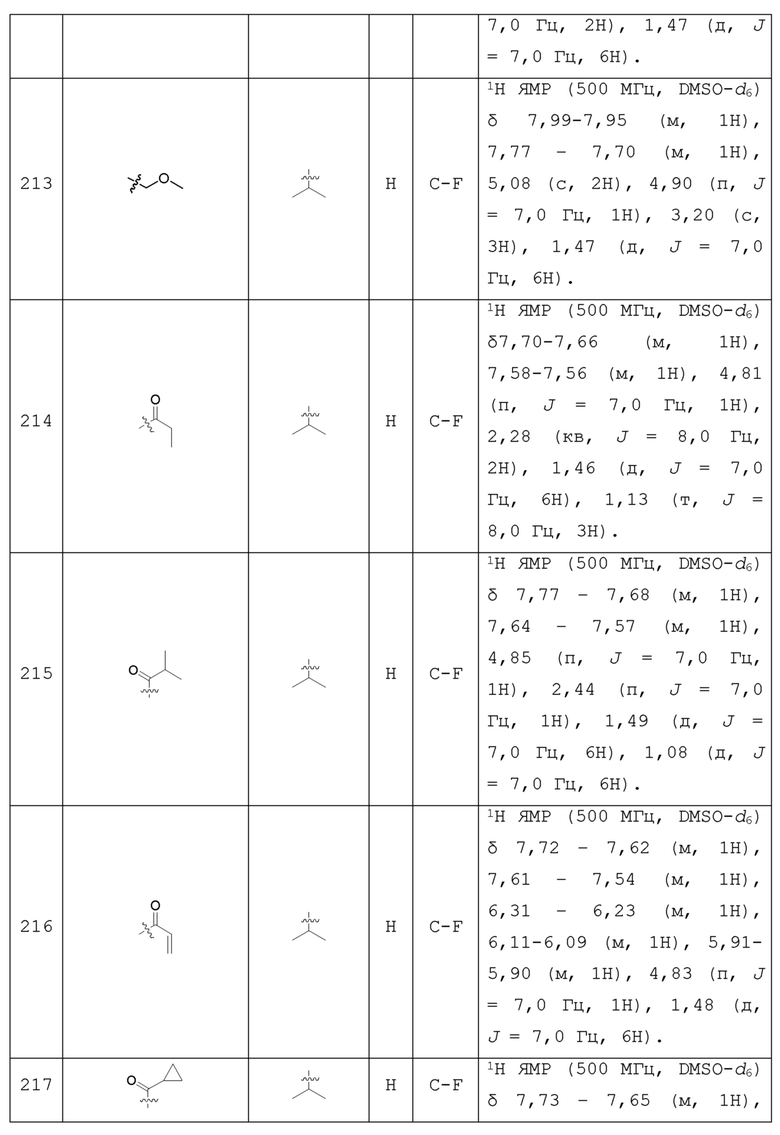
С учетом экономической эффективности и разнообразия форм соединения, авторами настоящего изобретения было синтезировано некоторое число предпочтительных соединений, часть из которых представлена в следующей таблице 1. Структура и информация, относящиеся к конкретному соединению, приведены в таблице 1. Соединения в таблице 1 представлены для более подробного объяснения настоящего изобретения, а не для какого-либо его ограничения. Специалистам в данной области не следует рассматривать приведенные далее соединения в качестве ограничений предмета настоящего изобретения.
Таблица 1. Структуры и данные 1H ЯМР соединений
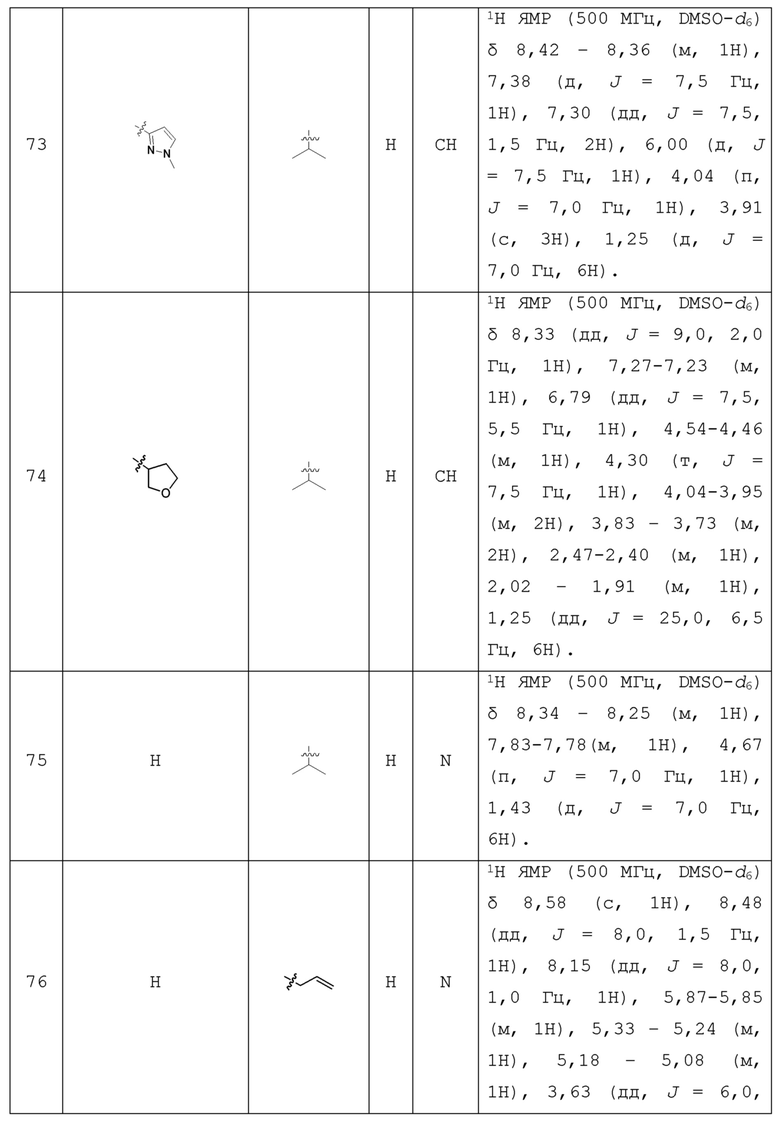
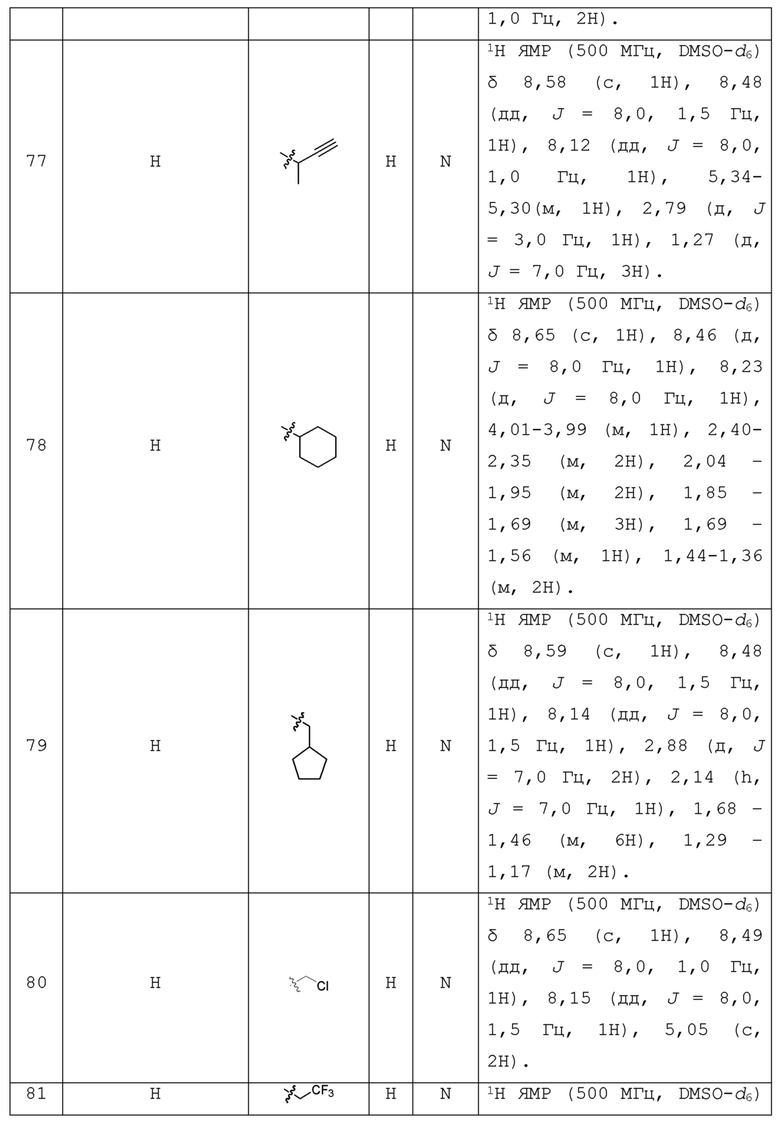
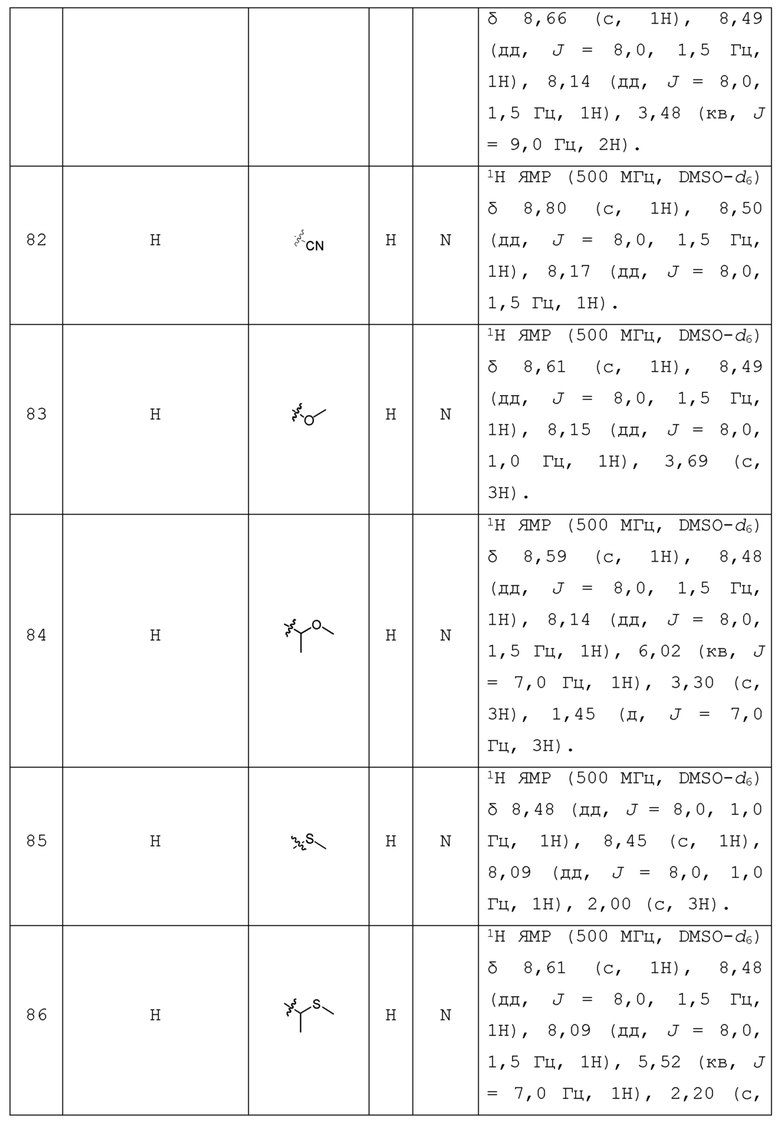
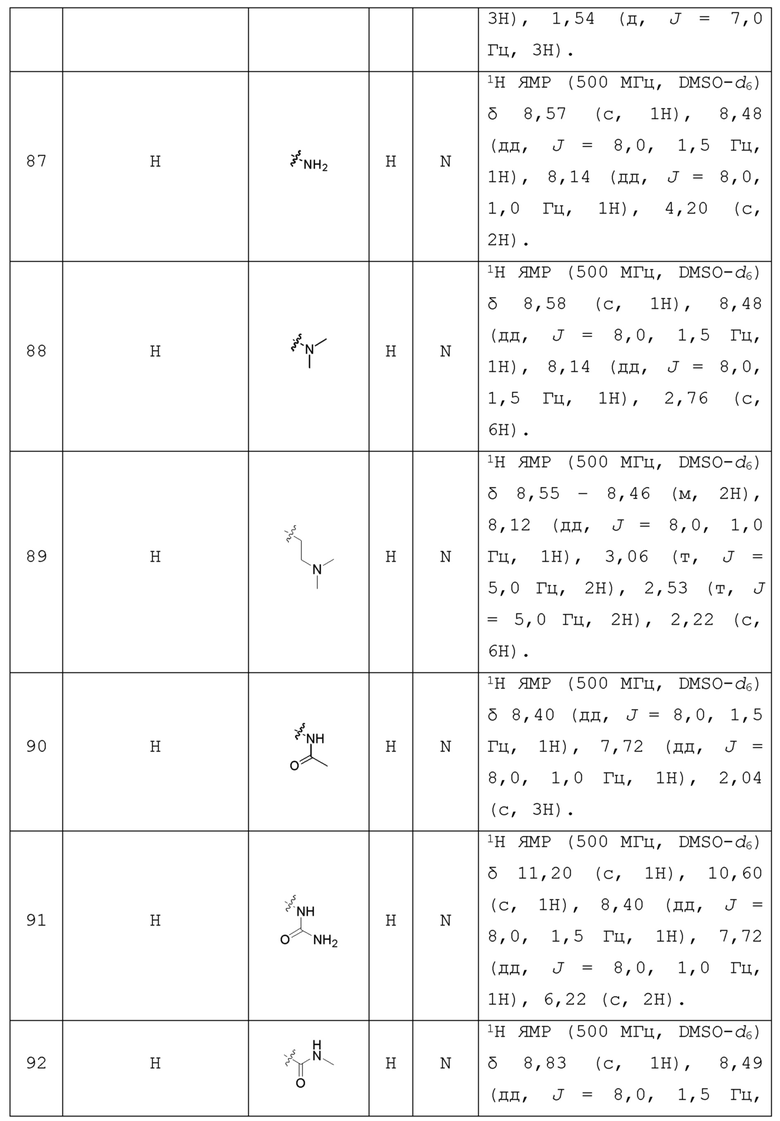
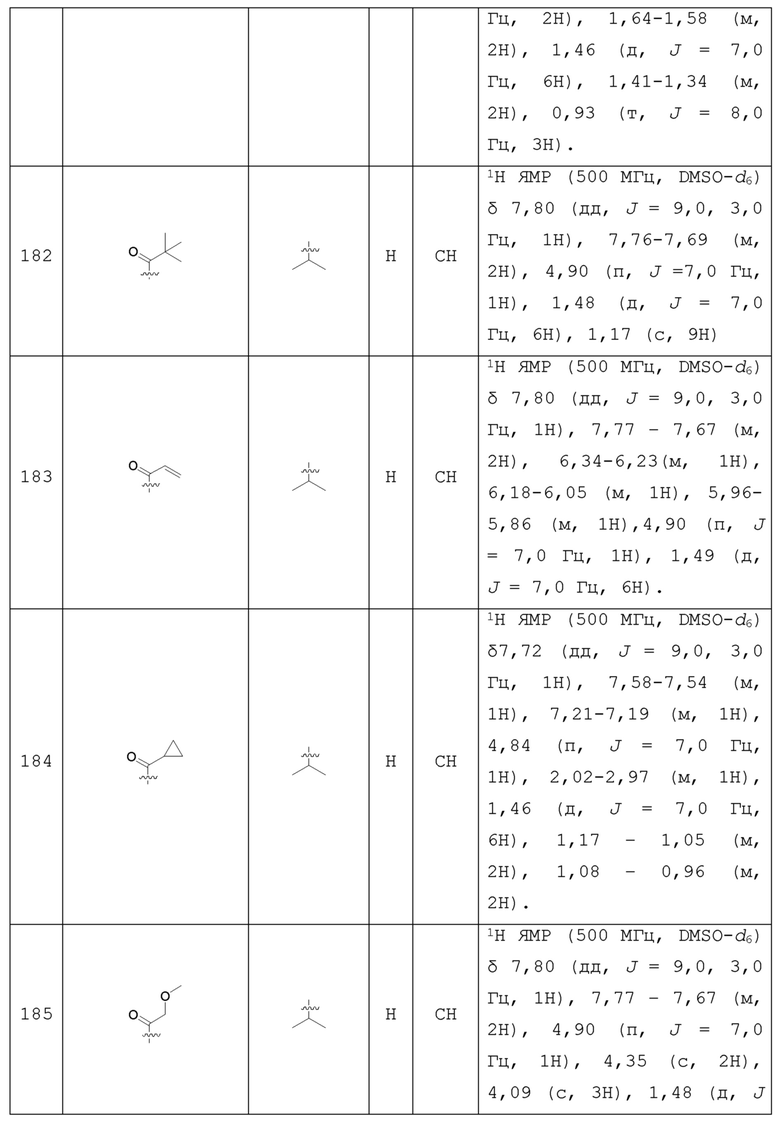
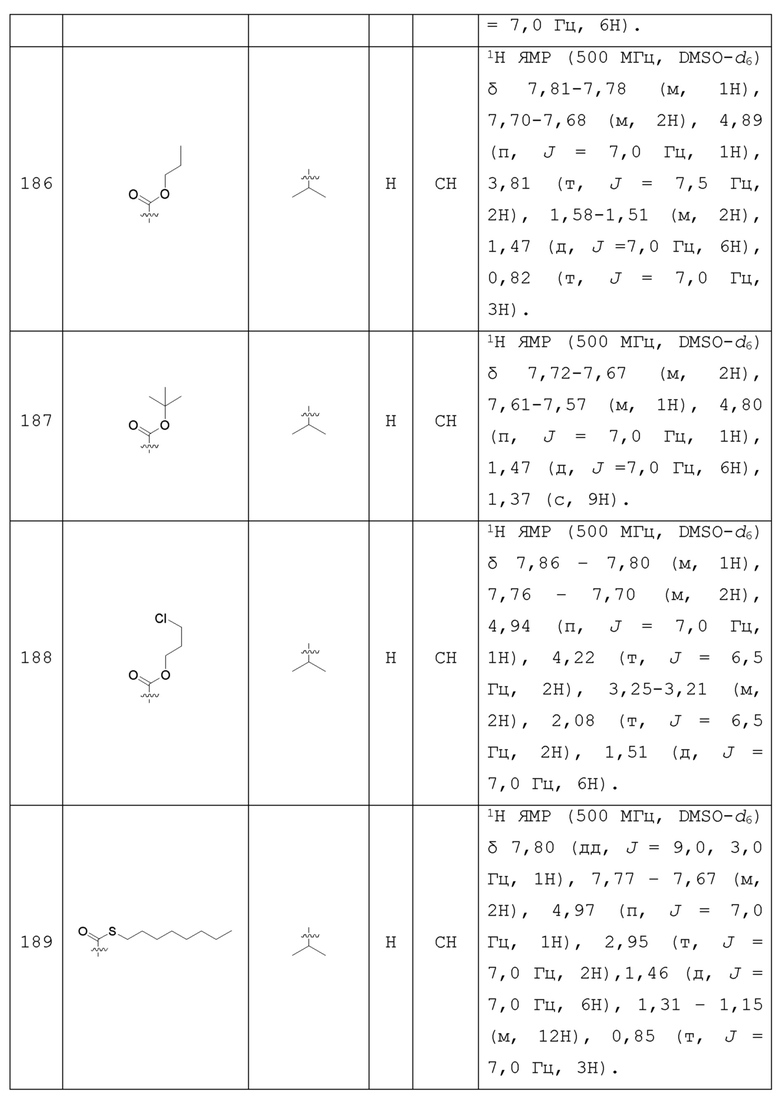
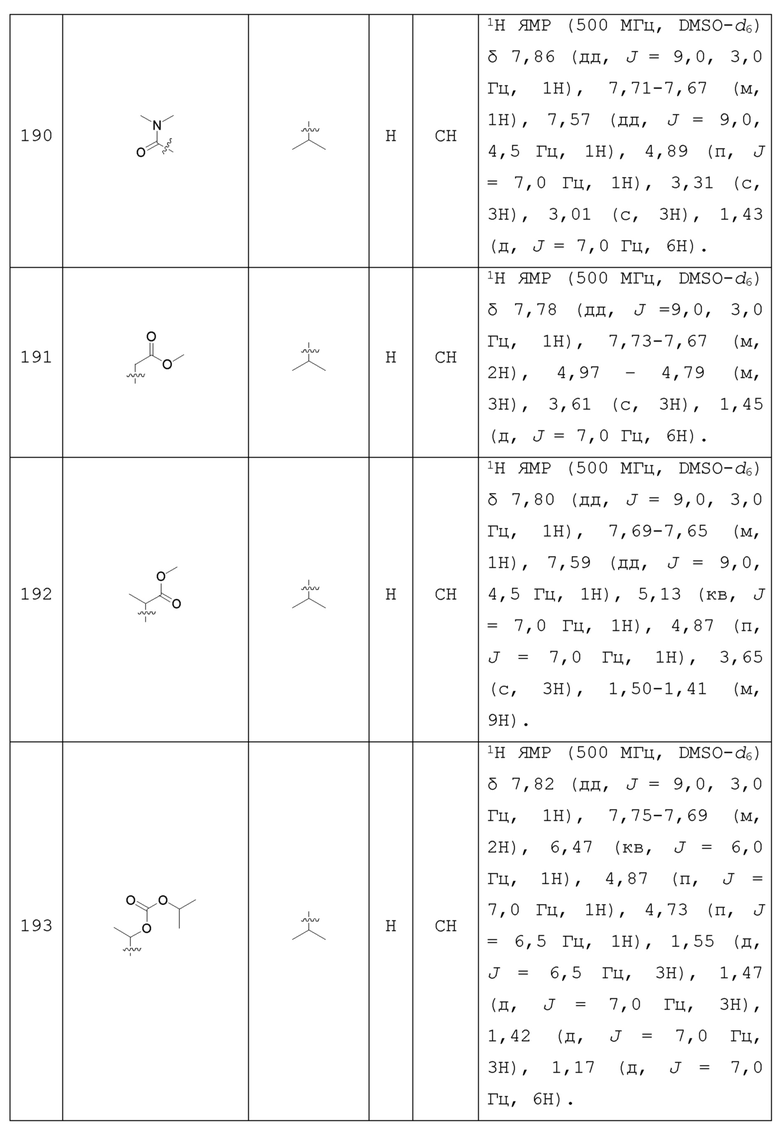
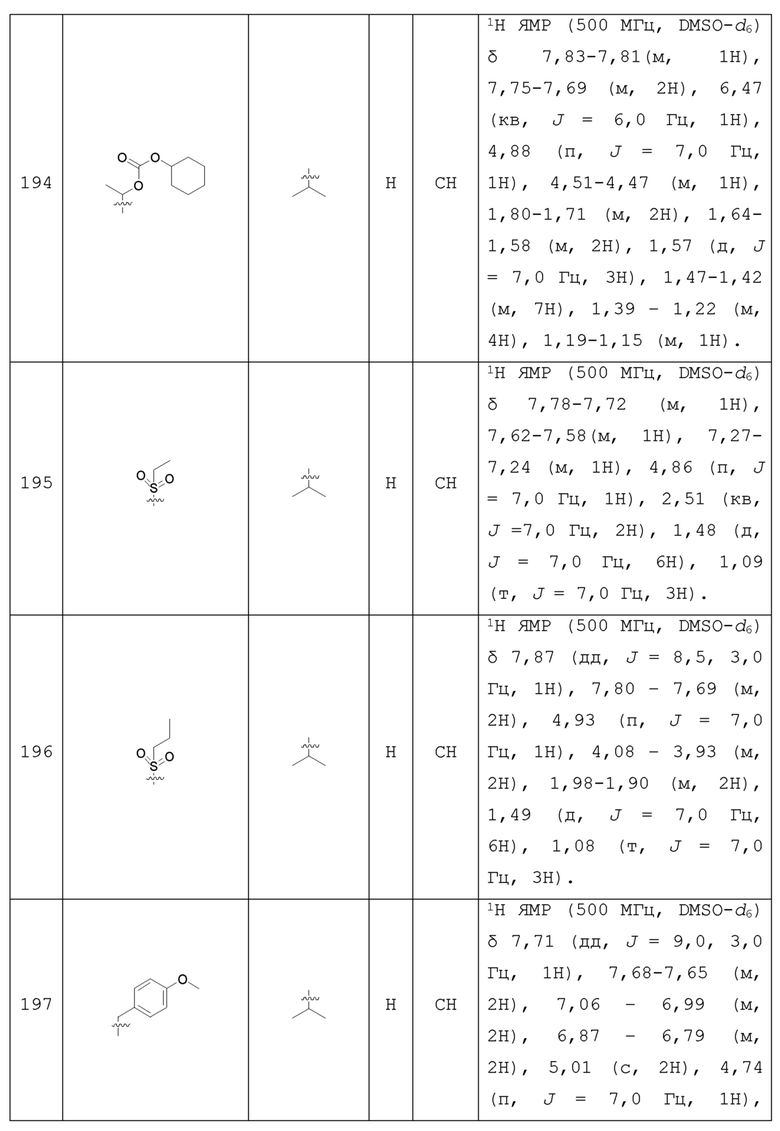
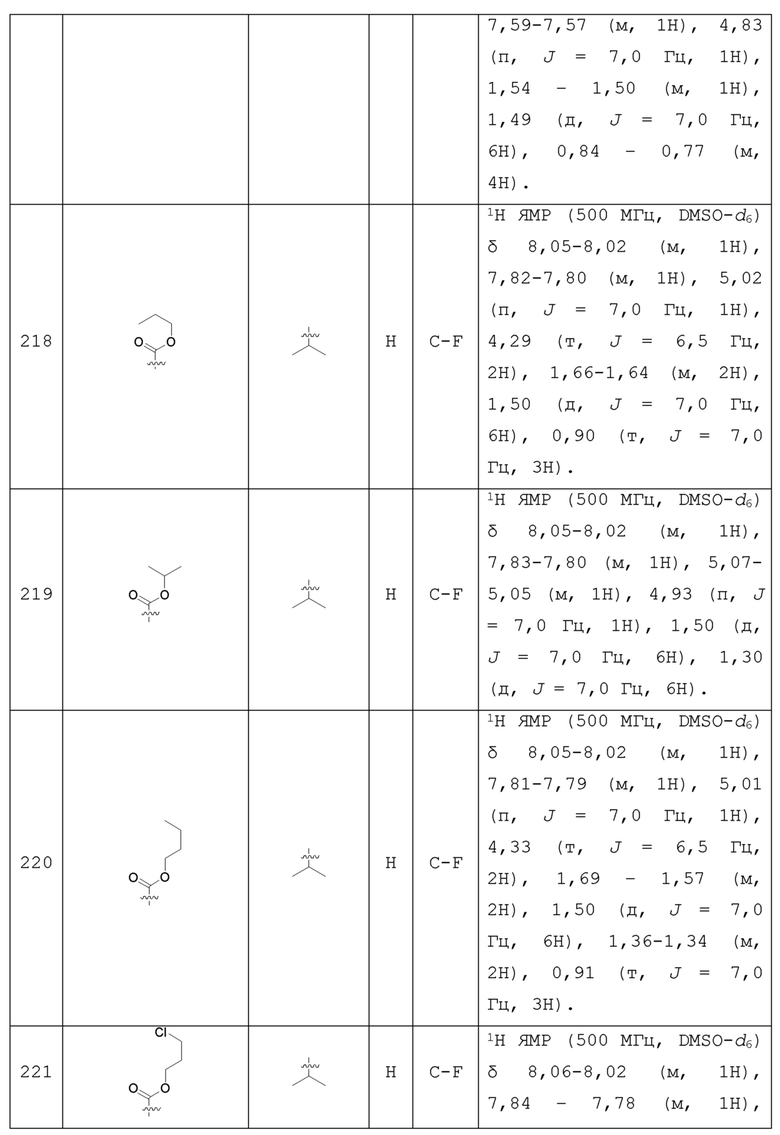
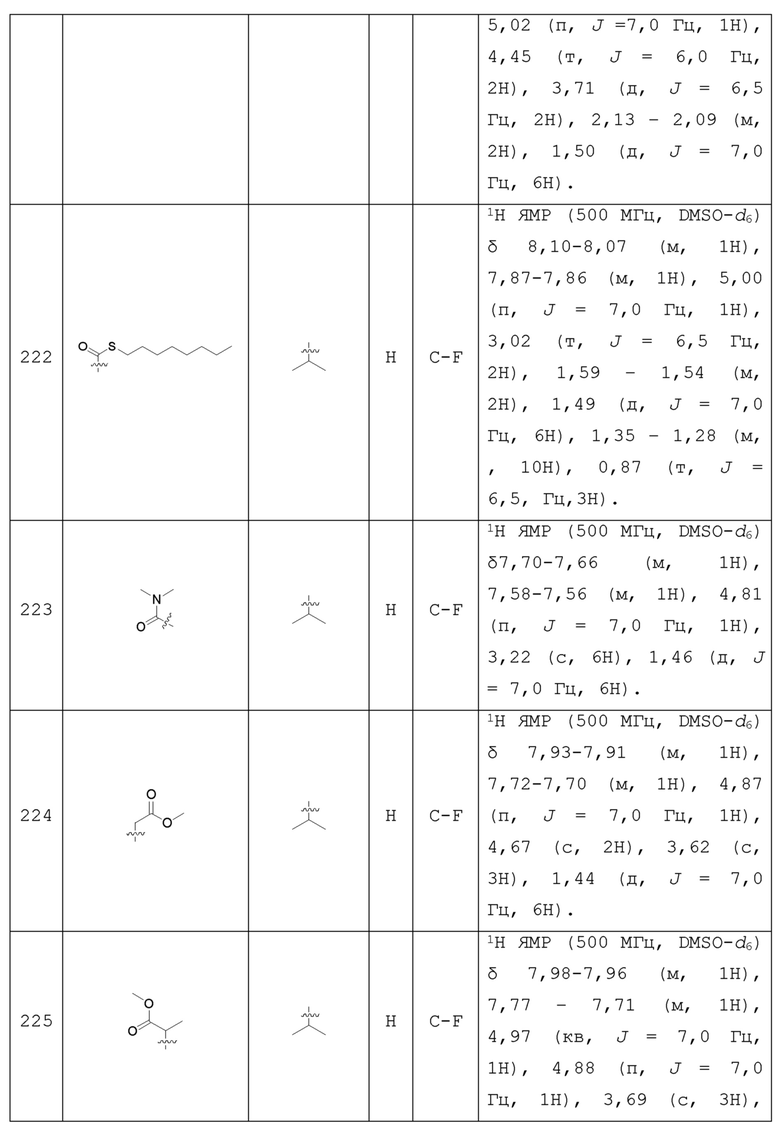
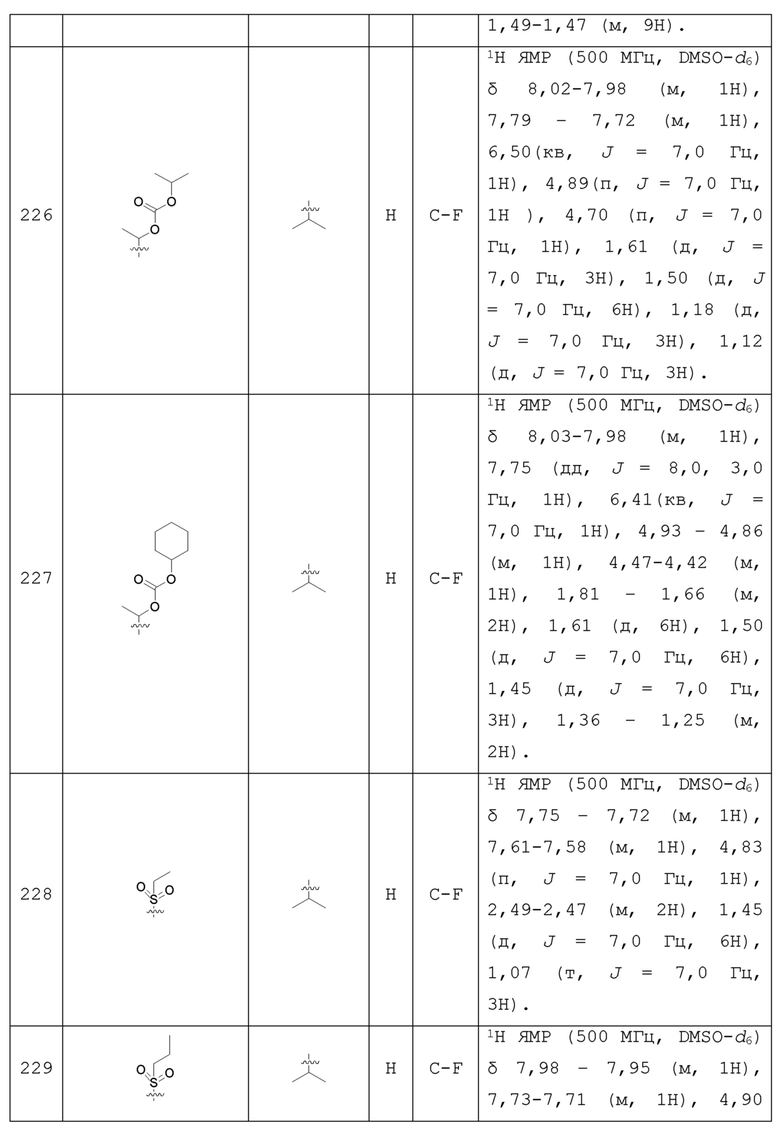

Способ получения соединения по изобретению будет подробно объяснен в приведенных далее схеме реакций и варианте осуществления. Реагенты могут быть приобретены у соответствующих фирм или получены известным способом, описанным в литературе, или проиллюстрированным на реакционной схеме. Для специалистов в данной области является очевидным, что соединение по настоящему изобретению может быть также синтезировано другим путем. Несмотря на то, что далее подробно описан синтез реагента и условия проведения реакции, тем не менее, может быть легко проведена замена на другой реагент и другие условия проведения реакции. Изомер соединения, например, полученный с помощью варианта способа получения по настоящему изобретению, включен в объем настоящего изобретения. Кроме того, приведенный далее способ получения может быть дополнительно модифицирован в соответствии с описанием настоящего изобретения с использованием обычного химического метода, известного специалистам в данной области, например, путем защиты соответствующей группы в процессе проведения реакции и других подобных действий.
Приведенный далее метод применения может быть использован для более глубокого понимания способа получения по настоящему изобретению. Для дополнительного объяснения настоящего изобретения были определены конкретный реагент, качество и условие, но они не являются какими-либо ограничениями обоснованного объема изобретения.
Далее приведены примеры получения типичных соединений, методы синтеза других соединений являются аналогичным и не будут подробно описаны в изобретении.
1. Синтез соединений 2
Соединение TEA (24 г, 236 ммоль), соединение b (5,25 г, 88,7 ммоль) и безводный 1,2-дихлорэтан (200 мл) добавляли в одногорлую колбу объемом 500 мл и охлаждали до 0°C на ледяной бане со льдом. Медленно добавляли по каплям хлорсульфоновую кислоту (6,9 г, 59 ммоль) при 0-10°C и перемешивали при 10°C в течение 10 минут, и в реакционную колбу добавляли соединение a (5 г, 28 ммоль). Реакционный раствор нагревали до 35°C и перемешивали в течение 30 минут. Добавляли по каплям оксихлорид фосфора (6,8 г, 8,87 ммоль) при 35°C, и реакционный раствор нагревали до 55°C и перемешивали в течение ночи. После практического завершения реакции исходных реагентов, определяемого анализом методом LC-MS, реакционный раствор охлаждали до комнатной температуры. Реакционный раствор промывали насыщенным водным раствором бикарбоната натрия (100 мл x 2), и органическую фазу сушили, концентрировали и очищали колоночной хроматографией с получением соединения 2-1 (8 г, с выходом 93%) в виде желтого масла.
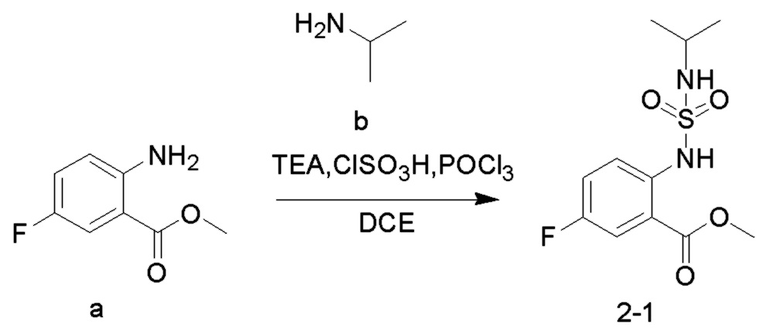
Соединение 2-1 (8 г, 27,6 ммоль) растворяли в безводном метаноле (100 мл), добавляли по каплям раствор метоксида натрия (30% метанольный раствор, 9,9 г, 55 ммоль) при комнатной температуре, и реакционный раствор нагревали до 65°C для проведения реакции в течение ночи. После завершения реакции исходных реагентов, определяемого анализом методом LC-MS, реакционный раствор концентрировали с удалением метанола, и неочищенный продукт растворяли в воде (50 мл), доводили величину рН до 5-6 с помощью разбавленной хлористоводородной кислоты (1M) и перемешивали в течение 30 минут. Образовывался осадок твердого вещества, и реакционную смесь фильтровали. Осадок на фильтре промывали водой (20 мл), сушили и концентрировали с получением соединения 2 (5 г, с выходом 70%) в виде светло-желтого твердого вещества.
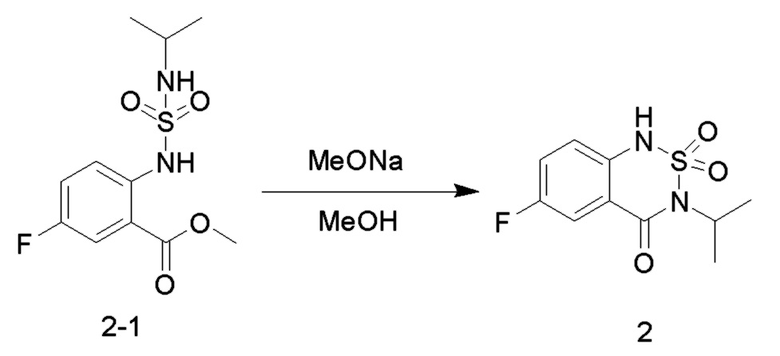
2. Синтез соединений 5
Соединение TEA (5,08 г, 50,25 ммоль), соединение 5-1 (1,01 г, 17,74 ммоль) и безводный 1,2-дихлорэтан (20 мл) добавляли в одногорлую колбу объемом 100 мл и охлаждали до 0°C на ледяной бане со льдом. Медленно добавляли по каплям хлорсульфоновую кислоту (1,38 г, 11,82 ммоль) при 0-10°C и перемешивали при 10°C в течение 10 минут, и добавляли в реакционную колбу соединение a (1 г, 5,91 ммоль). Реакционный раствор нагревали до 35°C и перемешивали в течение 30 минут. Добавляли по каплям оксихлорид фосфора (1,36 г, 8,87 ммоль) при 35°C, и реакционный раствор нагревали до 55°C и перемешивали в течение ночи. После практического завершения реакции исходных реагентов, определяемого анализом методом LC-MS, реакционный раствор охлаждали до комнатной температуры. Реакционный раствор промывали насыщенным водным раствором бикарбоната натрия (100 мл x 2), и органическую фазу сушили и концентрировали с получением соединения 5-2 (1,40 ммоль, 4,86 ммоль, с выходом 82,14%), в виде желтого масла.
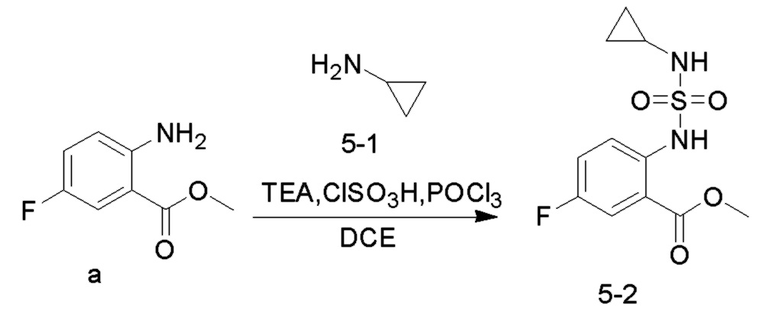
Соединение 5-2 (1,40 ммоль, 4,86 ммоль) растворяли в безводном метаноле (20 мл), добавляли по каплям раствор метоксида натрия (30% метанольный раствор, 1,75 г, 9,71 ммоль) при комнатной температуре, и реакционный раствор нагревали до 65°C для проведения реакции в течение ночи. После завершения реакции исходных реагентов, определяемого анализом методом LC-MS, реакционный раствор концентрировали с удалением метанола, и неочищенный продукт растворяли в воде (50 мл), доводили величину рН до 5-6 с помощью разбавленной хлористоводородной кислоты (1M) и перемешивали в течение 30 минут. Образовывался осадок твердого вещества, и реакционную смесь фильтровали. Осадок на фильтре промывали водой (20 мл), сушили и концентрировали с получением соединения 5 (1,0 ммоль, с выходом 80,36%) в виде желтого твердого вещества.
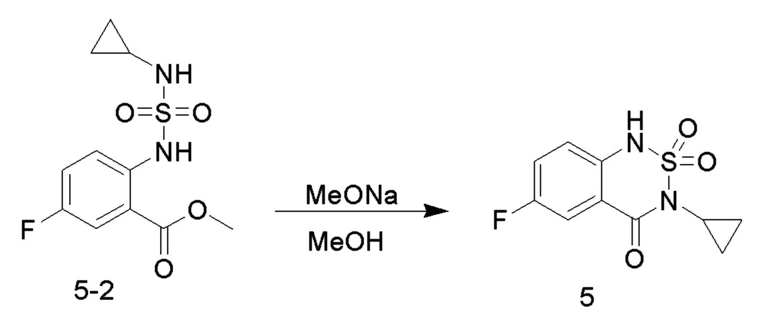
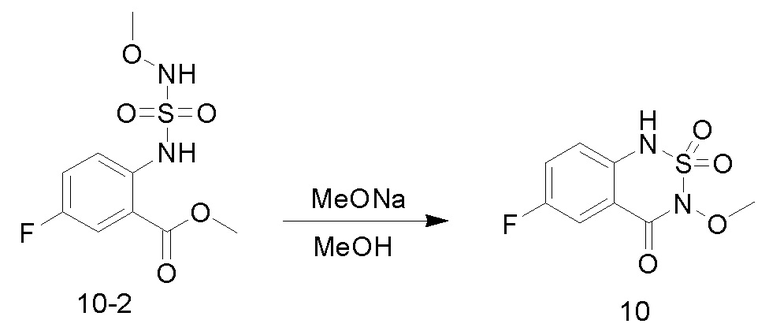
3. Синтез соединений 10
Соединение TEA (5,08 г, 50,25 ммоль), соединение 10-1 (0,84 г, 17,74 ммоль) и безводный 1,2-дихлорэтан (20 мл) добавляли в одногорлую колбу объемом 100 мл и охлаждали до 0°C на ледяной бане со льдом. Медленно добавляли по каплям хлорсульфоновую кислоту (1,38 г, 11,82 ммоль) при 0-10°C и перемешивали при 10°C в течение 10 минут, и в реакционную колбу добавляли соединение a (1 г, 5,91 ммоль). Реакционный раствор нагревали до 35°C и перемешивали в течение 30 минут. Добавляли по каплям оксихлорид фосфора (1,36 г, 8,87 ммоль) при 35°C, и реакционный раствор нагревали до 55°C и перемешивали в течение ночи. После практического завершения реакции исходных реагентов, определяемого анализом методом LC-MS, реакционный раствор охлаждали до комнатной температуры. Реакционный раствор промывали насыщенным водным раствором бикарбоната натрия (100 мл x 2), и органическую фазу сушили и концентрировали с получением соединения 10-2 (1,6 г, 5,75 ммоль, с выходом 97,27%) в виде светло-желтого твердого вещества.
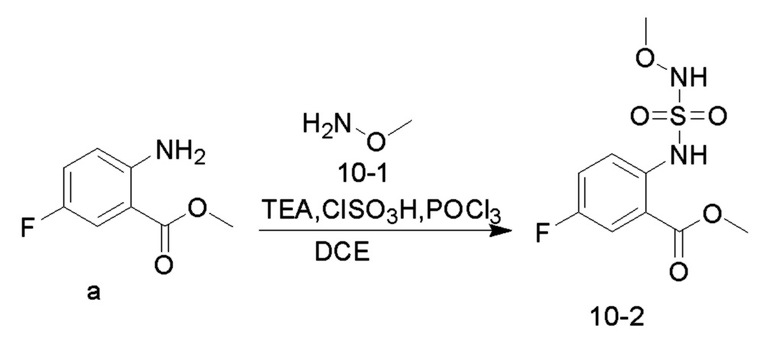
Соединение 10-2 (1,6 г, 5,75 ммоль) растворяли в безводном метаноле (20 мл), добавляли по каплям раствор метоксида натрия (30% метанольный раствор, 2,07 г, 11,50 ммоль) при комнатной температуре, и реакционный раствор нагревали до 65°C для проведения реакции в течение ночи. После завершения реакции исходных реагентов, определяемого анализом методом LC-MS, реакционный раствор концентрировали с удалением метанола, и неочищенный продукт растворяли в воде (50 мл), доводили величину рН до 5-6 с помощью разбавленной хлористоводородной кислоты (1M) и перемешивали в течение 30 минут. Образовывался осадок твердого вещества, и реакционную смесь фильтровали. Осадок на фильтре промывали водой (20 мл), сушили и концентрировали с получением соединения 10 (1,3 г, с выходом 91,82%), в виде светло-желтого твердого вещества.
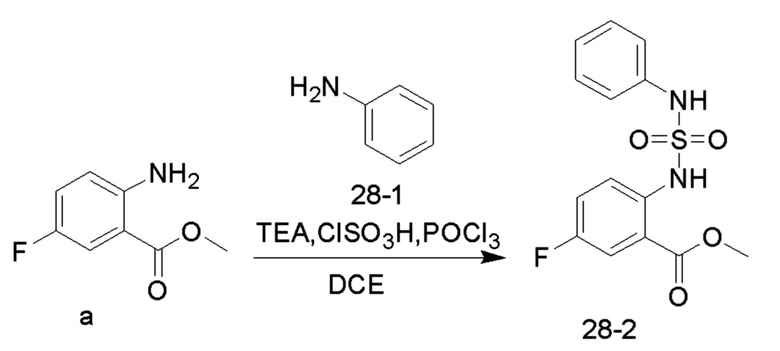
4. Синтез соединений 28
Соединение TEA (5,08 г, 50,25 ммоль), соединение 28-1 (1,65 г, 17,74 ммоль) и безводный 1,2-дихлорэтан (20 мл) добавляли в одногорлую колбу объемом 100 мл и охлаждали до 0°C на ледяной бане со льдом. Медленно добавляли по каплям хлорсульфоновую кислоту (1,38 г, 11,82 ммоль) при 0-10°C и перемешивали при 10°C в течение 10 минут, и добавляли в реакционную колбу соединение a (1 г, 5,91 ммоль). Реакционный раствор нагревали до 35°C и перемешивали в течение 30 минут. Добавляли по каплям оксихлорид фосфора (1,36 г, 8,87 ммоль) при 35°C, и реакционный раствор нагревали до 55°C и перемешивали в течение ночи. После практического завершения реакции исходных реагентов, определяемого анализом методом LC-MS, реакционный раствор охлаждали до комнатной температуры. Реакционный раствор промывали насыщенным водным раствором бикарбоната натрия (100 мл x 2), и органическую фазу сушили и концентрировали с получением соединения 28-2 (1,40 ммоль, 4,32 ммоль, с выходом 73,02%), в виде желтого твердого вещества.
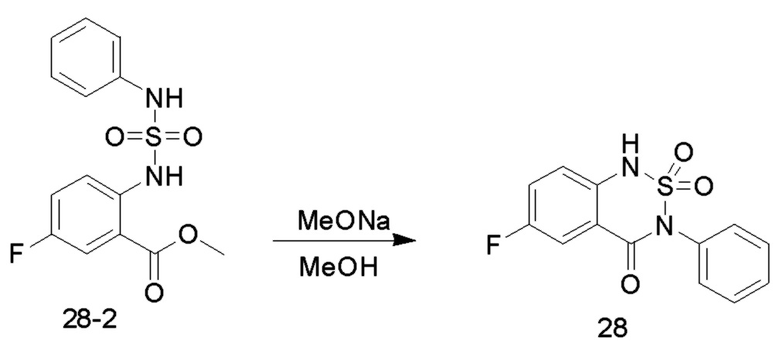
Соединение 28-2 (1,40 ммоль, 4,32 ммоль) растворяли в безводном метаноле (20 мл), добавляли по каплям раствор метоксида натрия (30% метанольный раствор, 1,55 г, 8,63 ммоль) при комнатной температуре, и реакционный раствор нагревали до 65°C для проведения реакции в течение ночи. После завершения реакции исходных реагентов, определяемого анализом методом LC-MS, реакционный раствор концентрировали с удалением метанола, и неочищенный продукт растворяли в воде (50 мл), доводили величину рН до 5-6 с помощью разбавленной хлористоводородной кислоты (1M) и перемешивали в течение 30 минут. Образовывался осадок твердого вещества, и реакционную смесь фильтровали. Осадок на фильтре промывали водой (20 мл), сушили и концентрировали с получением соединения 28 (1,1 г, с выходом 81,00%), в виде желтого твердого вещества.
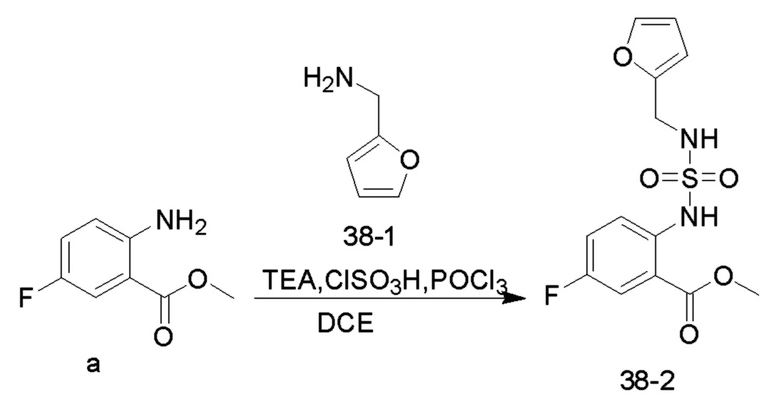
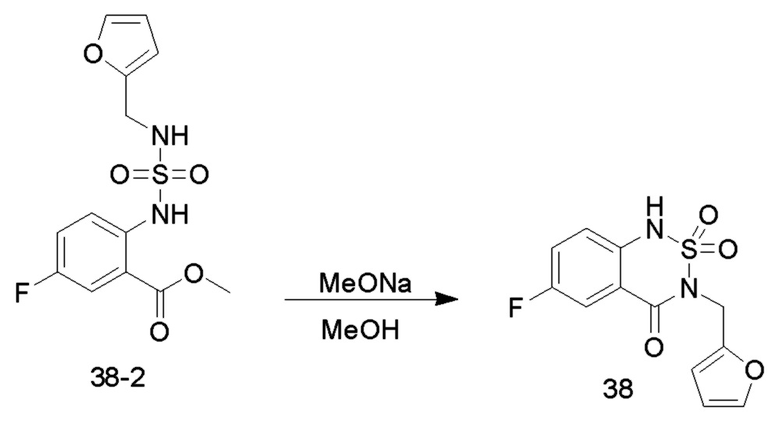
5. Синтез соединений 38
Соединение TEA (5,08 г, 50,25 ммоль), соединение 38-1 (1,72 г, 17,74 ммоль) и безводный 1,2-дихлорэтан (20 мл) добавляли в одногорлую колбу объемом 100 мл и охлаждали до 0°C на ледяной бане со льдом. Медленно добавляли по каплям хлорсульфоновую кислоту (1,38 г, 11,82 ммоль) при 0-10°C и перемешивали при 10°C в течение 10 минут, и добавляли в реакционную колбу соединение a (1 г, 5,91 ммоль). Реакционный раствор нагревали до 35°C и перемешивали в течение 30 минут. Добавляли по каплям оксихлорид фосфора (1,36 г, 8,87 ммоль) при 35°C, и реакционный раствор нагревали до 55°C и перемешивали в течение ночи. После практического завершения реакции исходных реагентов, определяемого анализом методом LC-MS, реакционный раствор охлаждали до комнатной температуры. Реакционный раствор промывали насыщенным водным раствором бикарбоната натрия (100 мл x 2), и органическую фазу сушили и концентрировали с получением соединения 38-2 (1,5 г, 4,57 ммоль, с выходом 77,28%) в виде желтого масла.
Соединение 38-2 (1,5 г, 4,57 ммоль) растворяли в безводном метаноле (20 мл), добавляли по каплям раствор метоксида натрия (30% метанольный раствор, 1,65 г, 9,14 ммоль) при комнатной температуре, и реакционный раствор нагревали до 65°C для проведения реакции в течение ночи. После завершения реакции исходных реагентов, определяемого анализом методом LC-MS, реакционный раствор концентрировали с удалением метанола, и неочищенный продукт растворяли в воде (50 мл), доводили величину рН до 5-6 с помощью разбавленной хлористоводородной кислоты (1M) и перемешивали в течение 30 минут. Образовывался осадок твердого вещества, и реакционную смесь фильтровали. Осадок на фильтре промывали водой (20 мл), сушили и концентрировали с получением соединения 38 (1,0 ммоль, с выходом 73,88%) в виде светло-желтого твердого вещества.
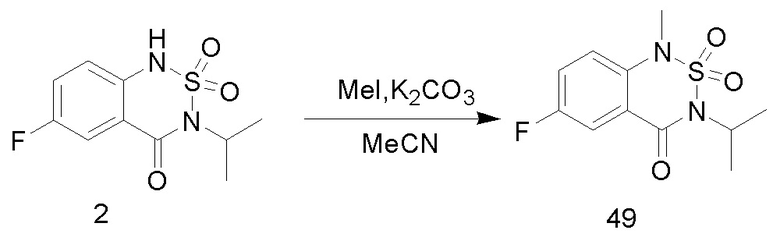
6. Синтез соединений 49
Соединение 2 (0,5 г, 1,94 ммоль), карбонат калия (535 мг, 3,87 ммоль), метилйодид (550 мг, 3,87 ммоль) и ацетонитрил (20 мл) добавляли в одногорлую колбу объемом 50 мл, нагревали до 80°C и перемешивали в течение 6 часов. После практического завершения реакции исходных реагентов, определяемого анализом методом LC-MS, реакционный раствор концентрировали и очищали колоночной хроматографией с получением соединения 49 (200 мг, с выходом 38%) в виде желтого масла.
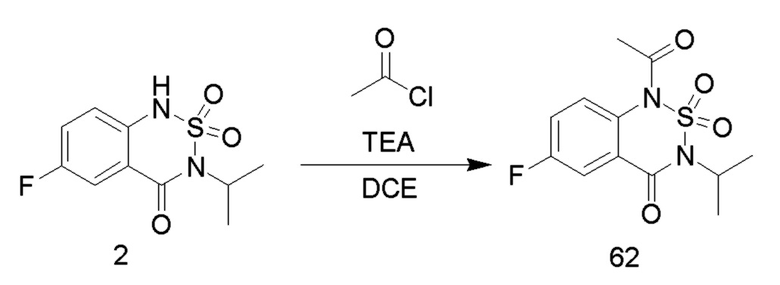
7. Синтез соединений 62
Соединение 1 (0,5 г, 1,94 ммоль), триэтиламин (391 мг, 3,87 ммоль) и 1,2-дихлорэтан (20 мл) добавляли в одногорлую колбу объемом 50 мл, охлаждали до 0-10°C, и медленно добавляли по каплям соединение 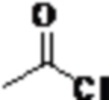 (228 мг, 2,9 ммоль). Реакционный раствор нагревали до комнатной температуры и перемешивали в течение 1 часа. После практического завершения реакции исходных реагентов, определяемого анализом методом LC-MS, реакционный раствор концентрировали и очищали колоночной хроматографией с получением соединения 62 (300 мг, с выходом 51%) в виде белого твердого вещества.
(228 мг, 2,9 ммоль). Реакционный раствор нагревали до комнатной температуры и перемешивали в течение 1 часа. После практического завершения реакции исходных реагентов, определяемого анализом методом LC-MS, реакционный раствор концентрировали и очищали колоночной хроматографией с получением соединения 62 (300 мг, с выходом 51%) в виде белого твердого вещества.
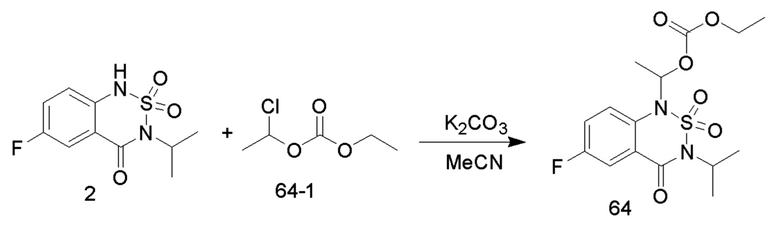
8. Синтез соединений 64
Соединение 2 (0,5 г, 1,94 ммоль), карбонат калия (535 мг, 3,87 ммоль), соединение 64-1 (443 мг, 2,90 ммоль) и ацетонитрил (20 мл) добавляли в одногорлую колбу объемом 50 мл, нагревали до 80°C и перемешивали в течение 6 часов. После практического завершения реакции исходных реагентов, определяемого анализом методом LC-MS, реакционный раствор концентрировали и очищали колоночной хроматографией с получением соединения 64 (300 мг, с выходом 41%) в виде белого твердого вещества.
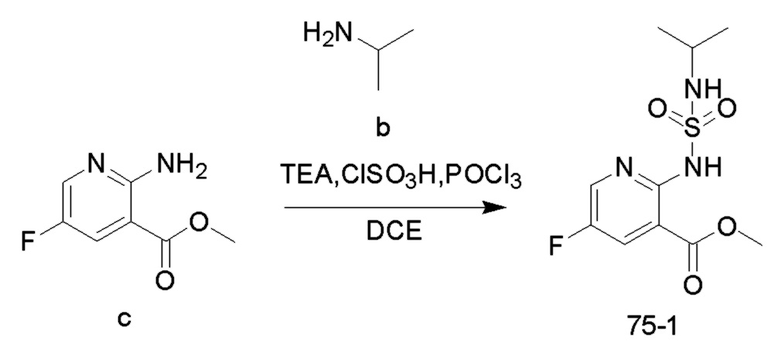
9. Синтез соединений 75
Соединение TEA (5,06 г, 49,96 ммоль), соединение b (1,04 г, 17,63 ммоль) и безводный 1,2-дихлорэтан (20 мл) добавляли в одногорлую колбу объемом 100 мл и охлаждали до 0°C на ледяной бане со льдом. Медленно добавляли по каплям хлорсульфоновую кислоту (1,37 г, 11,75 ммоль) при 0-10°C и перемешивали при 10°C в течение 10 минут, и в реакционную колбу добавляли соединение c (1 г, 5,88 ммоль). Реакционный раствор нагревали до 35°C и перемешивали в течение 30 минут. Добавляли по каплям оксихлорид фосфора (1,35 г, 8,82 ммоль) при 35°C, и реакционный раствор нагревали до 55°C и перемешивали в течение ночи. После практического завершения реакции исходных реагентов, определяемого анализом методом LC-MS, реакционный раствор охлаждали до комнатной температуры. Реакционный раствор промывали насыщенным водным раствором бикарбоната натрия (100 мл x 2), и органическую фазу сушили, концентрировали и очищали колоночной хроматографией с получением соединения 75-1 (1,5 г, 5,15 ммоль, с выходом 87%) в виде желтого масла.
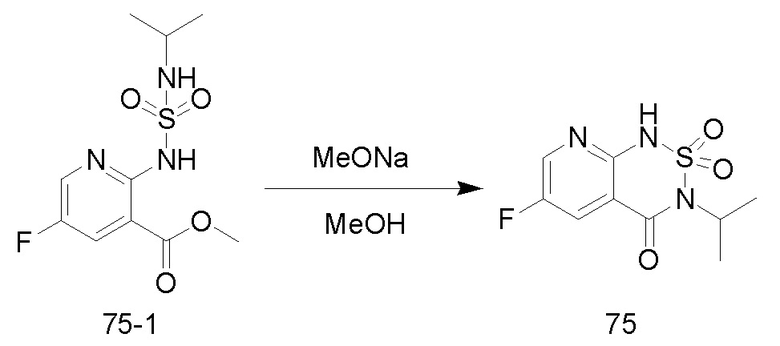
Соединение 75-1 (1,5 г, 5,15 ммоль) растворяли в безводном метаноле (20 мл), добавляли по каплям раствор метоксида натрия (30% метанольный раствор, 1,85 г, 10,30 ммоль) при комнатной температуре, и реакционный раствор нагревали до 65°C для проведения реакции в течение ночи. После завершения реакции исходных реагентов, определяемого анализом методом LC-MS, реакционный раствор концентрировали с удалением метанола, и неочищенный продукт растворяли в воде (50 мл), доводили величину рН до 5-6 с помощью разбавленной хлористоводородной кислоты (1M) и перемешивали в течение 30 минут. Образовывался осадок твердого вещества, и реакционную смесь фильтровали. Осадок на фильтре промывали водой (20 мл), сушили и концентрировали с получением соединения 75 (1 г, с выходом 74,9%) в виде светло-желтого твердого вещества.
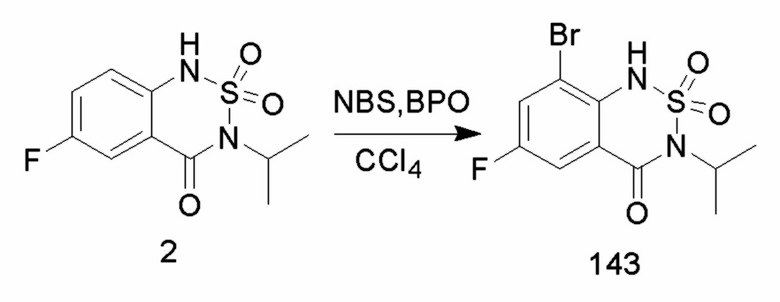
10. Синтез соединений 143
Соединение 2 (0,5 г, 1,94 ммоль), NBS (344 мг, 1,94 ммоль), каталитическое количество BPO (10 мг) тетрахлорид углерода (20 мл) добавляли в одногорлую колбу объемом 50 мл и перемешивали при 80°C в течение 12 часов. После практического завершения реакции исходных реагентов, определяемого анализом методом LC-MS, реакционный раствор охлаждали до комнатной температуры, органическую фазу промывали водным раствором бикарбоната натрия (50 мл x 2) и затем концентрировали, сушили и очищали колоночной хроматографией с получением соединения 143 (300 мг, с выходом 46%) в виде светло-желтого твердого вещества.
11. Синтез соединений 146
Соединение TEA (4,60 ммоль, 45,42 ммоль), соединение b (0,95 г, 16,03 ммоль) и безводный 1,2-дихлорэтан (20 мл) добавляли в одногорлую колбу объемом 100 мл и охлаждали до 0°C на ледяной бане со льдом. Медленно добавляли по каплям хлорсульфоновую кислоту (1,25 г, 10,69 ммоль) при 0-10°C и перемешивали при 10°C в течение 10 минут, и в реакционную колбу добавляли соединение d (1 г, 5,34 ммоль). Реакционный раствор нагревали до 35°C и перемешивали в течение 30 минут. Добавляли по каплям оксихлорид фосфора (1,23 г, 8,02 ммоль) при 35°C, и реакционный раствор нагревали до 55°C и перемешивали в течение ночи. После практического завершения реакции исходных реагентов, определяемого анализом методом LC-MS, реакционный раствор охлаждали до комнатной температуры. Реакционный раствор промывали насыщенным водным раствором бикарбоната натрия (100 мл x 2), и органическую фазу сушили, концентрировали и очищали колоночной хроматографией с получением соединения 146-1 (1,52 г, 4,93 ммоль, с выходом 92,27%) в виде желтого масла.
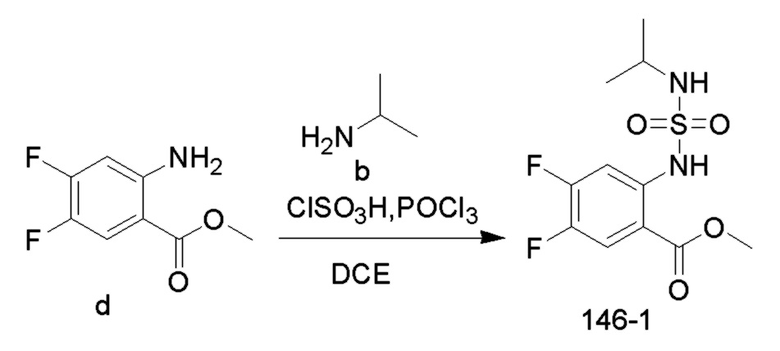
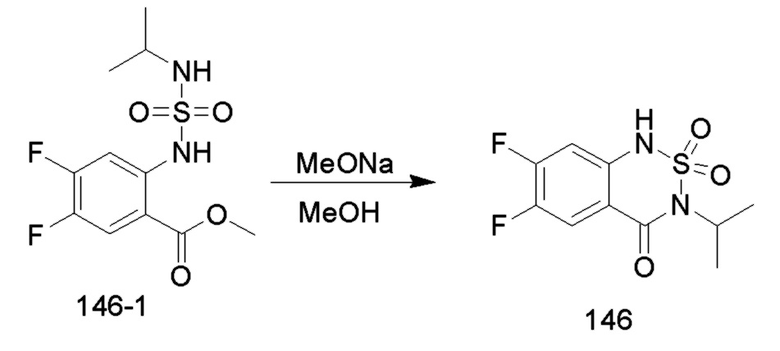
Соединение 146-1 (1,52 г, 4,93 ммоль) растворяли в безводном метаноле (20 мл), добавляли по каплям раствор метоксида натрия (30% метанольный раствор, 1,78 г, 9,86 ммоль) при комнатной температуре, и реакционный раствор нагревали до 65°C для проведения реакции в течение ночи. После завершения реакции исходных реагентов, определяемого анализом методом LC-MS, реакционный раствор концентрировали с удалением метанола, и неочищенный продукт растворяли в воде (50 мл), доводили величину рН до 5-6 с помощью разбавленной хлористоводородной кислоты (1M) и перемешивали в течение 30 минут. Образовывался осадок твердого вещества, и реакционную смесь фильтровали. Осадок на фильтре промывали водой (20 мл), сушили и концентрировали с получением соединения 146 (1,30 ммоль, с выходом 95,5%) в виде светло-желтого твердого вещества.
Оценка биологической активности
Критерии оценки уровня активности соединений по изобретению c точки зрения нанесения ими повреждения растению (то есть подавление скорости роста растения) являются следующими:
уровень 5: подавление скорости роста растения составляет величину большую чем 85%;
уровень 4: подавление скорости роста растения составляет величину большую чем или равную 60% и меньшую чем 85%;
уровень 3: подавление скорости роста растения составляет величину большую чем или равную 40% и меньшую чем 60%;
уровень 2: подавление скорости роста растения составляет величину большую чем или равную 20% и меньшую чем 40%;
уровень 1: подавление скорости роста растения составляет величину большую чем или равную 5% и меньшую чем 20%;
уровень 0: подавление скорости роста растения составляет величину меньшую чем 5%.
Приведенные выше величины подавления скорости роста растения рассчитаны на сырую массу растения.
Эксперимент по уничтожению сорняков в послевсходовый период.
Семена однодольных и двудольных сорняков и семена основных сельскохозяйственных культур (пшеницы, кукурузы, риса, сои, хлопчатника, рапса, просо, сорго) помещали в пластиковые горшки, заполненные почвой, затем засыпали сверху 0,5-2 см почвы, и выращивали в соответствующих тепличных условиях. Через 2-3 недели после посева, испытуемые растения подвергали обработке. Испытываемые соединения по настоящему изобретению соответственно растворяли в ацетоне, затем добавляли Tween 80, разбавляли определенным количеством воды для получения раствора с определенной концентрацией и распыляли из пульверизатора на растения. После обработки, растения выращивали в течение 3 недель в теплице, и затем результаты опытов по уничтожению сорняков были сведены в таблицу 2.
Таблица 2. Результаты по уничтожению сорняков в послевсходовый период
Примечание: норма нанесения активного ингредиента составляла 600 г/га, плюс 450 г воды. N обозначает отсутствие данных. Семена ширицы запрокинутой (Amaranthus retroflexus) собирали в уезде Наньцзян (Nenjiang) провинции Хэйлунцзян (Heilongjiang). Испытания показали, что сорняки были резистентны к обработке гербицидом фомесафеном.
Контрольное соединение A  ; контрольное соединение B
; контрольное соединение B 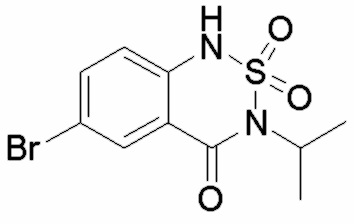 ; контрольное соединение C
; контрольное соединение C 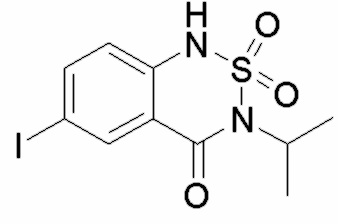 ; контрольное соединение D
; контрольное соединение D 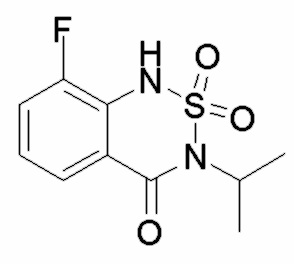 ; контрольное соединение E
; контрольное соединение E 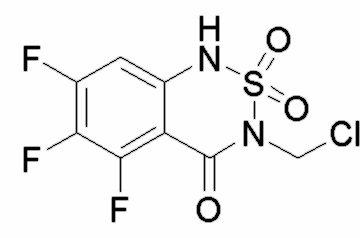 ; контрольное соединение F
; контрольное соединение F 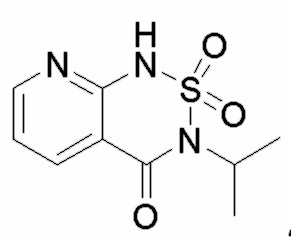 ; контрольное соединение G
; контрольное соединение G 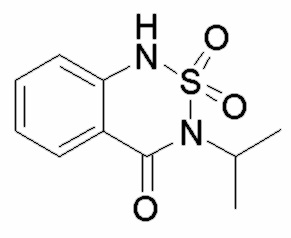 .
.
Ширица запрокинутая (Amaranthus retroflexus) и ширицевые сорняки являются наиболее часто встречающимися сорняками на соевых, кукурузных и рисовых полях. В частности, на полях сои, за исключением высокоэффективных гербицидов на основе ингибитора протопорфириногеноксидазы, действие применяемых в основном гербицидов, таких как бентазон, кломазон, клорансулам-метил, имазетапир и имазамокс, является неэффективным. В последние годы, в Северо-Восточном Китае широко распространяется ширица запрокинутая (Amaranthus retroflexus), которая становится все более и более резистентной к фомесафену, и эффективные методы борьбы с этим сорняком в настоящее время отсутствуют. По сравнению с бентазоном, соединение по настоящему изобретению обладает более высокой гербицидной активностью в отношении злаковых сорняков и широколистных сорняков, особенно они оказывают исключительное действие на основные ширицевые сорняки, такие как ширица запрокинутая (Amaranthus retroflexus), с высокой селективностью, что позволяет более эффективно решать проблемы борьбы с сорняками на полях таких культур, как соя, кукуруза, рис или пшеница.
Эксперимент по уничтожению сорняков в довсходовый период.
Семена однодольных и двудольных сорняков и основных сельскохозяйственных культур (например, пшеницы, кукурузы, риса, сои, хлопчатника, рапса, проса и сорго) помещали в пластиковый горшок с почвой и засыпали сверху слоем почвы 0,5-2 см. Испытуемые соединения по настоящему изобретению растворяли в ацетоне, затем добавляли Tween 80, разбавляли определенным количеством воды до достижения определенной концентрации и разбрызгивали сразу после посева. Получаемые семена инкубировали в течение 4 недель в теплице после разбрызгивания и наблюдали за результатами испытаний. Было обнаружено, что гербицид в основном оказывал исключительное действие при норме внесения 250 г/га, особенно в отношении таких сорняков, как ежовник обыкновенный (Echinochloa crus-gali), росичка кроваво-красная (Digitaria sanguinalis) и канатник Теофраста (Abutilon theophrasti) и другие подобные сорняки). Многие соединения обладали высокой селективностью в отношении кукурузы, пшеницы, риса, сои и других сельскохозяйственных культур.
Эксперименты с основными сорняками на пшеничных и рисовых полях показывают, что соединение по настоящему изобретению обычно обладает высокой эффективностью в борьбе с сорняками. Прежде всего, отмечено, что соединения по изобретению обладают чрезвычайно высокой активностью в отношении широколиственных сорняков и циперовых сорняков, которые резистентны к ингибитору ацетолактат-синтазы (ALS), таких как стрелолист трехлистный (Sagittaria trifolia), камыш (Scirpus juncoides), сыть разнородная (Cyperus difformis), дескурайния Софии (Descurainia Sophia), пастушья сумка обыкновенная (Capsella bursa-pastoris), воробейник полевой (Lithospermum arvense), подмаренник цепкий (Galium aparine L.), сыть круглая (Cyperus rotundus L.) и другие подобные сорняки, и имеют исключительно важное значение для экономики сельского хозяйства.
Оценка безопасности рассадного риса и оценка борьбы с сорняками на рисовом поле.
Почву, взятую с рисового поля, загружали в горшок, площадь которого составляла 1/1000000 га. Высевали семена ежовника обыкновенного (Echinochloa crus-gali), камыша (Scirpus juncoides) и череды трехраздельной (Bidens tripartita L.) и аккуратно засыпали их почвой, затем выдерживали в теплице при запасе воды на глубине 0,5-1 см. На следующий день или через 2 дня высаживали клубень стрелолиста трехлистного (Sagittaria trifolia). Затем все это выдерживали при запасе воды на глубине 3-4 см. Сорняки подвергали обработке путем обрызгивания с помощью пипетки препаратом смачивающегося порошка (WP) или концентрата суспензии (SC) в водных разбавителях, приготовленных в соответствии с обычным способом приготовления соединений по настоящему изобретению, до достижения указанного эффективного количества, когда Echinochloa crus-galli, Scirpus juncoides и Bidens tripartita L. достигали стадии образования 0,5 листа и Sagittaria trifolia достигал момента образования первого листа.
Кроме того, почву с рисового поля, загруженную в горшок, площадь которого составляла 1/1000000 га, выравнивали с сохранением запаса воды на глубине 3-4 см. Рис в стадии 3 листа (рис японский) пересаживали на глубину 3 см на следующий день. Соединение по настоящему изобретению вносили в почву таким же образом через 5 дней после пересадки риса.
Определяли визуально состояние репродуктивной функции Echinochloa crus-galli, Scirpus juncoides, Bidens tripartita L. и Sagittaria trifolia через 14 дней после обработки соединением по изобретению и состояние репродуктивной функции риса через 21 день после обработки соединением по изобретению, соответственно. Оценивали эффект борьбы с сорняками при указанном выше стандартном уровне активности. Многие соединения демонстрировали исключительно высокую активность и селективность.
Примечание: семена Echinochloa crus-gali, Scirpus juncoides, Sagittaria trifolia и Bidens tripartita L. были собраны в китайской провинции Хэйлунцзян. Испытания показали, что сорняки были резистентны к обычным дозам пиразосульфурон-этила.
В то же время, после проведения нескольких испытаний было обнаружено, что соединения и композиции по настоящему изобретению обладают высокой селективностью по отношению ко многим злаковым травам, таким как зоизия японская, бермудская трава, овсяница тростниковая, мятлик, плевел и морской паспалум и другие подобные злаковые травы, и они позволяют проводить борьбу с многими важными злаковыми сорняками и широколистными сорняками. Соединения также показали превосходную селективность и высокую значимость для экономики сельского хозяйства при испытаниях на сахарном тростнике, сое, хлопке, масличном подсолнечнике, картофеле, в фруктовых садах и на овощах при различных способах применения гербицидов.
Изобретение относится к диоксиду замещенного тиадиазинона, представленному общей формулой I, где R1 и R2 каждый независимо представляет водород, C1-C8 алкил, C2-C8 алкенил, C2-C8 алкинил, C3-C8 циклоалкил, C3-C8 циклоалкил-C1-C8 алкил, формил-C1-C8 алкил или гидроксил-C1-C8 алкил с галогеном или без галогена; арил, арил-C1-C8 алкил, гетероциклил, гетероциклил-C1-C8 алкил, R3-O-(C1-C8 алкил)n-, R3-(CO)-(C1-C8 алкил)n-, R3-(CO)-O-(C1-C8 алкил)n-, R3-O-(C1-C8 алкил)n-(CO)-, R3-S-(CO)-(C1-C8 алкил)n-, R3-O-(CO)-(C1-C8 алкил)-, R3-O-(CO)-O-(C1-C8 алкил)-, R3-SO2-(C1-C8 алкил)n-, R4R5N-(CO)-, R4R5N-(C1-C8 алкил)n-, R3-(CO)-NR6- или R4R5N-(CO)-NR6-; каждый R3 независимо представляет C1-C8 алкил, C2-C8 алкенил или C3-C8 циклоалкил с галогеном или без галогена; R4, R5, R6 каждый независимо представляет водород, C1-C8 алкил с галогеном или без галогена; n представляет 0 или 1; X представляет водород или галоген; Y представляет C-Z или N; Z представляет водород или галоген; и когда X представляет галоген, Z представляет водород; «арил» представляет собой фенил; «гетероциклил» представляет собой 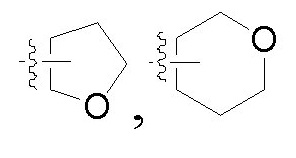 или «гетероарил», и «гетероарил» представляет собой ароматическую циклическую группу, имеющую 5 или 6 атомов в кольце и от 1 до 4 гетероатомов в кольце, которые выбраны из группы, состоящей из кислорода, азота и серы; "арил" или "гетероциклил" является незамещенным или замещен с помощью, по меньшей мере, одной из следующих групп: галоген, меркапто, гидроксил, C1-C8 алкил, OR" или SR" с галогеном или без галогена; каждый R” независимо представляет C1-C8 алкил. Изобретение также относится к гербицидной композиции и способу борьбы с сорняками на основе указанного соединения. Технический результат: получено новое соединение и гербицидная композиция на его основе, которые могут найти применение в сельском хозяйстве для борьбы с сорняками. 5 н. и 5 з.п. ф-лы, 2 табл.
или «гетероарил», и «гетероарил» представляет собой ароматическую циклическую группу, имеющую 5 или 6 атомов в кольце и от 1 до 4 гетероатомов в кольце, которые выбраны из группы, состоящей из кислорода, азота и серы; "арил" или "гетероциклил" является незамещенным или замещен с помощью, по меньшей мере, одной из следующих групп: галоген, меркапто, гидроксил, C1-C8 алкил, OR" или SR" с галогеном или без галогена; каждый R” независимо представляет C1-C8 алкил. Изобретение также относится к гербицидной композиции и способу борьбы с сорняками на основе указанного соединения. Технический результат: получено новое соединение и гербицидная композиция на его основе, которые могут найти применение в сельском хозяйстве для борьбы с сорняками. 5 н. и 5 з.п. ф-лы, 2 табл.
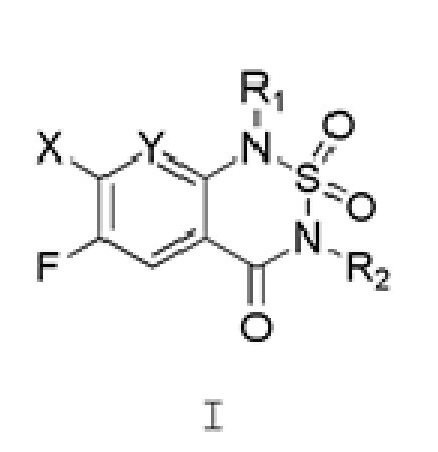
1. Диоксид замещенного тиадиазинона, представленный общей формулой I:
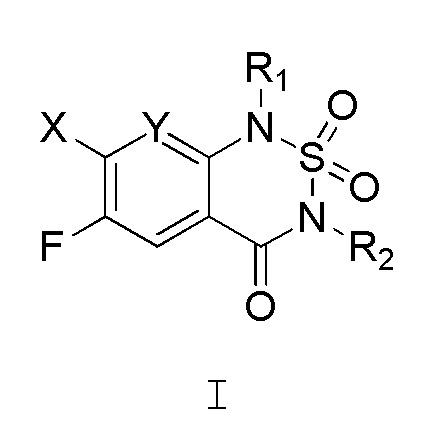
где
R1 и R2 каждый независимо представляет водород, C1-C8 алкил, C2-C8 алкенил, C2-C8 алкинил, C3-C8 циклоалкил, C3-C8 циклоалкил-C1-C8 алкил, формил-C1-C8 алкил или гидроксил-C1-C8 алкил с галогеном или без галогена; арил, арил-C1-C8 алкил, гетероциклил, гетероциклил-C1-C8 алкил, R3-O-(C1-C8 алкил)n-, R3-(CO)-(C1-C8 алкил)n-, R3-(CO)-O-(C1-C8 алкил)n-, R3-O-(C1-C8 алкил)n-(CO)-, R3-S-(CO)-(C1-C8 алкил)n-, R3-O-(CO)-(C1-C8 алкил)-, R3-O-(CO)-O-(C1-C8 алкил)-, R3-SO2-(C1-C8 алкил)n-, R4R5N-(CO)-, R4R5N-(C1-C8 алкил)n-, R3-(CO)-NR6- или R4R5N-(CO)-NR6-;
каждый R3 независимо представляет C1-C8 алкил, C2-C8 алкенил или C3-C8 циклоалкил с галогеном или без галогена;
R4, R5, R6 каждый независимо представляет водород, C1-C8 алкил с галогеном или без галогена;
n представляет 0 или 1;
X представляет водород или галоген; Y представляет C-Z или N; Z представляет водород или галоген; и когда X представляет галоген, Z представляет водород;
«арил» представляет собой фенил; «гетероциклил» представляет собой 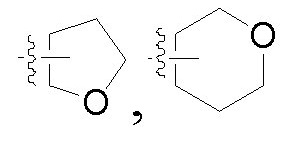 или «гетероарил», и «гетероарил» представляет собой ароматическую циклическую группу, имеющую 5 или 6 атомов в кольце и от 1 до 4 гетероатомов в кольце, которые выбраны из группы, состоящей из кислорода, азота и серы; "арил" или "гетероциклил" является незамещенным или замещен с помощью, по меньшей мере, одной из следующих групп: галоген, меркапто, гидроксил, C1-C8 алкил, OR" или SR" с галогеном или без галогена;
или «гетероарил», и «гетероарил» представляет собой ароматическую циклическую группу, имеющую 5 или 6 атомов в кольце и от 1 до 4 гетероатомов в кольце, которые выбраны из группы, состоящей из кислорода, азота и серы; "арил" или "гетероциклил" является незамещенным или замещен с помощью, по меньшей мере, одной из следующих групп: галоген, меркапто, гидроксил, C1-C8 алкил, OR" или SR" с галогеном или без галогена;
каждый R” независимо представляет C1-C8 алкил.
2. Диоксид замещенного тиадиазинона по п. 1, отличающийся тем, что:
R1 и R2 каждый независимо представляет водород, C1-C6 алкил, C2-C6 алкенил, C2-C6 алкинил, C3-C6 циклоалкил, C3-C6 циклоалкил-C1-C6 алкил, формил-C1-C6 алкил или гидроксил-C1-C6 алкил с галогеном или без галогена; арил, арил-C1-C6 алкил, гетероциклил, гетероциклил-C1-C6 алкил, R3-O-(C1-C6 алкил)n-, R3-(CO)-(C1-C6 алкил)n-, R3-(CO)-O-(C1-C6 алкил)n-, R3-O-(C1-C6 алкил)n-(CO)-, R3-S-(CO)-(C1-C6 алкил)n-, R3-O-(CO)-(C1-C6 алкил)-, R3-O-(CO)-O-(C1-C6 алкил)-, R3-SO2-(C1-C6 алкил)n-, R4R5N-(CO)-, R4R5N-(C1-C6 алкил)n-, R3-(CO)-NR6- или R4R5N-(CO)-NR6-;
каждый R3 независимо представляет C1-C6 алкил, C2-C6 алкенил или C3-C6 циклоалкил с галогеном или без галогена;
R4, R5 и R6 каждый независимо представляет водород, C1-C6 алкил с галогеном или без галогена;
n представляет 0 или 1;
X представляет водород или галоген; Y представляет C-Z или N; Z представляет водород или галоген; и когда X представляет галоген, Z представляет водород;
«арил» представляет собой фенил; «гетероциклил» представляет собой 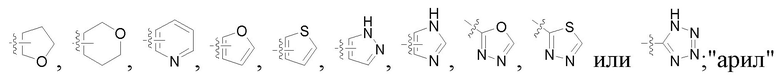
или "гетероциклил" является незамещенным или замещен с помощью, по меньшей мере, одной из следующих групп: галоген, меркапто, гидроксил; C1-C6 алкил, OR" или SR" с галогеном или без галогена;
каждый R” независимо представляет C1-C6 алкил.
3. Диоксид замещенного тиадиазинона по пп. 1-3, отличающийся тем, что:
R1 и R2 каждый независимо представляет водород; C1-C6 алкил, C2-C6 алкенил или C2-C6 алкинил с галогеном или без галогена; арил C1-C6 алкил, R3-O-(C1-C6 алкил)n-, R3-(CO)-(C1-C6 алкил)n-, R3-O-(C1-C6 алкил)n-(CO)-, R3-S-(CO)-(C1-C6 алкил)n-, R3-O-(CO)-(C1-C6 алкил)-, R3-O-(CO)-O-(C1-C6 алкил)-, R3-SO2-(C1-C6 алкил)n-, R4R5N-(CO)-;
каждый R3 независимо представляет C1-C6 алкил, C2-C6 алкенил или C3-C6 циклоалкил с галогеном или без галогена;
R4, R5 каждый независимо представляет водород; C1-C6 алкил с галогеном или без галогена;
n представляет 0 или 1;
X представляет водород или галоген; Y представляет C-Z или N; Z представляет водород или галоген; и когда X представляет галоген, Z представляет водород;
«арил» представляет фенил; «арил» является незамещенным или замещен с помощью, по меньшей мере, одной из следующих групп: меркапто, гидроксил, OR", SR";
каждый R” независимо представляет C1-C6 алкил.
4. Диоксид замещенного тиадиазинона по любому одному из пп. 1-3, отличающийся тем, что:
R1 представляет водород, C1-C6 алкил, C2-C6 алкенил, C2-C6 алкинил; арил-C1-C3 алкил, R3-O-(C1-C3 алкил)n-, R3-(CO)-(C1-C3 алкил)n-, R3-O-(C1-C3 алкил)n-(CO)-, R3-S-(CO)-(C1-C3 алкил)n-, R3-O-(CO)-O-(C1-C3 алкил)-, R3-SO2-(C1-C3 алкил)n- или R4R5N-(CO)-;
R2 представляет C1-C6 алкил;
каждый R3 независимо представляет C1-C6 алкил, C2-C6 алкенил или C3-C6 циклоалкил с галогеном или без галогена;
R4, R5 каждый независимо представляет C1-C6 алкил;
n представляет 0 или 1;
X представляет водород или фтор, Y представляет C-Z или N, Z представляет водород, фтор, хлор, бром или йод, и когда X представляет фтор, Y представляет C-Z, и Z представляет водород;
«арил» представляет собой фенил; «арил» является незамещенным или замещен по меньшей мере одной из следующих групп: OR”;
каждый R” независимо представляет C1-C6 алкил.
5. Диоксид замещенного тиадиазинона по любому одному из пп. 1-3, отличающийся тем, что его выбирают из:

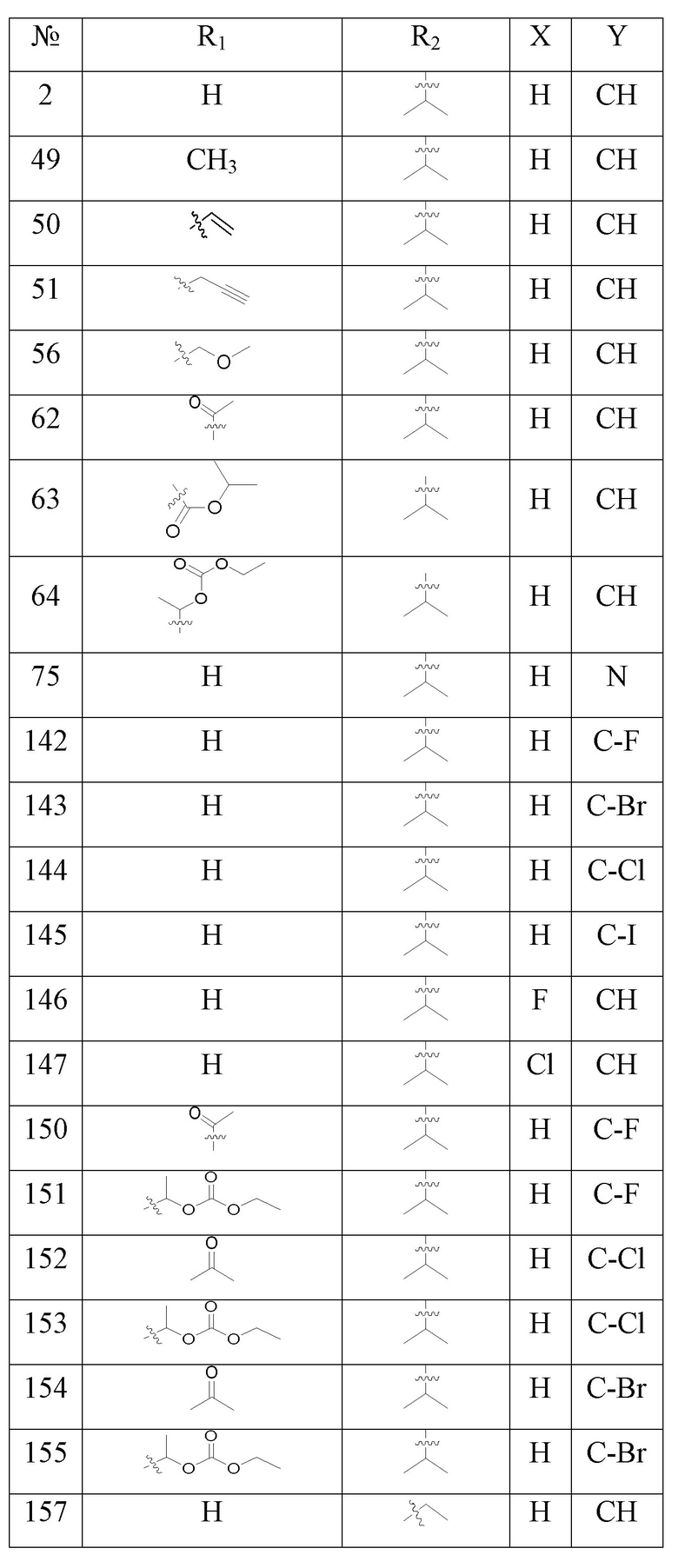
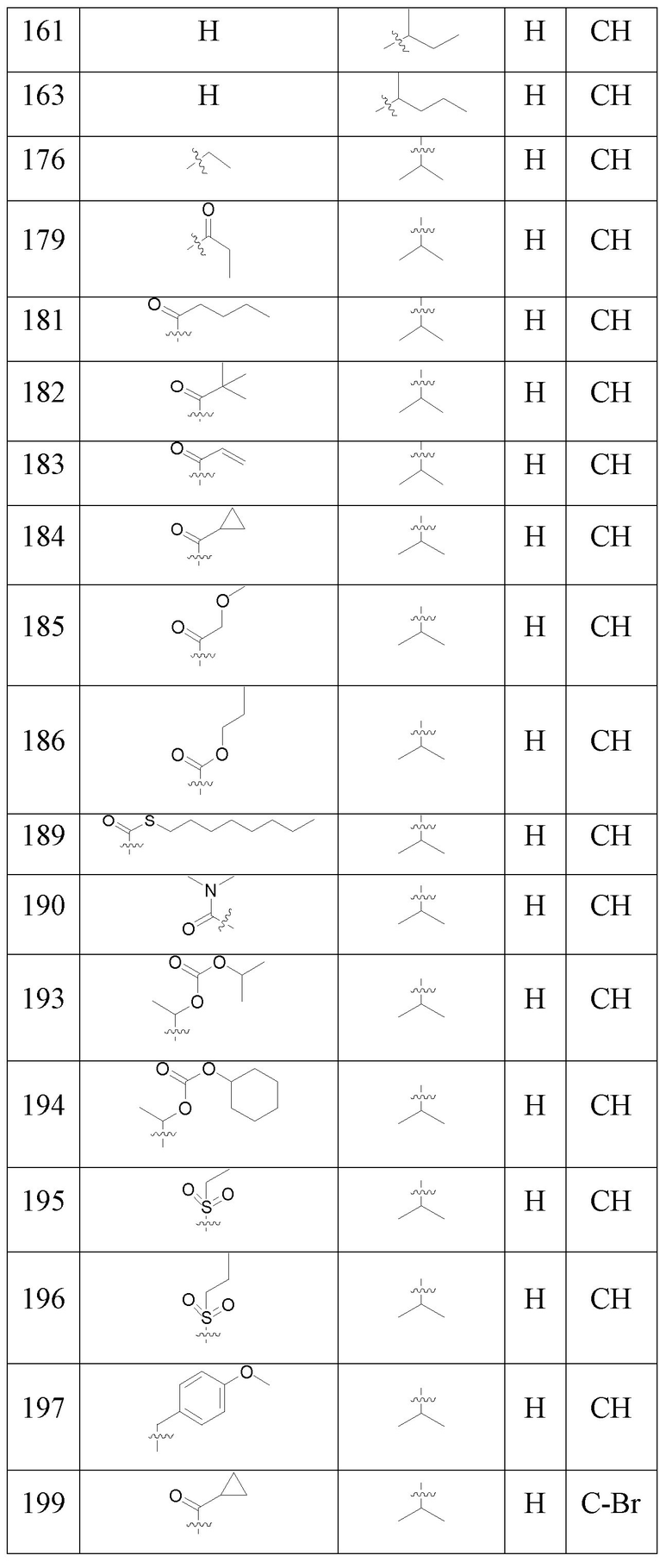
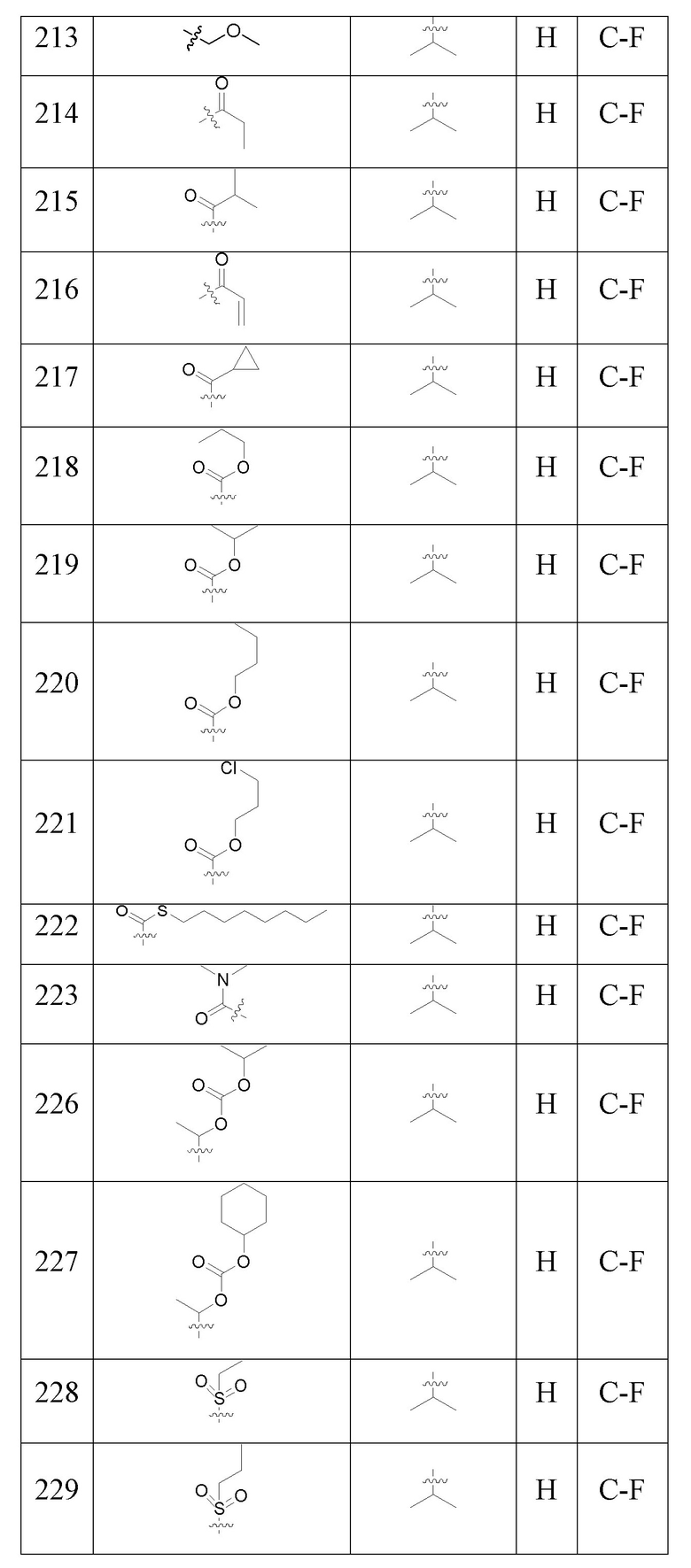
6. Способ получения диоксида замещенного тиадиазинона по любому одному из пп. 1-5, отличающийся тем, что
в случае, когда R2 в общей формуле I представляет собой R2', способ получения включает следующие стадии:
(1') получение соединения общей формулы II-2 из соединения общей формулы III в присутствии 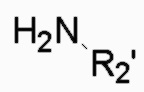 , электрофильного реагента
, электрофильного реагента 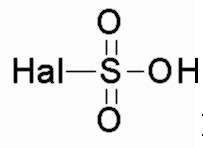 и дегидратирующего реагента;
и дегидратирующего реагента;
(2') проведение реакции внутримолекулярной циклизации соединения общей формулы II-2 с получением соединения общей формулы I-3;
(3') проведение реакции алкилирования соединения общей формулы I-3 и R1'-L с получением соединения общей формулы I-4;
где Hal и L каждый независимо представляет галоген; R1' и R2' соответственно представляют значения для R1 и R2 по любому одному из пп. 1-5, исключая водород; X и Y определены в одном любом из пп. 1-5;
схема химической реакции может быть представлена в следующем виде:
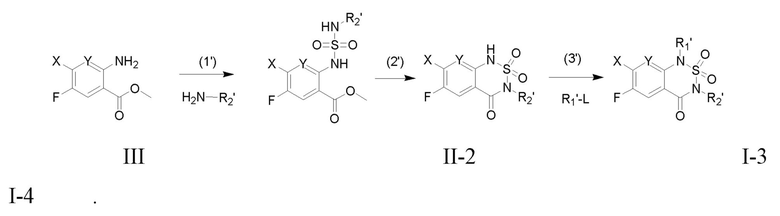
7. Способ получения диоксида замещенного тиадиазинона по п. 6, отличающийся тем, что стадии (1'), (2') и (3') все проводят в присутствии оснований и органических растворителей; каждое из оснований независимо выбирают из неорганических оснований или органических оснований; каждый из органических растворителей независимо выбирают из метанола, этанола, ацетонитрила, дихлорэтана, DMF, DMSO, диоксана, дихлорметана или этилацетата.
8. Гербицидная композиция для борьбы с сорняками, содержащая гербицидно эффективную дозу по меньшей мере одного диоксида замещенного тиадиазинона по любому одному из пп. 1-5.
9. Способ борьбы с сорняками, включающий нанесение гербицидно эффективной дозы по меньшей мере одного из диоксидов замещенного тиадиазинона по любому одному из пп. 1-5 или гербицидной композиции по п. 8 на растение или пораженный сорняками участок.
10. Применение по меньшей мере одного из диоксидов замещенного тиадиазинона по любому одному из пп. 1-5 или гербицидной композиции по п. 8 для борьбы с сорняками.
| US 4158559 A1, 19.06.1979 | |||
| US 3940389 A1, 24.02.1976 | |||
| Гербицидный состав | 1972 |
|
SU472489A3 |
| ГЕРБИЦИДНЫЙ СОСТАВ | 1970 |
|
SU416918A3 |
| ГЕРБИЦИДНЫЙ СОСТАВ | 0 |
|
SU404188A1 |
Авторы
Даты
2024-01-30—Публикация
2020-09-01—Подача