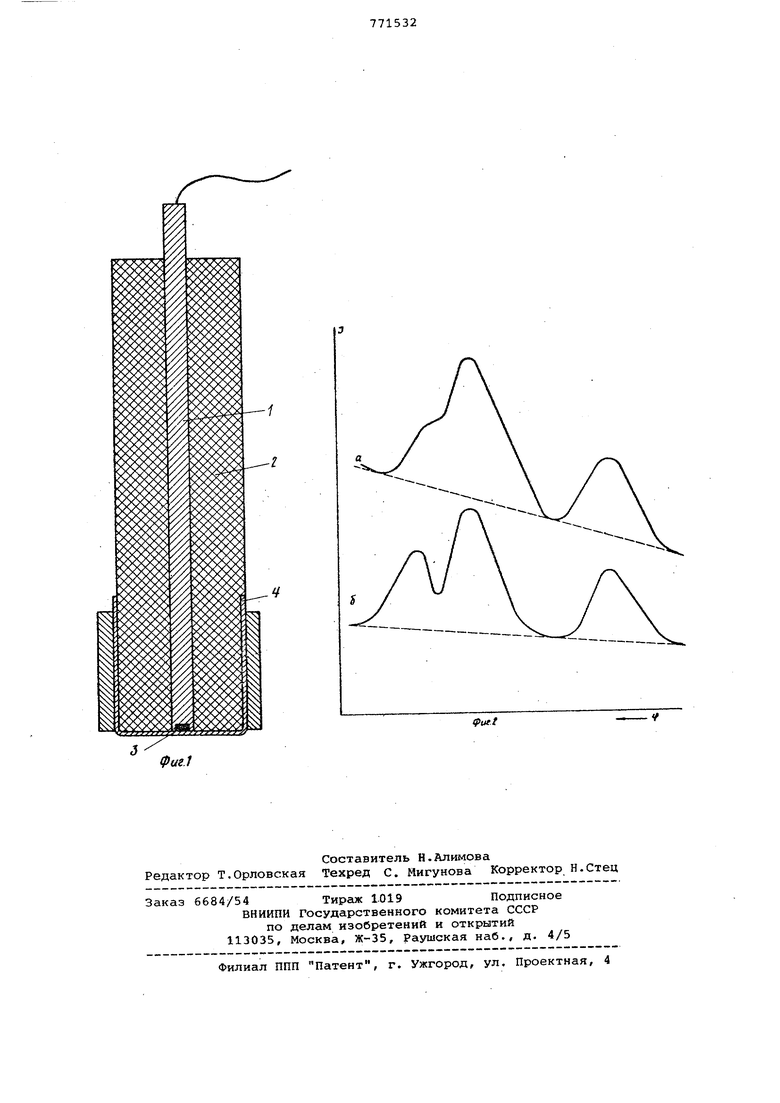
Изобретение относится к электроаналитической технике и может быть использовано при разработке высокочувствительных методов анализа с предварительным электролитическим конценурированием определяемых вещес на стационарном электроде. Известен амальгамный электрод для определения сконцентрированных примесей. Однако при снятии полярограмм наблюдается взаимное влияние определяемых веществ, что приводит к ошибкам при их определении из-за наложения токов электроокисления 1. Наиболее близким техническим реше нием к предложенному является стацио нарный ртутный электрод для одновременного определения нескольких вещес в анализируемой смеси, представляющи собой каплю или пленку ртути, нанесенную на подходящую основу, наприме торец серебряного стержня с изолированной боковой поверхностью 2 . Недостатком этого электрода является то, что в присутствии нескольки определяемых веществ пики анодных токов этих веществ плохо разделяются перекрываются или накладываются друг на друга, что сильно затрудняет определение веществ, а иногда делает невозможным их раздельное определение. Цель изобретения - повышение разрешающей способности электрода путем выделения сигналов отдельных веществ и устранение ошибок при определении веществ. Цоставленная цель достигается тем, что в электроде, состоящем из серебряного стержня с изолированной боковой поверхностью, в торце серебряного стержня выполняют углубление, которое заполняют ртутью и сверху накрывают пленкой из материала, набухающего в электролите и пропускающего ионы. На фиг. 1 показан предложенный электрод в разрезе; на фиг. 2 - сравнительные характеристики разрешающей способности электрода - прототипа (кривая а) и предложенного электрода (кривая б). Стационарный ртутный электрод состоит из серебряного стержня 1 диаметром 2 мм, запрессованного в изолирующую оболочку 2, например тефлоновую. В торце стержня выполнено углубление 3 для ртути размером 0,05-0,21УМ, которое закрыто тонкой пленкой 4 из
материала, набухающего в электролите и пропускающего ионы, например, из целлофана, закрепленной на электроде.
Электрод работает следующим образом. Для определения веществ в анализируемой смеси электрод помещак1т в электролитическую ячейку в которую опускают второй стандартный электрод, например каломельный, и наливают анализируемый раствор. Затем при достаточном отрицательном потенциале (1,4-1,6 в) и перемешивании раствора ведут длительное электролитическое концентрирование определяемых веществ после окончания которого прекращают перемешивание раствора и проводят электроокисление накопившегося вещества при линейном уменьшении потенциала от потенциала накопления до нуля. При этом нокопившиеся вещества последовательно окисляются и на полярограмме появляются анодные пики тока. По величине анодных пиков электроокисления веществ определяют концентрации или количества анализируемых веществ.
Наличие тонкой пленки в предлагаемой конструкции электрода создает особые условия диффузии вещества к электроду и от электрода, благодаря которым всю систему можно назйать квазитонкослойной. Эти условия приводят к четкому разделению определяемых пиков электроокисления и ПовьЕпению разрешающей способности электрода. Кроме того, наличие тонкой плен ки расширяет возможности использования электрода. Электрод предложенной конструкции может быть использован для анализа мутных растворов, так как на него не оказывают влияния присутствующие в растворе твердые частицы (суспензии).
В качестве примера можно привести определение кадмия и таллия при совместном присутствии их в смеси кадмий, таллий, цинк. В качестве фона при определении использовался 1 М водный раствор хлорида калия с добавкой сульфида натрия для удаления растворенного кислорода.
Концентрации таллия, кадмия и цинка по I-IO- м/л. В качестве стандартного электрода использовали каломельный электрод. Потенциал накопления 1,5 В, время накопления 7 мин. Скорость изменения потенциала при электроокислении 200 мв/мин.
На фиг. 2 видно, что с электродомпрототипом пики кадмия и таллия совершенно не разделяются и одновременное определение их невозможно; при использовании предложенного электрода разрешение чёткое, возможно пря-г мое и легкое одновременное определение кадмия и таллия.
В таблице приведена сравнительная количественная характеристика разрешающей способности предложенного электрода и электрода-прототипа. Для ха рактеристики использован критерий Рекка. Значение этого критерия, равное 1, соответствует полному разделению определяемых пиков, а значение, равное О, - полному их слиянию.
Условия анализа концентрации анализируемых веществ
Фон 1 М КС1 с добавкой , концентрации кадмия,таллия,цинка по 1-10 м/л, потенциал накопления - 15 В,время накопления 7 мин, скорость изменения потенциала 200 мв/мин.
Фон 0,1 М NH40H+ +0,1 М МНдС, концентрации кадмия,таллия,цинка по м/л. Потенциал накопления - 1,3 В,время накопления 3 миН, скорость изменения потенциала 200 мВ/мин
Из таблицы видно, что предложенны электрод обладает существенно большей разделяющей способностью.
Формула изобретения
стационарный ртутный электрод для полярографического анализа, состоящий из серебряного стержня с изолированной боковой поверхностью, на торец которого нанесена, ртуть, отличающийся тем, что, с целью повышения разрешающей способности, в торце серебряного стержня выполнено углубление, в которое помещена ртуть закрытое проницаемой для ионов и обЛсодающей способностью набухать в электролите пленкой.
Источники информации, принятые во внимание при экспертизе
1.Авторское свидетельство СССР № 441503, кл. G 01 N 27/30, 1973.
2.Сб. Полярография проблемы и перспективы. Рига, изд. Знание, 1977, с. 229-241 (прототип).
ut.t

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ ВИСМУТА В ВОДНЫХ РАСТВОРАХ МЕТОДОМ ИНВЕРСИОННОЙ ВОЛЬТАМПЕРОМЕТРИИ ПО ПИКАМ СЕЛЕКТИВНОГО ЭЛЕКТРООКИСЛЕНИЯ ВИСМУТА ИЗ ИНТЕРМЕТАЛЛИЧЕСКОГО СОЕДИНЕНИЯ AuBi | 2011 |
|
RU2478944C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ТАЛЛИЯ В ВОДНЫХ РАСТВОРАХ И ТЕХНОЛОГИЧЕСКИХ СЛИВАХ МЕТОДОМ ИНВЕРСИОННОЙ ВОЛЬТАМПЕРОМЕТРИИ | 2011 |
|
RU2494386C2 |
| Способ вольтамперометрического анализа | 1978 |
|
SU748222A1 |
| СПОСОБ ИНВЕРСИОННОГО ВОЛЬТАМПЕРОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ МИКРОПРИМЕСЕЙ МЕДИ (II) И СУРЬМЫ (III) В ЦИНКОВОМ ЭЛЕКТРОЛИТЕ | 2004 |
|
RU2297626C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ОСМИЯ ИНВЕРСИОННО-ВОЛЬТАМПЕРОМЕТРИЧЕСКИМ МЕТОДОМ В ПРИРОДНОМ И ТЕХНОГЕННОМ СЫРЬЕ НА ГРАФИТОВОМ ЭЛЕКТРОДЕ, МОДИФИЦИРОВАННОМ ЗОЛОТОМ | 2012 |
|
RU2490624C1 |
| ВОЛЬТАМПЕРОМЕТРИЧЕСКИЙ СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ L-ТИРОКСИНА | 2010 |
|
RU2428690C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ИОНОВ ИНДИЯ (III) В ТЕХНОЛОГИЧЕСКИХ РАСТВОРАХ СВИНЦОВО-ЦИНКОВОГО ПРОИЗВОДСТВА | 2009 |
|
RU2414701C2 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ЙОДА | 2002 |
|
RU2206086C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ЙОДА МЕТОДОМ ИНВЕРСИОННОЙ ВОЛЬТАМПЕРОМЕТРИИ | 2011 |
|
RU2459199C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПЛАТИНЫ В РУДАХ МЕТОДОМ ИНВЕРСИОННОЙ ВОЛЬТАМПЕРОМЕТРИИ | 2010 |
|
RU2426108C1 |


Авторы
Даты
1980-10-15—Публикация
1978-12-06—Подача