(54) ПОЛИМЕРНАЯ КОМПОЗИЦИЯ НИЛ с 3-4 С-атомами, бензил, алканоил с 2С-атомами или ашкеноил с 2-3 С-атомами} гидроксибензильная группа формулы где R и R - ал кил с 1-8 С-атомами R® - водород или метил, ЯТеслип-) - алкил с 1-20 С-атомам или алкил с 1-4 С-ато мамизамещенный группой -С(0) R{0) (),-, где R обозначает алки b 1-18 С-атомами, или группа форму Кь Key -/ -Е01) -/ где ft° - алкил с 1-4 С-атомами, а Y-0- или -NR-, или Я оэначает алкенил с 3-8 Cмами,а{ алкил с 7-9 С-атомами, фенил группу формулы IN, группу .формулы -O-C-{O)R или -MH-C(0)R где R может быть алкил с 1-12 С-а мами, фенил или замещенная двумя С -алкильными группами и гидро сильной группой фенил или фенилзти ловая группа, или группа формулы -СНз,-С(СО-У-к) 1 где R2 обозначает алкильный радикал с 1-6 С-атомами, бензил, -0-C-(0)R -NH-C(O)R или R , аR представля ет остаток формулы III , или Ri (если означает пряму связь,алкилен с 1--20 С-атомами, алкенилен с 4-6 С-атомами или арен-бис-алкилен с 8-14 С-атсяиами, при следующем соотношении компонентов, вес.%: Полимер99,0-99,98 Производное эфира гидроксибензил- малоновой кислоты 0,02-1,0 Получение соединений формулы I осуществляют с помощью различных сп собов, которые состоят из нескольки отдельных стадий, осуществляемых в различной последовательности. Отдельные стадии представляют собой известные реакции, прежде всего такие, которые известны из химии произво;цных малоновой кислоты. В качестве пластических масс могут быть применены полиэтилен высокой и низкой плотности, полипропи- I лек,сополимеры этилена и пропилена, полистирол, сополимеры стирола, бутадиена и акрилонитрила, смеси полиолефинов или полимеров стирола, поли.уреганы на основе простых или сложных полиэфиров в виде лаков, эластомеров или пенопластов. Стабилизаторы добдвляют к пластическим массам в концентрации 0,011 see. %,предпочтительно О ,2гО,6 вес; % в расчете на количество материала, подвергаемого стабилизации. Стабилизаторы вводят после полимеризации, например в расплав обычно используемыми в технике способами, до или во время формования, или же наносят (растворенные или диспергированные) на полимер, в некоторых случаях при последующем испарении растворителя. Новые соединения также могут быть добавлены к стабилизируемой пластической массе в форме маточной смеси, которая содержит эти соединения, например, в концентрации 2,525 вес.%. В случае сшитого полиэтилена стабилизирующие соединения добавляют к полиэтилену перед сшиванием . Кроме соединений формулы 1, к пластическим массам дополнительно могут быть прибавлены другие известные стабилизаторы и состабилизаторы. В качестве подобных добавок могут быть применены, например, антиокислители, средства, защищающие полимер от действия света, или металлические дезактиваторы, или такие состабилизаторы, как например, состабилизаторы типа эфиров фосфористой кислоты. Кроме того, могут быть добавлены обычные в технологии пластических масс средства, например огнезащитные, антистатические, пластификаторы, мягчители, порообразователи, пигменты, наполнители или усилители. Стабилизированные указанным способом пластические массы могут быть применены в самых различных формах, например, в виде пленок, волокон, лент,,профилированных изделий или в виде связующего для лаков, клеящих веществ или замазок. Получение и применение соединений формулы 1 дано в примерах. Примеры 1-32. 23,3 г (0,05 моль) диэфира (1,2,2,6,б-пентаметил-4-11Иперидинил)бутилмалоновой кислоты и 13,2 г (0,05 моль) N-(3,5-ди-трет-бутил-4--гидроксибензил)диметиламина растворяют в 200 мл толуола. После добавления 0,25 г амида лития смесь нагревают в течение 4 ч с обратным холодильником. После охЛс1жления ее нейтрализуют 1,5 мл 1%-ной уксусной кислоты и пpo вJвaют
органическую фазу несколько раз водой. После высушивания над Na,j,SO/j раствор упаривают в вакууме. Получают (1,2,2,6,6-пентаметил-4-пиперидинил) диэфир бутил-(3,5-ди-трет- бутил-4-гидроксибензил)-малоновой кислоты с температурой плавления 140°с.
Аналогично получают соединения. приведенные в табл. 1, здесь же даны их свойства.
Таблица 1
i
°
),liЕ












| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИЯ, СТАБИЛИЗИРОВАННАЯ ПРОТИВ ОКИСЛИТЕЛЬНОЙ, ТЕРМИЧЕСКОЙ ИЛИ ФОТОИНДУЦИРУЕМОЙ ДЕСТРУКЦИИ, И СПОСОБ СТАБИЛИЗАЦИИ ПОЛИАМИДА, ПОЛИЭФИРА И ПОЛИАЦЕТАЛЯ | 1998 |
|
RU2210578C2 |
| ИЗДЕЛИЯ ИЗ ПОЛИЭТИЛЕНА ИЛИ ПОЛИПРОПИЛЕНА | 2019 |
|
RU2820503C2 |
| СТАБИЛИЗАЦИЯ ОРГАНИЧЕСКОГО МАТЕРИАЛА СОЕДИНЕНИЯМИ МАННИХА НА ОСНОВЕ АМИНОТРИАЗИНА | 2012 |
|
RU2593997C2 |
| Стабилизированная полимерная композиция | 1972 |
|
SU584795A3 |
| ПОЛИЭТИЛЕНОВАЯ ТРУБА | 2018 |
|
RU2817113C2 |
| ТЕХНОЛОГИЧЕСКИЕ ДОБАВКИ И ИХ ПРИМЕНЕНИЯ В РОТАЦИОННОМ ФОРМОВАНИИ | 2011 |
|
RU2597918C2 |
| ТЕХНОЛОГИЧЕСКИЕ ДОБАВКИ И ИХ ПРИМЕНЕНИЯ В РОТАЦИОННОМ ФОРМОВАНИИ | 2011 |
|
RU2742578C2 |
| ПРОИЗВОДНЫЕ 5Н-ФУРАН-2-ОНА ДЛЯ СТАБИЛИЗАЦИИ ОРГАНИЧЕСКОГО МАТЕРИАЛА | 2012 |
|
RU2605940C2 |
| ИЗОЛЯЦИЯ КАБЕЛЯ | 2018 |
|
RU2750866C2 |
| 1,2-БИС-АДДУКТЫ СТАБИЛЬНЫХ НИТРОКСИДОВ С ЗАМЕЩЕННЫМИ ЭТИЛЕНАМИ И СТАБИЛИЗИРОВАННЫЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ | 1997 |
|
RU2187502C2 |

21Н
(2,2,6,6-Тетраметил 34Н9
-4-пиперидинил диэфир
бутил-(3,5-ди-трет-бутил-4-гидроксибен3ил)-малоновой кислоты 125
(2,2,6,6-Тетраметил-4-пиперкдинил)диэфир
бутил-(З-метил-5-трет-бутил-4-гидроксибензил)-малоновой кислоты
1 СИ,
(1,2,2,6,б-Пентаметил-4-пиперидинил)диэфир
бутил-(З-метил-5-трет-бутил-4-гидроксибензил)-малоновой кислоты
1 О
(1-Оксил-2,2,6,6-тетраметил-4-пиперидинил)диэфир бутил-(З,5-ди-трет-бутил-4-гидроксибензил)-малоновой кислоты
t-C4H9
Но- -сКг-
СНзСО
t-C4H9
t
НО (СНд)1
Н CHj
(1-Ацетил-2,2,6,6-тетраметил-4-пиперидинил)
диэфир бутил-( 3,5-ди-трет-бутйл-4-гидооксибензил)-мг1лоновой кислоты
(2,2,6,6-Тетраметил-4 пиперидинил)ди5фир изопропил-(З-метил-5-трет-бутил-4-гйдроксибензил)-малоновой кислоты
--- -,
Продолжение табл. 1
(12,2,6,6-Пентаметил v г 5 г -4-пиперидинил диэфир диэтилфосфонометил- (3,5 ди-трет-бутил-4-гидроксибензил)-ма- Вязкое лоновой кислоты масло
10
(2,2,6,б-ТетраметилСН2-4-пиперидинил)диэфир аллил-(З-метил-5-трет-бутил-4-гидроксибензил)-малоновой кислоты
150
11
1-С4Нэ
1 Л НоХО)--СНг12
-(еНг)з-Р(ОСгН5)г (2,2,6,б-Тетраметил-4пиперидинил)лиэфир-3диэтилфосфонопропил- (3,5-ди-трет-бутил-4-гидроксибензил)-малоновой кислоты
(2,2,6,6-ТетраметилМасло-4-пиперидинил)диэфир октил-(3,5,-ди-третбутил-4-гидроксибензил)-малоновой кислоты
13
(1,2,2,6,6-Пентаметил126-4-пиперидинил)диэфир додеЦил-(3,5-ди-третбутил-4-гидроксибензил)-малоновой кислоты
,-с-о-(Л-СН-CHj-d-O- КН
„ СНЦНз
(1,2,2,6,6-Пентаметилен. -4-пиперидинил)диэфир 1,2,2,6 ,6-пентаметил-4СНз СН} -пиперидинилоксикарбонилметил-(З-метил-5 трет-бутил-4-гидрокси.бензил)-малоновой кислоты
СНзСНз
о ,-V
11 / л
11,2,2,6,6-Пентаметилг4-пиперидинил)диэфир 1,2,2,6,6-пентаметил-4СНзСНз-пиперидинилоксикарбонилмётил-(3,5-ди-трет-бутил-4-гидроксибензил)-малоновой кислоты СНгСН2-С-ОЧ NH {2,2,6,6-ТетраметилПродолжение табл. 1 CHjCHa , О .-V и /
170 - .-4-пиперидинил)диэфир CHjCHj 2,2,6,6-тетраметил-4 -г -пиперидинйлоксикарбонилметил-{ 3,5-ди-трет-бутил-4-гидрокси6ензил)-малонов6й кислоты19
1,4-Ди-(3,5-ди-трет-бутил-4-гидроксифеНИЛ)-2,2,3,3-тетра-(1,2,2,6,6-пентаметил-4-пиперидинилоксикарбонил)бутан
20
1,7-Ди-(З-метил-5-трет- Масло -бутил-4-гидроксифенил)-2,2,б,6-тетра-(2,2,6,6-тетраметил-4-пиперпдинилоксикарбонил) -г.ептан
21
(1,2,2,6,6-Пентаметил125-4-пиперидинил)диэфир изопропил-(3,5-ди-трет-бутил-4-гидроксибензил)-малоновой кислоты
t-C4H9
CHj t-C4H9
(1,2,2,6,6-Пентаметил165-4-пиперидииил)диэфир метоксикарбонйлэтил-(3,5-ди-трет-бутил-4-гидроксибензил)-малоновой кислоты
:i::3:ii:::i:i:::::::4::::::: :::::
t-C«H9
231СЯз HO- cHgt-C4H9
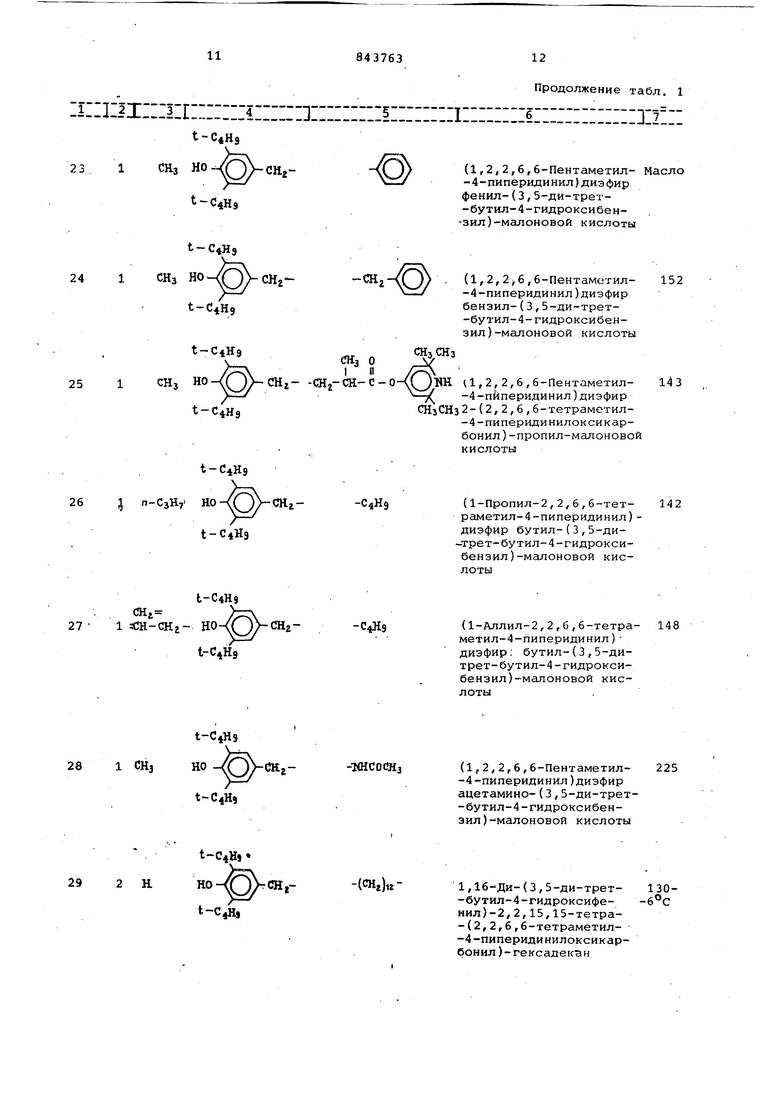
Продолжение табл. 1
:1::::::::б:::::::::::::з:7:::
(1,2,2,6,6-Пентаметил-4-пиперидинил)диэфир фенил-(3,5-ди-трет-бутил-4-гидроксибен«зил)-малоновой кислоты
CHa
(1,2,2у6,6-Пентаметил-4-пиперидинил)диэфир бензил-(3,5-ди-трет-бутил-4-гидроксибензил)-малоновой кислоты
СНз о
СНг- -CHj,-CH-C-0
CH,
26 п-СзНу
СН.
t-C4H9
t-C4H9
27 1 гСН-СНг-
281 CHjНО -)VcKj--11НСОСИз
t-C4H,
29 2 Н
,
СНэСНз I и
11,2,2,6,6-Пентаметил, -4-пйперидинил)диэфир CHjCHs 2-(2,2,6,6-тетрамстил-4-пиперидинилоксикарбонил)-пропил-малоновой кислоты
(1-Пропил-2,2,6,6-тет- 142 раметил-4-пиперидинил)диэфир бутил-(3,5-ди-трет-бутил-4-гидроксибензил)-малоновой кислоты
(1-Аллил-2,2,б,6-тетра- 148 метил-4-пиперидинил)диэфир; бутил-(3,5-дитрет-бутил-4-гидроксибензил)-малоновой кислоты
(1,2,2,6,6-Пентаметил-4-пиперидинил)диэфир ацетамино-(3,5-ди-трет-бутил-4-гидроксибензил)-малоновой кислоты
1,16-Ди-(3,5-ди-трет130-б С-бутил-4-гидроксифеиил)-2,2,15,15-тетра-(2,2,6,6-тeтpaмeтил-4-пипepидинилoкcикapбoнил )-гексадекан П р им еры 33-35, 26,2 г (О,05 моль)(2,3,6-триметил-2,6-диэтил-4-пиперидинил)-диэфира бутилмалоновой кислоты и 13,2 г (0,05 мо У-(3,5-ди-трет-бутил-4-гидроксибензил)диметиламина растворяют в 200м толуола. После добавления 0,25 г амида лития смесь нагревают в течение 4 ч до появления флегмы. После охлаждения нейтрализуют ее 1,5 мл 1-процентного раствора уксусной кис лоты и промывают органическую фазу несколько раз водой. После высушива ния под , раствор упаривают в
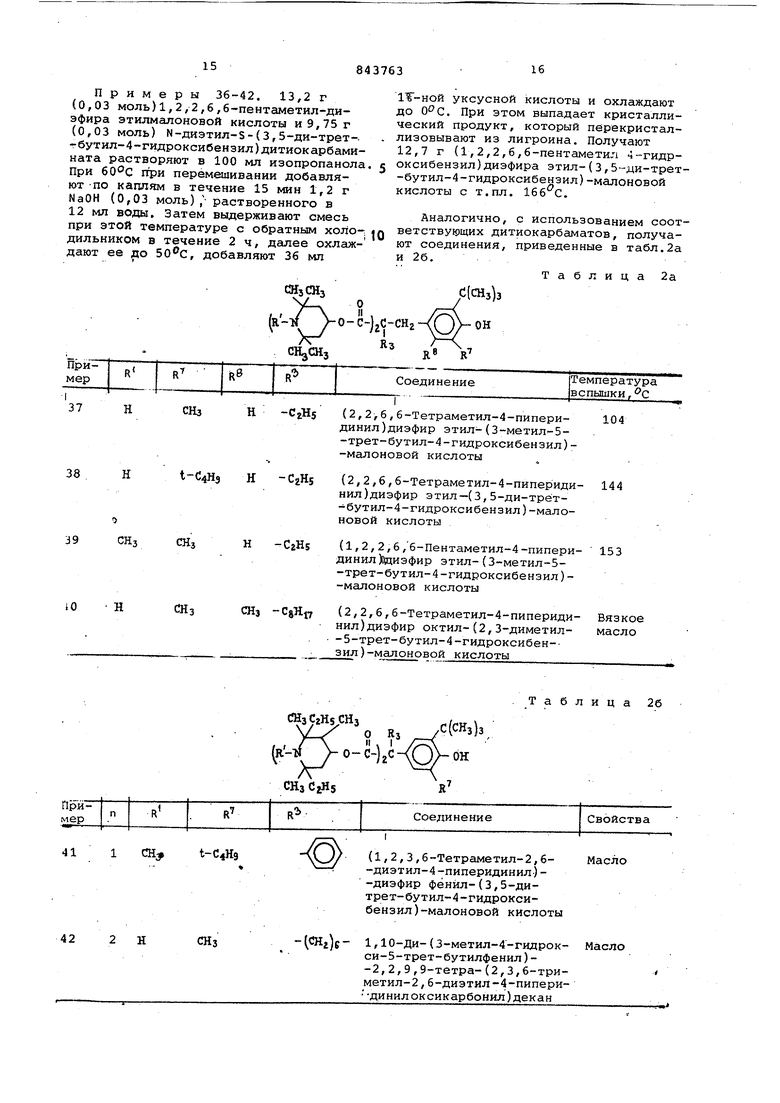
Продолжение табл. 1 вакууме. Таким образом получают (2,3,6-триметил-2,6-диэтил-4-пиперидинил) диэфир бутил- (3 ,5-ди-трет-бутил-4-гидроксибензил)-малоновой кислоты в .виде вязкого масла (соединение 1№ 32). Вычислено, %: С 74,54, Н 10,88, N 3,78.С бИроМаОзНайдено, %: С 74,7, Я 10,6, ИЗ,82. Аналогично получают соединения, приведенные в . 1а, здесь же даны их свойства. . Таблица .1а Примеры 36-42. 13,2 г (0,03 моль)1,2,2,6,6-пентаметил-диэфира этилмалоновой кислоты и 9, 75 г (0,03 моль) N-диэтил-S-(3,5-ди-тpeт-бутил-4-гидроксибензил)дитиокарбамината растворяют в 100 мл изопропанола. 5 При при перемешивании добавляют-по каплям в течение 15 мин 1,2 г NaOH (0,03 моль), растворенного в 12 мл воды. Затем выдерживают смесь при этой температуре с обратным холо- «Q дильником в течение 2 ч, далее охлаждают ее до , добавляют 36 мл г-С4Нэ Н -СгН5 Н -CzHs СНз -C8Ht7
«ffjCzHsCHs
У
(a-TTVo-c-l c
А CHsCzHs
Таблица 26 1Т-ной уксусной кислоты и охлаждают до ОС. При этом выпадает кристаллический продукт, который перекристаллизовывают из лигроина. Получают 12,7 г (1,2,2,6,6-пентаметил 4--гидроксибензил)диэфира этил-(3,5--ди-трет -бутил-4-гидроксибензил)-малоновой кислоты с т.пл. 166 С. Аналогично, с использованием соответствующих дитиокарбаматов, получают соединения, приведенные в табл.2а и 26. Таблица 2а (2,2,6,6-Тетраметил-4-пипери- 104 динил)диэфир этил-(З-метил-5-трет-бутил-4-гидроксибензил)-малоновой кислоты (2,2,6,6-Тетраметил-4-пипериди- 144 нил)диэфир этил-(3,5-ди-трёт-бутил-4-гидроксибензил)-малоновой кислоты (1,2,2,6,6-Пентаметил-4-пипери- 153 динил )0диэфир этил-(З-метил-5-трет-бутил-4-гидроксибензил)-малоновой кислоты (2,2,6,6-Тетраметил-4-пипериди- Вязкое нил)диэфир октил-(2,3-диметил- масло -5-трет-бутил-4-гидроксибен-зил)-малоновой кислоты
t-C4H9
СН41
(1,2,3,6-Тетраметил-2,6-диэтил-4-пиперидинил )-диэфир фенил-(3,5-дитpeт-бyтил-4-гидpoкcибензил)-малоновой кислоты -(Oli)- 1,10-Ди-(З-метил-4-гидрок -динил оксикарбонил) декан си-5-трет-бутилфенил)-2,2,9,9-тетра-(2,3,6-триметил-2,6-диэтил-4-пипериМасло
П р и м е р ы 43 - 46. К 24,6. т (0,06 моль) (2,2,6,6-тетраметил-4-пиперидинил)диэфира этилмалоновой кислоты, растворенной в 80 мл диметилформамида, добавляют 2,5 г суспен.зии NaOH (55-60%) , а затем 13,6 г (0,06 моль) 2,6-ди-метил-4-трет-бутил-3-гидроксибензилхлорида в 40 мл ДМФ. Перемешивают содержимое в течение 20 ч при 90-100 С, выливают затем реакционную смесь в ледяную воду, экстрагируют зфиром, высушивают эфирнук5 вытяжку над и после удаления растворителя в вакууме получают в виде.желтого маслянистого остатка (2,2,6,6-тетраметил-4-пиперидинил)диэфир (2,6-димнтил-4-трет-бутил -3-гидроксибензил)малоновой кислоты.
Аналогично получают (1,2,2,6,6-пентаметил-4-пиперидинил)диэфир этил- (2,6.-диметил-4-трет-бутил-3-гидроксибензил)-малоновой кислоты с т.пл. 1750с (пример 44): (1, 2 , 2 , 6 ,6-пентаметил-4-пиперидинил)диэфир бутил-(2,6-димехил-4-трет-бутил-3-гидроксибензил)-малоновой кислоты, желток масло (пример 45); (2,2,6,6-тетраметил-4-пиперидиНил)диэфир бутил-(2,6-ди-метил-4-трет-бутил-3-гидроксибензил)-малрновой кислоты,масло(пример 4
ft р и м е р 47. 21,9 г (0,05 моль) (1,2,2,6,6-пентаметил-4-пиперидинил) диэфира этилмалоновой кислоты, г (0,05 моль) (1,2,2,6,6-дентаметил-4-пиперидинил)диэфира малоновой кислоты, 1,5 г (0,05 моль) параформ-альдегида и 0,5 г NaOH перемешивают в 120 мл толуола в течение получаса при комнатной температуре, а затем в течение 7 ч при температуре кипения с обратным холодильником. После охлаждения добавляют 13,2 г (0,05 моль М-(3,5-ди-трет-бутил-4-гидроксибензил)-диметиламина и греют смесь в течение 4 ч с обратным холодильником. При дальнейшей последовательности операций, аналогичной примеру 1, получают в виде маслянистого остатка 1-(3,5-ди-трет-бутил-4-гидроксибензил)-2,2 ,4,4-тетра-(1,2,2,6,6-пентаметил-4-пиперидинилоксикарбонил)-гексан.
Найдено, %: С 70,3, H10,5,N 5,3. Вычислено, %: С 71,2, Н 10,3, N 5,2.
Пример ы 48 и 49. 39 г (2,3,6-триметил 2,6-диэтил-4-пиперидинил)диэфира бутил-(3,5-ди-трет-бутил-4-гидроксибензил)-малоновой кислоты (соединение 32) растворяют в 200 мл . ксилола,затем добавляют при комнатной температуре 20 г безводного карбоната калия и 10 г ангидрида уксусной кислоты и медленно нагревают суспензию до начала интенсивного выделения С0,. .Как только интенсивность выделения COrj ослабевает, температуру увеличивают до 1.30-135 С и перемешивают смес в течение 10 ч с обратным.холодильником. После охлаждения соль кальция отфильтровывают и упаривают ксилольный раствор в вакууме. Остается кориневое вязкое масло, представляющее собой сырой (1-ацетил-2,3,6-триметил-2,6-диэтил-4-пиперидинил)диэфир бутил- (3,5-ди-трет-бутш174-гидроксибензил) -малоновой кислоты.
Найдено, %: С 72,8, Н 10,1, N3,50
Вычислено, %: С 72,77, Н 10,26, .N 3,93. ..
Аналогично проводят реакцию между 32 г (2,2,6,6-тeтpaмeтил-4-пипepидинил)диэфиpoм бутил-(3,5-ди-трет-бутил-4-гидроксибензил)-малоновой кислоты и 10 г ангидрида уксусной кислоты в присутствии 20 г K,CO,j. Получают (1-ацетил-2,2,6,6-тетраметил-4-пиперидинил)диэфир бутил-(3,5-ди-трет-бутил-4-гидроксибензил)-малоновой кислоты, плавящейся при 120-124°С
Примеры 50-53.
i-
(СНз)зС
CKj -СНз
в
и А
cHfC-{cira-/ №i|
, ()зССНз CHj
Соединение 50,R С, Hg : 43 г N ,N -ди(2,2,6,6-тетраметил-4-пиперидинил)-диамида бутилмалоновой кислот (0,1 моль) и 26,4 г М-(3,5-ди-трет-бутил-4-гидроксибензил)диметиламина (0,1 моль) 4 ч нагревают с обратным холодильником в 450 мл толуола с добавкой 0,5 r-LiNH. После охлаждения нейтрализуют с О,4 г ледяной уксусной кислоты, отфильтровывают и выпа ивают. Таким образ ом, получают неочищенный N ,м-ди-(2,2,6,6-тетраметил-4-пиперидинил).гдиамид бутил-(3,5-ди-трет-бутил-4-гидрОксибензил)-малоновой кислоты,который после перекристаллизации из этанола плавится при 214°
Аналогично получают соединения 51 R , и 52, R С0Н„.
51: N , N-ДИ- (2,2-, 6,6-тетраметилпиперидин-4-ил)-диамид этил-(3,5-ди-трет-бутил-4-гидроксибенЗИЛ)-малоновой кислоты.Точка плавления 240-241 С
52: N,N -ди-(2,2,6 ,6-тетрс1метилпиперидин-4-ил)-диамин н-октил-(3,5-ди-трет-бутил-4 -гидроксибензил)- -малоновой кислоты. Точка плавления 182-1.84° С.
53: . N ,N -ди- (2,2,6,6-тетраметилпиперидин-4-ил)-диамид бензил-(3,5-ди-трет-бутил-4-гидроксибензил)-малоновой кислоты.
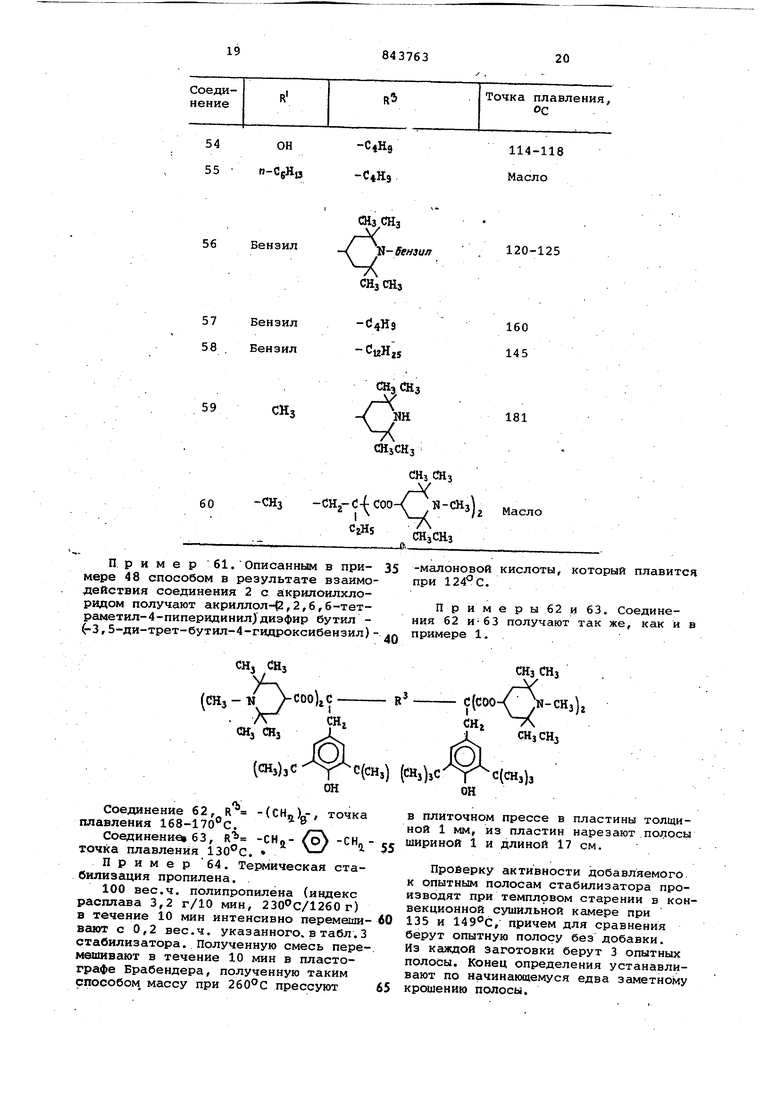
Примеры. 54-60. Описанным в примере 1 способом получают соеди-нение 54-60:
U-C4H9
СНз СНз
V
СНг-С-(СООЧ N-Rli
/
CHjCHs
56
Бензил
120-125
57 58
Бензил Бензил
59
СНз
-СНз -CH -e- COO-Tjw-CHj) Пример 61.Описанным в при- 35 мере 48 способом в результате взаимодействия соединения 2 с а крилоилхлоридом получают акриллол-(2,2,б,б-тетраметил-4-пиперидинил)диэфир бутил (-3,5-ди-трет-бутил-4-гидроксибензил)
% СНз
-11 у-СОо)гС. ) CHi СМз СНз
Ь
Соединение 62, R СНп)--, точка плавления 168-170с. .
Соединение 63, R /О СИ,, точка плавления . -
Пример 64. Термическая стабилизация пропилена.
100 вес.ч. полипропилена (индекс расплава 3,2 г/10 мин, 230 С/1260 г) в течение 10 мин интенсивно перемешиВсцот с 0,2 вес.ч. указанного, в табл. 3 стабилизатора. Полученную смесь перемешивают в течение 10 мин в пластографе Брабендера, полученную таким способом, массу при 260°С прессуют
-tJ4H9
160 -CuHw
145
ШзСНз
з181
ШзСНз
СНз СНч
Y
Л
cnijCHs
СНз СНз
.л/
С(СОО- И-СНз)г
СНг /N Г CHjCHj
С{СН,) (СНз)зС С{СНз)з
в плиточном прессе в пластины толщиной 1 мм, из пластин нарезают .полосы шириной 1 и длиной 17 см.
Проверку активности добавляемого к опытным полосам стабилизатора производят при темпловом старении в конвекционной сушильной камере при 135 и 149°С, причем для сравнения берут опытную полосу без добавки. Из каждой заготовки берут 3 опытных полосы. Конец определения устанавливают по начинающемуся едва заметному крошению полосы. -малоновой кислоты, который плавится при . Примерыб2и63. Соединения 62 и-63 получают так же, как и в примере 1.
21843-763
Таблица 3
22
Продолжение табл. 3
П р и м е р 65. Светостойкость полипропиле н а.
Отдельные из описанных в примере 64 образцов проверяют на светостойкость, а именно на светостойкость после изготовления, после облучения в течение 500 ч светом в ксенотесте фирмы Ханау, после обработки в течение 1 недели кипящей водой. Для определения интенсивности окраски используется эмпирическая цветовая шкала, в которой цифра 5 означает бесцветность, цифра 4 - едва воспринимаемое, легкое изменение окраски, 3,2 и 1 -последовательное интенсивное изменение цвета.
Таблица 4
-йССНз)з-С4Н 27660
-С(СНз)з .Известное р 507р
-СНз
- С4Н93 ,/ онИзвестное f2j 3680
гСН
-СН
. 1 2
Без стабилизатора Пример 69. Светозащитные , свойства полцй ретановых пленок. 100 вес.ч. ароматического полиэфирполиуретана (Эстане 5707 фирмы Гудрич) в холодном состоянии р.аство ряют в 400 вес.ч. диметилформамида. В полученный раствор добавляют каждый из приведенных в табл. 8 стабилиааторов. Отрегулированным на 500| устройством для вытягивания пленок на стеклянной пластине вытягивают пленки, в течение 20 мин при 120°С ijix сушат в конвекционной сушильной к
Продолжение табл. б У
Т
с(снз)а
С(СНз)з
6500
4
С(СНз)з
С1СНз)з
900
1100
300 Полученную смесь 2 мин при прес суют до получения пластин толщиной 2 мм, пластины затем испытывают в ксенотесте 450. Светостойкость проб определяют по увеличению карбонильных групп, которое регистрируется инфракрасным спектрометром. В табл.7 приведено время освещения, в течение которого отношение экс инкции карбонила к экстинкции при 1450 см возрастает до 0,1. Такая экстинкция карбонила соответствует воспроизводиMOMV4 падению ударной вязкости проб. Таблица 7 мере. Получают пленки толщииой примерно 60Ц . Пробы облучают светом в ксенотесте 1200. Определяют время, В течение которого пропускание (или соответственно поглощение) света с длиной волны 420 нм падает на 15%. Такое падение светопропускания является показателем образовавшегося пожелтения. Затем, при испытании на удлинение при растяжении, определяют промежуток времени, через который растяжение составляет 50% первоначального значения.
Таблица 8 Пример 70. 100 вес,ч. порош ка полипропилена (Moplen Fibre grade фирмы Монтэдисон) смешивают до однородной массы с 0,2 вес.ч, октадецилового сложного эфира В-(3,5-ди-трет -бутил-4-оксифенил)-пропионовой кислоты и 0,02 вес.ч. одного из стабили заторов, указанных в табл. 9. Смешив ние, осуществляют на пластографе БраЪендера при в течение 10 мин. Полученную массу как можно быстрее выгружают из смесителя и затем формуют на коленчатом прессе в пластину толщиной 2-3 мм. Часть полученной сырой пластины помещают между двумя полосами высокогладкой твердой алюминиевой фольги и прессуют на ручном гидравлическом лабораторном прессе в течение 6 мин при 260С и давлении 12 т до пленки толщиной 0,9 мм, которую немедленно подвергают вытяжке в холодной воде. Из этой пленки вырезают образцы размером каждый 60x44 мм и освещают их в ксенотесте 1300. Через определенные промежутки времени образцы вынимают из аппарата облучения и исследуют на содержание в них карбонильных групп аналогично описанному в примере 66. Результаты исследований представлены в табл. 9. Таблиц а9 Время облучения, ч Стабилизатор до экстинкции ,3 Известный Формула изобретения Полимерная композиция, содержгицая полимер, выбранный из группы, включаквдей полиолефины, полимеры стирола и полиуретан, и производное эфира гидроксибензилмалоновой кислоты, отличающаяся тем, что, с целью повышения эффекта термо-, светои окислительной стабилизации композиции,она содержит в качестве производного эфира гидроксибензилмалоновой кислоты соединение общей форму 1ы1| )
к
а)-(
R
t я п - 1 или 2; . 1 или этил; Rg, - водород или метил; X - О- или -NR-; R - водород, алкил с 1-12 С-атомами, аллил, или циклогексил/R - водород, -О, -ОН, алкил с 1-12 С-атомами, алкенил с 3-4 С-атомами, бензил, алканоил с 2-5 С-атомами или алкеноил с 2-3 С-атомами ; R - гидроксибензильная группа формулы (((} С R и R - алкил с 1-8 С-атомами и R - водород ,или метил ; слип-1)-алкил с 1-20 С-атомами или алкил с 1-4 С-атомами, замещенный rpyntroH -CO-YR или -R(0) (ORO),, где R -алкил с 1-18 С-атомами или группа формулы (ип алкил с 1-4 С атсмами, У группировка.-О- или -NR-, и .« означает алкеяил с 3-8 ами, аралкил с 7-9 С-атомами, , группу формулы III , группу ы -0-C(0)Rfl или -HH-C(O)R, может быть алкил с 1-12 С-ато.фенил или замещенный двумя / алкильными группами и гидрок31 84376 сильной группой фенил или фенилэтиловая группа, или R - группа фopмyлы{lv) it It I , -СН|-С e(CO-Y-R с . f. - .л где R - алкил о. 1-6 С-атомами, бензил, -O-C{O)R , -NH-C(O)R или f( а R представляет остаток формулы III или fft (если ) означает прямую Q связь, алкилен с 1-20 С-атомами, алкенилен с 4-6 С-атомами или арен-бис-алкилен с 8-14 С-атомами, при .32 следукедем соотношении компонентов, вес.%: Полимер 99,0-99,98 Производное эфира гидроксибензил-малоновой кислоты О,-1,0 Источники информёщии, принятые во внимание при экспертизе l. Фойгт и. стабилизация синтетических полимеров против действия света и тепла, М., Химия, 1972, с.95.2. Заявка ФРГ № 2456864, кл. С 07 D 211/46, выкл. 1975 (прбтотип) ,
Авторы
Даты
1981-06-30—Публикация
1976-11-05—Подача