(54) СПОСОБ ТИТРИМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ Изобретение OTI эсится к аналитической химии, в частности к титриметрическим методам опреаеления никеля в сложных объектах. Известны титриметрические методы определения никеля, в которых в качестве титранта используют комплексон Ш в присутствии различных металлохромных индикаторов, например, мурексида, пиридилаэорезордина, сульфарсааена, кромаэУрола и пр. Наибольшее практическое применение находит индикатор - мурексид. Титриметрический метоц определения никеля в присутствии индикатора мурексида выполняет ся с отделением никеля в виде диметилФляоксимата ij. Недостатки --комплексонометрического способа определения никеля в присутствии индикатора мурексида, используемого при анализе растворов электролитов, содержащих, железо (III) оо 1,5-мг в 100.мл тит руемого раствора, следующие.
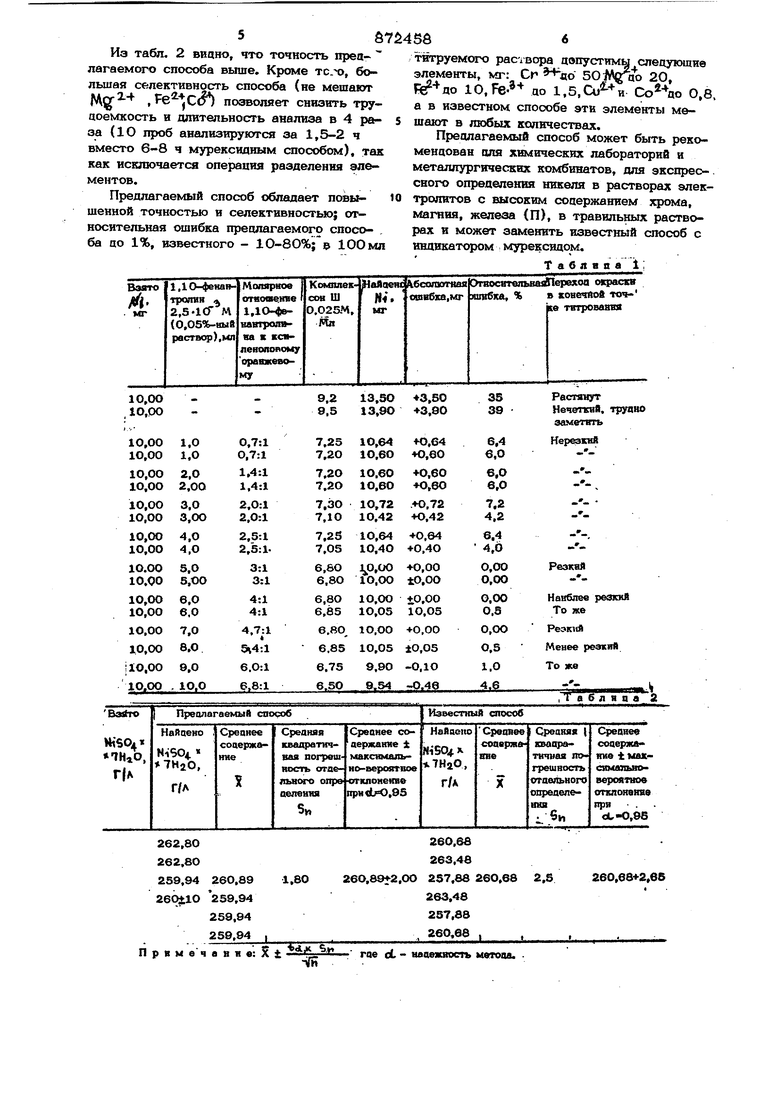
НИКЕЛЯ Сложность наблюдения за переходом окраски индикатора в конечной точке т1втрования, что объясняется способностью мурекснда существовать в виде трех развоокрашенвых форм с близкими константами диссодваднв в рЯ существования. Сложность установки рН (10) титрования обусловлена тем, что при рН 10 выпадают в осадок гидроксид в основные сопв никеля. Твтрсюаиие ведут в нейтральном растворе в в конце увелнчввают рН до 1О. Недостаточная селективность способа, так как шогне алемвнты: Co,Co,M,(ia,CrOtO,Fean),Fe(H),AtMAp.. Практическая недоступность мурексвоа (с 1964 г. его нет в продаже, он ве поступает в химические лаборатории). Наиболее близким к предлагаемому является способ твтрования горячих растворов солей никеля кся плексовом Ш в слабобокислой среде (рН4-5) в присутствии ввднкатора ссвленоловсхго оранжевого 2 Однако способ прямого титрования никеля кокошексойом Ш в присутствии ксиленопового оранжевого не нашел применения в практическом анализе из-за нечет ного, растянутого перехода окраски раствора в конечной точке титрования, вследствие малой скорости реакции взаимодействия соединения никель-ксиленоловый (фанжевый с комплексоном Ш и слабой конт встности реакции (фиолетово-красный цвет переходит в зеленовато-желтый в течение 0,5--4 ч}. Отсюда низкие точность и воспроизводимость результатов анализа. Кроме того, способ мало селективен, так как мешают любые количества меци, железа (Ш), кобальта, хрома и магния. Цель изобретения - повышение точности и селективности -титриметрического определения никеля. Цель достигается тем, что при титроваВИИ никелй комплексоном Ш в слабокислой сфеде в присутствии индикатора ксиленолового оранжевого, в титруемый раствор дополнительно вводят (1,2%-1,вО) /л 1ДО-фенантролина при соотношении 1ДО-фенантролина к ксиленоловому оранжевому 3-5:1. Оптимальными условиями титрования следует считать рН 5,5-5,О и нагревание раствора до кипения, так как при комнатной температуре растворы не титруются. Кислотность исходных растворов никеля не более, 2,0 я по серной или соляной кислоте. Замечено, что переход окраски расгвора. в конечной точке титрования более рез КИЙ В сернокислой, чем в солянокислой ере среде. Для нейтрализации исходных растворов до рН 5,О-5,5 используют растворы anetaTa натрия (1О%-ный) и серной кисло ты (1:4), Если кислотность исходных растворов никеля Bbmie 2,0 н, то после нейтрализации до рН 5,0 создается высокая концентрация посторонних электролитов (т.е. высокая ионнй сила раствора), которая ухудшает резкость перехода окраски раствора в конечной точке титрования (переход окраски от |фиолетово-красной в v. желтую). Опыты с переменной концентрацией 1,10-фенантролина показывают,что наиболее резкий переход окраски раствора набшодается при добавлении 5-7 мл 0,05%-но гЬ водного раствора 1,10-фенантролина в 100 мл титруемого раствора, что соо ветствует концентрации его (1,25-1,8О)Т 10 моль/л. При этом молярное отноше вве 1,1О-фенантролина к ксиленоповому оранжевому находится в пределах 3-5:1. Дальнейшее увеличение количества 1,10енантролина нецелесообразно, так как езкость перехода л не улучшается, а меньее содержание его не обеспечивает необходимой контрастности реакции. В табл. 1 представлены данные о влиянии 1,16-фенантролина на комплексометрическое определение никеля в присутствии силенолового оранжевого. Опыты проводятся при рН 5,5 в среде ацетатного буфера при добавлении 5 мл 0,05%-ного раствора ксиленолового оранжевого что соответствует концентрации его 510 моль/л. Изучение влияния посторонних элементов показывает, что в предлагаемом способе определению никеля (в 100 мл титруемого раствора} они не мешают в следующем количестве мг Сотносительная ошибка не более ): ДО 50,Mgfд o 20, Fe2 до 10, до 1,5, Си до 0,8. Влияние Fe до Ю мг может быть устранено 10 мл 1%-ного раЬтвора солянокислого гидроксиламина. Предлагаемый способ используют для определения никеля в производственном водном растворе электролита, содержащем от 3 до 250 г/л сульфатов кобальта, магния, никеля, железа (П). Пример. Определение никеля предлагаемым способом. Подготовка исследуемого раствора электролита. В мерную колбу емкостью ЮОмл берут 5 мл раствора электролита, доводят д перемешивают. Определение никеля. В колбу емкостью 25О мл берут аликвотную часть - 5 мл разбавленного раствора электролита, добавляют 80 мл воды и нагревают до кипения. К кипящему раствору цобавдяют 5 мл ацетатного буферного раствора (рН 5,5), 5 мл 0,05%-ного спиртового раствора ксиленолового оранхаввого и 6 мл 0,05%-ного водного раствора 1,10-фенантропина. Горячий pacTBt титруют 0,05 М раствором комплексона Ш до перехода окраски из фиолетово-красной в желтую. Концентрацию рйствора комплексона Ш устанавливают по стандартному раствору никеля, приготовленному из металлического никеля (99,99%), титрование у1;в присутствии индикатора ксиленолового оранжевого л 1,10 фенантролина. Результаты комплексонометрического определения никеля в электролите по предлагаемому способу в сравнении с мурексндным способом представлены в табл. 2. Из табл, 2 ввцно, что точность преолагаемого способа выше. Кроме тс.ч), большая селективность способа (не мешают .) позволяет снизить труцоемкость н длительность анализа в 4 раза (1О проб анализируются за 1,5-2 ч вместо 6-8 ч мурекснцным способом), так как исключается операция разделения элементов. Предлагаемый способ обладает ловышенной точностью и селективностью; относительная ошибка предлагаемого способа до 1%, известного - 10-8О%;е 100мл 6 56 титруемого pac-iBopa допустимы следующие элементы, мг: Сг о 5О1№ао 20 10,Fe.- до 1,5.0)- и СоЧо 0,8. а в известном способе эти элементы мешают в любых количествах. Предлагаемый способ может быть рекомендован для химических лабораторий и металлургических комбинатов, для экспрессного определения никеля в растворах электролитов с высоким содержанием хрома, магния, железа (П), в травильных растворах и может заменить известный способ с индикатором мурексидом. Табявпа 1;


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения никеля | 1983 |
|
SU1153286A1 |
| Индикаторная смесь для комплексонометрического определения переходных металлов | 1982 |
|
SU1125543A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ МЕДИ | 2012 |
|
RU2505810C1 |
| Способ комплексонометрического определения скандия | 1975 |
|
SU584246A1 |
| Способ титриметрического опреде-лЕНия ВОльфРАМА B СплАВАХ HA OCHO-BE ТАНТАлА | 1978 |
|
SU840716A1 |
| Способ извлечения скандия(III) для его последующего определения в системе, содержащей антипирин и сульфосалициловую кислоту | 2015 |
|
RU2645068C2 |
| Способ комплексонометрического определения циркония | 1980 |
|
SU893873A1 |
| Способ комплексонометрического опре-дЕлЕНия МЕди | 1979 |
|
SU834508A1 |
| Способ комплексонометрического определе-Ния МЕди(п) | 1979 |
|
SU833526A1 |
| Способ комплекснометрического определения меди | 1975 |
|
SU577457A1 |

1,8О 260, ,ОО 257,88 26О,68
26О,89
259,94 259,94 259.94
Првмечавив-Зс . V
ifh
а 6 л я па 2
26О,вв 263,48
260,68+2,65
2,5
263,46 257,88 26О.в8 I ,
roe oL - «воежяость метопа. Форму ft-а изобретени Способ титриметрического опреаеления никеля путем титрования комппексоном Ш в слабокислой среде в присутствии инаикатора ксиленолового оранжевого, о т л и ч аю щ и и с я тем, что, с целью повышения точности и селективности определения, в титруемый раствор дополнительно ввоцят 1,10-фенантролин цо концентрации (1,2858 1,8)г10 моль/л при соотношении к ксиг леноловому оранжевому 3-5:1. Источники информации, принятые во внимание при экспертизе 1. Шварценбах Г, Флашка Г. Комплексонометрическое титрование, М., Химия , 197О. с. 244... - 2. Пешкова В. М., Савостина В, М, Аналитическая химия никеля. М., Наука , il966, с. 86 (прототип).
Авторы
Даты
1981-10-15—Публикация
1979-11-06—Подача