СП
со
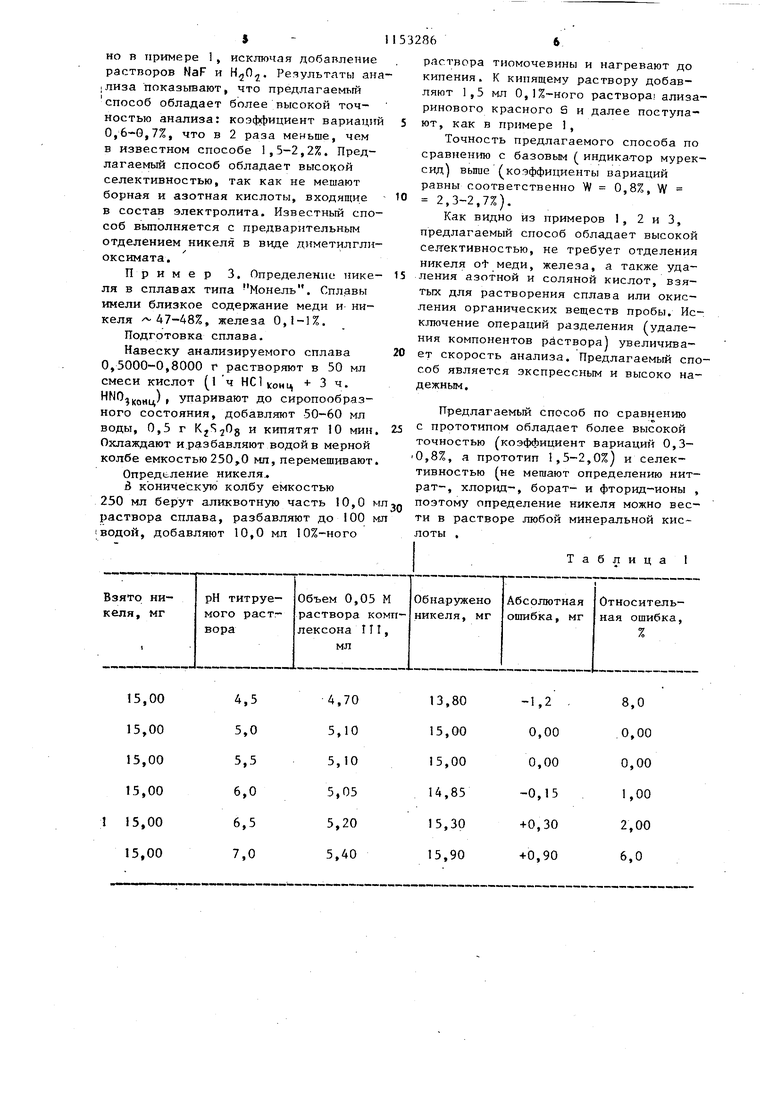
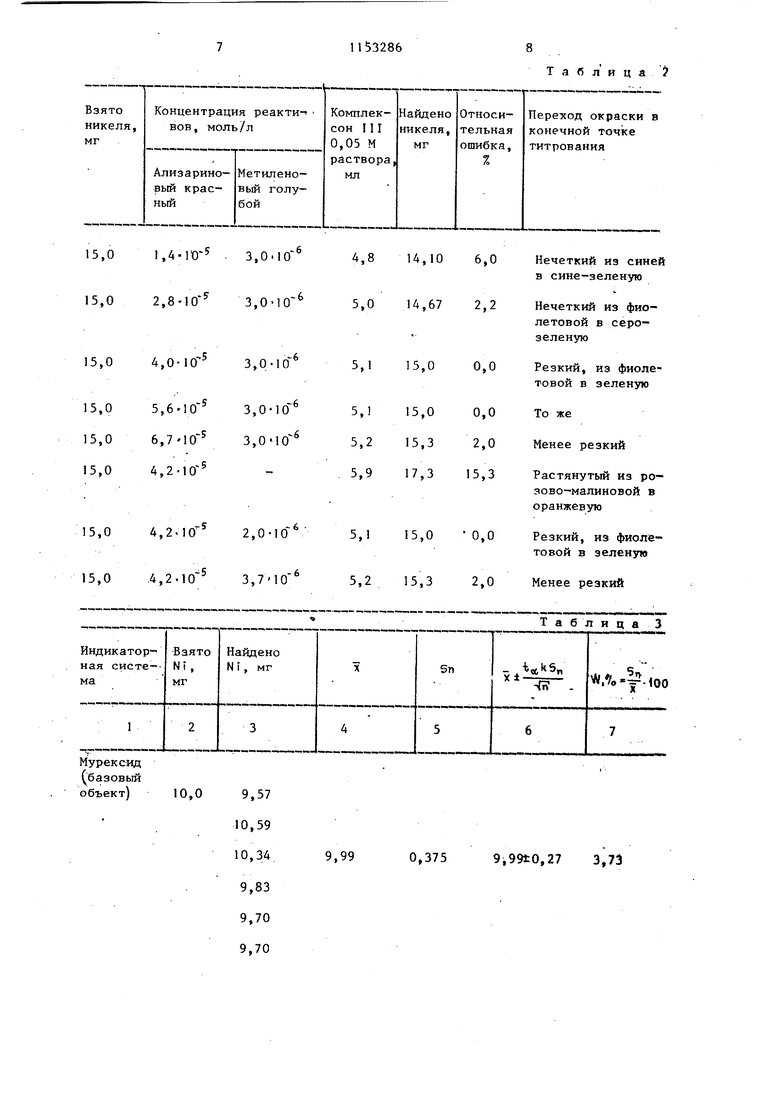
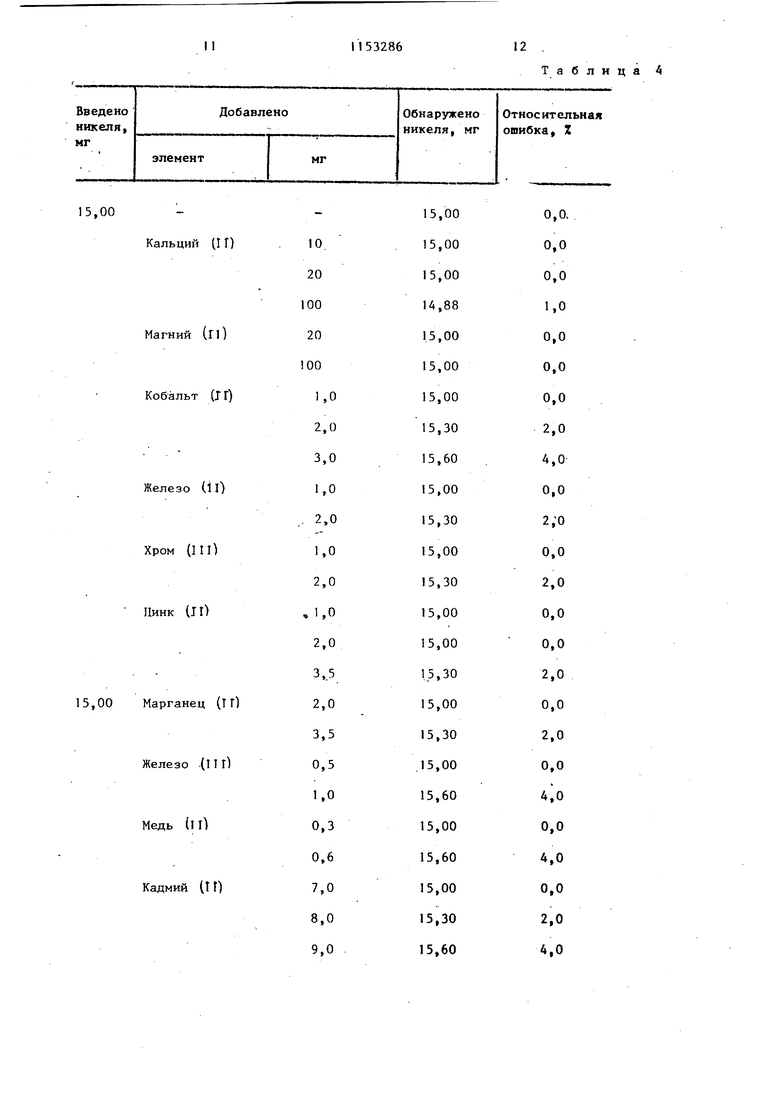
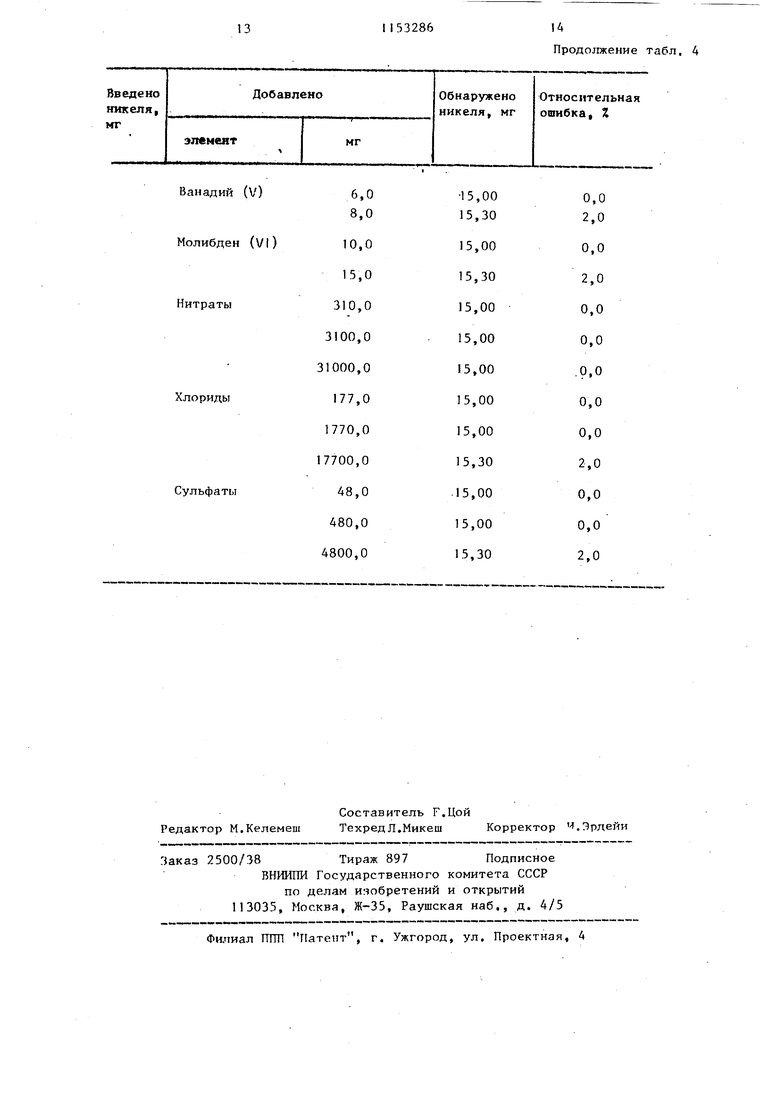
00 О) 1 Изобретение относится к аналитической химии, а именно титриметриче ким способам экспрессного определения никеля в электролитах,травильны растворах и других объектах сложног состава на металлургических предприятиях и химических лабораториях Известны способы определения никеля титрованием компексоном I И в присутствии различных металлохромны индикаторов: мурексида, сульфарсаэена, хромазурола, ксиленолового оранжевого D . Наибольшее практическое значение имеет способ комплексонометрическог титрования никеля с индикатором му- рексидом, включающий отделение нике ля в виде диметилглиоксимата, который является базовым в химическом анализе образцов сложного состава. Недостатки указанного способа невысокая точность и селективность анализа, а также практическая недоступность используемого индикатора. Определению никеля известным способом мешают медь, кобальт, farний, кальций хром (ТГТ), железо (П |железр (УГ1) , алюминий и др. Наиболее близким по технической сущности и достигаемым результатам к предлагаемому является способ определения никеля титрованием его го рячих растворов комплексоном lit в присутствии индикатора ксиленового оранжевого и 1,10-фенантролина в сл бокислой среде, преимущественно сер нокИслоацетатной. Известный способ обладает высокой селективностью по отношению к магнию (Т Г) , железу (П кобальту (П) 2 . Недостатками данного способа являются невысокая точность анализа коэффициент вариаци } 0,7-2,0%), а также недостаточная селективность анализа мешают нитрат-, хлорид-, фторид- и борат-ионы). Цель изобретения - повышение точ ности и селективности aHajni3at Поставленная цель достигается тем, что согласно способу определения никеля титрованием горячих раст воров комплексоном 111 с индикатором в слабокислой среде титрование осуществляют с использованием в качестве индикатора ализаринового кра ного б при концентрации (4,0-6,0) моль/л в присутствии (2,03,0)10 MOTib/n (Hciporo голу862бого, (1,0-Ь,0) моль/л борной кислоты и уротропина для создания слабокислой среды при рН 5,0-6,0. В предлагаемом способе титруют нагретые до кипения растворы никеля, . так как скорость образования комплекса никель-ЭДТА мала. Указанные условия титрования обеспечивают резкий переход окраски раствора из фиолетовой в изумрудно-зеленую в конечной точке титрования (от одной капли 0,05 М раствора комплексона ПТ). Результаты титрования никеля комплексоном 1Г1 в присутствии ализаринового красного 54,2-10 моль/л, метиленового голубого 2,5-10 моль/л и борной кислоты 3,210 моль/л при различном рН раствора ( З) при-, ведены в табл. 1, Из табл. 1 видно, что в интервале рН 5,0-6,0 наиболее высокая точность титрования растворов никеля 0,05 М комплексоном IГI. Заметим, что при нейтрализации кислых растворов никеля нужное значение рН 5,0-6,0 контролируют по изменению цвета индикатора ализаринового красного S в растворе (происходит переход окраски раствора из желтого в розовато-малиновую) . Для нейтрализации используют 30-40%-ный раствор уротропина. Использование растворов аммиака (:1) или едкого натра (10%-ного) не обеспечивает четкого пс;)скода п конечной точке титровггния ,вс: едсткие влияНИН конку))ирующего комплексообразования с аммиаком и гидроксид-ионами. Установлено, что наиболее резкий переход окраски в конечной точке титрования из фиолетовой в зеленую, наблюдается при добавлении (4,0-6,0)х I О моль/л ализаринового красного 5 и (2-3,0)10 моль/л метиленового голубого (табл. 2). Указанное количество компонентов обеспечивает высокую точность и воспроизводимость результатов титрования. Результаты подбора оптимальных концентраций используемых реагентов при концентрации борной кислоты 3,2-10 моль/л приведены в табл.2. Количество борной кислоты (1 5,0)- 10 моль/л обеспечивает высокую точность и воспроизводимость результатов титрования (относительная ошибка 0,00). Использование предлагаемой индикаторной системы ализариновый красный S, метиленопьй голубой и борная кислот;) и указанн{,п{количествах обеспечивает высокую точность компле.ксонометрического определения никеля (коэффициент вариаций ниже 1%, в прототипе , 2%). . В отсутствие нейтральных добавок (метиленового голубого и борной кислоты) переход окраски раствора в конечной точке титрования очень растянут от розово-малиновой до желтооранжевой (визуально переход трудно заметить. Наиболее резкий перехо окраски раствора наблюдается при содержании 2,5-25 MF никеля в 100 кл титруемого раствора. При меньшем содержании никеля переход окраски раст вора растянут, а при большем его количестве мешает собственная окраска соединения никель-комплексон ГГ1, Результаты сравнения трех индикаторных систем при комплексонометрическом титровании никеля приведены в табл. 3. Из табл. 3 видно, что большая точ ность определения достигается при использовании предлагаемой индикатор .ной системы, коэффициент вариаций YI| 0,93%. Это указывает на то, что точность определения никеля пред- лагаемьтм способом по сравнению с прототипом возрастает в 2 раза, а по сравнению с базовьм объектом - в 4 раза. . Влияние предельных количеств посторонних элементов показано в табл. 4, из которой видно, что определению никеля предлагаемым способом не мешают любые количества кальция и магния, а кобальта (п), железа (П), хрома (И1) - до 2 мг, желе за (ГП) - до 1 мг, меди (П) - до 0,6 мг, цинка (Г1) и марганца (11) до 3,5 мг, кадмия (11) и ванадия (V) до, 8 мг, молибдена (VI) - до 15 мг. Установлено также, что не мешают фто РИД-, нитрат- и хлорид-ионы, сульфаты и борная кислота - до 0,5 моль/л, ацетаты - до 0,2 моль/л, сегнетова соль - до 0,01 моль/л. Пример 1, Определение никел в электролите. Подготовка исследуемого раствора электролита. В мерную колбу емкостью 100,0 мп берут 10,0 мл раствора электролита, подкисляют раствором HWOj (1:4)до рН 1,0-2,0 (контроль по универсальной индикаторной бумаге) доводят до метки водой и перемешивают. Определение никеля. В колбу емкостью 250 мл берут апиквотную часть 5,0 мл разбавленного раствора электролита, добавляют 5,0 MJI HNO, (1:4), 20,0 мл 3%-ного раствора фторида натрия, разбавляют, водой до 100 мл и нагревают до кипения. К горячему раствору добавляют 1,5 мл 0,1%-ного раствора ализаринового красного (4,2 10 моль/л) нейтрализуют 40%-ным растворам уротропина до рН 5,0-6,0, т.е. до изменения окраски раствора из желтой в,розоватомалиновую, добавляют 0,4 мл 0,02%-него, раствора метиленового голубого (2,510 моль/л), 10 мл 1%-ного раствора перекиси водорода. Раствор снова нагревают до кипения, добавляют 0,2 г (о,03 моль/л) борной кислоты и титруют 0,05 М раствором комплексона 11 Г до перехода окраски из фиолетовой в малахитово-зеленую. Концентрацию раствора комплексона 111 устанавливают по стандартному раствору никеля, приготовленному из металлического никеля (99,99%) титрованием в присутствии предлагаемой индикаторной системы: ализариновый красный S, метиленрвый голубой и борная кислота. Результаты комплексонометрического определения никеля в производственном электролите предлагаемым способом в сравнении с известньм в присутствии ксиленового оранжевого показьгеают, что точность предлагае- . мого способа значительно выше (койф фициент вариаций по предлагаемому способу 0,4-0,5%, но прототипу t,5 ,t5/oj . Пример 2. Определение никеля в водном растворе производственного электролита никелирования. (электролит содержит до 400 г/л сульфата никеля, борную кислоту и.40 г/л и различные органические добавки, Подготовка исследуемого раствора электролита. В мерную колбу емкостью 200,0 мп берут 10,0 раствора электролита, подкисляют HNO (1J j ДО рН 1-2,0 (по универсальной индикаторной бу маге), доводят до метки водой и перемешивают. Определение никеля. В колбу емкостью 250 мл берут 5,0 мл разбавленного раствора элект ролита и далее поступают, как описаМО в примере 1, исключая добавление растворов NaF и . Результаты ан (Лиза показьшают, что предлагаемый способ обладает более высокой точностью анализа: коэффициент вариаци 0,6-0,7%, что в 2 раза меньше, чем в известном способе 1,5-2,2%. Предлагаемый способ обладает высокой селективностью, так как не мешают борная и азотная кислоты, входящие в состав электролита. Известный спо соб выполняется с предварительным отделением никеля в виде диметилгли оксимата. Пример 3. Определение пике ля в сплавах типа Монель. Сплавы имели близкое содержание меди и никеля -47-48%, железа 0,1-1%. Подготовка сплава. Навеску анализируемого сплава 0,5000-0,8000 г растворяют в 50 мл смеси кислот (1 ч + 3 ч. (,„ц) , упаривают до сиропообразного состояния, добавляют 50-60 мл воды, 0,5 г Kjij S кипятят 10 мин Охлаждают и.разбавляют водой в мерной колбе емкостью 250,0 мл, перемешивают Определение никеля.. В коническую колбу емкостью 250 мл берут аликвотную часть 10,0 раствора сплава, разбавляют до 100 iводой, добавляют 10,0 мл 10%-ного раствора тномочевины и нагревают до кипения. К кипящему раствору добавляют 1 ,5 мл 0,1%-ного раствора. ализаринового красного S и далее поступают, как в примере 1, Точность предлагаемого способа по сравнению с базовым ( индика-тор мурексид) вьпие (ко.эффициенты вариаций равны соответственно W 0,8%, W 2,3-2,7%). Как видно из примеров 1, 2 и 3, предлагаемый способ обладает высокой селективностью, не требует отделения никеля ot меди, железа, а также удаления азотной и соляной кислот, взятых для растворения сплава или окисления органических веществ пробы. Исключение операций разделения (удаления компонентов раствора увеличивает скорость анализа. Предлагаемый способ является экспрессным и высоко надежным. Предлагаемый способ по сравнению с прототипом обладает более высокой точностью (коэффициент вариаций 0,3- 0,8%, а прототип 1,5-2,0%) и селективностью не мешают определению нитрат-, хлорид-, борат- и фторид-иоиы , поэтому определение никеля можно вести в растворе любой минеральной кислоты . Таблица 1


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ титриметрического определения никеля | 1979 |
|
SU872458A1 |
| Индикаторная смесь для комплексонометрического определения переходных металлов | 1982 |
|
SU1125543A1 |
| СПОСОБ КОНТРОЛЯ КОНВЕРСИИ ЭПОКСИДНЫХ И ГИДРОКСИЛЬНЫХ ГРУПП ПРИ СОПОЛИМЕРИЗАЦИИ МЕТАКРИЛОВОЙ КИСЛОТЫ И ЭПОКСИДИАНОВОЙ СМОЛЫ | 1993 |
|
RU2110064C1 |
| @ , @ , @ , @ -Тетра-/ @ -карбоксиэтил/- @ -фенилендиамин в качестве комплексона для определения меди | 1982 |
|
SU1068421A1 |
| Способ комплекснометрического определения меди | 1975 |
|
SU577457A1 |
| Способ комплексонометрического определения скандия | 1975 |
|
SU584246A1 |
| Способ комплексонометрического определе-Ния МЕди(п) | 1979 |
|
SU833526A1 |
| Способ определения золота в электролитах золочения и технологических растворах | 1983 |
|
SU1161870A1 |
| Способ комплексонометрического определения циркония | 1980 |
|
SU893873A1 |
| Способ комплексонометрического определения висмута (ш) | 1982 |
|
SU1096575A1 |
1. СПОСОБ ОПРЕДЕЛЕНИЯ ЯМКЕЛЯ титрованием горячих растворов комплексоном 111 с индикатором в лабокислой среде, о Т л и ча ю щ и йс я тем, что, с целью повьшения точности и селективности анализа, титрование осуществляют с использованием в качестве индикатора ализаринового красного 5 при концентрации 
4,70 5,10 5,10 5,05 5,20 5,40
8,0
-1,2 .0,00
0,00 0,00
0,00 1,00
-0,15 2,00
+ 0,30 6,0
+0,90
Таблица
9,96
9,57
10,08
10,47
енолооранже+ 0-фен тотип) 10,00
9,95 10,09 10,23
9,68
9,68 10,09
9,88 10,09 10,23
9,95 4 9,96
10,00
9,96
,9,82
9,96
9,96
10,11
10,11
9,96
1153286
10
Продолжение табл. 3
0,198
9,9910,14 1,98
9,99
9,99±0,07 0,93
0,09
9,99
Таблица 4
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Шварценбах Г., Флагака Г | |||
| Комплексонометрическое титрование | |||
| М., Химия | |||
| Кинематографический аппарат | 1923 |
|
SU1970A1 |
| Нагревательный прибор для центрального отопления | 1920 |
|
SU244A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ титриметрического определения никеля | 1979 |
|
SU872458A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
1985-04-30—Публикация
1983-10-31—Подача