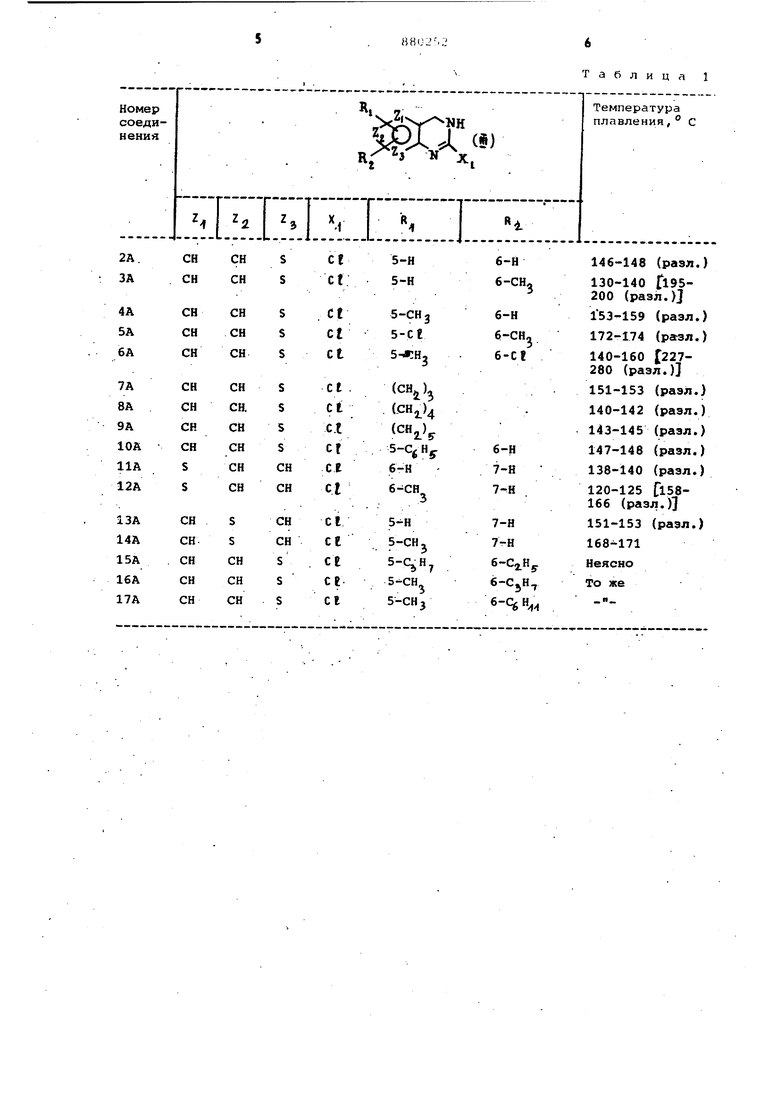
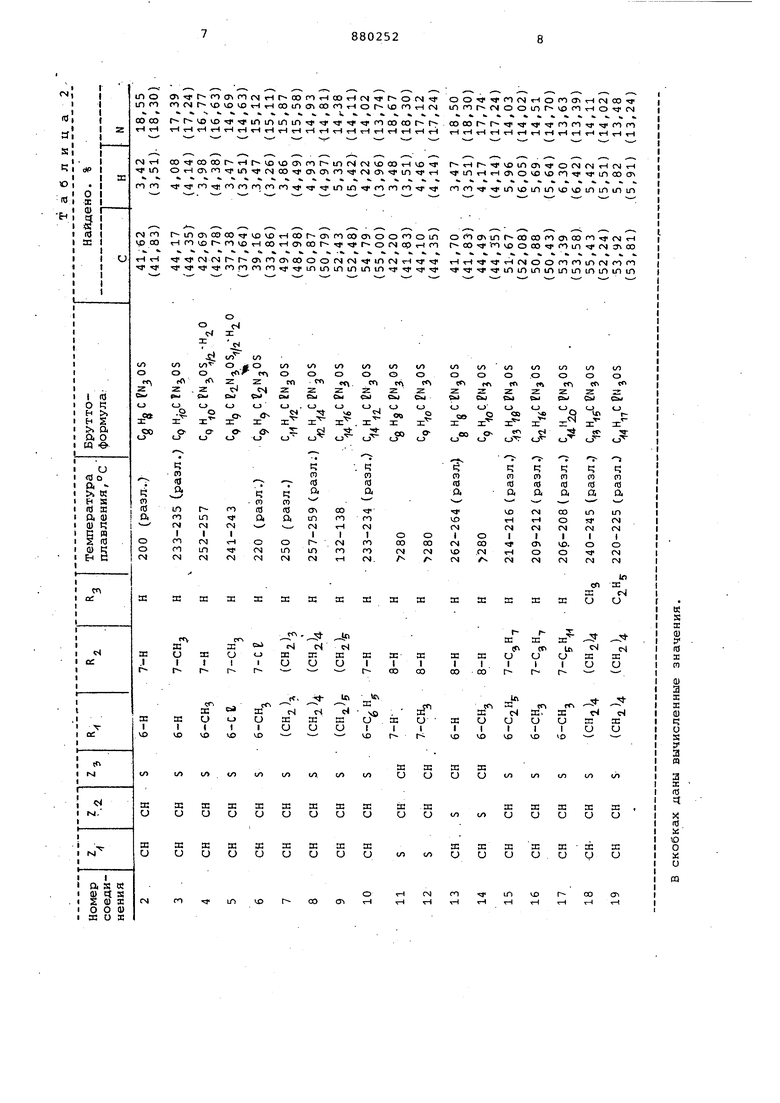
Изобретение относится к способу получения новых 1,2,3,5-тетрагИяроимидазотиенопиримидин-2-онов общей формулы где один из ры, а остальные два из . , он;,. R и R 2. f каждый, означает- атоМ водорода, алкильную группу, имеющую От 1 до 5 углеродных атомов, фениль ную группу, атом хлора либо R и R взятые вместе, представляют собой алкиленовую цепь, содержащую от 3 до 5 углеродных атомовj R - атом водорода или алкильная группа, имеющая от 1 до 5 углеродных атомов, однако, когда чает атом серы, R и Rj. не могут быть алкиленовой цепью, или их солей с активностью против агрегации тромбоцитов крови и может найти применение в качестве противотромботических агентов. Известен способ получения l,.2,J,b тетрагидроимидазо-(2,1-) -хиназолин-2-онов, заключающийся в том, что 2-хлор-3-этоксикарбонйлметил-5,6-диметилхиназолин подвергают взаимодействию с аммиаком в среде .спиртаTlJ Цель изобретения - синтез новых соединений, облгщающих ценными свойствами, позволяющими использовать их в медицине. Предложен способ получения соединений формулы I, заключающийся в том, что соединение формулы CHCOjK, где Zjj , Zj., Х.| - хлор вышеуказанные значения, или бром/ R4. - низший алкил, подвергают взаимодействию с аммиаком . в запаянном сосуде при 100-150 С, преимущественно при 120-130 С, в спиртовой среде с последукхоим выделением целевого продукта в свободном виде или в виде соли. Фармацевтически допустимые соли присоединены с кислотой соединений формулы I можно легко получить путем ,добавления выбранной нетоксичной кис лоты к метанольному раствору соединения I . Пригодными фармацевтически допустимыми солями присоединения с нетоксичными кислотами являются гидр хлорид, гидробромид, алкил- или арил сульфонат, фосфат, сульфат, фумарат малеатг сукцинат, тартрат, цитрат и другие соли нетоксичных кислот, кбто рые обычно используют в данной области. В приводимых ниже примерах, если не указано иначе, под частями, процентами понимают весовые части и пр центы. Пример. Получение 2-хлор-5,6-диметил-З,4-дигидротиено-(2,3-d)-пиримидина. К раствору 4,66 г 2,4-дихлор-5,6-диметилтено-(2,3-d)-пиримидина в 150 мл смеси этанол-хлброформ (1:1 по объему медленно добавляют при перемешивании 2,32 г борогидрида нат рия. Смеси перемешивают при комнатной температуре в течение 6 ч и раст воритель отгоняют в вакууме. К твердому остатку добавили 50 мл воды и нерастворимый продукт отфильтровывают, промывают водой, высушивают и перекристаллиаовывают из. бензола, по лучив 2,05 г 2-хлор-5,5-диметил-З,4дигидротиено-(2,3-d)-пиримидина, т.пл. 170-172с, Найдено,%: С 47,73; Н 4,47; N 13,68. C6HpC N2S. Вычислено, %: С 47,88; Н 4,52, N 13,96. П р и м е р 2. Аналогично примеру 1, но используя эквимолярнде коли чество замещенного 2,4-дихлоротиено пиримидина вместо 2,4-дихлоро-5,6 диметилтиен.о- (2 , 3-d ) -пиримидина, применяемого в примере 1, получают следующие замещенные 2-галоидо-3,4дигйдротиенопиримидиновые соединени (соединения от 2А до 17А) формулы ||| В этом примере реакцию ведут при 40 для соединений 5А, 7А, 8А, 15А и 17А,.при ВО-бО С для соединения 9А, при 40-45°С для соединения 16А и при комнатной температуре для ос тальных соединений. Перечень полученных соединений и их температуры плавления приведены табл.1. Примечание,. Как правило, эти соединения не дают четкой температуры плавления или разложения из-за нестабильности при нагревании, т.е. при нагревании эти соединения постепенно становятся мокрыми, а затем затвердевают при последующем разложении. 2. Цифра в скобках означает тем- пературу разложения после затвердевания. Примерз. Получение 6/7-димеТИЛ- ,2,3,5-тетрагидроимидазо-(1,)-. -тиено-(2,3-О)-пиримидин -2-она. Смесь 6,0 г 2-xлop-5,б-димeтил-3,4-дигидpoтиeнo-.(2 , ) -пиримидина, 5,52 г этилбромацетата и 12,5 г порошкового карбоната калия в 300 мл метилэтилкетона нагреваю т с обратным холодильником при перемешивании в атмосфере азота в течение 4 ч.. После охлаждения нерастворимую неорганическую соль отфильтровывают и фильтрат концентрируют в вакууме, получая неочищенное масло-2-хлор-З-этоксикарбрнилметил-5;6-диметил-З,4-дигидротиено-(2.,3-d)-пиримидин. Из-за нестабильности полученного соединения неочищенное масло используют в последующей реакции. Смесь полученного выше неочищенного масла в 50 мл 10%-ного аммиачноэтанольнрго раствора нагревают в за- , паянной пробирке при 120- 30с на масляной бане в течение 5ч. После охлаждения осажденные кристаллы отфильтровывают, промывают водой и высушивают, получив 3,0 г 6,7-диметил,2,3,5-тетрагидроимидазо-(,2-а)тиено-(2,3-d)-пиримидин-2-она. Хлористоводородную соль полученного соединения получают реакцией свободного соединения с соляной кислотой в метаноле, проводимой обычны образом. Продукт имеет т.пл. 249-255с (с разл.). Найдено,%: С 46,66; Н ,4, N . c oH c N oВычислено,%: С 46,60, Н 4,69, N 16,30. Аналогично примеру 3, но используя эквимолярное количество замещенного 2-галоид-3,4-дигидротиенопиримидина, который получен в примере 2, вместо 2-хлор- 5 ,6-диметил-З, 4-дигидротиено(2,3-d)-пиримидина (lA) , применяемого в примере 3, получают соединения 2-17 формулы I, приведенные в т%бл.2.
Таблица 1
« s a: Ш у fd
X
т Ш
a
s
X Ш с; и s э- 3 т
3
(С Ч
X
« « о о х и
m Формула изобретения 1. Способ получения 1,2,3,5-тeтpaгидpoимидaзoтиeнonиpимидин-2-oнoвгде один из радиксшов Z., Z и 2, является атомом серы, а другие два из радикалов 2 , Z 2. и Z представля ют собой группу СН R 2. каждый, является ато мом водорода, алКильной группой, имеквдей 1-5 атомов углерода, фенильной группой, атомом хлора или взятые вместе R и R представляют собой алкиленовую цепь с 3-5 атомами углерода;R 5 - атом водорода или алкильная группа, имеющая 1-5 атомов углерода, однако, когда Z означает атом серы, R R 2 ив могут быть алкиленовой цепью, или их солей, О.тличающ-ийся тем, что соединение общей формулы :co,ti где Z .Z.Z ,R , Rj и R имеют вышеуказанные значения, Х означает хлор или бром, R4 представляет собой низшую алкильную группу, подвергают взаимодействию с аммиаком в запаянном сосуде при 100-15О С, преимущественно при 120-130 С, в спиртовой среде с последующим вцделением целевого продукта в свободном виде или в виде соли. Источники информации, принятые во внимание при экспертизе 1. Патент OUR 3932407, кл, 260-256,4, опублик.1976.


| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНОЕ ТРИЦИКЛИЧЕСКОГО ПИРАЗОЛОПИРИМИДИНА | 2010 |
|
RU2520966C2 |
| ПРОИЗВОДНОЕ ПИРАЗОЛОПИРИМИДИНА | 2007 |
|
RU2420530C2 |
| АНТИГИПЕРТРИГЛИЦЕРИДЕМИЧЕСКАЯ КОМПОЗИЦИЯ (ВАРИАНТЫ), СПОСОБ ЕЕ ПОЛУЧЕНИЯ, СПОСОБ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ ГИПЕРТРИГЛИЦЕРИДЕМИИ | 1995 |
|
RU2166320C2 |
| МОРФОЛИНО-ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ БИЦИКЛИЧЕСКИХ ПИРИМИДИНМОЧЕВИНЫ ИЛИ КАРБАМАТА В КАЧЕСТВЕ ИНГИБИТОРОВ mTOR | 2012 |
|
RU2609208C2 |
| ПРОИЗВОДНЫЕ ИМИДАЗОПИРАЗИНА ИЛИ ИМИДАЗОДИАЗЕПИНА, АКТИВНЫЕ В ОТНОШЕНИИ РЕЦЕПТОРА СВ2 | 2008 |
|
RU2540074C2 |
| Способ получения -замещенных2-(5-нитро-2-фурил)-4-аминотиено (2,3- )пиримидинов | 1972 |
|
SU446967A1 |
| ПРОИЗВОДНЫЕ АЦЕТАМИДА (ВАРИАНТЫ), СПОСОБЫ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ), ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СРЕДСТВО | 1996 |
|
RU2160256C2 |
| ИНГИБИТОРЫ ALK-КИНАЗЫ | 2013 |
|
RU2675850C2 |
| ПОЛУЧЕНИЕ ДИГИДРОТИЕНО[3,2-d]ПИРИМИДИНОВ И ПРОМЕЖУТОЧНЫХ ПРОДУКТОВ, ПРИМЕНЯЮЩИХСЯ ДЛЯ ИХ СИНТЕЗА | 2008 |
|
RU2528340C2 |
| ФАРМАЦЕВТИЧЕСКОЕ СРЕДСТВО, СОДЕРЖАЩЕЕ ИНГИБИТОР НАТРИЙЗАВИСИМОГО ПЕРЕНОСЧИКА ФОСФАТА | 2015 |
|
RU2740008C2 |


Авторы
Даты
1981-11-07—Публикация
1979-08-10—Подача