(54) СПОСОБ ОПРЕДЕЛЕНИЯ АСКОРБИНОВОЙ ИЛИ ДЕГИДРОАСКОРБИНОВОЙ КИСЛОТЫ
1
Изобретение относится к способам определения аскорбиновой или дегидроаскорбиновой кислоты.
Определение аскорбиновой кислоты имеет большое значение, прежде всегоg
в химии пищевых продуктов, для оценки качества различных пищевых продуктов, таких, например, как фруктовые соки, свежие овощи, свежемороженные овощи и другие. Часто для прохладительных на- JQ питков требуется определенное содержание витамина С, следовательно, оно должно контролироваться. Аскорбиновую кислоту добавляют в качестве антиокислителя и осветлителя, и поэтому содержание ее|5
также должно определяться. При клиникодиагностических исследованиях обнаружение аскорбиновой кислоты в моче обеспечивает быструю диагностику различных заболеваний. Представляет интерес опре- 20 деление аскорбиновой кислоты в сыворотке для тропических стран, так как в условиях этих стран симптомы авитаминозов (цинги) настолько прикрываются симтт -мами других болезней, что их нэвозмож- 25
но выделить. Учитывая ЕЗЖНОСТЬ определения аскорбиновой кислоты, разработаны различные способы ее определения.
Все сказанное вьпые справедливо и для дегидроаскорбиновой кислоты, так как аскорбиновая кислота под действием кислорода воздуха легко переходит в дегидроаскорбиновую кислоту. Поэтому в испытуемых продуктах часто присутствует смесь аскорбиновой и дегидроаскорбиновой кислот. Поскольку дегидроаскорбиновая кислота оказывает такое же действие, как витамин С, то в большинстве случаев целесообразно определять содержание в испытуемом образце дегидроаскорбата.
Известны различные способы определения аскорбиновой или дегидроаскорбинсжой кислоты, например хроматографический способ Г1 .
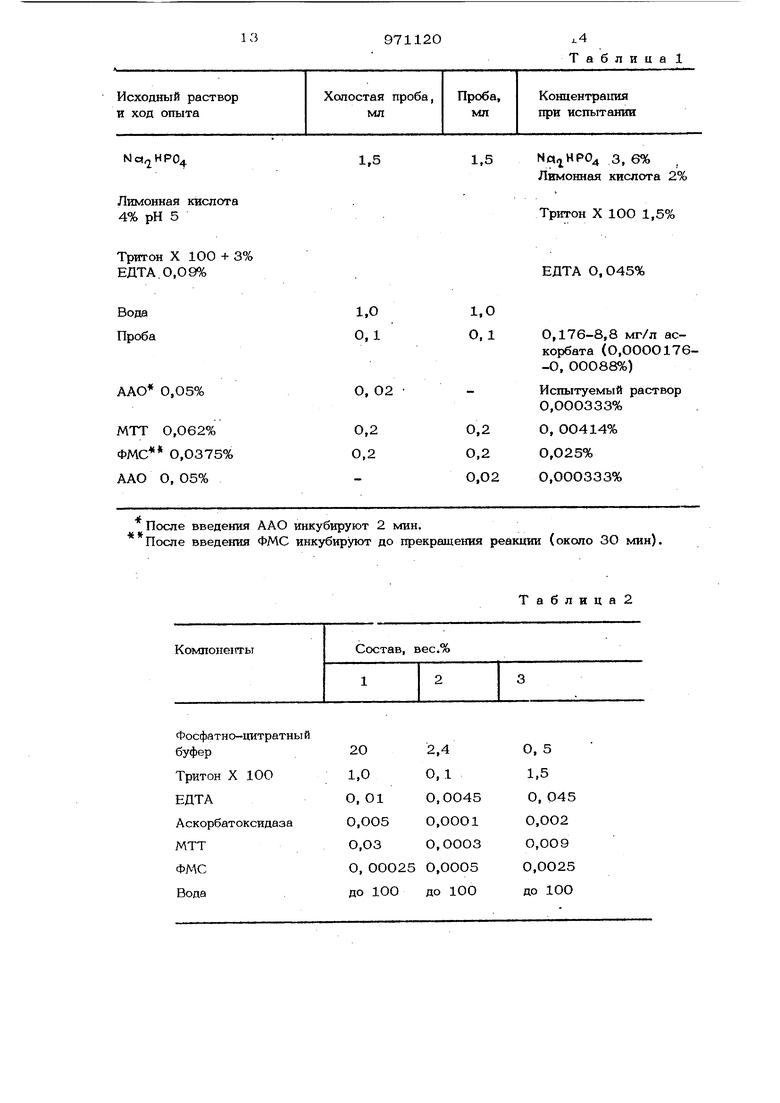
Время, необходшйое для определения по данному способу, очень велико (не менее 2 ч), причем при подготовке пробы к хроматографии теряется значительное количество аскорбата и поэтому количественное определение с помощью указанного способа практически невозможно. Изв€к;тен также способ, основанный на окислении аскорбиновой кислоты в догидроаскорбиновую и осаждении последней в виде производного гидразина 2 . Данный способ трудоемок и мало специфичен, так как все соединения с кетонными функциональными грултшми дают такую же реакцию. Наиболее близок к предлагаемому спо соб определения аскорбиновой или дегидр аскорбиновой кислоты путем обработки исследуемой пробы реагентом, содержащи четвертичную соль тетразоЛа и щелочной буферный раствор, с последующим измеpeiraoM И1 тенсивности окраски образующегося окрашенного соединения ГЗ , Недостатком известного способа является то, что его проводят в щелочной среде и многочисленные вещества оказы вают мешающее действие. Кроме того, указанный способ длителен. Цепь изобретения - сокращение длительности определения и повышение специфи шости. Поставленная цель достигас тся тем, что берут две пробы, к первой пробе добавляют реагент, содержащий фосфатноцитратный буфер, полиэтиленгликолевы и эф1ф октилфенола, этилендиаминтетрауксу ную кислоту, 3-(4,5-диметилтиазолил-2 -2,5-дифенилтетразолбромид, феназинмет сульфат и воду при следующем соотноще нии компонентов, вес,%: Фосфатно-цитратны и 0,5-20 буфер Полиэтиленгликолевый эфир октилфенола0,1-1,,5 Этилендиаминтетрауксусная кислота (ЕДТА) О,О045-0,045 3-( 4,5-Диметилтиазолил-2 ) -2,5 -дифенилтетразолбромид(МТТ) О, 0003-0,03 0,ООО25-0,О0 Феназинметосульфат До 100 Вода а к другой параллельной пробе добавляю указанный реагент, содержащий дополни тельно аскорбатоксидазу в когшчестве 0,0001-0,005 вес.%, вычитают экстин шпо параллельной пробы из экстинкции первой ,пробы и рассчитывают содержани аскорбиновой кислоты, причем в случае определения дегидроаскорбиновой кислот первую исследуемую пробу предваритель обрабатывают избытком гомоцистеина при рН 7-8 и содержание дегидроаскорбиновой кислоты определяют по разности ежду общим содержанием аскорбиновой дегидроаскорбиновой кислот и содержанием аскорбиновой кислоты. Предлагаемы способ осуществляют в слабокислой среде. При таких значениях рН больщинство мещакщих веществ не вступает в реакцию или скорость ее Настолько замедляется, что практически ею можно пренебречь. В такой кислой среде скорость взаимодействия реактива с аскорбиновой кислотой мала, поэтому определение аскорбиновой кислоты с ее помощью практически невозможно. Однако добавление феназинметосульфата в комбинации с детергентом ускоряет эту реакцию. Неож1зданно то, что указанные добавки не ускоряют реакцию реактива с мешающими веществами. Для установления рН, соответствующего слабокислой среде, предпочтительно в интервале между 4,0 и 6,О {особенно методу 4,8 и 5,3) могут использоваться различные буферные системы, в частности фосфатно-цитратный буфер, так как в этом случае при всех количествах аскорбата выполняется пропорциональность между экстинкцией образующегося окращенного вещества и концентрацией аскорбата. Предпочтительным детергентом, используемым в предлагаемом способе, является полиэтиленгликолевый эфир октилфенола (тритон х 10О). Скорость реакции увеличивает также Феназинметосульфат (ФМС), обеспечивая количественное протекание реакции. При использовании других известных переносчиков электронов такого ускоряющего действия не наблюдается. Концентрация ФМС 0,01 -1 ммоль/л (предпочтительнее 0,05-0,15 ммоль/л), так как в этом случае не происходит взаимодействия реактива с соединениями, содержащими 5 Н-группы, такими как гомоцистеин. Такие соединения с S Н-группами можно добавлять, когда имеющийся в пробе де- гидроаскорбат необходимо одновременно восстанавливать до аскорбата. Если в исследуемой пробе находятся ионы двухвалентных металлов, склонных к образованию хелатов, то могут образовьтаться хелаты в результате взаимодействия с получающимся окрашенным соединением формазина, что может влиять на результаты измерений. Хотя образование хелатов в значительной степени подавляется вследствие применения цитрат но-фосфатного буфера, однако целесообраз но добавлять дополнительно к пробе небольшгие количества комплексробразователей, таких как этилендиаминтетрауксус ная кислота с концентрацией 0,0045- 0,045 вес.%. В особых случаях, в частн сти при анализе проб с очень высоким содержанием ионов двухвалентных металлов, целесообразны и добавки в больших количествах, ; При осуществлении предлагаемого i способа используют параллельную пробу, дополнительно содержащую аскорбатоксид зу, которая избирательно окисляет содер жащийся в параллельной пробе аскорбат. По окончании реакции окисления параллел /ную пробу используют как холостую проб .для определения количества аскорбиновой кислоты, т.е. экстинкцию холостой пробы вычитают из экстинкции исследуемогс раствора и разность используют для расчета количества аскорбиновой кислоты, i Данный вариант осуществления способа повышает его специфичность, в особеннос ти в тех случаях, когда в исследуемом растворе присутствуют вещества, которые могут взаимодействовать с солью тетра- зола. При определезгаи дегидроаскорбиновой кислоты ее переводят в аскорбиновую кислоту и определяют описанным способом восстанавливают при помощи органического сульфгидрильного соединения7 предпочтительно гомоцистеина, который берется в избытке, в нейтральной или слабощелочной среде, при рН 7-8 (при использовании .гомоцистеина - при рН 7,5. Если затем для определения образующейся аскорбиновой кислоты устанавливают значение рН, соответствующее слабокислой среде, то взаимодействие реактива с аскорбиновой кислотой протекает без всяких осложнений т.е. избыток сульфгидрильного соединения не восстанавливает вновь образующуюся в ходе реакции дегидроаскорбиновую кислоту, и, таким образом, не происходит искажения результатов анализа. Способ позволяет определять дегидроаскорбиновую кислоту в присутствии аскорбиновой кислоты. Для этого вначале определяют в пробе содержание аскорбиновой кислоты, а затем во второй пробе восстанавливают дегидроаскорбиновую кислоту и определяют ее. ГЬ разности полученных результатов можно определить количество в пробе дегидроаскорбиновой кислоты. Реакция согласно предлагаемому способу протекает примерно ЗО мин, ; Измеряют интенсивность окраски образующегося окрашенного соединения, например, обычным фотоколориметром при подходящей длине волны, например при 578 нм. Однако для определения интенсивности окраски можно использовать и другие известные методы. Удовлетворительные результаты дает и оценка по сравнению полученной окраски с эталонной, в особенности, когда предлагаемый способ проводится с использованием индикаторных полос. А. Определение аскорбиновой кислоты. Готовят раствор следующего состава, /п (%): Nc(HP04 Лимонная кислота Тритон Х-11 0,45(0.045) 0,041(0,0041) В две кюветы (одна из них содержит робу, вторая - холостую пробу), заливают о 3,00 мл раствора и 0,1 мл исследуеой пробы. Пробу и холостую пробу наревают до 37°С. К холостой пробе доавляют 0,00033% аскорбатоксидазы 0,О1 мг/Змл) и инкубируют 2 мин. При том аскорбиновая кислота разлагается. атем к обеим пробам добавляют по ,О75 мг ФМС так, чтобы содержание аствора в них составляло 0,ОО25%. нова инкубируют 5 мин. После этого пределяют экстинкцию холостой пробы Е 1 ) и пробы (Ер). Рассчитывают лЕ о формуле E EP-ELСодержание аскорбиновой кислоты в робе рассчитывают исходя из общей асчетной формулы для определения конентрацийEcJVv-fOOO -испытуемый объем, мп; -объем пробы, мл; -молекулярный вес определяемого вещества; -толщина слоя, см; -коэффициент экстинкции МТТ-формазона (при 578 нм 16,9), л ммоль .см7. Отсюда для L, -аскорбиновой кислоты i,7o-tTfe,.b ; -Гб,9--I-0,0-.100 г I, -аскорбиновой кислоты на л раствора обы). Если предварительно пробу р збавляют то результат умножают на фактор разбав ления F . Б. Определение дегидроаскорбиновой кислоты (ДГА). Восстанавливают ДГА до аскорбиновой кислоты в присутствии гомоцистеина (пр рН 7,5). Определяют сумму аскорбиново кислоты и ДГА и рассчитывают в виде общего содержания аскорбиновой кислоты После Ъычета определенной в отдельном тесте аскорбиновой кислоты из разницы можно рассчитать количество Д1А. Приготовление растворов: а)буферный раствор (фосфат;ный буфе 0,1 ммоль/л, рН 7,5) 163 мг и 2,00 г растворяют примерно в 70 йл воды и доливают до 100 б)раствор гомоцистеина. 60 мг гомо шстеина растворяют в буферном раствор (а) и доливают до 50 мл. в)раствор пробы с аскорбиновой кислотой + ДГА (не больше 0,6 г/л). Значение рН пробы доводят до 7,5 раствором едкого калия (2мопь/л) (.,. и разбавляют водой до пригодной концентра шш. В пробирку вносят пипеткой по 50 мл растворов (а), (б) и (в), смеш1юают ш. и оставляют на 15 мин при комнатной ; температуре. 0,1 мл инкубированнохх) раствора исследуют на содержание аскор биновой кислоты согласно А. Расчет. 1. Общее количество аскорб шовой кислоты (ДГА + аскорбиновая кислота) г ..... пробЫ «3- -(000 где F - фактор разбавления пробы; Y - инкубационный объем, мл V - испытуемый объем, мп,V - объем раствора пробы (в) при инкубировании, мл5 V - объем инкубированного раствор в тесте, .мл; NVQ - молекулярный вес аскорбиновой кислоты, d - толщина слоя, см 6 - коэффициент экстинкции МТТформазона (при 578 нм 16,9), ЛММош -cMt т.е. , с. 5-г,1-(1Ь-,ЪдЕ 0,8442-РйЕ Ь,9 0,5-0,1--1НОО 2.Аскорбиновая кислота из расчета пробы (г/л пробы). 3.Дегидроаскорбиновая кислота. САГС( (результат из(1)- редуЛьтат из (2)) 0,9886 (г ДГА/л пробы) MQ174.13 0,9886 176,13 -MGc(cKop6 Исследуют сок черной смородины на содержание в нем аскорбиновой и дегидроаскорбиновой кислоты. 0,1 мл сока исследуют согласно А на содержание аскорбиновой кислоты, при этом д Е равно 0,43 .что соответствует содержанию 0,121 г/л или 0,О121%. Для определения содержания в нем депщроаскорбиновой кислоты 0,5 мл сока обрабатывают согласно Б гомоцистеином. О,1 мл полученного при этом инкубированного раствора исследуют согласно А на сумму аскорбата и дегидроаскорбата. Е при этом равно 0,38. Отсюда по указанной в Б формуле рассчитьгеают сумму аскорбата и дегидроаскорбата, равную 0,329 г/л или 0,0329%. Содержание дегидроаскорбата составляет 0,329-0,121 0,208 г/л или 0,0208%. Проведена серия опытов определения аскорбиновой или дегидродскорбшювой кислоты. Пример. Фосфатно.4штратный буфер, поверхностно-активное вещество, комплексообразователь, соль тетразола, ФМС, а также воду и исследуемую пробу, вводят в кювету обычного фотокалориметра. После осуществления реакции измеряют разность эксткнкшш по сравнению с воздухом шш водой. В параллельную холостую пробу вводят, кроме того, аскорбатоксидазу (ААО). Такое же количество А АО вводят в исследуемую пробу после окончания реакции, чтобы скомпенсировать разницу в экстинкции, обусловленную самой ААО. Подробности проведения спрсоба, при.меняемые реактивы и их количества приведены в табл. 1. Реактивом приведенного выше состава можно определять от 5 до 25О мг аскорбата в исследуемой жидкости. При более высоких концентрациях пробу необходимо соответствующим образом раз- бавить, при меньших концентрациях брать большее количество пробы. Количество воды при этом соответствующим образом должно быть уменьшено. При проведениивсех последующих определений используют составы реагент аналогично примеру 1 {табл. 2). П р и м е р 2. Определение аскорбата в апельсиновом соке, ОД мл апельсинового сока вводят в кювету в качестве пробы аналогично при меру 1, В результате обнаруживают концентрашпо витамина С 305 мг/л, что соответствует декларации (ЗОО мг/л). После анализа количество аскорбиновой кислоты, введенной в пробу, полностью ощюделяется (lOO%). Окраска с течени времени не изменяется. Небольшое пому 1нение апельсинового сока не оказывает влияния на результаты анализа. Пример 3. 2,0 лимонного напит ка растворяют в 2О мл воды и 0,1 мл полученного раствора вводят в кнвету по примеру 1. Находят 96 мг витаМгаш С на 1ОО г сухого вещества. Изменения окраски с течением времени не наблюда ется. Определяют 99,2% аскорбиновой кислоты, добавленной в пробу перед разбавлением. Небольшое помутнение раст вора не оказывает влияния на результаты анализа. П р и м е р 4. Определение аскорбат в плодах шиповника. 5 мл концентрата шиповника растворяют в 10О мл воды. ОД мл полученного раствора после центрифугирования вводят в кювету по примеру 1.. Находят 177О мг витамина С в расчете на 1 л концентрата. Небольшое изменение окрас во времени, наблюдавшееся в пробе и в холостой пробе, учитывают с помошью экстраполяшш. Аскорбиновой кислоты, добавленной к пробе перед разбавлением, обнаруживают 10О%. Легкое окрашивание разбавленного экстракта не оказывает влияния на результаты анализа. П р и м е р 5. Определение аскорбат в соке черной смородины. 1 мл сока черной смородины разбавля ют водой до Ю мл и О,1 мл полученног раствора вводят в кювету по примеру 1. Находят ЗОБ мг/л витамина С. Обнаруж вают 100% аскорбиновой кислоты, добавленной перед разбавлением. Изменения окраски с течением времени не наблюдается Чтобы проверить, не оказывает ли мешающего влияния неразбавленный сильно окрашенный сок, для снижения в нем содержания аскорбата его выдержи- вают в открытой посуде в течение 4 недель в холодильнике. Затем 0,1 мл не: разбавленного сока вводят в кювету. На ходят еше 93 мг/л витамина С. Интенси ная окраска исходной пробы не оказывает мешающего влияния. Изменения окраски с течением времени не наблюдается. Добавленная в пробу аскорбиновая кислота полностью определяется. Примере. Определение аскорбата в пиве. Чтобы обеспечить прозрачность и возможность консервирования в пиво можно добавить аскорбиновую кислоту, хотя для баварского пивоварения эта операшга не приемлема. Ни в светлом или темном бочковом пиве, ни в пиве в банках при проведении анализа по способу, описанному Б примере 1, аскс иновой кислоты нет. Моиающего влияния не обнаруживйают. Добавленное в пробу количество аскорбиновой кислоты полностью обнаруживают. П р и м е р 7. Осфеделение аскорбата 3 шпинате. Бланшированный свежемороженный шпинат после оттаивания тщательно перемешивают, 50 г его обрабатывают известным способом, но вместо НРО,используют метафосфорную кислоту. Вводят 0,2 мл экстракта, рН которого равен 5. При проведении способа аналогично примеру 1 находят 22 мг аскорбата в расчете на 1ОО г свежемороженного шпината при содержании в нем 8% сухой массы. Это соответствует 275 мг аскорбата в расчете на 1ОО г сухой массы. Из добавленного к шпинату перед экстрагированием количества аскорбиновой кислоты обнаруживают 99,8%. Изменения окраски с течением времени не наблюдают. П р и м е р 8. Определение аскорбата в картофеле. 50 г картофеля моют, измельчают и обрабатывают таким же образом, как и шпинат в примере 7. рН.экстракта устанавливают равньгм 5 и объем его доводят до 1ОО мл. После центрифугирования 50О мл вводят в кювету. Обнаруживают 18,9 мг аскорбата в расчете на 1 кг картофеля. эта величина составляет примерно -150 мг/кг. В данном случае используют старый картофель, сильно высохший и частично проросший. В этих . условиях содержание витамина С в нем сильно снижается или даже полностью исчезает. Для проверки к картофелю перед экстрагированием добавляют 75 мг аскориновой кислоты, после чего определяют ее в количестве 97%. Изменения окраски с течением времеи не наблюдают.. П р и м е р 9. Определение аскорбата сыворотке. Содержание аскорбиновой кислоты в сыворотке должно иаход11ться в пределах между 2 и 15 мг/лна 1 мл сыворотки, Из которой с помощью трихлоруксусной кислоты удаляют белок и испош зуют в качестве пробы. В шести различных сыворотках обнаруживают от -1,5 до 2,64мг/л аскорбата. Изменения окраски с течением времени не наблюдают. При добавке в пробу 17,2 мг аскорбата на 1 л сыворот ки вновь обнаруживают практически 1ОО% Пример 10. Опредепеш: е аскорбата в моче. аскорбата в моче может Содержание достигать значительных количеств. При нормальном питании в мочу попадает от 10 до 100 мг/л. При приеме доз, больше 100 мг 60-8О% принятого количеств обнаруживают в моче. Поэтому при потреблении аскорбиновой кислоты в количест вах, во много раз превышающих нормальное, следует ожидать и большее, чем 1ОО мг/л, содержание ее в моче. В свежей моче при объеме пробы О,1 мл обнаруживают 257 мг/л аскорбата. При этом вновь обнаруживают 98,3% добавленной перед анализом аскорбиновой кислоты. Изменения окраски с течением времени и других мешающих влияний не наблюдаю Прим ер 11. Большие количества витамина С в моче, найденные в примере Ю, могут частично или полностью подавлять образование окрашенных соедине1-щй на обычных индикаторных полоска на глюкозу, кровь или билирубин и т.д., основанное на окислении различных лейкоокрашенных соединений, и, таким бобра- зом, приводить к искажению результатов, что молсет быть установлено с помощью индикаторной бумаги. Круглый фильтр из испытуемой бумаги-тщательно промывают раствором О,2 моль, /О, 1 моль лимоннокислого буфера с рН 5, отсасываю на вакуумном фильтре и сушат в вакууме при комнатной температуре. Затем на фильтр, лежащ:ий в чашке Петри, наливают смесь, соответствующую по сославу холостой пробе примера 1, но не содержащую пробы и аскорбатоксидазы, после чего его снова сушат в вакууме лри комнатной температуре в тегиноте. На подготовленны таким образом фильтр наносят по калле растворы, содержащие 2; 5; 10; 25 и 50м аскорбата/100 мл. В течение 1 мин на бумаге образуются сине-фиолетовые пятна, интенсивность окраски которых возрастает с увеличением концентрации аскор бата. При накапывании воды наблюдают только легкое желтое окрашивание. Пример 12. Определение дегидроскорбиновой кислоты. Исследуемый материал экстрагируют в случае необходимости разбавляют так, тобы содержание дегидроаскорбата сосавляло 75-1500 мг/л (0,005-0,10%). ля раствора устанавливают показатель Н, равный 7,5. К двум частям этого аствора добавляют две части К-фосфатноо буфера (рН 7,5, О,1 ммоль/л, 1%, иапазон 0,1-2%). 0,1 мл приготовленноо таким образом раствора исследуют через 15 мин аналогично примеру 1 на аскорбат и определяют сумму аскорбата дегидроаскорбата. Принимая коэффициент разбавления F равным 2,5, можно определить после вычитания полученного ранее содержания аскорбата содержание в пробе дегидроаскорбата. Спустя 2 ч после введения О, 5 г аскорбиновой кислоты у человека берут на анализ мочу, которую делят на 3 порции: первую (l) используют неизменной, вторую (2) дополняют О,О05% гомоцистеина и третью (3) - 0,01% дегидроаскорбиновой кислоты. Исследуют их по описанному в А способу на содержание аскорбиновой кислоты (способ I). Для сравненияиспользуют известные способы: окисление аскорбиновой кислоты и осаждение в виде производного гидразина (способ П) и восстановление дихлорфенолиндофенолом (реактив Тиллманна) в качестве титриметри- ческого метода (способ 111). Результаты представлены в табл. 3. I В каждой порции должно быть одинаковое количество аскорбиновой кислоты, и только предлагаемый способ (способ I) .дает одинаковые значения. Способ П частично выявляет добавленную дегидроаскорбиновую кислоту (отклонение в порциях 1 и 2 вызвано неточностью способа). Способ иг зачастую дает сильное искажение вследствие введения гомо1шстеина, которыйг включается в качестве восстановителя. Однако дегидроаскорбиновая кислота также вызывает значительное увеличение значения, Предлагаемый способ определения аскорбиновой кислоты (витамина С) и дегидроаскорбиновой кислоты прост и по сравнению с известными способами значительно более специфичен, более устойчив к мешающему влиянию других веществ и менее длителен.
Лимонная кислота 4% рН 5
Тритон X 100 + 3% ЕДТА.0,09%
Вода Проба
ААО О, О 5%
МТТ 0,062% ФМС О,О375% АЛО О, 05% После введения ААО инкубируют 2 мин. После введения ФМС инкубируют до прекращения
1,5Nct HPO 3, 6%
Лимонная кислота 2%
Тритон X 10О 1,5%
ЕДТА 0,045%
1.0 0.1
0,176-8,8 мг/л аскорбата (О,ОООО176-О, 00088%)
Испытуемый раствор 0,000333%
О, 00414%
0,2
0,О25% 0.2 О,О2
0,ОООЗЗЗ% реакции (около ЗО мин).






| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЭФФЕКТИВНОСТИ ЗАЩИТЫ ЛИМФОЦИТОВ ОТ ПЕРЕОКИСЛЕНИЯ | 2013 |
|
RU2525183C1 |
| СПОСОБ ОЦЕНКИ ЭФФЕКТИВНОСТИ ЗАЩИТЫ ЛИМФОЦИТОВ ОТ АПОПТОЗА | 2014 |
|
RU2568886C1 |
| СПОСОБ СОЗДАНИЯ РЕАГЕНТА ДЛЯ ОПРЕДЕЛЕНИЯ САХАРОВ В ПРИСУТСТВИИ РЕДУЦИРУЮЩИХ ВЕЩЕСТВ | 2011 |
|
RU2485515C1 |
| СПОСОБ ЗАЩИТЫ КЛЕТОК ОТ АПОПТОЗА | 2013 |
|
RU2541774C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАННЕЙ СТАДИИ АПОПТОЗА | 2013 |
|
RU2540500C2 |
| СПОСОБ ОЦЕНКИ ЭФФЕКТИВНОСТИ СТИМУЛЯЦИИ АНТИОКСИДАНТНОЙ АКТИВНОСТИ | 2013 |
|
RU2516925C1 |
| Способ определения содержания креатинина, креатина и саркозина в биологической жидкости | 1986 |
|
SU1582993A3 |
| Способ контроля качества биохимической очистки сточных вод и состояния активного ила | 1987 |
|
SU1474545A1 |
| ПРЕПАРАТ, СОДЕРЖАЩИЙ КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ ЖЕЛЕЗА (III) И АКТИВНОЕ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНОЕ ВЕЩЕСТВО | 2006 |
|
RU2394597C2 |
| СПОСОБ ОБНАРУЖЕНИЯ КОЛИЧЕСТВА ЛИМОННОЙ КИСЛОТЫ И ЕЕ СОЛЕЙ | 2000 |
|
RU2229710C2 |

но-цитратны и
X 100
атоксидаза
Таблица2
О, 5
20 1.0
0.1
О, 045
0.0045 О, О1 О,002
О.ОО01 0,О05 О,ОО9
О.ОООЗ О.ОЗ О.ОО25
О. 00025 0,0005 до 10О до 1ОО до 100
971120
15
О, 133(О,О133) 0,130(0,0130) 0,134 (О,О134) 0,140 {0„0140) 0,155 (0,0155) 0,255(0,0255) ОД44(0„0144) 0,201(0,0201) 0,162(0,0162)
Формула изобретения
Способ определения аскорбиновой щш дегидроаскорбтюовой кислоты с использованием обработки исследуемой пробы реагентом, содержащим четвертичную соль тетразолия и буферный раствор, с последующим измерением интенсивности окраски образующегося окрашенного соединения
отличающийся тем, что, с целью сокращения длительности определения и повышения специфичности, берут две пробы, к первой пробе добавляют
реагепт, содержащий фосфатно-цнтратныШ буфер, полиэтиленгликолевый эфир октилфенола, этилендиаминтетрауксусную кислоту 3-(4,5-диметилтиазолил-2)-2,5-дифенилтетразолбромид, феназинметосульфат и воду при следующем соотнощении компонентов, вес.%;
Фосфатпо-цитратны и
буфер0,5-20
Полиэтиленгликолевый
эфир октилфенола 0,1-1,5
Этилендиаминтетрауксусная кислота О,0045-О, О45
3-(4,5-диметилтиазолил-2)-2,516Т а б л и .ц а 3
-дифенилтетразолбромид0,ОООЗ-О,ОЗ
Феназинметосульфат 0,00025-0,0025
ВодаДо 1ОО
и к другой параллельной пробе добавляют указанный реагент, содержащий дополнително аскорбатоксидазу в количестве О,ОО010, ОО5 вес.%, вычитают экстинкцию параллельной пробы из экстинкшга первой пробы и рассчитывают содержание аскорбиновой кислоты, причем в случае определения дегидроаскорбиновой кислоты первую исследуемую пробу предварительно обрабатывают избытком гомоцистеина при рН 7-8 и содержание дегидроаскорбиновой кислоты определяют по разности между общим содержанием аскорбиновой и дегидроаскорбиновой кислот и содержанием аскорбиновой кислоты.
Источники информашш, принятые во внимание при экспертизе

Авторы
Даты
1982-10-30—Публикация
1978-08-25—Подача