Изобретение относится к области биоорганической химии, в частности, к улучшенному способу получения N4-ацильных производных 2 -дезоксицитидина общей формулы
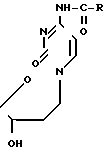 (1) где R = CH3, -СН(СН3)2 или С6Н5.
(1) где R = CH3, -СН(СН3)2 или С6Н5.
Указанные соединения применяются в качестве промежуточных продуктов в химическом синтезе олигонуклеотидов, широко использующихся для исследований в области биотехнологии и молекулярной биологии.
Современной тенденцией в этой области является разработка эффективных способов получения N, O-защищенных мономеров, несущих легко удаляемые N-защитные группировки. Применение таких мономеров существенно упрощает и ускоряет синтез олигонуклеотидов.
Известен способ получения N-ацильных производных дезоксинуклеозидов, в частности N4-бензоил-2' -дезоксицитидина (bz4dC), состоящий из 5 стадий:
взаимодействие дезоксицитидина (dC) с избытком триметилхлорсилана (TMSCl) в пиридине в течение 0,25 ч и ≈ 25оС; ацилирование полученного 5' , 3' -О-ТMS производного dC бензоилхлоридом в пиридине в течение 2 ч при той же температуре; гидролиз реакционной смеси в течение 0,1 ч при 0оС; аммонолиз О-TMS защитных групп в течение 0,25 ч при ≈ 25о; выделение продукта известными методами.
Выход целевого продукта составляет 95 % , длительность процесса - 2,6 ч. Недостатками данного способа являются его многостадийность, трудоемкость и излишняя длительность, что обусловлено введением и последующим удалением временных О-ТМS защитных групп. Это приводит, во-первых, к большому расходу довольно дорогого TMSCl (255 руб/кг) и, во-вторых, сопряжено с риском аммонолиза N4-защитных группировок, особенно более щелочелабильных , чем N-бензоильная, на 4 стадии процесса.
Наиболее близким к описываемому способу является способ получения N4-ацильных производных дезоксицитидина, состоящий из двух стадий: ацилирования dC ангидридом карбоновой кислоты в кипящем этаноле (78оС), с добавлением ангидрида четырьмя равными (1 - 2,5 мол. эквивалента) порциями через промежутки времени, равные 1 ч, и выделения продукта известными методами. Выход N4-ацетилдезоксицитидина составляет 83 - 89% ; N4-бензоилдезоксицитидина - 90% , длительность процесса 5 ч, соотношение компонентов dC: ангидрид: растворитель 1 : (1 х 4): 100 (по массе) и 1 : (1 - 2,5) х 4 : 400 (моль).
Недостатки:
сложность процесса, заключающаяся в его высокой длительности и необходимости нагревания реакционной смеси, а также порционной загрузке ангидрида;
низкая скорость образования целевого продукта из-за побочной реакции растворителя, взятого в большом избытке, с ангидридом карбоновой кислоты.
Неудачный выбор растворителя выражается в его способности реагировать с ангидридом, что приводит е дополнительному расходу последнего и закислению среды, а также - в его недостаточной растворяющей способности, что не позволяет создать высокие концентрации реагентов и достигнуть высокой скорости реакции;
труднодоступность сухого (100% ) этанола.
Задачей изобретения является упрощение процесса за счет сокращения его длительности и снижения трудоемкости.
Поставленная цель достигается тем, что реакцию ацилирования проводят в апротонном растворителе при комнатной температуре с соотношением компонентов (dC : ангидрид : растворитель (в молях) = 1 : (4 - 15) : (26 - 40). Растворитель выбирают преимущественно из группы: N, N' -диметилформамид, диметилсульфоксид, триметилфосфат (ДМФ, ДМСО, ТМФ соответственно).
Сущность способа заключается в следующем.
Дезоксицитидин растворяют в соответствующем апротонном растворителе, при перемешивании добавляют ангидрид карбоновой кислоты и выдердивают при комнатной температуре в течение 0,5 - 1 ч и продукт выделяют. 
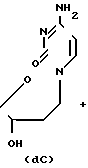
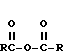


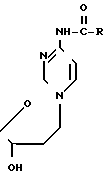 где R = -CH3; -CH(CH3)2; -C6H5(фенил).
где R = -CH3; -CH(CH3)2; -C6H5(фенил).
Выход целевых продуктов составляет 90 - 94% , длительность процесса 0,5 - 1 ч, в зависимости от типа ацильного остатка и условий реакции. Чистота и характеристики полученных продуктов - на уровне прототипа.
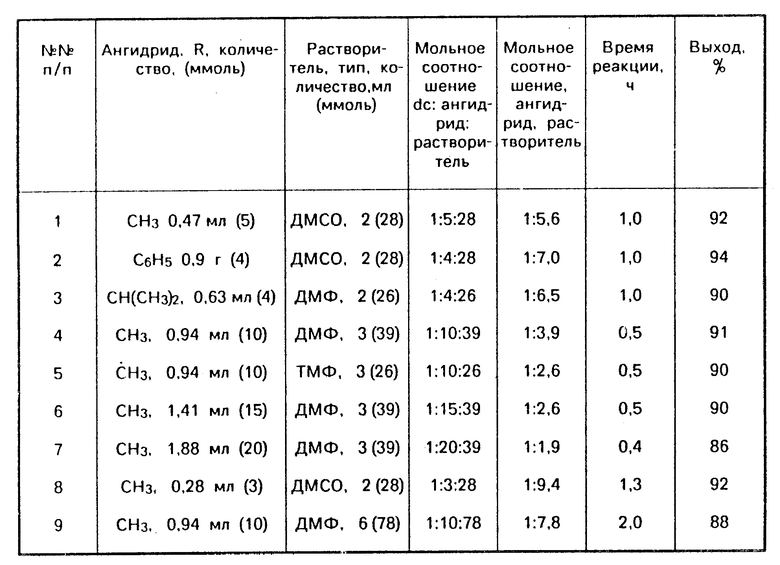
Зависимость скорости реакции ацилирования (время полного ее окончания) и выхода целевого продукта от соотношения компонентов реакционной смеси (в расчете на 1 ммоль dC) представлена в таблице 1.
П р и м е р 1. Синтез N4-ацетилдезоксицитидина. К раствору dC (0,227 г, 1 ммоль) в 2 мл ДМСО добавляют уксусный ангидрид (0,47 мл, 5 ммоль), перемешивают, выдерживают в течение 1 ч при комнатной температуре. Продукт осаждают смесью пентан-эфир (9 : 1), (200 мл), охлаждая смесь при -20оС, 1 ч, центрифугируют осадок, промывают его той же смесью (2 х 50 мл), сушат в вакууме над Р2О5 2 ч. Получают 0,252 г (92% ) целевого продукта, гомогенного при ТСХ в системе хлороформ-этанол (4 : 1) на силикагеле, Rf = 0,55. УФ-спектр (Н2О) : λmax 215 нм (19300), 247 нм (15100) и 297 нм (8700). λmin 227 нм (6050) и 272 нм (4700). Скорость реакции деацетилирования ( τ1/2} при 24; в смеси 25% , NH4OH-этанол, 3 : 1, по объему) - 142 с.
П р и м е р 2. Синтез N4-бензоилдезоксицитидина. Синтез проводят аналогично примеру 1, используя для ацилирования 1 ммоль dC 0,91 г (4 ммоль) бензойного ангидрида, 2 мл ДМСО, время реакции 1 ч. После осаждения смесью эфир - пентан (1 : 1, 200 мл) и промывки осадка теплым эфиром (3 х 50 мл) от бензойной кислоты получают 0,311 г (94% ) целевого продукта. Он гомогенен при ТСХ в условиях примера 1. Rf = 0,60. УФ-спектр (Н2О) : λmax 257 нм (22100) и 302 нм (12200), λmin218 нм (8400) 282 нм (9100). Скорость деацилирования в условиях примера 1 - τ1/2} = 74 мин.
П р и м е р 3. Синтез N4-изобутилирилдезоксицитидина. Синтез проводят аналогично примеру 1, используя 1 ммоль dC 0,84 мл (5 ммоль) изомасляного ангидрида, 2 мл ДМФ и проводя ацилирование в течение 1 ч. Продукт переосаждают из хлороформа в пентан, получая 0,283 г (90% ). Продукт гомогенен на ТСХ в условиях примера 1, Rf = 0,68. УФ-спектр (Н2О) : λmax 216 нм (17300), 249 нм (15000) и 300 нм (8000), λmin 229 и 274 нм, скорость деацилирования (в условиях примера 1) τ1/2} = 690 с.
П р и м е р 4. Синтез N4-ацетилдезоксицитидина. Синтез проводят в услвоиях примера 1, используя для ацилирования 1 ммоль dC 4 мл триметилфосфата (для получения раствора dC нагревают в нем 2 мин при 120oС), 0,94 мл (10 ммоль) уксусного ангидрида, время реакции 0,5 ч. Выход продукта 0,23 г (90% ). Характеристики аналогичны приведенным в примере 1.
Использование описываемого способа получения N4-ацильных производных 2 -дезоксицитидина обеспечивает следующие преимущества:
ускорение процесса в 5 - 10 раз (с 5 ч до 0,5 - 1 ч) при одновременном снижении температуры процесса на 55оС (с 78 до 23оС).
Упрощение процесса в результате исключения нагревания реакционной смеси и применения одноразовой загрузки ангидрида вместо 4-разовой в прототипе.
Увеличение выхода целевого продукта на 4 - 7% . (56) G. S. Ti, B. L. Gafney, R. A. Iones, I. Amer, Chem. Soc, 1982, 104, NO 5,1315.
B. A. Otter. I. I. Fox, in "Synthetic procedures in nucleis acid chemistry", v. 1, N. Y. 1968, р. 285.
Использование: в качестве промежуточного продукта в синтезе олигонуклеотидов. Сущность: продукт N4-ацильные производные 2'-дезоксицитидина формулы, указанной в описании. Выход 90 - 94% . Реагент 1: 2'-дезоксицитидин. Реагент 2: уксусный ангидрид, бензойный ангидрид, изомасляный ангидрид. Условия реакции: в среде N, N' - диметилформамида, диметилсульфоксида или триметилфосфата при молярном соотношении дезоксицитидин : ангидрид : растворитель = 1 : (4 - 15) : (26 - 40). 1 з. п. ф-лы.

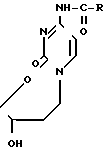
где R- -CH3, -CH(CH3)2, -C6H5,
ацилированием 2'-дезоксицитина избытком ангидрида карбоновой кислоты в органическом растворителе с последующим выделением целевого продукта, отличающийся тем, что, с целью упрощения процесса, ацилирование проводят в апротонном растворителе при молярном соотношении компонентов дезоксицитидин : ангидрид : растворитель 1 : 4 - 15 : 26 - 40.
Авторы
Даты
1994-02-15—Публикация
1991-03-05—Подача