Изобретение относится к новым химическим соединениям, а именно к гидрохлоридам производных 1-бензил-4-инданон)-метилпиперидина формулы I 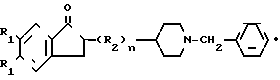 HCl где R1 - H или метокси;
HCl где R1 - H или метокси;
R2 - метилен;
n - целое число 1 или 2, которые обладают высокой и строго селективной антиацетилхолинэстеразной активностью и могут найти применение в медицине.
Целью изобретения является разработка новых соединений, которые могут быть получены с помощью известных способов получения аналогичных соединений и обладают полезными фармацевтическими свойствами.
П р и м е р 1. 1 -бензил-4-[2-[-1-инданон)-2-илиденил] ] этилпиперидин гидрохлорид.
0,32 г 60 % -ного гидрида натрия промывают гексаном и к этому добавляют 10 мл ТГФ. К этому прикапывают раствор 2,12 г диэтил-(1-инданон-2-ил) фосфоната в 30 мл ТГФ при 0оС. Полученную смесь перемешивают при комнатной температуре в течение 30 мин и снова охлаждают до 0оС с последующим добавлением раствора 4,43 г 1-бензил-4-пиперидинацетоальдегида в 10 мл ДМФА. Полученную смесь перемешивают при комнатной температуре в течение 2 ч и при 50оС в течение 2 ч, а затем кипятят в течение 2 ч при нагревании смеси. К реакционной смеси добавляют метанол и 20 % серную кислоту при 0оС. Через 10 мин после добавления реакционную смесь подщелачивают водным раствором гидроокиси натрия и экстрагируют этилацетатом. Органическую фазу промывают насыщенным солевым раствором, сушат над сульфатом магния и концентрируют в вакууме. Полученный остаток очищают на хроматографической колонке силикагелем (метилен-хлорид: метанол = 500 : 1). Элюат концентрируют в вакууме, а остаток растворяют в метилен-хлориде. К полученному раствору добавляют 10 % -ный раствор соляной кислоты в этилацетате, а затем концентрируют в вакууме до получения 0,73 г (выход 27 % ) указанного в заглавии соединения. При этом выделяют также 1,37 г диэтил(1-инданон-2-ил)фосфоната.
П р и м е р 2. 1-бензил-4-[2-[(1-индинанон)-2-ил] ] этилпиперидингидрохлорид (1).
0,37 г 1-бензил-4-[2-[(1-инданон)-2-илиденил] ] -этилпиперидина растворяют в 10 мл метанола, а затем добавляют 0,1 г 5 % родия на угле. Полученную смесь гидрируют при комнатной температуре при атмосферном давлении в течение 24 ч. Катализатор отфильтровывают, и полученный фильтрат концентрируют в вакууме. Остаток очищают на хроматографии концентрируют в вакууме. Остаток очищают на хроматографической колонке (метиленхлорид : метанол = = 200 : 1), полученный элюат концентрируют в вакууме, а остаток растворяют в метиленхлориде. К полученному раствору добавляют 10 % -ный раствор соляной кислоты в этилацетате, а затем концентрируют в вакууме до получения кристаллов, которые перекристаллизовывают изосмеси метанол/IPE до получения 0,33 г (выход 80 % ) указанного в заглавии соединения со следующими характеристиками:
Т. пл. 224-225оС.
С23H27Na ˙ HCl
Рассчитано, % : С 74,68; Н 7,63; N 3,79.
Найдено, % : С 74,66; Н 7,65; N 3,77.
П р и м е р 3. 1-бензил-4-[(5, 6-диметокси-1-инданон)-2-ил] -метилпиперидин-гидр-охлорид (2)  HCl 0,4 г 1-бензил-4-[(5, 6-диметокси-1-инданон)-2-илиденил] -метилпиперидина растворяют в 16 мл ТГФ, затем добавляют 0,04 г 10 % палладия на угле. Полученную смесь гидрируют при комнатной температуре при атмосферном давлении в течение 6 ч. Катализатор отфильтровывают, а полученный фильтрат концентрируют в вакууме. Остаток очищают, используя хроматографическую колонку с силикагелем (метиленхлорид : метанол = 50 : 1). Полученный элюат концентрируют в вакууме, а остаток растворяют в метиленхлориде. К полученному раствору добавляют 10 % -ный раствор соляной кислоты и этилацетате, а затем концентрируют в вакууме с получением кристаллов, которые перекристаллизируют из смеси метанол/IPE, получая 0,36 г (выход 82 % ) указанного в заготовке соединения со следующими свойствами:
HCl 0,4 г 1-бензил-4-[(5, 6-диметокси-1-инданон)-2-илиденил] -метилпиперидина растворяют в 16 мл ТГФ, затем добавляют 0,04 г 10 % палладия на угле. Полученную смесь гидрируют при комнатной температуре при атмосферном давлении в течение 6 ч. Катализатор отфильтровывают, а полученный фильтрат концентрируют в вакууме. Остаток очищают, используя хроматографическую колонку с силикагелем (метиленхлорид : метанол = 50 : 1). Полученный элюат концентрируют в вакууме, а остаток растворяют в метиленхлориде. К полученному раствору добавляют 10 % -ный раствор соляной кислоты и этилацетате, а затем концентрируют в вакууме с получением кристаллов, которые перекристаллизируют из смеси метанол/IPE, получая 0,36 г (выход 82 % ) указанного в заготовке соединения со следующими свойствами:
Т. плавления: 211-212оС (с разложением)
Рассчитано, % : С 69,30, Н 7,27; N 3,37.
С24Н29NO3 ˙ HCl
Найдено, % : С 69,33; Н 7,15; N 3,22.
Изучено ацетилхолинэстеразное ингибирующее действие соединений 1 и 2 in vitro. В качестве источника ацетилхолинэстеразы брали гомогенат мышиного мозга. Ингибирующую активность ацетилхолинэстеразы образца выражали в единицах концентрации 50 % -ного ингибирования (ИК50). ИК50соединения 1 и 2 составляет соответственно 0,23 мкМ и 0,053 мкМ.
Таким образом, соединения изобретения проявляют высокую атиацетилхолинэстеразную активность. (56) Общая органическая химия. / Под ред. Бартон Д. И. и Оллис У. Д. т. 5 Соединение фосфора и серы. М. : Химия, 1983, с. 82.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ПИРРОЛИДИНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1990 |
|
RU2024506C1 |
| ПОЛИМОРФНЫЕ МОДИФИКАЦИИ ДОНЕПЕЗИЛА ГИДРОХЛОРИДА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЯ, СОПРОВОЖДАЮЩЕГОСЯ АКТИВНОСТЬЮ АЦЕТИЛХОЛИНЭСТЕРАЗЫ | 1997 |
|
RU2190603C2 |
| ЗАМЕЩЕННЫЕ ЛИПОСАХАРИДЫ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ЭНДОТОКСИКОЗА | 1996 |
|
RU2170738C2 |
| ПРОИЗВОДНЫЕ ЦИКЛИЧЕСКОГО АМИДА ИЛИ ИХ ФАРМАКОЛОГИЧЕСКИ ПРИЕМЛЕМАЯ СОЛЬ, ОБЛАДАЮЩАЯ АНТИАЦЕТИЛХОЛИНЭСТЕРОДНОЙ АКТИВНОСТЬЮ | 1991 |
|
RU2010794C1 |
| НОВЫЕ ПИРИДИНОВОЕ ПРОИЗВОДНОЕ И ПИРИМИДИНОВОЕ ПРОИЗВОДНОЕ (1) | 2005 |
|
RU2330021C2 |
| СОЕДИНЕНИЕ, ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМАЯ СОЛЬ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1992 |
|
RU2095366C1 |
| ПРОИЗВОДНЫЕ АМИНОКИСЛОТ, ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМАЯ СОЛЬ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1991 |
|
RU2057124C1 |
| ПРОИЗВОДНЫЕ ПЕПТИДОВ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, ПОСРЕДНИКОМ КОТОРЫХ ЯВЛЯЕТСЯ ТАХИКИНИН | 1991 |
|
RU2073683C1 |
| ГЕТЕРОЦИКЛО-ЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ АМИНОВ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ИНГИБИРОВАНИЯ ХОЛИНЭСТЕРАЗЫ, СПОСОБ ПОЛУЧЕНИЯ СОЕДИНЕНИЙ | 1992 |
|
RU2119920C1 |
| ПРОИЗВОДНЫЕ ПЕПТИДОВ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ | 1992 |
|
RU2043365C1 |



Использование: в качестве веществ, обладающих антиацетилхолинэстеразной активностью. Сущность изобретения: продукт - гидрохлориды производных 1-бензил-4-(1-инданон)метилпиперидина общей формулы 1, где R1 - атом водорода или метоксигруппа, R2 - группа -CH2-, n = 1 или 2. 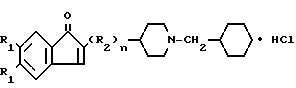
Гидрохлориды производных 1-бензил-4-(1-инданон)-метилпиперидина общей формулы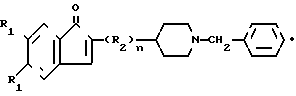 HCl/
HCl/
где R1 - водород или метоксигруппа;
R2 - группа -CH2-;
n = 1 или 2.
Авторы
Даты
1994-03-15—Публикация
1988-06-21—Подача