Изобретение относится к химическим способам защиты растений, конкретно к способу уничтожения паразитов, акарид и моллюсков.
Известно использование нитропирролов для борьбы с насекомыми и клещами. Однако известные нитропирролы являются недостаточно эффективными при их использовании в химических способах защиты растений.
Целью изобретения является повышение эффективности способа.
Указанная цель достигается за счет обработки паразитов, акарид и моллюсков, а также мест их распространения и обитания производным пиррола формулы (I) где W - циано- или нитрогруппа;
(I) где W - циано- или нитрогруппа;
Х - циано, бром, хлор, йод или трифторметил;
Y - водород, бром, хлор, йод или трифторметил;
Z - водород, бром, хлор, йод;
B - водород, С1-С6-алкил, С1-С2-алкил, замещенный С1-С4-алкоксигруппой, возможно замещенный хлором, алкил, пропинил, С1-С2-алкил, замещенный циано- или гидроксигруппой, незамещенный или замещенный хлором, бензил, замещенный хлором бензоил, триметилсилил или COR, где R - низший алкил, фенил или цианогруппа в количестве 0,05-4 кг/га.
Настоящее изобретение иллюстрируется следующими примерами.
П р и м е р 1. Получение 1-метил-5-нитропиррол-2-карбонитрила.
К раствору 300 мг 5-нитропиррол-2-карбонитрила (2,14 ммоль) в 15 мл ацетона добавляется 360 мг карбоната калия (2,6 ммоль) и 0,165 мл йодистого метила (1,6 ммоль, 372 мг). Затем смесь перемешивается при комнатной температуре в течение 24 ч. Реакционная смесь выливается в смесь льда с водой (100 мл) и выпадающий осадок, который образуется при этом, собирается, чтобы получить 200 мг (62% ), т. пл. 86-87оС 1-метил-5-нитропиррол-2-карбонитрила.
П р и м е р 2. Получение 1-этоксиметил-5-нитропиррол-2-карбонитрила.
К раствору 560 мл 5-нитропиррол-2-карбонитрила (4 ммоль) и 20 мл сухого ТГФ добавляется 515 мг трет бутоксида калия (4,6 ммоль). После добавления 0,45 мл хлорметилэтилового эфира (4,8 ммоль) к смеси она перемешивает в течение 4 ч, затем разбавляется эфиром (30 мл) и водой (50 мл). Органический слой отделяется, промывается водным MgSO4 (20 мл) и высушивается над MgSO4. После выпаривания растворителя получается красное масло (600 мл, 75% ) 1-этоксиметил-5-нитропиррол-2-карбонитрила.
Анализ.
Вычислено, % : C 49,23 H 4,65 N 21,53
Найдено, % : C 49,40 H 4,07 N 21,30
П р и м е р 3. Получение диэтилацеталя 3-трифторацетил-3-цианопропионового альдегида.
К перемешиваемой при 40-45оС суспензии промытого гексаном гидрида натрия (5,5 г 60% -й дисперсии, 0,14 моль) в 200 мл высушенного тетрагидрофурана добавляется по каплям раствор этилового эфира трифторуксусной кислоты (15 г, 0,11 моль) и диэтилацеталя 3-цианопропионового альдегида (17 г, 0,11 моль) в 100 мл сухого тетрагидрофурана. Первоначально серая суспензия медленно превращается в светло-коричневый цвет. Реакционная смесь перемешивается при 50-55оС в течение ночи до погашения реакции медленным добавлением 2-пропанола (15 мл). Выпаривание роторным испарителем легколетучих элементов дает темное масло, к которому добавляется 150 мл воды рН 7. Непрореагировавшие исходные вещества удаляются путем промывки водного слоя диэтиловым эфиром (3 х 30 мл). Основная водная фаза подкисляется затем 12 н раствором соляной кислоты и экстрагируется этилацетатом (2 х 100 мл). Объединенные органические слои промываются один раз насыщенным раствором бикарбоната натрия (40 мл) и один раз рассолом (15 мл) перед высушиванием над сульфатом магния. Выпаривание с помощью роторного испарителя дает красноватое масло, которое подвергается флеш-хроматографии над силикагелью, используя смесь гексана и этилацетата (4: 1) в качестве элюента, чтобы выработать целевой продукт (9 г, 32% ) в виде желтого масла.
П р и м е р 4. Получение 3-трифторацетил-3-цианопропионового альдегида.
Смесь 4,4-диэтилацеталя-2-трифторацетилцианопропионового альдегида (5,0 г, 0,02 моль) и дигидрата щавелевой кислоты (1,2 г, 0,01 моль) в 75 мл воды нагревается до температуры кипения с обратным холодильником в течение 20 мин. После этого смесь охлаждается, добавляется бикарбонат натрия (1,7 г, 0,02 моль) и затем 100 мл этилацетата. Слои разделяются и органическая фаза промывается один раз рассолом (15 мл) до процесса высушивания над сульфатом магния. Выпаривание роторным испарителем дает темное масло, которое используется немедленно в следующей стадии реакции.
П р и м е р 5. Получение 2-(трифторметил)-пиррол-3-карбонитрила.
Сырой альдегид, выделенный из предыдущей стадии, (4,5 г) растворяется в 50 мл ледяной уксусной кислоты, после этого добавляют ацетат аммония (1,5 г, 0,02 моль). Смесь нагревается до 65-70оС в течение часа, охлаждается, а затем выливается в 100 мл воды. Проводится экстракция этилацетатом (2 х 75 мл), после этого осуществляют промывание бикарбонатом объединенных органических фаз до тех пор, пока не исчезнет кислота. Красный раствор высушивается над сульфатом магния и выпаривается роторным испарителем до темного масла. Очистка над силикагелью, используя смесь гексана и этилацетата (4: 1) в качестве элюента, дает 2-трифторметил-3-цианопиррол (0,7 г, 4,3 ммоль, 22% в расчете на ацеталь) в виде светло-желтого твердого вещества, т. пл. 122-124оС.
П р и м е р 6. Получение 1-(этоксиметил)-2-(трифторметил)-пиррол-3-карбонитрила.
Перемешиваемый раствор 2-трифторметил-3-цианопиррола (1,0 г, 6,2 ммоль) в сухом тетрагидрофуране обрабатывается с помощью NaH (0,30 г, 7,5 ммоль) в виде 60% -й дисперсии в нефти в атмосфере азота при комнатной температуре. Спустя 20 мин реакционная смесь обрабатывается по каплям раствором хлорметилэтилового эфира (0,77 г, 8,1 ммоль) в сухом тетрагидрофуране, перемешивается энергично в течение 3 ч и обрабатывается смесью 1н раствора HCl и этилацетата. Фазы разделяются и органическая фаза промывается рассолом, высушивается над MgSO4 и концентрируется в вакууме, чтобы получить остаток. Флеш-хроматография остатка, используя силикагель и смесь гексана и этилацетат (3: 5: 1), дает названное выше соединение в виде бледно-желтого масла 0,83 г (61% ).
П р и м е р 7. Получение 4,5-дибром-2-(трифторметил)-пиррол-3-карбонитрила.
К раствору 2-(трифторметил)-пиррол-3-карбонитрила (1,0 г, 6,2 ммоль) в 40 мл тетрагидрофурана добавляется N-бромсукцинамид (2,2 г, 13 ммоль) по частям. Реакционной смеси позволяют перемешиваться в течение ночи при комнатной температуре, после чего гасят реакцию насыщенным водным раствором тиосульфата натрия (5 мл). Добавляется вода (15 мл) и диэтиловый эфир (50 мл) и слои разделяются. Органический слой промывается рассолом (10 мл) и высушивается над сульфатом магния. Выпаривание роторным испарителем дает сырое твердое вещество, которое подвергается флеш-хроматографии, используя смесь гексана и этилацетата (2: 1) с добавкой уксусной кислоты (2 мл на 300 мл растворителя) в качестве элюента Целевой 2-трифторметил-3-циано-4,5-дибромпиррол (0,8 г, 2,5 ммоль, 40% ) выделяется в виде бледно-желтого твердого вещества.
П р и м е р 8. Получение 4,5-дибром-1-метил-2-(трифторметил)-пиррол-3-карбонитрила.
К раствору 2-трифторметил-3-циано-4,5-дибромпиррола (0,5 г, 1,6 ммоль) в 30 мл сухого тетрагидрофурана добавляется по частям третбутоксид калия (0,2 г, 1,9 ммоль). Окрашенному в розовый цвет раствору позволяют перемешиваться в течение 20 мин, а затем аккуратно добавляют йодистый метил (0,6 г, 4,2 ммоль). Полученная суспензия перемешивается в течение 5 ч, после чего реакция гасится добавлением 10 мл воды. Добавляется также диэтиловый эфир (50 мл) и слои разделяются. Органическая фаза промывается рассолом (10 мл) и высушивается над сульфатом магния. Выпаривание роторным испарителем дает сырое твердое вещество, которое подвергается флеш-хроматографии над силикагелью, используя смесь гексана и этилацетата (4: 1) в качестве элюента, чтобы получить N-метилированный пиррол (0,4 г, 1,2 ммоль, 77% ) в виде светло-желтого твердого вещества, т. пл. 123-125оС.
Используя подобную методику и заменяя алкилирующий агент на хлорметил- этиловый эфир, получают 4,5-дибром-1-(этоксиметил)-2-(трифторметил)-пиррол-3-карбонитрил в виде белого твердого вещества, т. пл. 65-67оС.
П р и м е р 9. Получение 3,4-дибром-5-нитропиррол-2-карбонитрила.
Образец 5-нитропиррол-2-карбонитрила (0,4 г, 0,003 моль) легко растворяется в 10 мл разбавленного раствора гидроокиси натрия (0,4 г, 0,01 моль). По каплям добавляется бром (0,96 г, 0,006 моль), что приводит к выпадению в осадок твердого вещества. Дополнительное количество 10% -го раствора гидроокиси натрия добавляется до тех пор, пока все твердое вещество не растворится. Затем раствор перемешивается в течение 15 мин, после чего подкисляется разбавленным раствором соляной кислоты. Выпадающий белый осадок собирается и высушивается. Продукт реакции (0,5 г, 56% ) имеет т. пл. 181-186оС.
П р и м е р 10. Получение 3,5-дибром-4-нитропиррол-2-карбонитрила.
4-нитропиррол-2-карбонитрил (0,6 г, 0,042 моль) легко растворяется в 15 мл воды, содержащей гидроокись натрия (0,5 г, 0,012 моль). По каплям добавляется бром (1,34 г, 0,008 моль), что приводит к образованию твердого осадка. Затем гидроокись натрия (10% -й раствор) добавляется до тех пор, пока твердое вещество не растворится. Получающийся раствор перемешивается в течение 15 мин, после чего этот раствор подкисляется разбавленной соляной кислотой. Выпадающий белый осадок (1,0 г, 83% ) имеет т. пл. 170-175оС.
Вычислено для
C5HBr2 N3O2 % :
C 20,35 H 0,33 N 14,24 Br 54,20
Найдено, % :
C 20,72 H 0,23 N 14,16 Br 53,50.
П р и м е р 11. Получение 2,4,5-трихлорпиррол-3-карбонитрила.
К перемешиваемой смеси 1,50 г (16,3 ммоль) пиррол-3-карбонитрила в 50 мл ледяной уксусной кислоты быстро добавляется по каплям 4,1 мл (51,0 ммоль) хлористого сульфурила с помощью шприца через каучуковую перегородку. При этом добавлении температура реакционной смеси повышается примерно от 22 до 32оС. Смесь перемешивается 1,5 ч, а затем разбавляется со 100 мл воды. Получающиеся твердые вещества собираются фильтрацией и промываются водой. После высушивания выход составляет 2,23 г (70% ) белого твердого вещества, т. пл. более 300оС.
П р и м е р 12. Получение 2,4,5-трибромпиррол-3-карбонитрила.
К перемешиваемой смеси 1,50 г (16/3 ммоль) пиррол-3-карбонитрила в 20 мл хлороформа добавляется по каплям из капельной воронки смесь 2,5 мл (48,5 ммоль) брома в 7,5 мл хлороформа в пределах примерно 30 мин. Температура смеси повышается до 38оС и образуется липкая твердая масса, которая требует добавления дополнительного количества хлороформа (25 мл) и некоторого подогревания, чтобы достигнуть хорошего перемешивания. Смесь перемешивается в течение дополнительных 2 ч при комнатной температуре, твердый продукт реакции собирается фильтрацией и промывается хлороформом. Собранные твердые вещества составляют 4,55 г. Концентрирование фильтрата дает дополнительно 0,58 г продукта реакции. Объединенные твердые вещества превращаются в шламообразное состояние с помощью кипящего хлористого метилена. После охлаждения и фильтрации получают 3,66 г бледно-оранжевого порошка, т. пл. 253-255оС.
Анализ.
Вычислено для
C5HBr3N2, % : C 18,26 H 0,31 N 8,52
Br 72,91
Найдено, % :
С 18,28 H 0,35 N 8,52
Br 72,74
П р и м е р 13. Получение 2,4,5-трийодпиррол-3-карбонитрила.
4-цианопиррол-2-карбоновая кислота (1,36 г, 0,01 моль) добавляется к подогретой суспензии бикарбоната натрия (16,8 г, 0,2 моль) в воде (150 мл). После того как вся кислота растворится, раствор йода (8,3 г, 0,033 моль) и йодистого калия (11,0 г, 0,66 моль) в воде (50 мл) медленно добавляется с перемешиванием в пределах одного часа. Смесь нагревается при 70-80оС в течение 2 ч и охлаждается в ледяной бане, а затем оставляется в холодильнике в течение ночи. Твердые вещества собираются, тщательно промываются водой и высушиваются. Колоночная флеш-хроматография на силикагеле, заполненном в хлористом метилене, дает продукт реакции в виде желтого твердого вещества при кристаллизации их этилацетата (0,65 г); т. пл. 257-258оС.
П р и м е р 14. Получение 1-метил-2,4,5-трихлорпиррол-3-карбонитрила.
К перемешиваемой смеси 0,70 г (6,2 ммоль) трет-бутоксида калия в 25 мл сухого ТГФ в атмосфере азота добавляется по каплям из капельной воронки 1,00 г (5,12 ммоль) 2,4,5-трихлорпиррол-3-карбонитрила в 20 мл сухого ТГФ в течение 15 мин. Спустя 15 мин с помощью шприца в течение 10 мин добавляется по каплям 0,50 мл (8,03 ммоль) йодистого метила. Твердые вещества образуются и после перемешивания в течение примерно 3 ч смесь разбавляется со 100 мл воды. Мутная смесь экстрагируется дважды этилацетатом и объединенные органические слои промываются последовательно разбавленной NaOH, водой и насыщенным солевым раствором. После высушивания над сульфатом магния органическая смесь фильтруется и концентрируется под вакуумом, чтобы получить 0,99 г не совсем белого твердого вещества. Очистка хроматографией на силикагеле, используя хлористый метилен, дает 0,68 г не совсем белого твердого вещества. Очистка хроматографией на силикагеле, используя хлористый метилен, дает 0,68 г желтовато-белого твердого вещества, которое превращается в шлам с помощью гексана и извлекается фильтрацией; т. пл. 110-114оС.
Анализ.
Вычислено для C6H3Cl3N3, % :
C 34,40 H 1,44 N 13,38 Cl 50,78
Найдено, % :
C 34,25 H 1,50 N 13,36 Cl 50,88
П р и м е р 15. Получение 1-метил-2,4,5-трибромпиррол-3-карбонитрила.
К перемешиваемой смеси 0,87 г (7,75 ммоль) третбутоксида калия в 30 мл сухого ТГФ в атмосфере азота добавляется по каплям из капельной воронки 2,10 г (6,39 ммоль) 2,4,5-трибромпиррол-3-карбонитрила в 20 мл сухого ТГФ. Спустя 15 мин добавляется с помощью шприца в пределах 2 мин 0,64 мл (10,3 ммоль) йодистого метила. После нескольких часов при комнатной температуре смесь разбавляется со 100 мл воды и 75 мл этилацетата. Разделенная водная фаза экстрагируется снова этилацетатом и объединенные органические слои промываются разбавленной гидроокисью натрия, водой и насыщенным раствором соли. После высушивания над сульфатом магния смесь встряхивается вместе с активированным углем и фильтруется. Концентрация под вакуумом дает белое твердое вещество, которое превращается в шлам с помощью гексана и перекристаллизовывается из этилацетата, чтобы получить названное выше соединение в виде белого твердого вещества, т. пл. 151-152оС.
Используя аналогичную методику и применяя 4,5-дибромпиррол-3-карбонитрил в качестве субстрата, получают 1-метил-4,5-дибромпиррол-3-карбонитрил в виде белого твердого вещества; т. пл. 138-139оС.
П р и м е р 16. Получение 1-бензил-2,4,5-трибромпиррол-3-карбонитрали.
К перемешиваемой смеси 1,00 г (3,04 ммоль) 2,4,5-трибромпиррол-3-карбонитрила и 0,68 г (6,1 ммоль) третбутоксида калия в 30 мл сухого ТГФ в атмосфере азота добавляется 1,10 мл бромистого бензила. Смесь нагревается до кипения с обратным холодильником и перемешивается в течение ночи. После разбавления со 100 мл воды и 150 мл этилацетата органическую смесь разделяют и промывают с помощью солевого раствора, высушивают над сульфатом магния и концентрируют под вакуумом, чтобы получить 2,34 г оранжевого масла. Масло растирается в порошок под смесью гексана и эфира (5: 1), чтобы получить белое твердое вещество, собираемое фильтрацией (0,81 г); т. пл. 100-103оС. Фильтрат дает вторую массу вещества (0,11 г); т. пл. 100-103оС.
П р и м е р 17. Получение 1-аллил-2,4,5-трибромпиррол-3-карбонитрила.
К раствору 2,4,5-трибромпиррол-3-карбонитрила (2,0 г, 6,1 ммоль) в безводном тетрагидрофуране (20 мл) добавляется по частям при комнатной температуре третбутоксид калия (0,75 г, 6,7 ммоль), после 30 мин добавляется по каплям аллил йодистый (1,12 г, 6,7 ммоль), а затем смесь нагревается с обратным холодильником в течение 2 ч. Обработка по описанному в примере 15 методу дает продукт реакции в виде бледно-розовой жидкости (2,1 г).
П р и м е р 18. Получение этилового эфира 2,4,5-трибром-3-цианопиррол-1-уксусной кислоты.
К раствору 2,4,5-трибромпиррол-3-карбонитрила (2,0 г, 6,1 ммоль). После 30 мин добавляется по каплям этиловый эфир бромуксусной кислоты (1,12 г, 6,7 ммоль) и смесь перемешивается в течение 4-5 ч при комнатной температуре. Обработка по описанной в примере 15 методике дает продукт реакции в виде белого твердого вещества (0,42 г); т. пл. 140-143оС.
П р и м е р 19. Получение 2,4,5-трибром-1-этилпиррол-3-карбонитрила.
К раствору 2,4,5-трибромпиррол-3-карбонитрила (2,0 г 6,1 ммоль) в безводном тетрагидрофуране (20 мл) добавляется по частям при комнатной температуре третбутоксид калия (0,75 г, 6,7 ммоль). После 30 мин добавляется по каплям йодистый этил (1,04 г, 6,7 ммоль). Реакционная смесь перемешивается при комнатной температуре в течение 30 мин, а затем нагревается с обратным холодильником в течение 90 мин. Смесь охлаждается, разбавляется водой и экстрагируется этилацетатом. Органический слой промывается водой и насыщенным раствором хлористого натрия и высушивается (Na2SO4). Выпаривание растворителя и кристаллизация из смеси эфира и гексана дает твердое вещество, которое далее очищается колоночной флеш-хроматографией на силикагеле, уплотненном вместе с хлористым метиленом, и элюируется 3% -ым раствором этилацетата в хлористом метилене. Аналитически чистый образец в конце концов кристаллизуется из смеси хлористого метилена и гексана в виде белого твердого вещества (1,55 г); т. пл. 108,5-109,5оС.
Аналогичным путем, описанным для получения 2,4,5-трибром-1-этилпиррол-3-карбонитрила в примере 19, используя требуемые цианотригалоидпиррол и соответствующий алкилирующий агент, получают представленные ниже дополнительные аналоги (табл. 1).
П р и м е р 33. Получение 2,4,5-трибромпиррол-1,3-дикарбонитрил.
К раствору 2,4,5-трибромпиррол-3-карбонитрила (1,50 г, 4,56 ммоль) в безводном тетрагидрофуране (20 мл) добавляется по частям при комнатной температуре третбутоксид калия (614 мг, 5,74 ммоль). После 15 мин по каплям добавляется раствор бромистого циана (177 мг, 5,74 ммоль) в тетрагидрофуране (5 мл). Реакционный раствор перемешивается при комнатной температуре в течение ночи и становится мутным. Смесь разбавляется водой и экстрагируется этилацетатом. Органический слой промывается водой и насыщенным водным раствором хлористого натрия и высушивается над Na2SO4. Выпаривание растворителя и кристаллизация остатка из эфира дает белое твердое вещество (1,20 г); т. пл. 195,0-197,5оС.
П р и м е р 34. Получение 3,4,5-трибромпиррол-2-карбонитрила.
Гидроокись натрия (3,2 г, 0,08 моль) растворяется в 100 мл воды, за которым следует добавление пиррол-2-карбонитрила (2,6 г, 0,027 ммоль). Добавляется несколько миллилитров диоксана, чтобы смесь стала гомогенной. Затем малыми порциями добавляется при 28-35оС и с периодическим охлаждением 12,96 г брома (0,081 моль). Прежде чем завершится добавление, твердые вещества начинают выпадать в осадок. Содержание переводится обратно в раствор добавлением 10% -й гидроокиси натрия. Затем остающийся бром добавляется в раствор, перемешивается в течение 15 мин до подкисления смеси разбавленной соляной кислотой. Белое твердое вещество (7,4 г, 84% ) собирается и после высушивания имеет т. пл. 215-218оС.
Вычислено для C5HN2Br3, % :
C 18,25 H 0,30 N 8,51 Br 72,92.
Найдено, % :
C 18,06 H 0,37 N 8,39 Br 72,72
П р и м е р 35. Получение 3,4,5-трибром-1-метилпиррол-2-карбонитрила.
3,4,5-трибром-пиррол-2-карбонитрил (1,0 г, 0,003 моль) растворяется в смеси ацетона и диметоксиэтана. Добавляется карбонат калия (0,45 г, 0,0033 моль) и йодистый метил (0,478 г, 0,0033 моль). После перемешивания в течение ночи при комнатной температуре реакционная смесь выливается в воду и фильтруется. Отжатый осадок на фильтре высушивается на воздухе, чтобы получить названное выше соединение в виде белого твердого вещества 0,8 г (80% ); т. пл. 115-119оС.
Используя аналогичную методику и подставляя пропаргил бромистый в качестве алкилирующего агента, получают 3,4,5-трибром-1-(2-пропинил)-пиррол-2-кар- бонитрил в виде желтого твердого вещества; т. пл. 95-105оС.
П р и м е р 36. Получение 3,5-дибром-пиррол-2,4-дикарбонитрила.
Пиррол-2,4-дикарбонитрил (0,5 г, 0,004 моль) легко растворяется в 15 мл воды, содержащий гидроокись натрия (0,5 г, 0,012 моль). Затем добавляется бром (1,34 г, 0,008 моль) и раствор перемешивается в течение 15 мин. Тонкослойная хроматография (90/10 метиленхлористый/ацетонитрил) показывает, что реакция не завершилась. Дополнительное количество брома добавляется и реакция прослеживается с помощью ТСХ. Когда реакция завершается, смесь подкисляется и собирается белое твердое вещество. Твердое вещество (0,47 г, 40,8% ) после перекристаллизации из дихлорэтана (30 мл) имеет т. пл. 227-232оС.
Вычислено для C6HBr2N3, % :
C 26,20 H 0,36 N 15, 28 Br 58,15
Найдено, % :
C 26,25 H 0,58 N 15,17 Br 58,35
П р и м е р 37. Получение 3,5-дибром-1-метилпиррол-2,4-дикарбонитрила.
Образец (1,0 г, 0,036 моль) 3,5-дибромпиррол-2,4-дикарбонитрила легко растворяется в 20 мл ацетона. Добавляется безводный карбонат калия (0,64 г, 0,0046 моль) и в то время, когда шлам перемешивается, добавляется йодистый метил (0,68 г, 0,0047 моль). Реакция может контролироваться с помощью ТСХ. Когда реакция завершается, смесь выливается в воду и выпадает белое твердое вещество. Продукт реакции (0,77 г, 74% ) имеет т. пл. 175-178оС.
Вычислено для C7H3Br2N3, % :
C 29,08 H 1,04 N 14,54 Br 55,33
Найдено, % :
C 29,09 H 1,42 N 14,54 Br 54,95.
П р и м е р 38. Получение 3-бром-2,5-дихлор-4-нитропиррола.
Указанное соединение может быть получено растворением образца 2,5-дихлор-3-нитропиррола (0,54 г, 0,003 моль) в 10 мл разбавленной гидроокиси натрия (0,25 г, 0,006 моль) и добавлением брома. До того как добавят весь бром, может быть прибавлено дополнительное количество основания. Когда добавление завершится, раствор может быть подкислен разбавленной соляной кислотой, чтобы целевой продукт реакции выпал в осадок.
П р и м е р 39. Получение 4-(трифторметил)-пиррол-3-карбонитрила.
Смесь паратолилсульфонилметилизоцианида (0,72 г, 3,2 ммоль) и гидрида натрия (0,09 г, 3,8 ммоль) в безводном этиловом эфире обрабатывается по каплям раствором 4,4,4-трифторкротононитрила (0,38 г, 3,2 ммоль) в эфире и диметилсульфоксиде в течение 35 мин, перемешивается при комнатной температуре в течение 20 мин и реакция гасится водой. Фазы разделяются и водяная фаза экстрагируется эфиром. Органические фазы собираются, промываются солевым раствором, высушиваются над MgSO4 и концентрируются под вакуумом, чтобы получить оранжевый твердый остаток. Остаток подвергается флеш-хроматографии, используя силикагель и смесь петролейного эфира, этилового эфира и уксусной кислоты (100: 100: 1), затем добавляют 100% -й хлористый метилен, чтобы получить названный выше продукт реакции в виде белого твердого вещества; т. пл. 96-97оС.
П р и м е р 40. Получение 2,5-дибром-4-(трифторметил)-пиррол-3-карбонитрила.
Смесь 4-(трифторметил)-пиррол-3-карбонитрила (0,10 г, 0,63 ммоль) и ацетата натрия (0,2 г, 2,4 ммоль) в уксусной кислоте обрабатывается по каплям раствором брома (0,23 г, 1,4 ммоль) в уксусной кислоте, перемешивается в течение 6 ч при 25оС и выливается в водный раствор метабисульфита. Полученная смесь фильтруется и отжатый на фильтре осадок промывается водой и высушивается воздухом, чтобы получить названное выше соединение в виде белого твердого вещества 0,11 г (58% ); т. пл. 198-200оС.
П р и м е р 41. Получение 2,5-дибром-1-метил-4-(трифторметил)-пиррол-3-карбони- трила.
Раствор 2,5-дибром-4-(трифторметил)-пиррол-3-карбонитрила (0,10 г, 0,30 ммоль) в тетрагидрофуране обрабатывается твердым третбутоксидом калия (0,053 г, 0,49 ммоль), перемешивается в течение 1 ч при 25оС, обрабатывается по каплям йодистым метилом (0,067 г, 0,47 ммоль), перемешивается в течение 2 ч при 25оС, в течение 1 ч при 50оС и разбавляется водой и эфиром. Фазы разделяются и органическая фаза промывается последовательно водой и солевым раствором, высушивается над MgSO4 и концентрируется под вакуумом, чтобы получить названное выше соединение в виде твердого белого вещества 0,09 г; т. пл. 101-104оС.
П р и м е р 42. Получение 4,5-дибром-1-метилпиррол-2-карбонитрила.
Раствор 1-метилпиррол-2-карбонитрила (1,06 г, 0,01 моль) в тетрагидрофуране обрабатывается N-бромсукцинимидом (5,34 г, 0,03 моль) при 25-30оС, перемешивается в течение 18 ч при 25оС и концентрируется под вакуумом, чтобы получить остаток. Остаток переносится в четыреххлористый углерод, фильтруется и фильтрат концентрируется под вакуумом, чтобы получить твердый остаток. Перекристаллизация из смеси этанола и воды дает названное выше соединение в виде серого твердого вещества; т. пл. 104-105оС.
П р и м е р 43. Получение этилового эфира 4-(трифторметил)-пиррол-3-карбоновой кислоты.
Раствор третбутоксида калия (8,11 г, 0,075 моль) в тетрагидрофуране при -60оС обрабатывается по каплям смесью этилового эфира 4,4,4-трифторкротоновой кислоты (10,5 г, 0,063 моль) и пара толилсульфонилметилизоцианида (12,2 г, 0,063 моль) в тетрагидрофуране в течение 1 ч, перемешивается при -60оС в течение 30 мин, смеси позволяют нагреваться до комнатной температуры и реакция гасится водой. Реакционная смесь экстрагируется эфиром и этилацетатом. Объединенные экстракты промываются солевым раствором, высушиваются (MgSO4) и концентрируются под вакуумом, чтобы получить твердый остаток. Перекристаллизация из 1,2-дихлорэтана дает названное выше соединение в виде рыжевато-коричневого твердого вещества, 7/3 г (56% ); т. пл. 163-164оС.
П р и м е р 44. Получение этилового эфира 1-метил-4-(трифторметил)-пиррол-3-карбоновой кислоты.
Раствор третбутоксида калия (4,5 г, 0,04 моль) в тетрагидрофуране обрабатывается по каплям раствором этилового эфира 4-(трифторметил)-пиррол-3-карбоновой кислоты (8,3 г, 0,04 моль) в тетрагидрофуране в течение 20 мин при 20-25оС, перемешивается в течение 30 мин, обрабатывается по каплям йодистым метилом (5,7 г, 0,04 моль), перемешивается при комнатной температуре в течение 24 ч и выливается в воду. Полученная смесь экстрагируется эфиром и объединенные экстракты промываются солевым раствором, высушиваются (MgSO4) и концентрируются под вакуумом, чтобы получить коричневый маслянистый остаток. Остаток перегоняется, используя перегонный аппарат Кугельохра, чтобы получить смолообразное твердое вещество при 80-85оС/0,2 мм рт. ст. Твердое вещество очищается, используя эфир и основную окись алюминия, чтобы получить названное выше соединение в виде прозрачного масла 6,37 г (72% ), идентифицированное с помощью ЯМР и элементарного анализа.
П р и м е р 45. Получение 1-метил-4-(трифторметил)-пиррол-3-карбоновой кислоты.
Смесь этилового эфира 1-метил-4-(трифторметил)-пиррол-3-карбоновой кислоты (4,4 г, 0,02 моль) и 4н. раствора гидроокиси натрия (5 мл, 0,02 моль) в этаноле перемешивается в течение 24 ч при комнатной температуре, разбавляется водой и экстрагируется эфиром. Водная фаза подкисляется 10% -ым раствором HCl и фильтруется. Отжатый на фильтре осадок промывается водой и высушивается под вакуумом при 45оС, чтобы получить названное выше соединение в виде не совсем белого твердого вещества, 2,4 г (62% ); т. пл. 210-212оС.
П р и м е р 46. Получение 1-метил-4-(трифторметил)-пиррол-3-карбонитрила.
Смесь 1-метил-4-(трифторметил)-пиррол-3-карбоновой кислоты (1,93 г, 0,01 моль) в ацетонитриле при 40-45оС обрабатывается по каплям хлорсульфонилизоцианатом (1,41 г, 0,01 моль), нагревается при 40оС в течение 24 ч, охлаждается до комнатной температуры, обрабатывается диметилформамидом (1,46 г, 0,02 моль) нагревается при 40оС в течение 8 ч, охлаждается до комнатной температуры и выливается в воду. Полученная смесь экстрагируется этилацетатом. Экстракты объединяются, промываются последовательно водой и солевым раствором, высушиваются (MgSO4) и концентрируются под вакуумом, чтобы получить масляный твердый остаток. Остаток обрабатывается в этилацетате, промывается 1% -ым водным раствором гидроокиси натрия, высушивается (MgSO4) и концентрируется под вакуумом, чтобы получить желтый маслянистый остаток. Перегонка на аппарате Кугельрохра при 100-110оС/2 мм рт. ст. дает названный выше продукт реакции в виде белого твердого вещества, 0,95 г (54% ).
П р и м е р 47. Получение фенилового эфира 2,3,5-трибром-4-цианопиррол-1-карбоновой кислоты.
Смесь 7,0 г 2,4,5-трибромпиррол-3-карбонитрила и 2,9 г третбутоксида калия в тетрагидрофуране обрабатывается с 13,8 г фенилового эфира хлормуравьиной кислоты, нагревается с обратным холодильником при температуре кипения в течение 12 ч, охлаждается, выливается в воду и фильтруется. Твердый отжатый на фильтре осадок промывается водой и высушивается под вакуумом, чтобы получить названное выше соединение. Образец перекристаллизовывается из смеси этилацетата и метилциклогексана, чтобы получить бесцветные кристаллы; т. пл. 128-129оС.
П р и м е р 48. Получение метилового эфира 2,3,5-трибром-4-цианопиррол-1-карбоновой кислоты.
Раствор 2,4,5-трибромпиррол-3-карбонитрила (3,0 г, 0,091 моль) в тетрагидрофуране обрабатывается порциям и третбутоксида калия (1,33 г, 0,012 моль) при комнатной температуре, перемешивается в течение 2,5 дней, выливается в воду и экстрагируется эфиром. Объединенные эфирные экстракты промываются солевым раствором, высушиваются над MgSO4 и кон центрируются под вакуумом, чтобы получить коричневый твердый остаток. Остаток перекристаллизовывается из смеси этилацетат и гексанов, чтобы получить указанное соединение в виде рыжевато-коричневого твердого вещества, 1,4 г (39,5% ), т. пл. 119,5-122оС.
Используя приведенную методику и заменяя соответствующий хлорформиат, получаются следующие соединения


OCH= CH2 112-113
OCH2CH= CH2 86-89
П р и м е р 49 . Получение 2,4,5-трибром-1-(парахлорбензоил)-пиррол-3-карбонитрила.
Смесь 2,4,5-трибромпиррол-3-карбонитрила (5,0 г, 0,015 моль) и третбутоксида калия (2,0 г, 0,018 моль) в сухом тетрагидрофуране перемешивается в течение 10 мин при комнатной температуре, обрабатывается по каплям раствором хлорангидрида парахлорбензойной кислоты (3,25 г, 0,019 моль) в тетрагидрофуране, нагревается с обратным холодильником при температуре кипения в течение 3 ч, охлаждается и разбавляется смесью воды и этилацетата. Органическая фаза разделяется, промывается солевым раствором, высушивается над Na2SO4 и концентрируется под вакуумом, чтобы получить рыжевато-коричневый твердый остаток. Перекристаллизация из бензола дает названное выше соединение в виде окрашенного в кремовый цвет твердого вещества, 2,0 г (41,4% ); т. пл. 154-157оС.
Используя приведенную методику и заменяя на хлорангидрид параметоксибензойной кислоты получают 2,4,5-трибром-1-(параметоксибензоил)-пиррол-3-карбонитрил, т. пл. 86-89оС.
П р и м е р 50. Инсектицидные и акарицидные оценки циано- и нитро-пирролов.
В этих испытаниях оценки осуществляются, используя техническое вещество, растворенное в смеси ацетона и воды (50: 50). Все концентрации, приводимые в описании, зависят от использования действующего ингредиента. Испытания проводятся в лаборатории при температуре, поддерживаемой, примерно, при 27оС. Система оценок, применяется при этом, является следующей: с = эффект отсутствует 5= 56-65% гибели 1= 10-25% гибели 6= 66-75% гибели 2= 26-35% гибели 7= 76-85% гибели 3= 36-45% гибели 8= 86-99% гибели 4= 46-55% гибели 9= 100% гибели
10 = пониженная
подкормка.
Испытанные виды насекомых и акаридов, используемых в настоящих оценках вместе с конкретными методиками испытаний, описываются ниже.
Личинки 3-й возрастной стадии, южная совка луговая Spodoptera eridania.
Листва фасоли лимской, распустившаяся до 7-8 см по длине, погружается в испытуемый раствор с встряхиванием в течение 3 с и помещается под колпак для высушивания. Листва помещается затем в чашку Петри размером 100 х 10 мм, содержащую увлажненную фильтровальную бумагу на дне и десять гусениц 3-й возрастной стадии. Содержимое чашки Петри существует в течение 5 дней до того, как делаются наблюдения на летальность, пониженную подкормку или любое препятствие с нормальной линькой.
Spodoptera eridania - 7-дневный остаток.
Растения, обработанные по указанному испытанию, содержатся под действием ламп высокой интенсивности в теплице в течение 7 дней. Эти лампы удваивают действия яркого солнечного дня в июне в Нью-Джерси и продолжают длину дня на 14 ч. После 7 дней листва опробируется и испытывается так, как это приведено выше.
Aphis fabae - смешанная возрастная стадия, тля свекловичная.
Горшочек, содержащий единичные растения настурции Fropacodum sp высотой, примерно, 5 см, заражаются, примерно, 100-200 тлями за день до испытания. Каждый горшочек опрыскивается испытуемым раствором в течение 2 оборотов на поворотном круге со скоростью 4 об/мин под колпаком, используя мелкокапельный опрыскиватель типа 154 декилбисс. Кончик опрыскивателя держится на расстоянии 15 см от растения и струя направляется так, чтобы получить полное покрытие растений и тлей. Опрысканные горшочки помещаются бок о бок в лотки, покрытые белой эмалью, и содержатся в течение 2 дней, после чего делается оценка на летальность.
Fetranychus urticae (Р-устойчивый штамм), 2-пятнистый паутинный клещ.
Растения фасоли лимской с первичными листочками, распущенными на 7-8 см по длине, выбираются и прореживаются до одного растения на горшочек. Маленький кусочек срезается от листочка, взятого из основной колонии, и помещается на каждый листочек испытуемых растений. Это проделывается за 2 ч до обработки, чтобы позволить клещам двигаться повсюду по испытуемому растению и откладывать яйца. Размер срезаемого кусочка меняется, чтобы получить примерно 100 клещей на листочек. За время обработки кусочек листочка, используемого для переноса клещей, удаляется и отбрасывается. Зараженный клещами растения погружаются в испытуемый раствор на 3 с со встряхиванием и помещаются под колпак для высушивания. Растения содержаться в течение 2 дней, прежде чем делают оценки гибели взрослой особи, используя первый листок. Второй листок сохраняется на расстоянии в течение еще 5 дней, прежде чем фиксируются наблюдения гибели яиц и/или недавно вылупившихся бабочек.
Dialrotic undecimpunetata hawrdi - южная блошка длинноусая 3-й возрастной стадии.
Один см3 тонкоразмолотого талька помещается в стеклянную широкогорлую баночку с завинчивающейся крышкой и объемом 30 мл. Один мл соответствующего ацетонового раствора наносится пипеткой на тальк так, чтобы обеспечить 1,25 и 0,25 мг действующего ингредиента на баночку. Баночки помещаются под слабый ток воздуха до тех пор, пока не испарится ацетон. Высушенный тальк разрыхляется, добавляется 1 см3 семян просо, чтобы быть полезным в качестве питания для насекомых, и 25 мл влажной почвы в каждую баночку. Баночка закрывается крышкой и содержимое тщательно смешивается на миксере типа Вортекс. Вслед за этим десять длинноусых блошек 3-й возрастной стадии добавляются в каждую баночку и баночки неполностью закрываются крышкой, чтобы осуществляется воздушный обмен для личинок. Обработки проводятся в течение 6 дней, прежде чем делается подсчет летальности. Отсутствующие личинки являются предположительно погибшими, так как они разлагаются быстро и не могут быть обнаружены. Концентрации, используемые в этом испытании, соответствуют приблизительно к 50 и 10 кг/га соответственно.
Полученные данные представляются в табл. 2.
Когда проводятся два или более испытаний с данным соединением, оценки усредняются. Кроме того, когда испытания не были проведены, оценка представляется в виде знака (-).
П р и м е р 51. Инсектицидные оценки.
Инсектицидные оценки проводятся с растворами испытуемых соединений, растворенных или диспергированных в смесях ацетона и воды (50: 50). Испытуемое соединение является техническим веществом, растворенным или диспергированным в указанных смесях ацетона и воды в достаточном количестве, чтобы обеспечить представленные в табл. 3 концентрации. Система оценок, используемая при этом, является такой же системой оценок, что и описанная в примере 38. Применяемые методики описываются ниже для оценок против специфических видов насекомых. Когда проводятся два или более испытаний, используя одно и то же соединение, сообщаются средние величины результатов испытаний.
Empoasca abrupta - взрослые особи, цикадка картофельная (щападной картофели).
Листок фасоли лимской длиной 5 см погружается в испытуемый раствор на 3 с с встряхиванием и помещается под колпак для высушивания. Листок ставится в чашку Петри размером 100 х 10 мм, содержащую влажный фильтр на дне чашки. В каждую чашку добавляется примерно 10 взрослых особей цикадок и обработки продолжаются в течение 3 дней, прежде чем делаются подсчеты гибели (летальности).
Heliotis vivscens - совка табачная 3-й возрастной степени (стадии).
Хлопковые семядоли погружаются в испытуемый раствор и высушивается под колпаком. После высушивания каждая семядоля разрезается на четыре части, десять частей помещаются отдельно в пластмассовые медицинские чашки объемом 30 мл, содержащие кусочек влажного зубного тампона длиной 5-7 мм. В каждую чашку добавляется одна гусеница третьей возрастной стадии, картонная крышка ставится на чашку. Обработки содержаться в течение 3 дней, прежде чем делаются подсчеты гибели и определения понижения порчи питания.
Spodoptera eridania - системное поглощение, личинки (гусеницы) 3-й возрастной стадии, южная совка луговая.
Соединение вводится в состав в виде эмульсии, содержащей 0,1 г испытуемого вещества, 0,2 г эмульгатора типа эмульгатор Е-620, 10 мл ацетона и 90 мл воды. Эта смесь разбавляется 10-кратно водой, чтобы получить для каждого испытания эмульсию с концентрацией в 100 м. д. При необходимости осуществляются последующие 10-кратные разбавления водой. Растения фасоли лимской с первичными листочками, распушенными до 7-8 см длины, подрезаются по меньшей мере на 3 см выше уровня почвы, чтобы избежать заражения почвенными бактериями, которые вызывают разложение стебелька во время испытания. Подрезанные стебельки помещаются в испытуемые эмульсии и каждый стебелек обертывается небольшим количеством ваты, чтобы содержать стебелек вне дна бутыли и чтобы ограничивать выпаривание и улетучивание соединения. Испытания проводится в течение 3 дней при 27оС, чтобы позволить соединениям проникнуть в растение. Вслед за этим один листок удаляется от растений и помещается в чашку Петри размером 100 х 10 мм с 10-ю совками луговыми. Подсчет гибели и наблюдения порчи питания (подкормки) производятся спустя 3 и 5 дней. Подобная методика осуществляется для оценки испытуемых соединений против Empoasca abrupta взрослых особей, цикадки западной картофели. Полученные данные представляются в табл. 3.
Blatella germanica - испытание приманки, взрослая особь самца рыжего таракана.
0,1% -я приманка получается отмериванием пипеткой 1 мл ацетонового раствора испытуемого соединения 1000 м. д. концентрации на 1 г кукурузной муки в широкогорлой бутыли объемом 30 мл. Приманка высушивается пропусканием слабого тока воздуха в бутыль, помещается в широкогорлую банку Масона объемом в 1 пинту (0,57 л) и добавляется 10 взрослых особей рыжих тараканов. Решетчатая крышка накрывается на банку и маленький кусочек ваты, пропитанной в 10% -ом меду, ставится на верх решетчатой крышки. Подсчеты гибели осуществляются после 3 дней.
Blatella germanica - испытание осадка, взрослая особь самца рыжего таракана.
1 мл ацетонового раствора испытуемого вещества 1000 м. д. концентрации наносится пипеткой медленно на дно чашки Петри размером 150 х 15 мм с тем, чтобы получить однородное покрытие насколько это возможно. После высушивания осадка в каждую чашку помещаются 10 взрослых особей самцов рыжих тараканов и крышка накрывается. Подсчеты гибели осуществляются после 3-х дней.
Полученные данные приведены в табл. 3 и 4.
П р и м е р 52. Оценка испытуемых соединений для борьбы со слизняками видов Arion subfuscus.
Оценка А.
5% -я приманка каждого испытуемого соединения получается путем смешивания 0,10 г технического вещества с 1,90 г приманки, состоящей из 46% необработанной отруби, 6% мелессы и 48% воды. Одно испытуемое место действия устанавливается для каждой обработки путем помещения 2 г приманки на крышку от одноунциевой (28,3 г) банки и, ставя крышку на 8-унциевую (226,4 г) чашку, покрытую воском и обшитую изнутри влажной фильтровальной бумагой. Каждая чашка заражается 5-ю собранными на поле улитками вида Arion subfuscus. Пластмассовая крышка с мелкими отверстиями сквозь нее ставится поверх каждой чашки. Испытание устанавливается и заражается собранными на поле улитками. Испытуемые обработки исследуются периодически и показания гибели снимаются после 3 и 4 дней. Улитки, которые не реагируют на уколы, считаются погибшими. Улитки, которые реагируют намного более медленно, чем необработанные контрольные улитки, рассматриваются погибающими.
Соединение Гибель улиток
вида Arion
subfuscus, %
2,4,5-трибромпиррол-3- карбонитрил 100
2,4,5-трихлор-1-метил- пиррол-3-карбонитрил 100
2,4,5-трибром-1-метилпир- рол-3-карбонитрил 100
1-бензил-2,4,5-трихлорпир- рол-3-карбонитрил 100
1-бензил-2,4,5-трибромпир- рол-3-карбонитрил 100
2,4,5-трибромпиррол-1,3- дикарбонитрил 100
1-(этоксиметил)-5-нитропир- рол-2-карбонитрил 100
Оценка В.
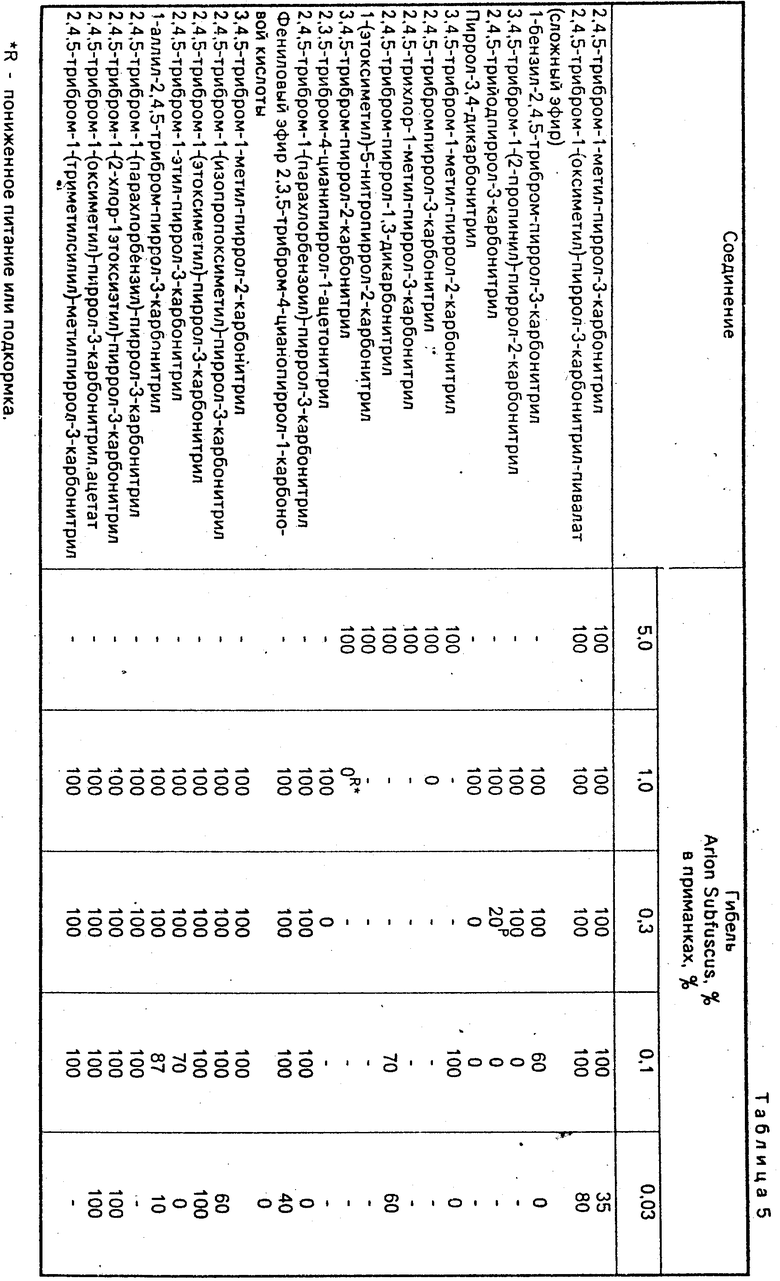
Испытуемые соединения взвешиваются и разбавляются в ацетоне для достижения соответствующей концентрации, 1 мл каждого испытуемого раствора добавляет к 1 г необработанной отруби. Затем ацетон удаляется выпариванием. Приманковая композиция получается смешиванием 1 г обработанной по указанной методике необработанной отруби с 1 мл мелассовой смеси, состоящей из 4 мл мелассы и 30 мл воды. Полученная таким образом приманковая композиция помещается на крышку 1-унциевой (28,3 г) банки, которая затем помещается на дно 8-унциевой (226,4 г) чашки из покрытой воском бумаги, которая облицовывается изнутри влажной фильтровальной бумагой. Каждая чашка поражается затем 5-ю улитками. Контрольная чашка, которая содержит 0% испытуемого соединения в приманочной композиции, также подготавливается и инфицируется. Испытуемые обработки исследуются ежедневно в течение 4 дней и проценты питания и гибели регистрируются. Полученные данные представляются в табл. 5.
П р и м е р 53. Оценка пирролкарбонитрилов и нитропирролов в качестве средств борьбы с наземными улитками вида Helix aprorce Helix aprosca, покупаются из Вордс Биоложикл Супплай Компани. Испытуемые соединения производят в виде приманочных смесей следующим образом: 5% -я приманка получается смешиванием технического вещества (50 мг) в отрубевой приманке (950 мг). Приманка создается из 46% необработанной отруби, 6% мелассы и 48% воды. Обработанная приманка помещается во взвешенную лодочку (7 мл) из полистирола. Размещенная приманка вставляется в пластмассовый сосуд (500 мл) с одним влажным зубным тампоном. Затем в каждую обработку добавляются две улитки и поверх каждого сосуда крепко накрывается прозрачная пластмассовая крышка с отверстиями для аэрации. Сосуды исследуются 24 ч спустя после начала испытания. Полученные данные представляются в табл. 6.
П р и м е р 54. Опыт на наземных улитках с помощью пирролкарбонитрилов.
Bulimulus maria (наземные улитки из Каролина Биоложикал Супплай Компани, код 480) испытываются в 30 мл широкогорлых банках, используется 5% -я приманка с кукурузной мукой, т. е. 25 мг соединения, смешанного в 450 мг кукурузной муки. Приманка увлажняется каждые 2 дня. Одна улитка добавляется в каждую банку и крышки накрываются неплотно поверх банок. Фекалии показывают питание улиток. Гибель наблюдается путем опробирования животного шпателем. Если животное является живым, сокращения являются очевидными. Медленное вытекание и/или полное исчезновение в оболочке показывает гибель. Соединение Гибель за
1 неделю, %
2,4,5-трибром-1-метилпир- рол-3-карбонитрил 100
П р и м е р 55. Активность пиррола на пресноводных улитках.
Пресноводные водянистые улитки вида Gyzaulis используются для испытания активности пирролов. Улитки собираются в и содержатся в резервуаре, заполненном прудовой водой, которая подвергается аэрации с помощью фильтра на дне резервуара. Ряд членов пиррольной серии составляются в аэрированной водопроводной воде (рН одинаков с прудовой водой) при двух дозировках - 100 и 33 м. д. Соединения имеют относительно низкую растворимость в воде при 100 м. д. , но при перемешивании и действии ультразвука растворимость значительно улучшается. Три здоровых улитки добавляются в каждый стаканчик объемом 150 мл, содержащий 80 мл обработанной воды. Испытуемыми концентрациями являются 100 и 33 м. д. Необработанный контроль также включается. Соединение М. д. Гибель за 18 ч, % 2,4,5-трибромпир- рол-3-карбонитрил 100 100
33 100 2,4,5-трихлор-1- метилпиррол-3- карбонитрил 33 100 2,4,5-трибром-1- метилпиррол-3- карбонитрил 33 100
П р и м е р 55. Активность пирролов на прудовые улитки (физиды).
Физиды вида Physa, полученные из Вордс Биоложикл Супплай Компани, используются для оценки арилпирролов. Ряд членов пирролкарбонитрильной серии составляются в аэрированной водопроводной воде при двух дозировках - 10 и 1 м. д. Три здоровых улитки погружаются в 10 мл обработанной воды в 20-миллилитровых сцинтилляционных склянках. Крышки неплотно накрываются на каждую склянку. Соединение М. д. Гибель за 18 ч, %
2,4,5-трибромпир- рол-3-карбонитрил 10 100
1 100 2,4,5-трибром-1- метилпиррол-3- карбонитрил 10 100
1 100
П р и м е р 56. Анализ с помощью пропитки листьев проводили с целью измерения токсичности выбранных инсектицидов для личинки южной совки (Spodoptera eridania) на третьей возрастной стадии. Листья фасоли погружали в ацетон - водные (50: 50) инсектицидные растворы, а затем осушали воздухом. После этого один абсолютно сухой обработанный лист помещали в чашку Петри, содержащую влажную фильтровальную бумагу, и десять личинок южной совки на третьей стадии развития. Чашки выдерживали в лаборатории при постоянной температуре 27оС. Гибель личинок оценивали через 72 ч после обработки. Отдельные концентрации инсектицида повторяли 4 раза (один лист с 10-ю личинками на одну копию). Данные по уничтожению личинок подвергали пробит-анализам для получения величины LC50(летальная концентрация - 50% ). Результаты представлены в табл. 7.
П р и м е р 57. Анализы проводили в целях определения токсического действия некоторых акарицидных соединений на двухпятнистый паутинный клещ (Tefranychus artical). Инфицированные личинками клеща листья фасоли, еще находящиеся на растениях, погружали на 3 с в ацетон/водные (50: 50) акарицидные растворы. Затем обработанные растения выдерживали в лаборатории при постоянной температуре 27оС и относительной влажности 60% . Процент гибели взрослых клещей определяли через 3 дня после обработки. Данные уничтожения взрослых клещей подвергали пробит-анализам для определения величин LC50 (летальная концентрация - 50% ). Результаты представлены в табл 8.
П р и м е р 58.
В каждую клетку в 1 м2, содержащую слой почвы и несколько листьев латука-салата, добавляли 17 особей сетчатого слизня Deroceras reticulatum. Через 2 дня вручную вводили пестицидную приманку. Каждую обработку дублировали 3 раза и через 3 дня определяли процент гибели слизня. Результаты представлены в табл. 9.
П р и м е р 59. 2,4,5-трибромо-1-(гидроксиметил)-пиррол-3-карбонитрилпивалат (сложный эфир) смешивали до однородности с компонентами сухой приманки при концентрации активного ингредиента 0,5 и 1,0 мас. % . Компоненты сухой приманки состояли из 90 мас. % тонкоизмельченного корма для домашней птицы на основе кукурузы и сои и 10 мас. % пшеничного крахмала. Сухие компоненты смешивали с лагерным пивом в соотношении 500 г пива на 1150 г сухого продукта. Эту смесь экструдировали через сито с круглыми отверстиями в 2,5 мм, разрезали на кусочки 4-6 мм длиной и высушивали. После этого приготавливали 0,5% -ю приманку, содержащую 1-метил-2,4,5-трибромопиррол-3-карбонит- рил.
4% -я приманка (Вауе) из метиокарба и 5% -я приманка из метальдегида (Desangosse) являются готовыми коммерческими продуктами.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ ПРОИЗВОДНЫЕ ПИРРОЛА | 1993 |
|
RU2109012C1 |
| N-АЦИЛИРОВАННОЕ СОЕДИНЕНИЕ АРИЛПИРРОЛА, СПОСОБ БОРЬБЫ С НАСЕКОМЫМИ, СПОСОБ ПОЛУЧЕНИЯ N-АЦИЛИРОВАННЫХ СОЕДИНЕНИЙ АРИЛПИРРОЛА | 1991 |
|
RU2099326C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-(АЛКОКСИМЕТИЛ)ПИРРОЛЬНЫХ СОЕДИНЕНИЙ | 1994 |
|
RU2137758C1 |
| ТРИЦИКЛИЧЕСКИЕ ДИАЗЕПИНОВЫЕ АНТАГОНИСТЫ ВАЗОПРЕССИНА И АНТАГОНИСТЫ ОКСИТОЦИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЛЕЧЕНИЯ | 1994 |
|
RU2126006C1 |
| ПРОИЗВОДНЫЕ АРИЛПИРРОЛА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1990 |
|
RU2037485C1 |
| ПРОИЗВОДНЫЕ ИМИДАЗОЛИНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1991 |
|
RU2095359C1 |
| 2,6-ДИЗАМЕЩЕННЫЕ ПИРИДИНЫ ИЛИ 2,4-ДИЗАМЕЩЕННЫЕ ПИРИМИДИНЫ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ БОРЬБЫ С НЕЖЕЛАТЕЛЬНОЙ РАСТИТЕЛЬНОСТЬЮ | 1996 |
|
RU2134261C1 |
| 5,6-ДИЗАМЕЩЕННЫЕ 3-ПИРИДИЛМЕТИЛАММОНИЙ ГАЛОГЕНИДЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И СПОСОБЫ ПОЛУЧЕНИЯ 5-(ЗАМЕЩЕННЫЙ МЕТИЛ)-2,3-ПИРИДИНДИКАРБОНОВЫХ КИСЛОТ | 1993 |
|
RU2090558C1 |
| Способ получения производных пиразоло-/1,5- @ /пиримидина | 1980 |
|
SU1077571A3 |
| СПОСОБ ПОЛУЧЕНИЯ 23-(C-C-АЛКИЛОКСИМОВ)-LL-F-28249 | 1990 |
|
RU2030416C1 |





Использование: сельское хозяйство, химический способ уничтожения паразитов, акарид и моллюсков. Сущность изобретения: обработку паразитов, акарид и моллюсков осуществляют производным пиррола приведенной в описании формулы. 9 табл.
СПОСОБ УНИЧТОЖЕНИЯ ПАРАЗИТОВ, АКАРИД И МОЛЛЮСКОВ, включающий обработку указанных паразитов, мест их распространения и обитания производным пиррола, отличающийся тем, что в качестве производного пиррола используют соединение формулы
где W - циано или нитрогруппа;
X - циано, бром, хлор, йод и трифторметил;
Y - водород, бром, хлор, йод или трифторметил;
Z - водород, бром, хлор, йод;
B - водород, С1 - С6-алкил, С1 - С2-алкил, замещенный С1 - С4-алкоксигруппой, возможно замещенной хлором, аллил, пропинил, С1 - С2-алкил, замещенный циано или гидроксигруппой, незамещенный или замещенный хлором бензил, замещенный хлором бензоил, триметилсилил или COR, где R - низший алкил, фенил или цианогруппа в количестве 0,05 - 4 кг/га.
Авторы
Даты
1994-04-30—Публикация
1989-12-04—Подача